Металлы.ppt
- Количество слайдов: 119
 ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ Лекция Металлы 1. Общая характеристика металлов. 2. Способы получения металлов. 3. Химические свойства металлов. 4. Биологическая роль металлов. Лектор: Ирина Викторовна Ганзина кандидат биологических наук, доцент кафедры химии
ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ Лекция Металлы 1. Общая характеристика металлов. 2. Способы получения металлов. 3. Химические свойства металлов. 4. Биологическая роль металлов. Лектор: Ирина Викторовна Ганзина кандидат биологических наук, доцент кафедры химии
 Металлы (от лат. metallum — шахта, рудник) — группа элементов, обладающая характерными металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск. Металлы — один из самых распространённых материалов, используемых цивилизацией на протяжении практически всей её истории.
Металлы (от лат. metallum — шахта, рудник) — группа элементов, обладающая характерными металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск. Металлы — один из самых распространённых материалов, используемых цивилизацией на протяжении практически всей её истории.
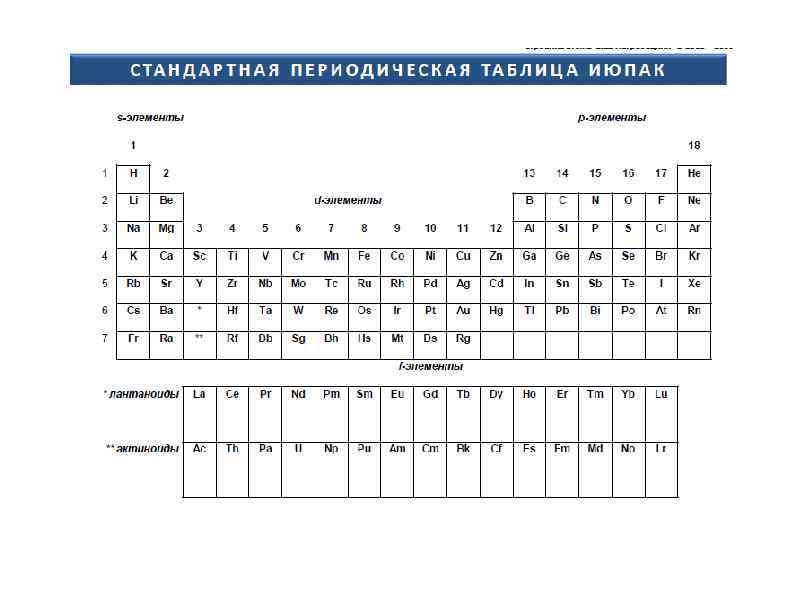
 Положение металлов в периодической системе Из элементов групп А ( главных групп ) металлами являются все элементы групп IA ( кроме водорода ) и IIА, а также часть элементов групп IIIА – VIА, расположенных ниже условленной границы от бора к астату. Это s-элементы I и II групп, p-элементы главных подгрупп ниже диагонали Be - At и все d и f элементы. К металлам относятся все элементы групп В периодической системы. Металлы в ПС составляют 80% от всех элементов.
Положение металлов в периодической системе Из элементов групп А ( главных групп ) металлами являются все элементы групп IA ( кроме водорода ) и IIА, а также часть элементов групп IIIА – VIА, расположенных ниже условленной границы от бора к астату. Это s-элементы I и II групп, p-элементы главных подгрупп ниже диагонали Be - At и все d и f элементы. К металлам относятся все элементы групп В периодической системы. Металлы в ПС составляют 80% от всех элементов.
 Периодическая система Д. И. Менделеева
Периодическая система Д. И. Менделеева
 ОСОБЕННОСТИ СТРОЕНИЯ АТОМОВ МЕТАЛЛОВ 1. На внешнем энергетическом уровне у большинства металлов 1 или 2 электрона (исключение составляют Ge, Sn, Pb – 4 электрона, Bi – 5 электронов и Ро – 6 электронов). 2. Атомы металлов имеют большое число свободных валентных орбиталей и могут являться акцепторами электронов при образовании химических связей. 2. Валентными могут быть электроны как внешнего, так и предвнешнего уровней ( число валентных электронов равно номеру группы).
ОСОБЕННОСТИ СТРОЕНИЯ АТОМОВ МЕТАЛЛОВ 1. На внешнем энергетическом уровне у большинства металлов 1 или 2 электрона (исключение составляют Ge, Sn, Pb – 4 электрона, Bi – 5 электронов и Ро – 6 электронов). 2. Атомы металлов имеют большое число свободных валентных орбиталей и могут являться акцепторами электронов при образовании химических связей. 2. Валентными могут быть электроны как внешнего, так и предвнешнего уровней ( число валентных электронов равно номеру группы).
 МЕТАЛЛЫ В ПРИРОДЕ Многие металлы широко распространены в природе. В земной коре следующее содержание некоторых металлов: алюминия — 8, 2% железа — 4, 1% кальция — 4, 1% натрия — 2, 3% магния — 2, 3% калия - 2, 1 % титана — 0, 56% Большое количество натрия и магния содержится в морской воде: — 1, 05%, — 0, 12%.
МЕТАЛЛЫ В ПРИРОДЕ Многие металлы широко распространены в природе. В земной коре следующее содержание некоторых металлов: алюминия — 8, 2% железа — 4, 1% кальция — 4, 1% натрия — 2, 3% магния — 2, 3% калия - 2, 1 % титана — 0, 56% Большое количество натрия и магния содержится в морской воде: — 1, 05%, — 0, 12%.
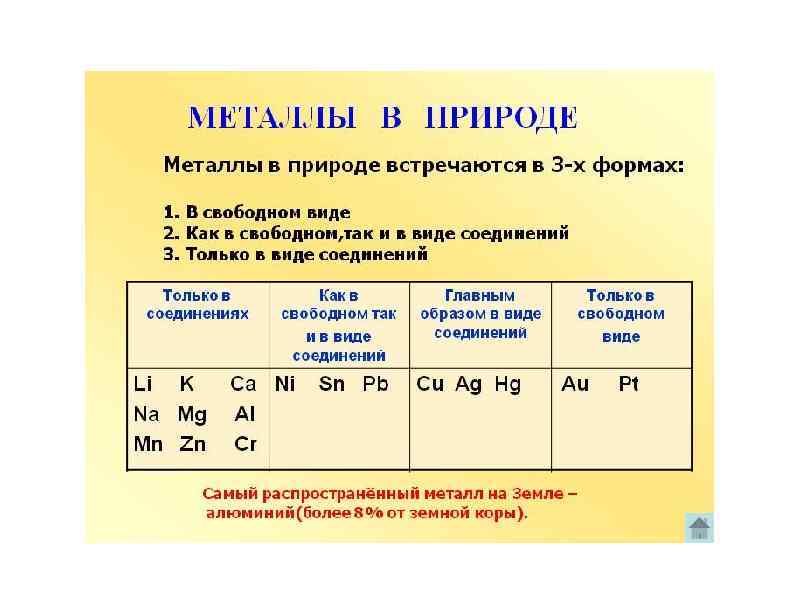
 В природе металлы встречаются в различном виде: • в самородном состоянии: серебро , золото , платина , медь , иногда ртуть • в виде оксидов: магнетит Fe 3 O 4, гематит Fe 2 О 3 и др. • в виде смешанных оксидов: каолин Аl 2 O 3 • 2 Si. O 2 • 2 Н 2 О, алунит (Na, K)2 O • Аl. О 3 • 2 Si. O 2 и др.
В природе металлы встречаются в различном виде: • в самородном состоянии: серебро , золото , платина , медь , иногда ртуть • в виде оксидов: магнетит Fe 3 O 4, гематит Fe 2 О 3 и др. • в виде смешанных оксидов: каолин Аl 2 O 3 • 2 Si. O 2 • 2 Н 2 О, алунит (Na, K)2 O • Аl. О 3 • 2 Si. O 2 и др.
 В виде различных солей: ü карбонатов: мел, мрамор Са. СО 3, магнезит Мg. СО 3. ü сульфидов: галенит Pb. S, киноварь Нg. S, ü хлоридов: сильвин КСl, галит Na. Cl, сильвинит КСl • Nа. Сl, карналлит КСl • Мg. Сl 2 • 6 Н 2 О ü сульфатов: барит Ва. SO 4 ü фосфатов: апатит Са 3(РО 4)2 Источник получения металлов – руды. Состоят обычно из нескольких металлов – полиметаллические (медноцинковые, свинцовосеребрянные).
В виде различных солей: ü карбонатов: мел, мрамор Са. СО 3, магнезит Мg. СО 3. ü сульфидов: галенит Pb. S, киноварь Нg. S, ü хлоридов: сильвин КСl, галит Na. Cl, сильвинит КСl • Nа. Сl, карналлит КСl • Мg. Сl 2 • 6 Н 2 О ü сульфатов: барит Ва. SO 4 ü фосфатов: апатит Са 3(РО 4)2 Источник получения металлов – руды. Состоят обычно из нескольких металлов – полиметаллические (медноцинковые, свинцовосеребрянные).
 В технике металлы делятся на: • Черные (Fe и его сплавы, Mn, Cr) • Драгоценные (Au, Ag, Pt, Ir, Os, Pd) • Редкие (Ti, Ge, Zr, La, In, Be, Mo, V) • Остальные металлы (включая Mg и Al) – цветные. Делятся на легкие: Ca, Al, Mg и тяжелые: Cu, Pb, Sn, Zn и др. Кроме того различают: • Щелочные (Li, Na, K, Rb, Cs) • Щелочно-земельные (Ca, Sr, Ba)
В технике металлы делятся на: • Черные (Fe и его сплавы, Mn, Cr) • Драгоценные (Au, Ag, Pt, Ir, Os, Pd) • Редкие (Ti, Ge, Zr, La, In, Be, Mo, V) • Остальные металлы (включая Mg и Al) – цветные. Делятся на легкие: Ca, Al, Mg и тяжелые: Cu, Pb, Sn, Zn и др. Кроме того различают: • Щелочные (Li, Na, K, Rb, Cs) • Щелочно-земельные (Ca, Sr, Ba)
 Большинство металлов встречается в природе в виде различных соединений, только наименее активные металлы встречаются в природе в самородном, свободном состоянии. Получить металлы из соединений можно, применяя различные металлургические процессы, причем любой из них сводится к восстановлению ионов металла с помощью восстановителей. В зависимости от способа проведения металлургического процесса различают пирометаллургию, гидрометаллургию и электрометаллургию.
Большинство металлов встречается в природе в виде различных соединений, только наименее активные металлы встречаются в природе в самородном, свободном состоянии. Получить металлы из соединений можно, применяя различные металлургические процессы, причем любой из них сводится к восстановлению ионов металла с помощью восстановителей. В зависимости от способа проведения металлургического процесса различают пирометаллургию, гидрометаллургию и электрометаллургию.
 Способы получения металлов 1. Пирометаллургия - восстановление металлов из руд при высоких температурах с помощью восстановителей Пирометаллургия в зависимости от восстановителя делится на виды: а) карботермия (восстановители C или CO) Cu 2 O + C = 2 Cu + CO Cu 2 O + CO = 2 Cu + CO 2 б) металлотермия ( восстановители металлы, например алюминотермия, магнийтермия) Fe 2 O 3 + 2 Al = Al 2 O 3 + 2 Fe в) водородотермия Cu. O + H 2 = Cu + H 2 O
Способы получения металлов 1. Пирометаллургия - восстановление металлов из руд при высоких температурах с помощью восстановителей Пирометаллургия в зависимости от восстановителя делится на виды: а) карботермия (восстановители C или CO) Cu 2 O + C = 2 Cu + CO Cu 2 O + CO = 2 Cu + CO 2 б) металлотермия ( восстановители металлы, например алюминотермия, магнийтермия) Fe 2 O 3 + 2 Al = Al 2 O 3 + 2 Fe в) водородотермия Cu. O + H 2 = Cu + H 2 O
 2. Гидрометаллургия – способ получения металлов из растворов солей. Оксид металла растворяют в кислоте, получают электролит. Затем металл восстанавливают или выделяют электролизом Cu. O + H 2 SО 4 = Cu. SО 4 + H 2 O Cu. SО 4 + Fe = Cu + Fe. SО 4 Таким образом получают Au, Ag, Zn, Cd.
2. Гидрометаллургия – способ получения металлов из растворов солей. Оксид металла растворяют в кислоте, получают электролит. Затем металл восстанавливают или выделяют электролизом Cu. O + H 2 SО 4 = Cu. SО 4 + H 2 O Cu. SО 4 + Fe = Cu + Fe. SО 4 Таким образом получают Au, Ag, Zn, Cd.
 3. Электрометаллургия – способ получения металлов путем восстановления их из различных оксидов, щелочей или хлоридов с помощью электрического тока. Так получают очень чистые Na, Al, Mg, щелочноземельные металлы электролизом расплавов природных соединений. Для получения металлов высокой степени чистоты из очищаемого металла изготавливают анод. При электролизе он растворяется, ионы металла переходят в раствор, а на катоде они восстанавливаются и осаждаются на нем. Электролитически чистые металлы: Cu, Ag, Ni, Pb, Fe.
3. Электрометаллургия – способ получения металлов путем восстановления их из различных оксидов, щелочей или хлоридов с помощью электрического тока. Так получают очень чистые Na, Al, Mg, щелочноземельные металлы электролизом расплавов природных соединений. Для получения металлов высокой степени чистоты из очищаемого металла изготавливают анод. При электролизе он растворяется, ионы металла переходят в раствор, а на катоде они восстанавливаются и осаждаются на нем. Электролитически чистые металлы: Cu, Ag, Ni, Pb, Fe.
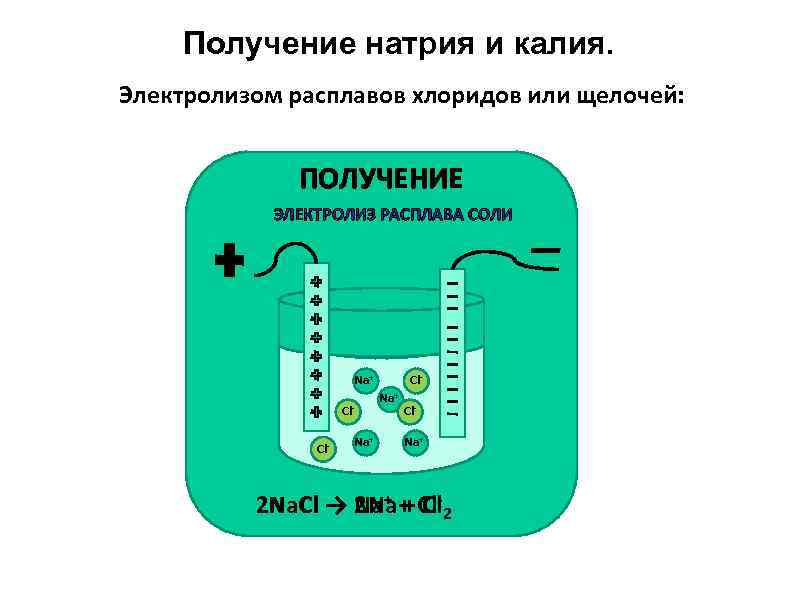 Получение натрия и калия. Электролизом расплавов хлоридов или щелочей: ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗ РАСПЛАВА СОЛИ Na+ Cl. Cl- Na+ Cl. Na+ 2 Na. Cl → 2 Na + Cl-2 Na. Cl → Na+ + Cl
Получение натрия и калия. Электролизом расплавов хлоридов или щелочей: ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗ РАСПЛАВА СОЛИ Na+ Cl. Cl- Na+ Cl. Na+ 2 Na. Cl → 2 Na + Cl-2 Na. Cl → Na+ + Cl
 Физические свойства металлов Для металлов наиболее характерны следующие свойства: • металлический блеск, • твердость, • пластичность, • ковкость • хорошая проводимость тепла и электричества.
Физические свойства металлов Для металлов наиболее характерны следующие свойства: • металлический блеск, • твердость, • пластичность, • ковкость • хорошая проводимость тепла и электричества.
 Металлический блеск – способность отражать свет. Наблюдается, если металл в куске. В раздробленном состоянии (кроме Mg и Al) металлы представляют собой порошки черного или темно- серого цвета. Чем меньше поглощают света, тем ярче блеск. Поэтому серебро Ag и палладий Pd можно использовать для изготовления зеркал. На свойстве металлов полностью отражать радиоволны основана радиолокация.
Металлический блеск – способность отражать свет. Наблюдается, если металл в куске. В раздробленном состоянии (кроме Mg и Al) металлы представляют собой порошки черного или темно- серого цвета. Чем меньше поглощают света, тем ярче блеск. Поэтому серебро Ag и палладий Pd можно использовать для изготовления зеркал. На свойстве металлов полностью отражать радиоволны основана радиолокация.
 Твердое агрегатное состояние (кроме Hg) – обусловлено прочностью пространственной кристаллической металлической решетки. Cr – по твердости приближается к алмазу, но при этом Na, K – легко режутся ножом
Твердое агрегатное состояние (кроме Hg) – обусловлено прочностью пространственной кристаллической металлической решетки. Cr – по твердости приближается к алмазу, но при этом Na, K – легко режутся ножом
 Электрическая проводимость – способность проводить электрический ток. Лучшие проводники электричества являются Ag и Cu, худшие Hg и Pb. При нагревании электрическая проводимость падает, при охлаждении растет. Около абсолютного 0 наблюдается эффект сверхпроводимости металлов. Теплопроводность- наибольшей теплопроводностью обладают металлы с наилучшей электрической проводимостью.
Электрическая проводимость – способность проводить электрический ток. Лучшие проводники электричества являются Ag и Cu, худшие Hg и Pb. При нагревании электрическая проводимость падает, при охлаждении растет. Около абсолютного 0 наблюдается эффект сверхпроводимости металлов. Теплопроводность- наибольшей теплопроводностью обладают металлы с наилучшей электрической проводимостью.
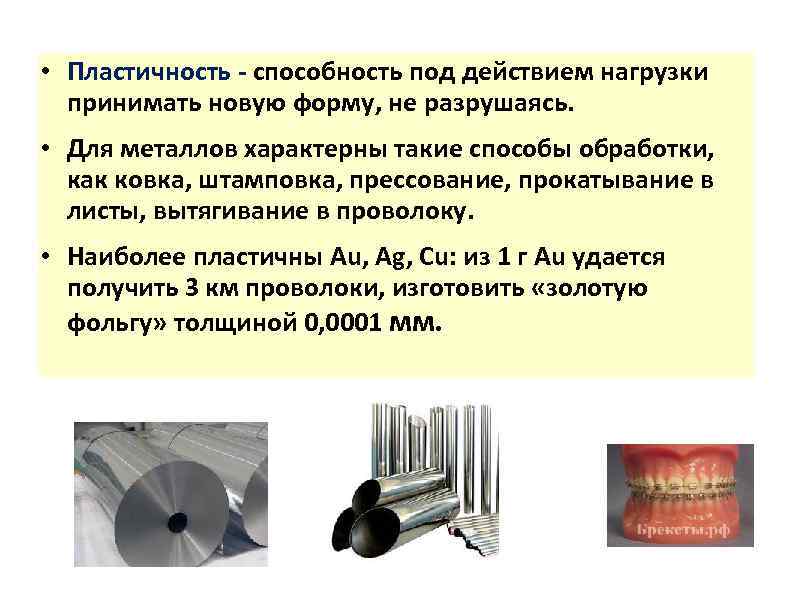 • Пластичность - способность под действием нагрузки принимать новую форму, не разрушаясь. • Для металлов характерны такие способы обработки, как ковка, штамповка, прессование, прокатывание в листы, вытягивание в проволоку. • Наиболее пластичны Au, Ag, Cu: из 1 г Au удается получить 3 км проволоки, изготовить «золотую фольгу» толщиной 0, 0001 мм.
• Пластичность - способность под действием нагрузки принимать новую форму, не разрушаясь. • Для металлов характерны такие способы обработки, как ковка, штамповка, прессование, прокатывание в листы, вытягивание в проволоку. • Наиболее пластичны Au, Ag, Cu: из 1 г Au удается получить 3 км проволоки, изготовить «золотую фольгу» толщиной 0, 0001 мм.
 Плотность металлов. По плотности металлы подразделяются на: Легкие металлы (ρ < 5 г/см 3) обычно легкоплавкие. Например, Cs плавится при 280˚С. Тяжелые металлы (ρ > 5 г/см 3) тугоплавкие. Температура плавления W 3380 ˚C. Самый легкий из металлов Li (ρ=0, 53 г/см 3) Самый тяжелый - Os (ρ=22, 48 г/см 3)
Плотность металлов. По плотности металлы подразделяются на: Легкие металлы (ρ < 5 г/см 3) обычно легкоплавкие. Например, Cs плавится при 280˚С. Тяжелые металлы (ρ > 5 г/см 3) тугоплавкие. Температура плавления W 3380 ˚C. Самый легкий из металлов Li (ρ=0, 53 г/см 3) Самый тяжелый - Os (ρ=22, 48 г/см 3)
 Температура кипения. Металлы имеют очень высокие температуры кипения. Например, K 760 ˚C, Cu 2300 ˚C, Fe 3000 ˚C, W 5900 ˚C. В парообразном состоянии металлы одноатомны. Полиморфизм. Это свойство металлов принимать различные кристаллические формы в твердом состоянии. Эти формы имеют разные физические и химические свойства. Обозначается полиморфная структура греческими буквами: α , β, γ … Например, Co существует в α- и β- модификациях; Fe существует в α-, β-, γ- модификациях.
Температура кипения. Металлы имеют очень высокие температуры кипения. Например, K 760 ˚C, Cu 2300 ˚C, Fe 3000 ˚C, W 5900 ˚C. В парообразном состоянии металлы одноатомны. Полиморфизм. Это свойство металлов принимать различные кристаллические формы в твердом состоянии. Эти формы имеют разные физические и химические свойства. Обозначается полиморфная структура греческими буквами: α , β, γ … Например, Co существует в α- и β- модификациях; Fe существует в α-, β-, γ- модификациях.
 ОСОБЕННОСТИ НЕКОТОРЫХ МЕТАЛЛОВ Ag Pt – самые блестящие Ag Cu Au Al – лучшие проводники Аu – лучший по ковкости и пластичности Os – самый тяжёлый ( 22. 48 г/мл) Li – самый лёгкий (0. 52 г/мл) Hg – самый легкоплавкий (Тпл = -38. 87 °С) W – cамый тугоплавкий (3370 °С) К – самый мягкий Cr – самый твёрдый
ОСОБЕННОСТИ НЕКОТОРЫХ МЕТАЛЛОВ Ag Pt – самые блестящие Ag Cu Au Al – лучшие проводники Аu – лучший по ковкости и пластичности Os – самый тяжёлый ( 22. 48 г/мл) Li – самый лёгкий (0. 52 г/мл) Hg – самый легкоплавкий (Тпл = -38. 87 °С) W – cамый тугоплавкий (3370 °С) К – самый мягкий Cr – самый твёрдый
 Строение металлической кристаллической решетки В узлах пространственной кристаллической решетки металла расположены атомы и положительные ионы, а между ними перемещаются свободные электроны – «электронный газ» . Переходя от одного положительного иона к другому, они как бы осуществляют связь между ионами и превращают кристаллы металла в единое целое.
Строение металлической кристаллической решетки В узлах пространственной кристаллической решетки металла расположены атомы и положительные ионы, а между ними перемещаются свободные электроны – «электронный газ» . Переходя от одного положительного иона к другому, они как бы осуществляют связь между ионами и превращают кристаллы металла в единое целое.
 Для металлов характерны кристаллические решетки, в которых каждый ион окружен 8 -12 другими ионами, т. е. с большим координационным числом. Если в кристалле одного металла ион имеет координационное число 12, а в кристалле другого – только 10, то структура 1 -го более компактна, чем 2 -ого.
Для металлов характерны кристаллические решетки, в которых каждый ион окружен 8 -12 другими ионами, т. е. с большим координационным числом. Если в кристалле одного металла ион имеет координационное число 12, а в кристалле другого – только 10, то структура 1 -го более компактна, чем 2 -ого.
 Основные типы кристаллических металлических решеток Объемно-центрированная кубическая: α – Fe, Na, K, α – Cr и др.
Основные типы кристаллических металлических решеток Объемно-центрированная кубическая: α – Fe, Na, K, α – Cr и др.
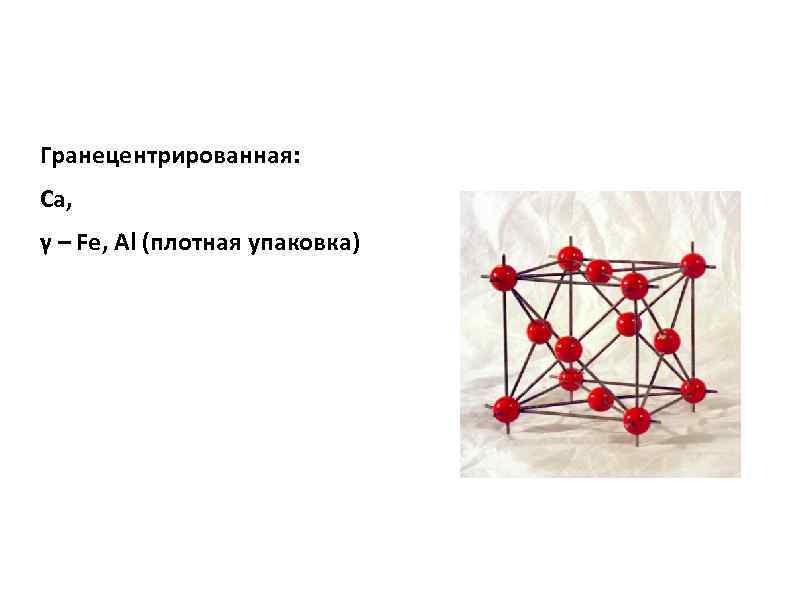 Гранецентрированная: Ca, γ – Fe, Al (плотная упаковка)
Гранецентрированная: Ca, γ – Fe, Al (плотная упаковка)
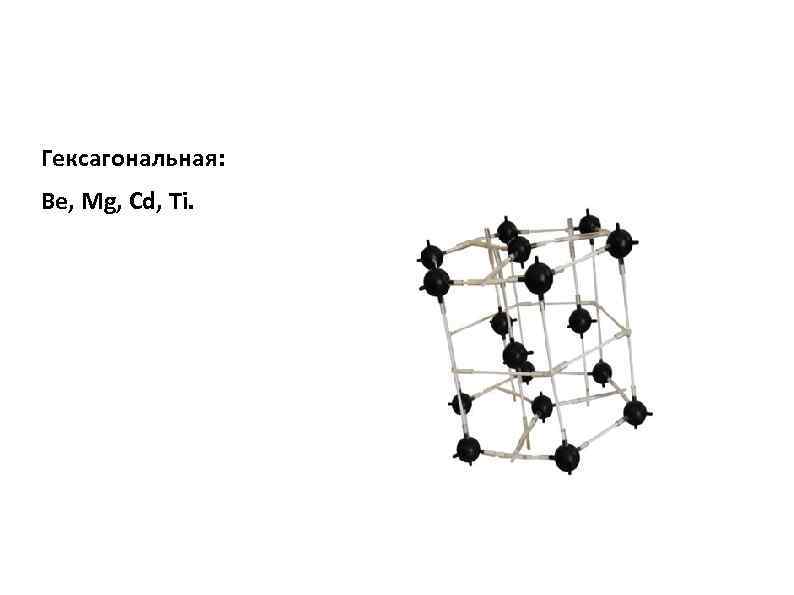 Гексагональная: Be, Mg, Cd, Ti.
Гексагональная: Be, Mg, Cd, Ti.
 Химические свойства металлов По степени химической активности металлы располагаются в ряд напряжений (электрохимический ряд напряжений): Li, K, Ba, Ca, Na, Mg, Al, Be, Mn, Zn, Cr, Fe, Co, Ni, Sn, Pb, H 2, Cu, Hg, Ag, Pt, Au Уменьшается активность металлов, т. е. их восстановительные свойства
Химические свойства металлов По степени химической активности металлы располагаются в ряд напряжений (электрохимический ряд напряжений): Li, K, Ba, Ca, Na, Mg, Al, Be, Mn, Zn, Cr, Fe, Co, Ni, Sn, Pb, H 2, Cu, Hg, Ag, Pt, Au Уменьшается активность металлов, т. е. их восстановительные свойства
 В ряду напряжений металлы располагаются в порядке возрастания напряжения, создаваемого гальваническим элементом, в котором один из электродов все время остается постоянным (стандартный электрод), а другой изготавливают из того металла, положение которого в ряду напряжений хотят определить. В качестве стандартного электрода применяют так называемый водородный электрод, представляющий собой платиновую (Pt) пластинку, опущенную в кислый раствор, через который непрерывно пропускают газообразный водород при давлении 1 атм.
В ряду напряжений металлы располагаются в порядке возрастания напряжения, создаваемого гальваническим элементом, в котором один из электродов все время остается постоянным (стандартный электрод), а другой изготавливают из того металла, положение которого в ряду напряжений хотят определить. В качестве стандартного электрода применяют так называемый водородный электрод, представляющий собой платиновую (Pt) пластинку, опущенную в кислый раствор, через который непрерывно пропускают газообразный водород при давлении 1 атм.
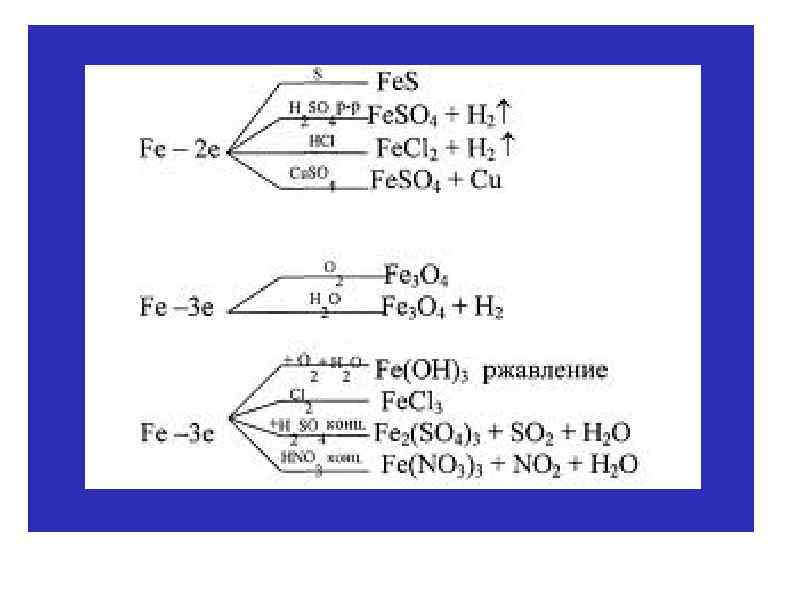
 На внешнем электронном уровне у большинства металлов небольшое количество электронов (1 -3), поэтому они в большинстве реакций выступают как восстановители (то есть «отдают» свои электроны). ( 1. Реакции с простыми веществами а) С кислородом реагируют все металлы, кроме золота, С кислородом платины. Реакция с серебром происходит при высоких температурах, но оксид серебра(II) практически не образуется, так как он термически неустойчив. В зависимости от металла на выходе могут оказаться оксиды, пероксиды, надпероксиды:
На внешнем электронном уровне у большинства металлов небольшое количество электронов (1 -3), поэтому они в большинстве реакций выступают как восстановители (то есть «отдают» свои электроны). ( 1. Реакции с простыми веществами а) С кислородом реагируют все металлы, кроме золота, С кислородом платины. Реакция с серебром происходит при высоких температурах, но оксид серебра(II) практически не образуется, так как он термически неустойчив. В зависимости от металла на выходе могут оказаться оксиды, пероксиды, надпероксиды:
 4 Li + O 2 = 2 Li 2 O оксид лития 2 Na + O 2 = Na 2 O 2 пероксид натрия K + O 2 = KO 2 надпероксид калия Чтобы получить из пероксида оксид, пероксид восстанавливают металлом: Na 2 O 2 + 2 Na = 2 Na 2 O Со средними и малоактивными металлами реакция происходит при нагревании: 3 Fe + 2 O 2 = Fe 3 O 4 2 Hg + O 2 = 2 Hg. O 2 Cu + O 2 = 2 Cu. O
4 Li + O 2 = 2 Li 2 O оксид лития 2 Na + O 2 = Na 2 O 2 пероксид натрия K + O 2 = KO 2 надпероксид калия Чтобы получить из пероксида оксид, пероксид восстанавливают металлом: Na 2 O 2 + 2 Na = 2 Na 2 O Со средними и малоактивными металлами реакция происходит при нагревании: 3 Fe + 2 O 2 = Fe 3 O 4 2 Hg + O 2 = 2 Hg. O 2 Cu + O 2 = 2 Cu. O
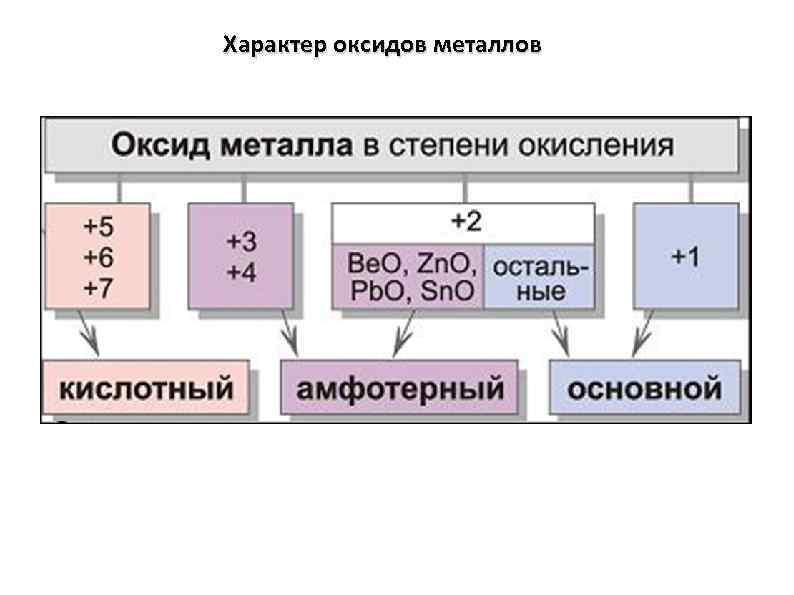 Характер оксидов металлов
Характер оксидов металлов
 б) С азотом реагируют только самые активные металлы, С азотом при комнатной температуре взаимодействует только литий, образуя нитриды: 6 Li + N 2 = 2 Li 3 N При нагревании: 2 AL + N 2 = 2 Al. N 3 Ca + N 2 = Ca 3 N 2 в) С серой реагируют все металлы, кроме золота и С серой платины. Железо взаимодействует с серой при нагревании, образуя сульфид: Fe + S = Fe. S
б) С азотом реагируют только самые активные металлы, С азотом при комнатной температуре взаимодействует только литий, образуя нитриды: 6 Li + N 2 = 2 Li 3 N При нагревании: 2 AL + N 2 = 2 Al. N 3 Ca + N 2 = Ca 3 N 2 в) С серой реагируют все металлы, кроме золота и С серой платины. Железо взаимодействует с серой при нагревании, образуя сульфид: Fe + S = Fe. S
 г) С водородом реагируют только самые активные С водородом металлы, то есть металлы IA и IIA групп кроме Be. Реакции осуществляются при нагревании, при этом образуются гидриды. В реакциях металл выступает как восстановитель, степень окисления водорода в гидридах − 1: 2 Na + H 2 = 2 Na. H Mg + H 2 = Mg. H 2
г) С водородом реагируют только самые активные С водородом металлы, то есть металлы IA и IIA групп кроме Be. Реакции осуществляются при нагревании, при этом образуются гидриды. В реакциях металл выступает как восстановитель, степень окисления водорода в гидридах − 1: 2 Na + H 2 = 2 Na. H Mg + H 2 = Mg. H 2
 д) С углеродом реагируют только наиболее активные С углеродом металлы. При этом образуются карбиды. Среди них выделяют ацетилениды и метаниды. Ацетилениды при взаимодействии с водой дают ацетилен, метаниды — метан. 2 Na + 2 C = Na 2 C 2 + 2 H 2 O = 2 Na. OH + C 2 H 2 Са. C 2 + 2 H 2 O = Сa(OH)2 + C 2 H 2 Al 4 C 3 + 12 H 2 O = 4 Al(OH)3↓ + 3 CH 4↑
д) С углеродом реагируют только наиболее активные С углеродом металлы. При этом образуются карбиды. Среди них выделяют ацетилениды и метаниды. Ацетилениды при взаимодействии с водой дают ацетилен, метаниды — метан. 2 Na + 2 C = Na 2 C 2 + 2 H 2 O = 2 Na. OH + C 2 H 2 Са. C 2 + 2 H 2 O = Сa(OH)2 + C 2 H 2 Al 4 C 3 + 12 H 2 O = 4 Al(OH)3↓ + 3 CH 4↑
 2. Реакции с кислотами. а) Металлы, стоящие до водорода в электрохимическом ряду напряжений вытесняют H 2 из HCl, разбавленной H 2 SO 4 и других типичных кислот: Zn + 2 HCl = Zn. Cl 2 + H 2
2. Реакции с кислотами. а) Металлы, стоящие до водорода в электрохимическом ряду напряжений вытесняют H 2 из HCl, разбавленной H 2 SO 4 и других типичных кислот: Zn + 2 HCl = Zn. Cl 2 + H 2
 б) Концентрированная серная кислота в реакциях с металлами не выделяет водород. H 2 SO 4 конц. является окислителем за счет S+6 , поэтому при взаимодействии с металлами разной активности образуются продукты: акт. металлы - Н 2 S-2 H 2 SO 4 конц. неакт. металлы - S+4 О 2 пассивирует AI, Cr, Fe
б) Концентрированная серная кислота в реакциях с металлами не выделяет водород. H 2 SO 4 конц. является окислителем за счет S+6 , поэтому при взаимодействии с металлами разной активности образуются продукты: акт. металлы - Н 2 S-2 H 2 SO 4 конц. неакт. металлы - S+4 О 2 пассивирует AI, Cr, Fe
 Cu + 2 H 2 SO 4 конц. → Cu. SO 4 + SO 2+ 2 H 2 O 4 Cа + 5 H 2 SO 4 конц. → 4 Cа. SO 4 + Н 2 S + 4 H 2 O
Cu + 2 H 2 SO 4 конц. → Cu. SO 4 + SO 2+ 2 H 2 O 4 Cа + 5 H 2 SO 4 конц. → 4 Cа. SO 4 + Н 2 S + 4 H 2 O
 в) Взаимодействие азотной кислоты с металлами 1. Ни один металл никогда не выделяет из азотной кислоты водород. Выделяются разнообразные соединения азота: N+4 O 2, N+2 O, N 2+1 O, N 20, N– 3 H 3 (NH 4 NO 3) 2. С азотной кислотой реагируют металлы, стоящие до и после водорода в ряду активности. 3. Азотная кислота не взаимодействует с Au, Pt 4. Концентрированная азотная кислота пассивирует металлы: Al, Fe, Be, Cr, Ni, Pb (за счет образования плотной оксидной пленки). При нагревании и при разбавлении азотной кислоты данные металлы в ней растворяются.
в) Взаимодействие азотной кислоты с металлами 1. Ни один металл никогда не выделяет из азотной кислоты водород. Выделяются разнообразные соединения азота: N+4 O 2, N+2 O, N 2+1 O, N 20, N– 3 H 3 (NH 4 NO 3) 2. С азотной кислотой реагируют металлы, стоящие до и после водорода в ряду активности. 3. Азотная кислота не взаимодействует с Au, Pt 4. Концентрированная азотная кислота пассивирует металлы: Al, Fe, Be, Cr, Ni, Pb (за счет образования плотной оксидной пленки). При нагревании и при разбавлении азотной кислоты данные металлы в ней растворяются.
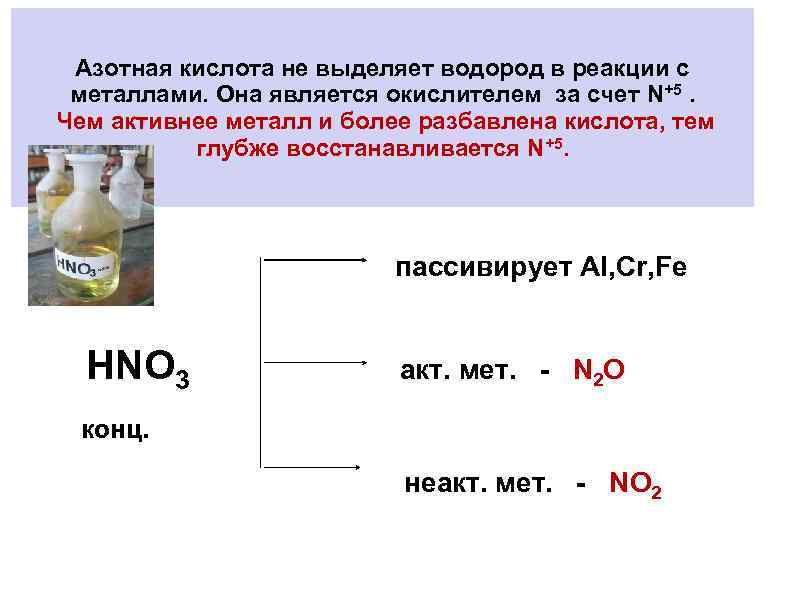 Азотная кислота не выделяет водород в реакции с металлами. Она является окислителем за счет N+5. Чем активнее металл и более разбавлена кислота, тем глубже восстанавливается N+5. пассивирует AI, Cr, Fe НNO 3 акт. мет. N 2 О конц. неакт. мет. NО 2
Азотная кислота не выделяет водород в реакции с металлами. Она является окислителем за счет N+5. Чем активнее металл и более разбавлена кислота, тем глубже восстанавливается N+5. пассивирует AI, Cr, Fe НNO 3 акт. мет. N 2 О конц. неакт. мет. NО 2
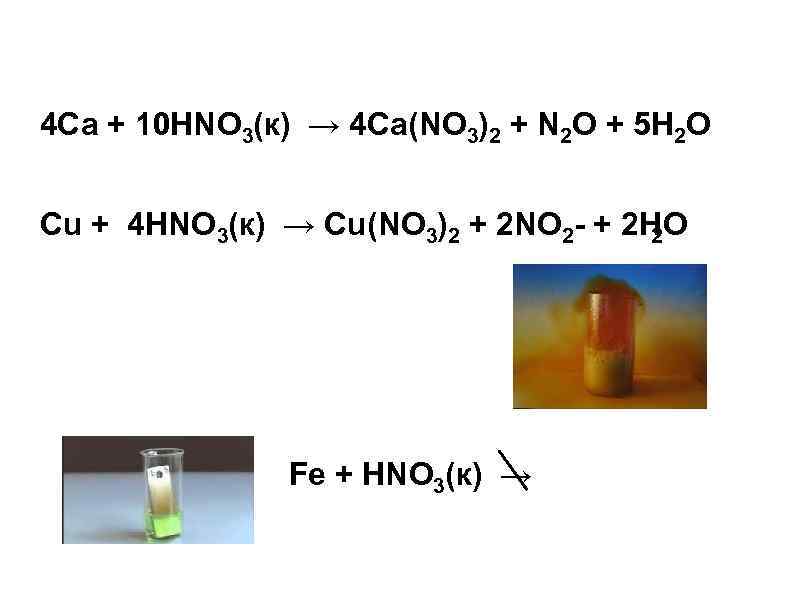 4 Cа + 10 HNO 3(к) → 4 Cа(NO 3)2 + N 2 O + 5 H 2 O Cu + 4 HNO 3(к) → Cu(NO 3)2 + 2 NO 2 + 2 H O 2 Fe + HNO 3(к) →
4 Cа + 10 HNO 3(к) → 4 Cа(NO 3)2 + N 2 O + 5 H 2 O Cu + 4 HNO 3(к) → Cu(NO 3)2 + 2 NO 2 + 2 H O 2 Fe + HNO 3(к) →
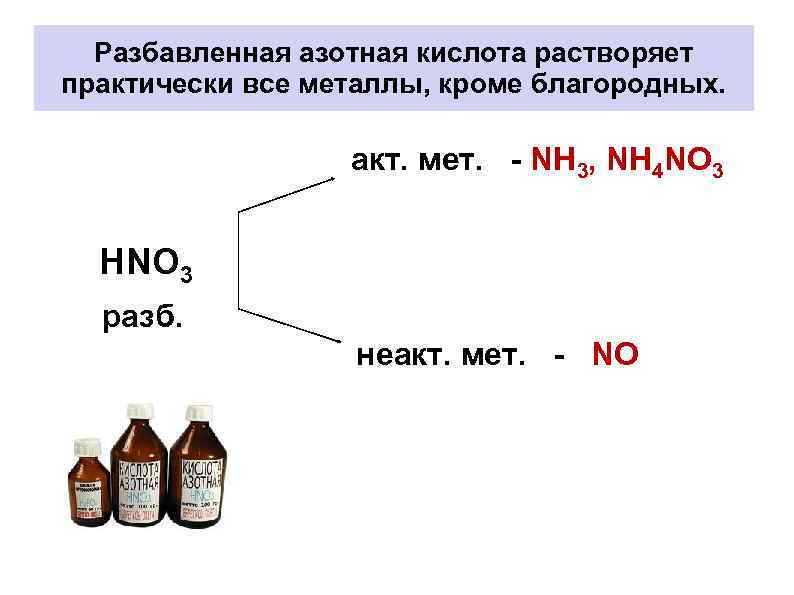 Разбавленная азотная кислота растворяет практически все металлы, кроме благородных. акт. мет. NН 3, NН 4 NО 3 НNO 3 разб. неакт. мет. NО
Разбавленная азотная кислота растворяет практически все металлы, кроме благородных. акт. мет. NН 3, NН 4 NО 3 НNO 3 разб. неакт. мет. NО
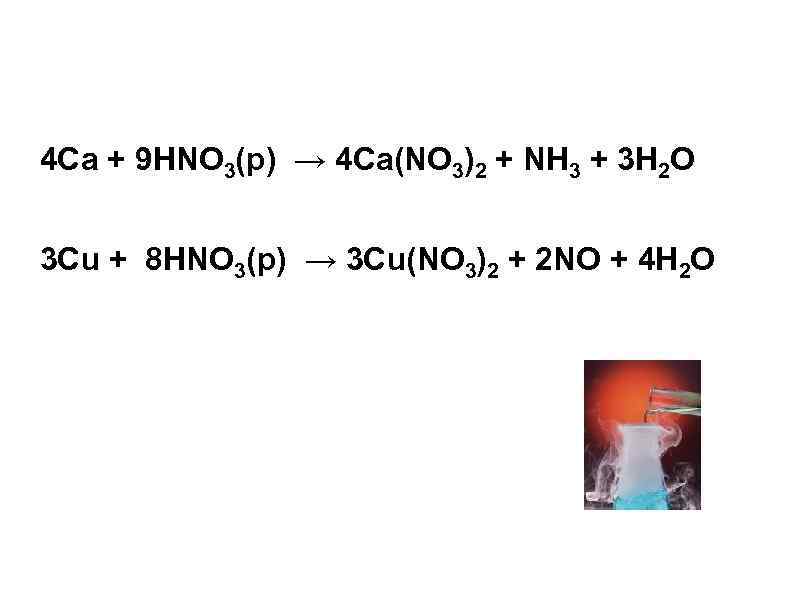 4 Cа + 9 HNO 3(р) → 4 Cа(NO 3)2 + NН 3 + 3 H 2 O 3 Cu + 8 HNO 3(р) → 3 Cu(NO 3)2 + 2 NO + 4 H 2 O
4 Cа + 9 HNO 3(р) → 4 Cа(NO 3)2 + NН 3 + 3 H 2 O 3 Cu + 8 HNO 3(р) → 3 Cu(NO 3)2 + 2 NO + 4 H 2 O
 3. С растворами солей Левее стоящий металл вытесняет из раствора соли металлы, расположенные правее в электрохимическом ряду напряжений Fe + Cu. SO 4 = Fe. SO 4 + Cu (исключение составляет Pb. SO 4 – более активный металл из раствора соли свинец не вытесняет) Не следует писать химические уравнения щелочных металлов с растворами кислот и растворами солей, так как при этом они сами взаимодействуют с водой.
3. С растворами солей Левее стоящий металл вытесняет из раствора соли металлы, расположенные правее в электрохимическом ряду напряжений Fe + Cu. SO 4 = Fe. SO 4 + Cu (исключение составляет Pb. SO 4 – более активный металл из раствора соли свинец не вытесняет) Не следует писать химические уравнения щелочных металлов с растворами кислот и растворами солей, так как при этом они сами взаимодействуют с водой.
 4. С водой при обычных условиях реагируют металлы, стоящие до магния в ряду активности металлов. Некоторые металлы средней активности реагируют при нагревании или с участием кислорода.
4. С водой при обычных условиях реагируют металлы, стоящие до магния в ряду активности металлов. Некоторые металлы средней активности реагируют при нагревании или с участием кислорода.
 5. Со щелочами металлы не взаимодействуют, за исключением переходных металлов –AI, Zn, Ве, Тi оксиды и гидроксиды которых имеют выраженный амфотерный характер. Алюминий легко растворяется в едкой щёлочи с образованием хорошо растворимого комплекса — тетрагидроксиалюмината натрия и водорода: 2 АI 0 + 2 Na. OH + 6 H 2 O → 3 H 2↑ + 2 Na[Al(OH)4] 2 Al 0 + 2 Na+ + 2 OH− + 6 H 2 O→ 3 H 2↑ +2 Na++ 2[Al 3+(OH)− 4]−
5. Со щелочами металлы не взаимодействуют, за исключением переходных металлов –AI, Zn, Ве, Тi оксиды и гидроксиды которых имеют выраженный амфотерный характер. Алюминий легко растворяется в едкой щёлочи с образованием хорошо растворимого комплекса — тетрагидроксиалюмината натрия и водорода: 2 АI 0 + 2 Na. OH + 6 H 2 O → 3 H 2↑ + 2 Na[Al(OH)4] 2 Al 0 + 2 Na+ + 2 OH− + 6 H 2 O→ 3 H 2↑ +2 Na++ 2[Al 3+(OH)− 4]−
 Использование важнейших металлов и сплавов На протяжении тысячелетий человек использовал металлы и сплавы. Об этом свидетельствуют раскопки археологов. Вначале человек использовал изделия из серебра и золота. Когда люди научились выплавлять медь и изготавливать из неё изделия, наступил «медный век» . «Медный век» сменился «бронзовым» , а затем «железным» . Конец XVIII и начало XIX в. в. можно смело называть эпохой стали.
Использование важнейших металлов и сплавов На протяжении тысячелетий человек использовал металлы и сплавы. Об этом свидетельствуют раскопки археологов. Вначале человек использовал изделия из серебра и золота. Когда люди научились выплавлять медь и изготавливать из неё изделия, наступил «медный век» . «Медный век» сменился «бронзовым» , а затем «железным» . Конец XVIII и начало XIX в. в. можно смело называть эпохой стали.
 В настоящее время из-за высокой химической стойкости благородные металлы используют для изготовления элементов аппаратуры и приборов, которые предназначены для работы в агрессивных средах. Ещё в древности люди заметили, что вода, находящаяся в серебряных сосудах, не портится при хранении, способствует заживлению ран.
В настоящее время из-за высокой химической стойкости благородные металлы используют для изготовления элементов аппаратуры и приборов, которые предназначены для работы в агрессивных средах. Ещё в древности люди заметили, что вода, находящаяся в серебряных сосудах, не портится при хранении, способствует заживлению ран.
 • Из меди делают проволоку и токопроводящие детали аппаратуры, инструменты для работы во взрывных и пожарных цехах, её широко используют в химическом машиностроении. Бронза Латунь
• Из меди делают проволоку и токопроводящие детали аппаратуры, инструменты для работы во взрывных и пожарных цехах, её широко используют в химическом машиностроении. Бронза Латунь
 • Присущие алюминию легкость, высокая электропроводность, дешевизна послужили причиной его широкого распространения в электротехнике, авиа- и автомобилестроении, химической промышленности и бытовой технике.
• Присущие алюминию легкость, высокая электропроводность, дешевизна послужили причиной его широкого распространения в электротехнике, авиа- и автомобилестроении, химической промышленности и бытовой технике.
 Железо является конструктивным металлом многих сплавов, широко применяемых в промышленности • Нержавеющая сталь сплав железа с хромом и никелем • Чугун
Железо является конструктивным металлом многих сплавов, широко применяемых в промышленности • Нержавеющая сталь сплав железа с хромом и никелем • Чугун
 Биологическая роль металлов Химические элементы, находящиеся в живом организме и обладающие выраженной биологической ролью – называются биогенными элементами. В составе живых организмов обнаружено около 70 химических элементов периодической системы.
Биологическая роль металлов Химические элементы, находящиеся в живом организме и обладающие выраженной биологической ролью – называются биогенными элементами. В составе живых организмов обнаружено около 70 химических элементов периодической системы.
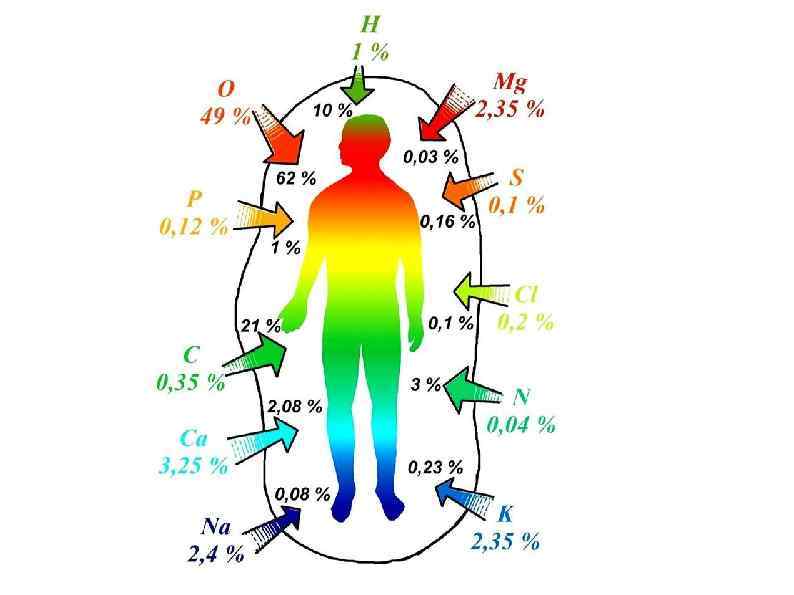
 Например, если вес человека составляет 70 кг, то в нём содержится (в граммах): Са – 1700 г. Mg – 42 г. К – 250 г. Fe – 5 г. Na – 70 г. Zn – 3 г. В целом на долю металлов приходится 2, 1 кг.
Например, если вес человека составляет 70 кг, то в нём содержится (в граммах): Са – 1700 г. Mg – 42 г. К – 250 г. Fe – 5 г. Na – 70 г. Zn – 3 г. В целом на долю металлов приходится 2, 1 кг.
 К числу биогенных элементов относится и ряд металлов, выполняющих особенно важные биологические функции. Это «МЕТАЛЛЫ ЖИЗНИ» Ca, K, Na, Mg Fe, Zn, Cu, Mn, Mo, Co Их дефицит приводит к нарушению нормальной жизнедеятельности организма.
К числу биогенных элементов относится и ряд металлов, выполняющих особенно важные биологические функции. Это «МЕТАЛЛЫ ЖИЗНИ» Ca, K, Na, Mg Fe, Zn, Cu, Mn, Mo, Co Их дефицит приводит к нарушению нормальной жизнедеятельности организма.
 • Например, недостаток цинка в организме проявляется в следующих симптомах: - замедление роста у детей - позднее половое созревание - плохое заживление ран - раздражительность и потеря памяти - появление угрей - очаговое выпадение волос - потеря аппетита, вкусовых ощущений и обоняния - ломкость ногтей - частые инфекции - нарушение усвоения витаминов А, С и Е - повышение уровня холестерина
• Например, недостаток цинка в организме проявляется в следующих симптомах: - замедление роста у детей - позднее половое созревание - плохое заживление ран - раздражительность и потеря памяти - появление угрей - очаговое выпадение волос - потеря аппетита, вкусовых ощущений и обоняния - ломкость ногтей - частые инфекции - нарушение усвоения витаминов А, С и Е - повышение уровня холестерина
 Поступлению в организм химических элементов способствует питание и потребляемая вода. В соответствии с рекомендацией диетологической комиссии Национальной академии США ежедневное поступление химических элементов с пищей должно находиться на определенном уровне. Дефицит и избыток биогенного элемента наносит вред организму. Все живые организмы реагируют на недостаток и избыток или неблаго приятное соотношение элементов.
Поступлению в организм химических элементов способствует питание и потребляемая вода. В соответствии с рекомендацией диетологической комиссии Национальной академии США ежедневное поступление химических элементов с пищей должно находиться на определенном уровне. Дефицит и избыток биогенного элемента наносит вред организму. Все живые организмы реагируют на недостаток и избыток или неблаго приятное соотношение элементов.
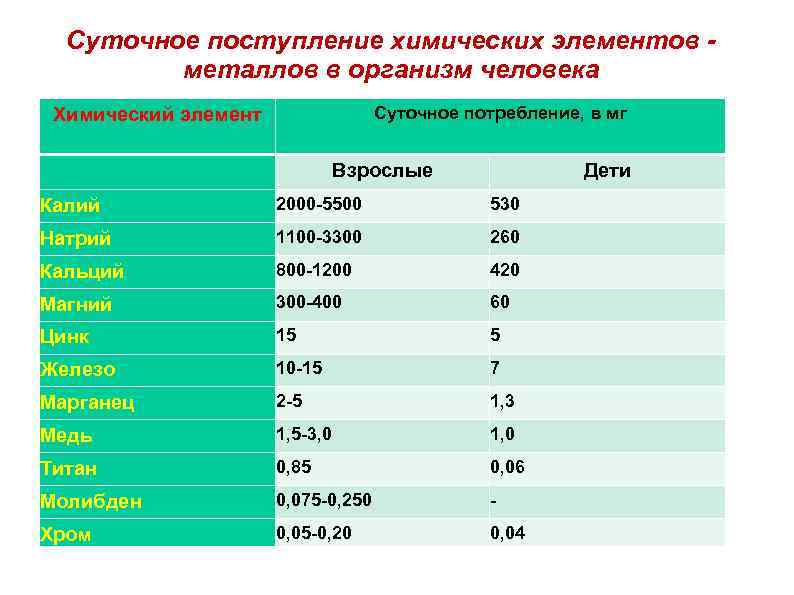 Суточное поступление химических элементов - металлов в организм человека Суточное потребление, в мг Химический элемент Взрослые Дети Калий 2000 5500 530 Натрий 1100 3300 260 Кальций 800 1200 420 Магний 300 400 60 Цинк 15 5 Железо 10 15 7 Марганец 2 5 1, 3 Медь 1, 5 3, 0 1, 0 Титан 0, 85 0, 06 Молибден 0, 075 0, 250 Хром 0, 05 0, 20 0, 04
Суточное поступление химических элементов - металлов в организм человека Суточное потребление, в мг Химический элемент Взрослые Дети Калий 2000 5500 530 Натрий 1100 3300 260 Кальций 800 1200 420 Магний 300 400 60 Цинк 15 5 Железо 10 15 7 Марганец 2 5 1, 3 Медь 1, 5 3, 0 1, 0 Титан 0, 85 0, 06 Молибден 0, 075 0, 250 Хром 0, 05 0, 20 0, 04
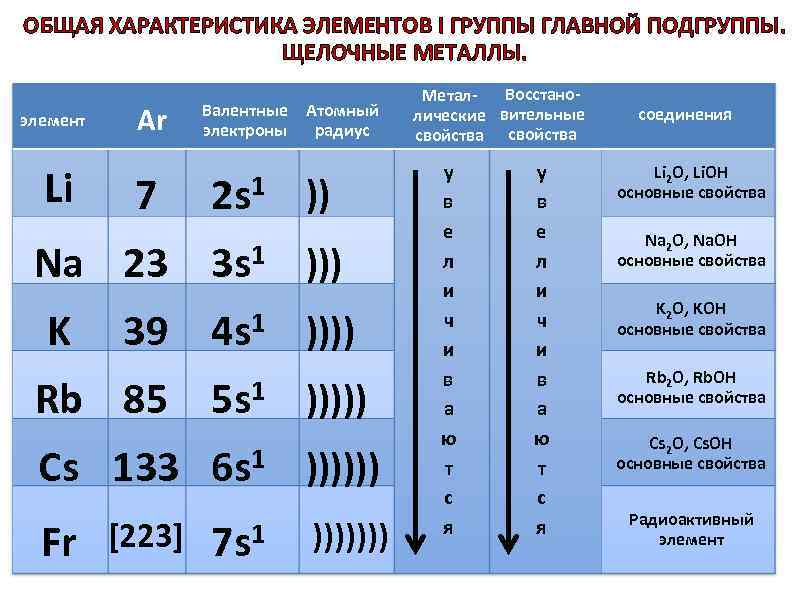 ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ I ГРУППЫ ГЛАВНОЙ ПОДГРУППЫ. ЩЕЛОЧНЫЕ МЕТАЛЛЫ. элемент Li Аr 7 Na 23 K Валентные Атомный электроны радиус 1 2 s 1 3 s )) ))) 39 4 s 1 )))) Rb 85 5 s 1 ))))) Cs 133 6 s 1 )))))) Fr [223] 1 7 s ))))))) Восстано. Металлические вительные свойства у в е л и ч и в а ю т с я соединения Li 2 O, Li. OH основные свойства Na 2 O, Na. OH основные свойства K 2 O, KOH основные свойства Rb 2 O, Rb. OH основные свойства Cs 2 O, Cs. OH основные свойства Радиоактивный элемент
ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ I ГРУППЫ ГЛАВНОЙ ПОДГРУППЫ. ЩЕЛОЧНЫЕ МЕТАЛЛЫ. элемент Li Аr 7 Na 23 K Валентные Атомный электроны радиус 1 2 s 1 3 s )) ))) 39 4 s 1 )))) Rb 85 5 s 1 ))))) Cs 133 6 s 1 )))))) Fr [223] 1 7 s ))))))) Восстано. Металлические вительные свойства у в е л и ч и в а ю т с я соединения Li 2 O, Li. OH основные свойства Na 2 O, Na. OH основные свойства K 2 O, KOH основные свойства Rb 2 O, Rb. OH основные свойства Cs 2 O, Cs. OH основные свойства Радиоактивный элемент
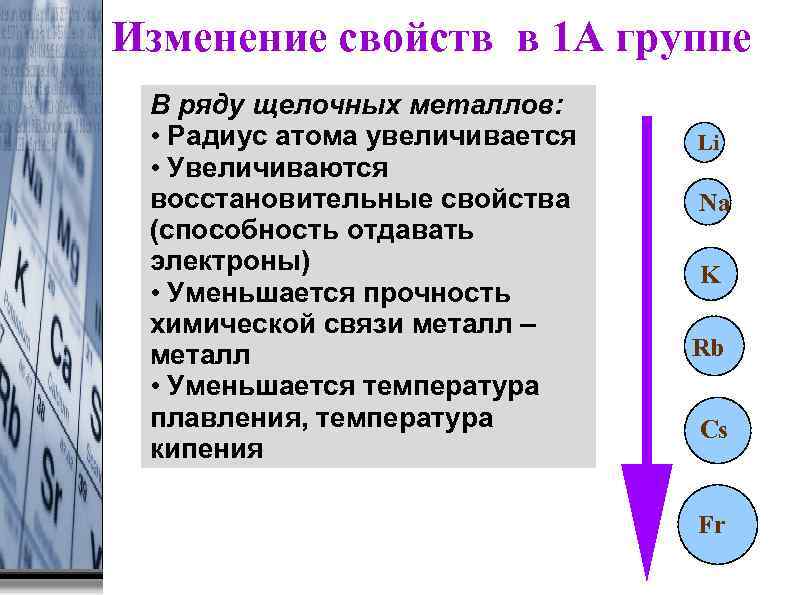 Изменение свойств в 1 А группе В ряду щелочных металлов: • Радиус атома увеличивается • Увеличиваются восстановительные свойства (способность отдавать электроны) • Уменьшается прочность химической связи металл – металл • Уменьшается температура плавления, температура кипения Li Na K Rb Cs Fr 02. 2018
Изменение свойств в 1 А группе В ряду щелочных металлов: • Радиус атома увеличивается • Увеличиваются восстановительные свойства (способность отдавать электроны) • Уменьшается прочность химической связи металл – металл • Уменьшается температура плавления, температура кипения Li Na K Rb Cs Fr 02. 2018
 ОТКРЫТИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ Литий был открыт шведским химиком Й. Арведсоном в 1817 г. по предложению Й. Берцелиуса назван литием (от греч. литос – камень) Гемфри Дэви (1778 – 1829) Натрий и калий были впервые получены английским химиком и физиком Г. Дэви в 1807 г. при электролизе едких щелочей Й. Берцелиус предложил назвать один новый элемент натрием (от араб. натрун – сода), а второй элемент по предложению Гильберта назван калием (от араб. алкали – щелочь) Йенс-Якоб Берцелиус (1779– 1848) 63
ОТКРЫТИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ Литий был открыт шведским химиком Й. Арведсоном в 1817 г. по предложению Й. Берцелиуса назван литием (от греч. литос – камень) Гемфри Дэви (1778 – 1829) Натрий и калий были впервые получены английским химиком и физиком Г. Дэви в 1807 г. при электролизе едких щелочей Й. Берцелиус предложил назвать один новый элемент натрием (от араб. натрун – сода), а второй элемент по предложению Гильберта назван калием (от араб. алкали – щелочь) Йенс-Якоб Берцелиус (1779– 1848) 63
 Наиболее важные природные соединения Na и K. Na. Cl –поваренная (каменная) соль Na 2 SO 4 · 10 H 2 O – глауберова соль Na. Cl · KCl – сильвинит KCl · Mg. Cl 2 · 6 H 2 O – карналлит
Наиболее важные природные соединения Na и K. Na. Cl –поваренная (каменная) соль Na 2 SO 4 · 10 H 2 O – глауберова соль Na. Cl · KCl – сильвинит KCl · Mg. Cl 2 · 6 H 2 O – карналлит
 Получение натрия и калия. 1) Электролизом расплавов хлоридов или щелочей: В результате электролиза расплава KOH образуется: Калий также получают из расплава KCl, действуя на него металлическим натрием в вакууме.
Получение натрия и калия. 1) Электролизом расплавов хлоридов или щелочей: В результате электролиза расплава KOH образуется: Калий также получают из расплава KCl, действуя на него металлическим натрием в вакууме.
 ФИЗИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ МЕТАЛЛИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА Li Rb Na Cs K Твердые вещества серебристо-белого цвета Электропроводны и теплопроводны Легкоплавкие. пластичные
ФИЗИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ МЕТАЛЛИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА Li Rb Na Cs K Твердые вещества серебристо-белого цвета Электропроводны и теплопроводны Легкоплавкие. пластичные
 ХИМИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ
ХИМИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ
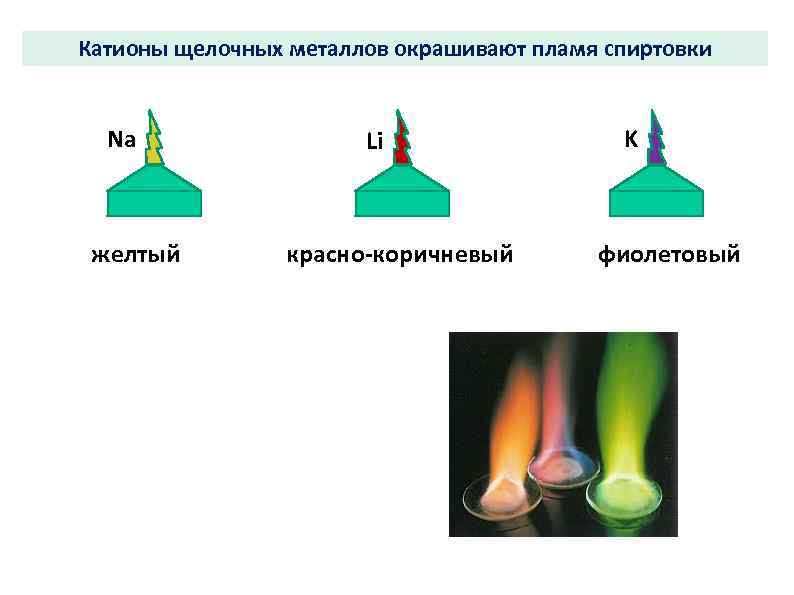 Катионы щелочных металлов окрашивают пламя спиртовки Na желтый Li K красно-коричневый фиолетовый
Катионы щелочных металлов окрашивают пламя спиртовки Na желтый Li K красно-коричневый фиолетовый
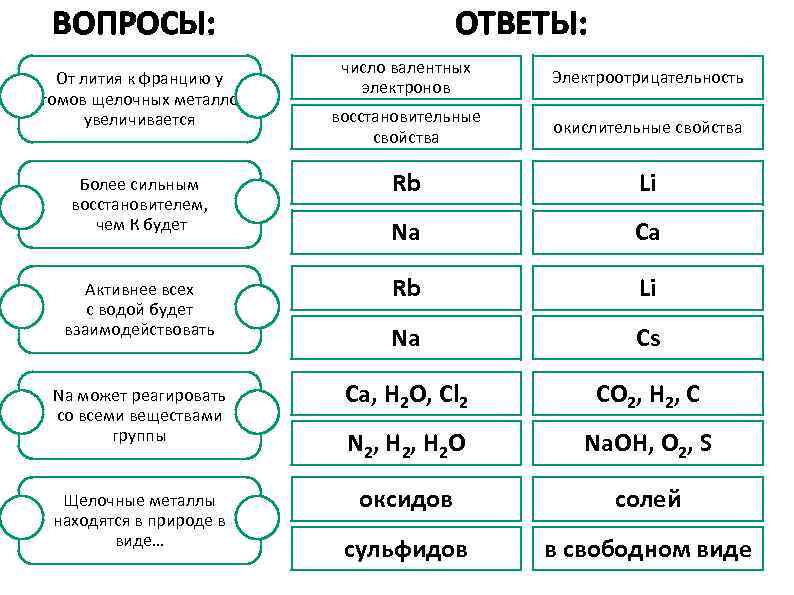 ВОПРОСЫ: ОТВЕТЫ: число валентных электронов Электроотрицательность восстановительные свойства окислительные свойства Rb Li Na Ca Rb Li Na Cs Na может реагировать со всеми веществами группы Сa, H 2 O, Cl 2 CO 2, H 2, C N 2, H 2 O Na. OH, O 2, S Щелочные металлы находятся в природе в виде… оксидов солей сульфидов в свободном виде От лития к францию у атомов щелочных металлов увеличивается Более сильным восстановителем, чем К будет Активнее всех с водой будет взаимодействовать
ВОПРОСЫ: ОТВЕТЫ: число валентных электронов Электроотрицательность восстановительные свойства окислительные свойства Rb Li Na Ca Rb Li Na Cs Na может реагировать со всеми веществами группы Сa, H 2 O, Cl 2 CO 2, H 2, C N 2, H 2 O Na. OH, O 2, S Щелочные металлы находятся в природе в виде… оксидов солей сульфидов в свободном виде От лития к францию у атомов щелочных металлов увеличивается Более сильным восстановителем, чем К будет Активнее всех с водой будет взаимодействовать
 Соединения щелочных металлов. Оксиды. Гидроксиды. Пероксиды. Гидриды. Соли. А. С. Егоров: стр. 299 -300 Оксиды R 2 О – твердые вещества. Имеют ярко выраженные основные свойства: взаимодействуют с водой, кислотами и кислотными оксидами. Оксиды натрия Na 2 O и калия K 2 O получают, прокаливая пероксиды с соответствующими металлами, например: 0 2 Na + +1 -1 Na 2 O 2 t +1 -2 = 2 Na 2 O
Соединения щелочных металлов. Оксиды. Гидроксиды. Пероксиды. Гидриды. Соли. А. С. Егоров: стр. 299 -300 Оксиды R 2 О – твердые вещества. Имеют ярко выраженные основные свойства: взаимодействуют с водой, кислотами и кислотными оксидами. Оксиды натрия Na 2 O и калия K 2 O получают, прокаливая пероксиды с соответствующими металлами, например: 0 2 Na + +1 -1 Na 2 O 2 t +1 -2 = 2 Na 2 O
 Гидроксиды щелочных металловщелочи. Гидроксиды RОН – твердые белые вещества. Очень гидроскопичны. Хорошо растворяются в воде, с выделением большого количества теплоты. Их относят к щелочам. Гидроксид натрия Na. OH в технике известен как едкий натр, каустическая сода, каустик. KOH - техническое название гидроксида калия – едкое кали. Едкий натр применяют для очистки нефтепродуктов, в бумажной и текстильной промышленности, для производства жидкого мыла. Едкое кали применяют для производства жидкого мыла.
Гидроксиды щелочных металловщелочи. Гидроксиды RОН – твердые белые вещества. Очень гидроскопичны. Хорошо растворяются в воде, с выделением большого количества теплоты. Их относят к щелочам. Гидроксид натрия Na. OH в технике известен как едкий натр, каустическая сода, каустик. KOH - техническое название гидроксида калия – едкое кали. Едкий натр применяют для очистки нефтепродуктов, в бумажной и текстильной промышленности, для производства жидкого мыла. Едкое кали применяют для производства жидкого мыла.
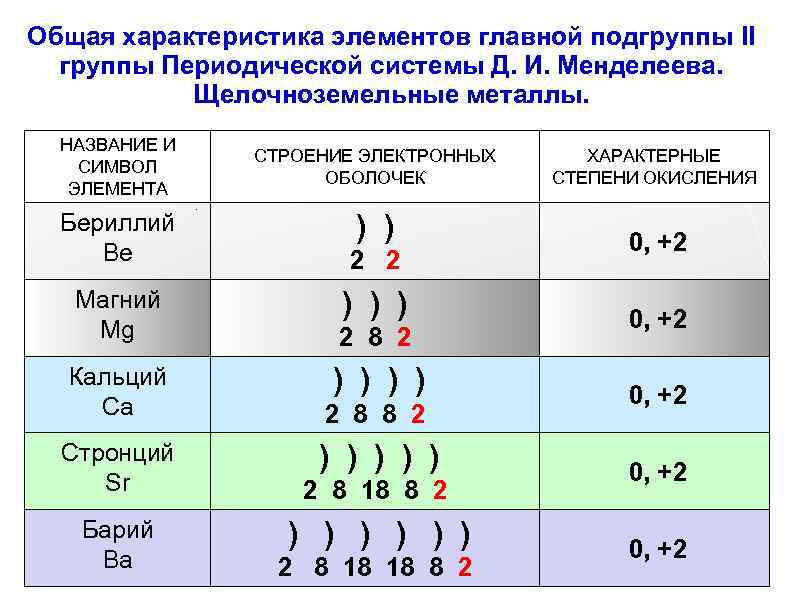 Общая характеристика элементов главной подгруппы II группы Периодической системы Д. И. Менделеева. Щелочноземельные металлы. НАЗВАНИЕ И СТРОЕНИЕ ЭЛЕКТРОННЫХ ХАРАКТЕРНЫЕ СИМВОЛ ХАРАКТЕРНЫЕ ОБОЛОЧЕК СТЕПЕНИ ОКИСЛЕНИЯ НАЗВАНИЕ И СИМВОЛ СТРОЕНИЕ ЭЛЕКТРОННЫХ ЭЛЕМЕНТА СТЕПЕНИ ЭЛЕМЕНТА ОБОЛОЧЕК ОКИСЛЕНИЯ Бериллий ) ) Be 2 2 Магний Mg ) ) ) 2 8 2 Кальций Ca ) ) Стронций Sr ) ) ) Барий Ba 2 8 8 2 2 8 18 8 2 ) ) ) ) 2 8 18 18 8 2 0, +2 0, +2
Общая характеристика элементов главной подгруппы II группы Периодической системы Д. И. Менделеева. Щелочноземельные металлы. НАЗВАНИЕ И СТРОЕНИЕ ЭЛЕКТРОННЫХ ХАРАКТЕРНЫЕ СИМВОЛ ХАРАКТЕРНЫЕ ОБОЛОЧЕК СТЕПЕНИ ОКИСЛЕНИЯ НАЗВАНИЕ И СИМВОЛ СТРОЕНИЕ ЭЛЕКТРОННЫХ ЭЛЕМЕНТА СТЕПЕНИ ЭЛЕМЕНТА ОБОЛОЧЕК ОКИСЛЕНИЯ Бериллий ) ) Be 2 2 Магний Mg ) ) ) 2 8 2 Кальций Ca ) ) Стронций Sr ) ) ) Барий Ba 2 8 8 2 2 8 18 8 2 ) ) ) ) 2 8 18 18 8 2 0, +2 0, +2
 В ряду щелочно-земельных металлов: IIА гр. • Радиус атома увеличивается • Увеличиваются восстановительные свойства (способность отдавать электроны) • Уменьшается прочность химической связи металл – металл • Уменьшается температура плавления, температура кипения
В ряду щелочно-земельных металлов: IIА гр. • Радиус атома увеличивается • Увеличиваются восстановительные свойства (способность отдавать электроны) • Уменьшается прочность химической связи металл – металл • Уменьшается температура плавления, температура кипения
 Нахождение в природе Ca Ca. CO 3 – кальцит (известняк, мрамор и др. ) Ca 3(PO 4)2 – апатит, фосфорит Ca. SO 4 • 2 H 2 O – гипс Ca. SO 4 – ангидрит Ca. F 2 – плавиковый шпат (флюорит) Sr Sr. SO 4 – целестин Sr. CO 3 – стронцианит Ba Ba. SO 4 – барит Ba. CO 3 – витерит
Нахождение в природе Ca Ca. CO 3 – кальцит (известняк, мрамор и др. ) Ca 3(PO 4)2 – апатит, фосфорит Ca. SO 4 • 2 H 2 O – гипс Ca. SO 4 – ангидрит Ca. F 2 – плавиковый шпат (флюорит) Sr Sr. SO 4 – целестин Sr. CO 3 – стронцианит Ba Ba. SO 4 – барит Ba. CO 3 – витерит
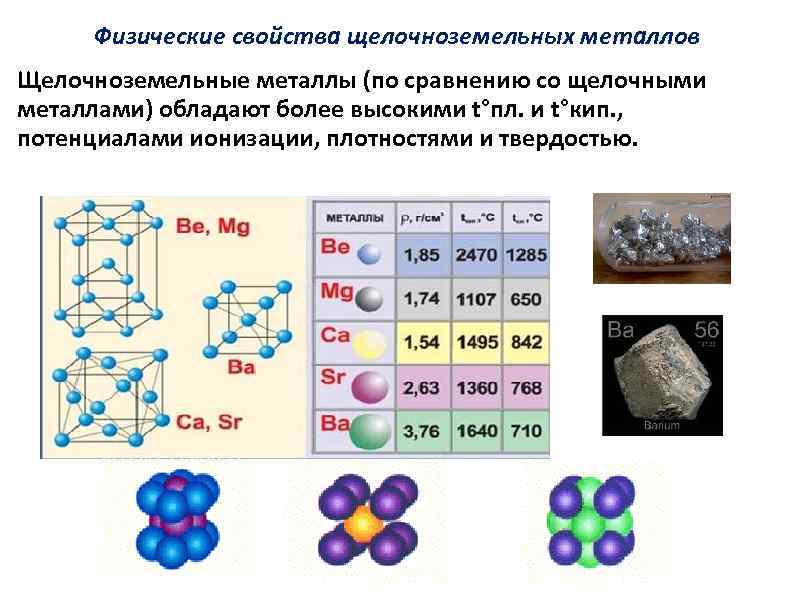 Физические свойства щелочноземельных металлов Щелочноземельные металлы (по сравнению со щелочными металлами) обладают более высокими t°пл. и t°кип. , потенциалами ионизации, плотностями и твердостью.
Физические свойства щелочноземельных металлов Щелочноземельные металлы (по сравнению со щелочными металлами) обладают более высокими t°пл. и t°кип. , потенциалами ионизации, плотностями и твердостью.
 Получение металлов Барий получают восстановлением оксида (при t°): 3 Ba. O + 2 Al = 3 Ba + Al 2 O 3 Остальные металлы получают электролизом расплавов хлоридов: Ca. Cl 2 = Ca + Cl 2 катод: Ca 2+ + 2ē = Ca 0 анод: 2 Cl- – 2ē = Cl 20
Получение металлов Барий получают восстановлением оксида (при t°): 3 Ba. O + 2 Al = 3 Ba + Al 2 O 3 Остальные металлы получают электролизом расплавов хлоридов: Ca. Cl 2 = Ca + Cl 2 катод: Ca 2+ + 2ē = Ca 0 анод: 2 Cl- – 2ē = Cl 20
 Химические свойства металлов Ве единственный металл этой группы для соединений которого характерны амфотерные свойства. Мg типичный активный металл. Ca, Sr, Ва-щелочно-земельные металлы высокой активности. 1. Реакция с водой. Реагируют с водой при комнатной температуре (кроме Be и Mg) с выделением водорода. В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде. При нагревании: Mg + H 2 O = Mg. O + H 2 В отличие от них Ca, Sr и Ba растворяются в воде с образованием гидроксидов, которые являются сильными основаниями: Ca + 2 H 2 O = Ca(OH)2 + H 2
Химические свойства металлов Ве единственный металл этой группы для соединений которого характерны амфотерные свойства. Мg типичный активный металл. Ca, Sr, Ва-щелочно-земельные металлы высокой активности. 1. Реакция с водой. Реагируют с водой при комнатной температуре (кроме Be и Mg) с выделением водорода. В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде. При нагревании: Mg + H 2 O = Mg. O + H 2 В отличие от них Ca, Sr и Ba растворяются в воде с образованием гидроксидов, которые являются сильными основаниями: Ca + 2 H 2 O = Ca(OH)2 + H 2
 2. Реакция с кислородом. Все металлы образуют оксиды RO, барий пероксид – Ba. O 2: Ba + O 2 = Ba. O 2 2 Сa + O 2 =2 Сa. O
2. Реакция с кислородом. Все металлы образуют оксиды RO, барий пероксид – Ba. O 2: Ba + O 2 = Ba. O 2 2 Сa + O 2 =2 Сa. O
 3. С другими неметаллами образуются бинарные соединения: Ba + S = Ba. S (сульфиды) Ca + H 2 = Ca. H 2 (гидриды) Ca + 2 C = Ca. C 2 (карбиды) 3 Ba + 2 P = Ba 3 P 2 (фосфиды) 4. Растворяются в кислотах: Ca + 2 HCl = Ca. Cl 2 + H 2 4 Ca + 5 H 2 SO 4(к) = 4 Ca. SO 4 + H 2 S + 4 H 2 O 4 Ca + 10 HNO 3(р) = 4 Ca(NO 3)2 + NH 4 NO 3 + 3 H 2 O 4 Ca + 10 HNO 3(к) = 4 Ca(NO 3)2 + N 2 O + 5 H 2 O
3. С другими неметаллами образуются бинарные соединения: Ba + S = Ba. S (сульфиды) Ca + H 2 = Ca. H 2 (гидриды) Ca + 2 C = Ca. C 2 (карбиды) 3 Ba + 2 P = Ba 3 P 2 (фосфиды) 4. Растворяются в кислотах: Ca + 2 HCl = Ca. Cl 2 + H 2 4 Ca + 5 H 2 SO 4(к) = 4 Ca. SO 4 + H 2 S + 4 H 2 O 4 Ca + 10 HNO 3(р) = 4 Ca(NO 3)2 + NH 4 NO 3 + 3 H 2 O 4 Ca + 10 HNO 3(к) = 4 Ca(NO 3)2 + N 2 O + 5 H 2 O
 5. Качественная реакция на катионы щелочноземельных металлов – окрашивание пламени в следующие цвета: Ca – кирпично красный Sr – карминово красный Ba – зеленовато желтый Катион Ba 2+ обычно открывают обменной реакцией с серной кислотой или ее солями. Ba 2+ + SO 4 2 - → Ва SO 4 Сульфат бария – белый осадок, нерастворимый в минеральных кислотах.
5. Качественная реакция на катионы щелочноземельных металлов – окрашивание пламени в следующие цвета: Ca – кирпично красный Sr – карминово красный Ba – зеленовато желтый Катион Ba 2+ обычно открывают обменной реакцией с серной кислотой или ее солями. Ba 2+ + SO 4 2 - → Ва SO 4 Сульфат бария – белый осадок, нерастворимый в минеральных кислотах.
 Важнейшие соединения щелочноземельных металлов. Оксиды. Гидроксиды. Соли. А. С. Егоров: стр. 307 -308
Важнейшие соединения щелочноземельных металлов. Оксиды. Гидроксиды. Соли. А. С. Егоров: стр. 307 -308
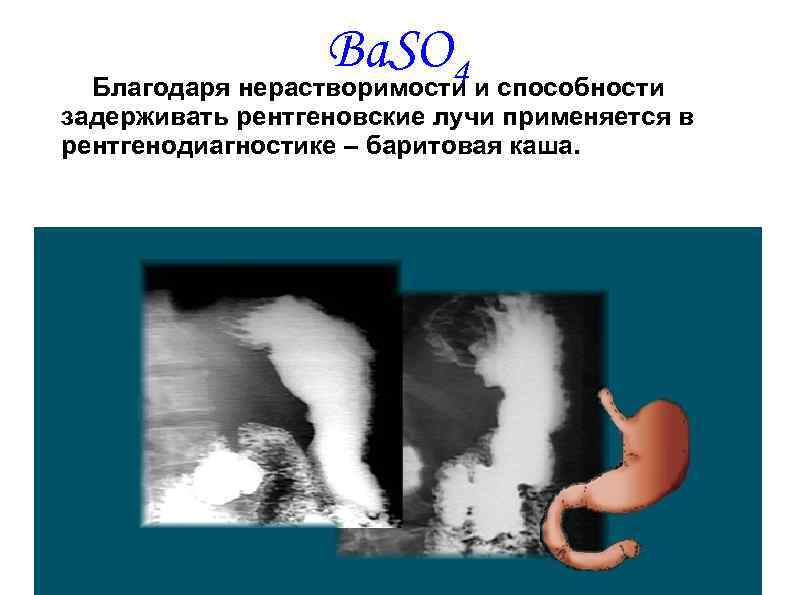 Ba. SO 4 Благодаря нерастворимости и способности задерживать рентгеновские лучи применяется в рентгенодиагностике – баритовая каша.
Ba. SO 4 Благодаря нерастворимости и способности задерживать рентгеновские лучи применяется в рентгенодиагностике – баритовая каша.
 Ca 3(PO 4)2 Входит в состав фосфоритов и апатитов, а также в состав костей и зубов. В организме взрослого человека содержится 1 кг Са в виде фосфата кальция.
Ca 3(PO 4)2 Входит в состав фосфоритов и апатитов, а также в состав костей и зубов. В организме взрослого человека содержится 1 кг Са в виде фосфата кальция.
 Ca. CO 3 Карбонат кальция – одно из самых распространённых на Земле соединений. Его содержат горные породы – мел, мрамор, известняк.
Ca. CO 3 Карбонат кальция – одно из самых распространённых на Земле соединений. Его содержат горные породы – мел, мрамор, известняк.
 Ca. SO 4∙ 2 H 2 O Встречается в природе в виде минерала гипса, представляющего собой кристаллогидрат. Используется в строительстве, в медицине для наложения гипсовых повязок, для получения слепков.
Ca. SO 4∙ 2 H 2 O Встречается в природе в виде минерала гипса, представляющего собой кристаллогидрат. Используется в строительстве, в медицине для наложения гипсовых повязок, для получения слепков.
 Mg. CO 3 Широко применяется в производстве стекла, цемента, кирпича, а также в металлургии для перевода пустой породы в шлак.
Mg. CO 3 Широко применяется в производстве стекла, цемента, кирпича, а также в металлургии для перевода пустой породы в шлак.
 Са(ОН)2 Гидроксид кальция или гашёная известь с песком и водой называется известковым раствором и широко используется в строительстве. При нагревании разлагается на оксид и воду.
Са(ОН)2 Гидроксид кальция или гашёная известь с песком и водой называется известковым раствором и широко используется в строительстве. При нагревании разлагается на оксид и воду.
 Тест 1) Какой металл при н. у. является жидким? А) Mg Б) Cd В) Hg Г) Pb 2) Как называется кристаллическая решетка металлов? А) атомная Б) ионная В) металлическая Г) молекулярная 3) Какой металл встречается в природе в самородном состоянии? А) Ca Б) Mg В) Ag Г) Al 4) Какой из перечисленных оксидов обладает амфотерными свойствами? А) Na 2 O Б) Ca. O В) Zn. O Г) Cr. О 3 5) Be и Mg не относятся к щелочноземельным металлам, так как: А) относятся к неметаллам Б) атомы Be и Mg имеют небольшое число электронных слоев В) являются переходными металлами Г) свойства их гидроксидов отличаются от свойств гидроксидов щелочноземельных металлов
Тест 1) Какой металл при н. у. является жидким? А) Mg Б) Cd В) Hg Г) Pb 2) Как называется кристаллическая решетка металлов? А) атомная Б) ионная В) металлическая Г) молекулярная 3) Какой металл встречается в природе в самородном состоянии? А) Ca Б) Mg В) Ag Г) Al 4) Какой из перечисленных оксидов обладает амфотерными свойствами? А) Na 2 O Б) Ca. O В) Zn. O Г) Cr. О 3 5) Be и Mg не относятся к щелочноземельным металлам, так как: А) относятся к неметаллам Б) атомы Be и Mg имеют небольшое число электронных слоев В) являются переходными металлами Г) свойства их гидроксидов отличаются от свойств гидроксидов щелочноземельных металлов
 Биологическая роль и применение в медицине соединений Ca и Mg А. С. Егоров: стр. 311 -312
Биологическая роль и применение в медицине соединений Ca и Mg А. С. Егоров: стр. 311 -312
 Алюминий и его соединений Электронная формула атома в основном электронном состоянии: 1 S 22 S 2 2 Р 6 23 S 2 3 Р 1 В возбужденном состоянии: 1 S 22 S 2 2 Р 6 23 S 1 3 Р 2 , что отвечает валентности (III) Типичная степень окисления +3
Алюминий и его соединений Электронная формула атома в основном электронном состоянии: 1 S 22 S 2 2 Р 6 23 S 2 3 Р 1 В возбужденном состоянии: 1 S 22 S 2 2 Р 6 23 S 1 3 Р 2 , что отвечает валентности (III) Типичная степень окисления +3
 Алюминий впервые получен химическим путем датским химиком Х. К. Эрстедом в 1825 г. В 1854 г. французский химик А. Э. Сент Клер Девиль выделил его электрохимическим методом.
Алюминий впервые получен химическим путем датским химиком Х. К. Эрстедом в 1825 г. В 1854 г. французский химик А. Э. Сент Клер Девиль выделил его электрохимическим методом.
 Нахождение в природе Алюминий является самым распространенным в природе металлом. Содержание его в земной коре составляет 8, 05 %. Важнейшие природные соединения алюминия— алюмосиликаты, боксит, корунд. Алюмосиликаты составляют основную массу земной коры. Продукт их выветривания —глина и полевые шпаты (ортоклаз, альбит, анортит). Основу глин составляет каолин Аl 2 O 3· 2 Si. O 2· 2 Н 2 О.
Нахождение в природе Алюминий является самым распространенным в природе металлом. Содержание его в земной коре составляет 8, 05 %. Важнейшие природные соединения алюминия— алюмосиликаты, боксит, корунд. Алюмосиликаты составляют основную массу земной коры. Продукт их выветривания —глина и полевые шпаты (ортоклаз, альбит, анортит). Основу глин составляет каолин Аl 2 O 3· 2 Si. O 2· 2 Н 2 О.
 Боксит —горная порода, из которой получают алюминий. Состоит главным образом из гидратов оксида алюминия Аl 2 O 3·n. Н 2 О.
Боксит —горная порода, из которой получают алюминий. Состоит главным образом из гидратов оксида алюминия Аl 2 O 3·n. Н 2 О.
 Физические свойства Алюминий — серебристо белый легкий металл, плавящийся при 660 °С. Очень пластичный, легко вытягивается в проволоку и раскатывается в листы: из него можно изготовить фольгу толщиной менее 0, 01 мм. Алюминий обладает очень большой тепло и электропроводностью. Его сплавы с различными металлами прочны и легки.
Физические свойства Алюминий — серебристо белый легкий металл, плавящийся при 660 °С. Очень пластичный, легко вытягивается в проволоку и раскатывается в листы: из него можно изготовить фольгу толщиной менее 0, 01 мм. Алюминий обладает очень большой тепло и электропроводностью. Его сплавы с различными металлами прочны и легки.
 Химические свойства Алюминий — активный металл. В ряду напряжений он стоит после щелочных и щелочноземельных металлов. Однако на воздухе он довольно устойчив, так как его поверхность покрывается очень плотной пленкой оксида Аl 2 О 3, предохраняющей металл от контакта с воздухом.
Химические свойства Алюминий — активный металл. В ряду напряжений он стоит после щелочных и щелочноземельных металлов. Однако на воздухе он довольно устойчив, так как его поверхность покрывается очень плотной пленкой оксида Аl 2 О 3, предохраняющей металл от контакта с воздухом.
 1. Если с алюминиевой проволоки снять защитную оксидную пленку, то алюминий начнет энергично взаимодействовать с кислородом и водяными парами воздуха, превращаясь в рыхлую массу— гидроксид алюминия: 4 Аl + 3 O 2 + 6 Н 2 О = 4 Аl(ОН)3
1. Если с алюминиевой проволоки снять защитную оксидную пленку, то алюминий начнет энергично взаимодействовать с кислородом и водяными парами воздуха, превращаясь в рыхлую массу— гидроксид алюминия: 4 Аl + 3 O 2 + 6 Н 2 О = 4 Аl(ОН)3
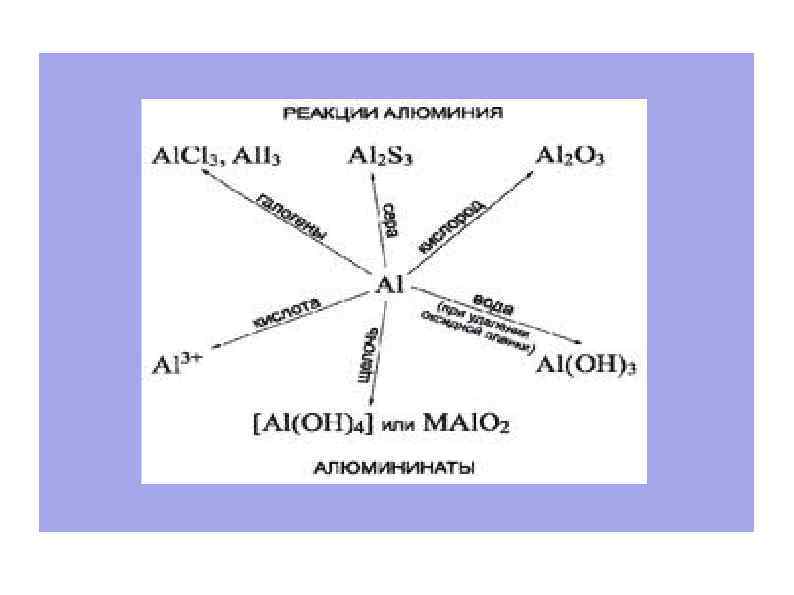
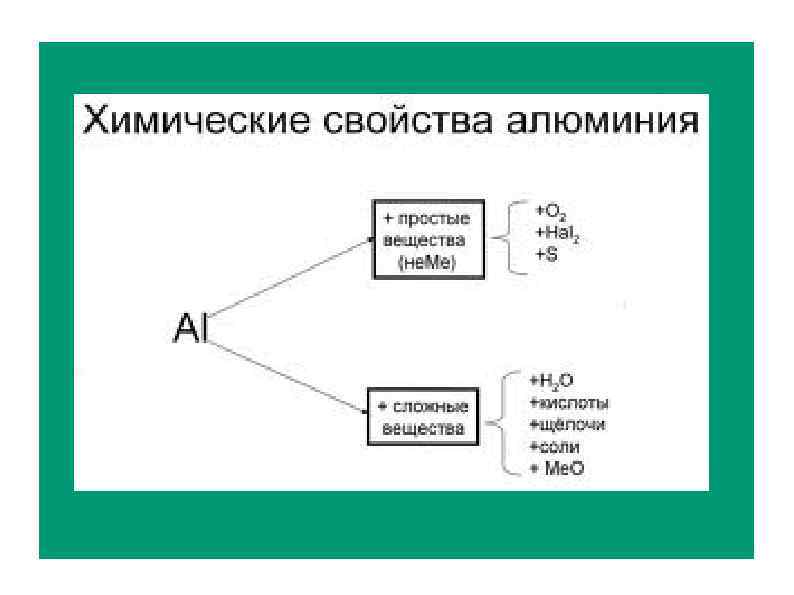
 2. Порошкообразный алюминий легко взаимодействует с галогенами, кислородом и всеми неметаллами. Для начала реакций необходимо нагревание, затем они протекают очень интенсивно и сопровождаются выделением большого количества теплоты: 2 Аl + 3 Вr 2 = 2 Аl. Вr 3 (бромид алюминия) 4 Аl + 3 O 2 = 2 Аl 2 O 3 (оксид алюминия) 2 Аl + 3 S = Аl 2 S 3 (сульфид алюминия 2 Аl + N 2 = 2 Аl. N (нитрид алюминия) 4 Аl + 3 С = Аl 4 С 3 (карбид алюминия)
2. Порошкообразный алюминий легко взаимодействует с галогенами, кислородом и всеми неметаллами. Для начала реакций необходимо нагревание, затем они протекают очень интенсивно и сопровождаются выделением большого количества теплоты: 2 Аl + 3 Вr 2 = 2 Аl. Вr 3 (бромид алюминия) 4 Аl + 3 O 2 = 2 Аl 2 O 3 (оксид алюминия) 2 Аl + 3 S = Аl 2 S 3 (сульфид алюминия 2 Аl + N 2 = 2 Аl. N (нитрид алюминия) 4 Аl + 3 С = Аl 4 С 3 (карбид алюминия)
 3. Очищенный от защитной оксидной пленки алюминий взаимодействует с водой с выделением водорода: 2 Аl + 6 Н 2 О = 2 Аl(ОН)3 + 3 Н 2 4. Алюминий хорошо растворяется в разбавленных серной и соляной кислотах: 2 Аl + 6 НСl = 2 Al. Сl 3 + 3 Н 2 2 Аl + 3 Н 2 SO 4 = Аl 2(SO 4)3 +3 Н 2
3. Очищенный от защитной оксидной пленки алюминий взаимодействует с водой с выделением водорода: 2 Аl + 6 Н 2 О = 2 Аl(ОН)3 + 3 Н 2 4. Алюминий хорошо растворяется в разбавленных серной и соляной кислотах: 2 Аl + 6 НСl = 2 Al. Сl 3 + 3 Н 2 2 Аl + 3 Н 2 SO 4 = Аl 2(SO 4)3 +3 Н 2
 5. Разбавленная азотная кислота при нагревании растворяет алюминий с выделением монооксида азота или аммиака, например: 8 Аl + 30 НNО 3 = 8 Аl(NО 3)3 + 3 N 2 О + 15 Н 2 О Концентрированная азотная кислота пассивирует алюминий на холоду.
5. Разбавленная азотная кислота при нагревании растворяет алюминий с выделением монооксида азота или аммиака, например: 8 Аl + 30 НNО 3 = 8 Аl(NО 3)3 + 3 N 2 О + 15 Н 2 О Концентрированная азотная кислота пассивирует алюминий на холоду.
 6. Алюминий легко растворяется в едкой щёлочи с образованием хорошо растворимого комплекса — тетрагидроксиалюмината натрия и водорода: 2 АI 0 + 2 Na. OH + 6 H 2 O → 3 H 2↑ + 2 Na[Al(OH)4]
6. Алюминий легко растворяется в едкой щёлочи с образованием хорошо растворимого комплекса — тетрагидроксиалюмината натрия и водорода: 2 АI 0 + 2 Na. OH + 6 H 2 O → 3 H 2↑ + 2 Na[Al(OH)4]
 7. Алюминий легко отнимает кислород и галогены у оксидов и солей других металлов. Реакция сопровождается выделением большого количества теплоты: 8 Al + 3 Fе 3 О 4 = 9 Fе + 4 Аl 2 O 3 Алюмотермией пользуются при получении некоторых редких металлов, которые образуют прочную связь с кислородом (ниобий, тантал, молибден, вольфрам), а также для сваривания рельсов.
7. Алюминий легко отнимает кислород и галогены у оксидов и солей других металлов. Реакция сопровождается выделением большого количества теплоты: 8 Al + 3 Fе 3 О 4 = 9 Fе + 4 Аl 2 O 3 Алюмотермией пользуются при получении некоторых редких металлов, которые образуют прочную связь с кислородом (ниобий, тантал, молибден, вольфрам), а также для сваривания рельсов.
 Получение 1. Впервые алюминий был получен восстановлением из хлорида алюминия металлическим натрием: Аl. Сl 3 + 3 Nа = 3 Nа. Сl + Аl
Получение 1. Впервые алюминий был получен восстановлением из хлорида алюминия металлическим натрием: Аl. Сl 3 + 3 Nа = 3 Nа. Сl + Аl
 2. В настоящее время его получают электролизом расплавленных солей в электролитических ваннах. В качестве электролита служит расплав, содержащий 85 90 % криолита — комплексной соли Nа 3 [Аl. F 6] и 10 15 % глинозема — оксида алюминия Аl 2 O 3. Такая смесь плавится при температуре около 1000 °С. 2 Аl 2 O 3 → 4 Аl + 3 O 2
2. В настоящее время его получают электролизом расплавленных солей в электролитических ваннах. В качестве электролита служит расплав, содержащий 85 90 % криолита — комплексной соли Nа 3 [Аl. F 6] и 10 15 % глинозема — оксида алюминия Аl 2 O 3. Такая смесь плавится при температуре около 1000 °С. 2 Аl 2 O 3 → 4 Аl + 3 O 2
 Применение Алюминий используется очень широко. • Из него изготовляют фольгу, применяемую в радиотехнике и для упаковки пищевых лродуктов. • Алюминием покрывают стальные и чугунные изделия в целях предохранення их от коррозии: изделия нагревают до 1000°С в смеси алюминиевого порошка (49 %), оксида алюминия (49 %) и хлорида алюминия (2 %). Этот процесс называется алитированием. Алитированные изделия выдерживают нагревание до 1000 °С, не подвергаясь коррозии.
Применение Алюминий используется очень широко. • Из него изготовляют фольгу, применяемую в радиотехнике и для упаковки пищевых лродуктов. • Алюминием покрывают стальные и чугунные изделия в целях предохранення их от коррозии: изделия нагревают до 1000°С в смеси алюминиевого порошка (49 %), оксида алюминия (49 %) и хлорида алюминия (2 %). Этот процесс называется алитированием. Алитированные изделия выдерживают нагревание до 1000 °С, не подвергаясь коррозии.
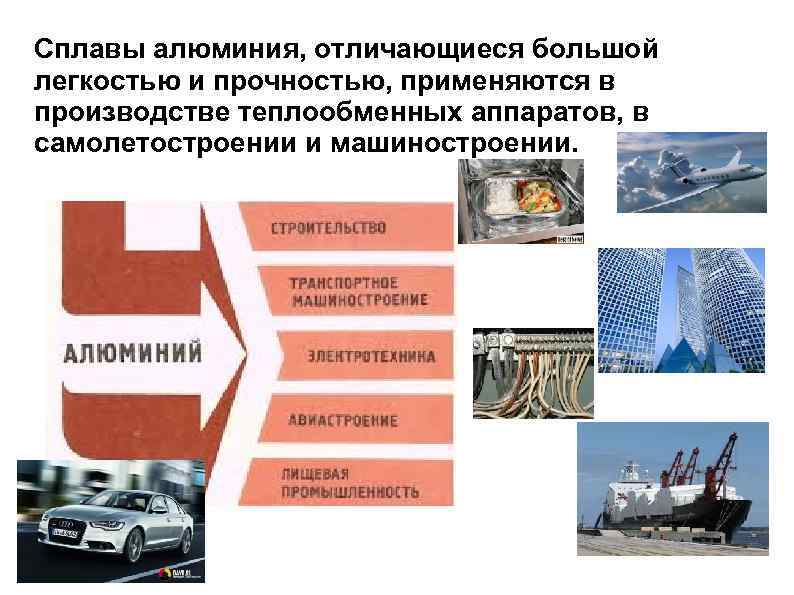 Сплавы алюминия, отличающиеся большой легкостью и прочностью, применяются в производстве теплообменных аппаратов, в самолетостроении и машиностроении.
Сплавы алюминия, отличающиеся большой легкостью и прочностью, применяются в производстве теплообменных аппаратов, в самолетостроении и машиностроении.
 Оксид алюниния Аl 2 O 3 Представляет собой белое вещество с температурой плавления 2050 °С. В природе оксид алюминия встречается в виде корунда и глинозема. Иногда встречаются прозрачные кристаллы корунда красивой формы и окраски. Корунд, окрашенный соединениями хрома в красный цвет, называют рубином, а окрашенный соединениями титана и железа в синий цвет—сапфиром. Рубин и сапфир являются драгоценными камнями. В настоящее время их довольно легко получают искусственно.
Оксид алюниния Аl 2 O 3 Представляет собой белое вещество с температурой плавления 2050 °С. В природе оксид алюминия встречается в виде корунда и глинозема. Иногда встречаются прозрачные кристаллы корунда красивой формы и окраски. Корунд, окрашенный соединениями хрома в красный цвет, называют рубином, а окрашенный соединениями титана и железа в синий цвет—сапфиром. Рубин и сапфир являются драгоценными камнями. В настоящее время их довольно легко получают искусственно.
 Природный корунд —очень твердое вещество. Он применяется для изготовления наждачных кругов и шлифовальных порошков. Рубин используют для изготовления втулок часовых и других точных механизмов.
Природный корунд —очень твердое вещество. Он применяется для изготовления наждачных кругов и шлифовальных порошков. Рубин используют для изготовления втулок часовых и других точных механизмов.
 Оксид алюминия обладает амфотерными свойствами, но он не растворяется в воде, при нагревании частично растворяется в кислотах и щелочах. При кипячении в концентрированном растворе щелочи он лишь частично переходит в раствор. Аl 2 О 3 + 6 НСI → 2 Аl. СI 3 + 3 Н 2 О Аl 2 О 3 + 2 КОН + 3 Н 2 О = 2 К[Аl(ОН)4]
Оксид алюминия обладает амфотерными свойствами, но он не растворяется в воде, при нагревании частично растворяется в кислотах и щелочах. При кипячении в концентрированном растворе щелочи он лишь частично переходит в раствор. Аl 2 О 3 + 6 НСI → 2 Аl. СI 3 + 3 Н 2 О Аl 2 О 3 + 2 КОН + 3 Н 2 О = 2 К[Аl(ОН)4]
 Оксид алюминия переводят в растворимое состояние при сплавлением со щелочами или карбонатами: АI 2 О 3 + 2 КОН = 2 КАl. O 2 + Н 2 О Аl 2 O 3 + К 2 СО 3 = 2 КАl. O 2 + СО 2 • Полученные сплавы растворяются в воде. КАl. O 2 + 2 Н 2 О → КОН + Аl(ОН)3
Оксид алюминия переводят в растворимое состояние при сплавлением со щелочами или карбонатами: АI 2 О 3 + 2 КОН = 2 КАl. O 2 + Н 2 О Аl 2 O 3 + К 2 СО 3 = 2 КАl. O 2 + СО 2 • Полученные сплавы растворяются в воде. КАl. O 2 + 2 Н 2 О → КОН + Аl(ОН)3
 Гидроксид алюминия Аl(ОН)3 Представляет собой белое вещество, которое при нагревании теряет воду, превращаясь в оксид алюминия. Гидроксид алюминия обладает амфотерными свойствами. Свежеосажденный гидроксид легко растворяется в кислотах и щелочах 2 Аl(ОН)3 + 3 Н 2 SO 4 = Аl 2(SO 4)3 + 6 Н 2 О Аl(ОН)3 + 3 КОН = К[Аl(ОН)4]
Гидроксид алюминия Аl(ОН)3 Представляет собой белое вещество, которое при нагревании теряет воду, превращаясь в оксид алюминия. Гидроксид алюминия обладает амфотерными свойствами. Свежеосажденный гидроксид легко растворяется в кислотах и щелочах 2 Аl(ОН)3 + 3 Н 2 SO 4 = Аl 2(SO 4)3 + 6 Н 2 О Аl(ОН)3 + 3 КОН = К[Аl(ОН)4]
 • Гидроксид алюминия является слабым основанием и еще более слабой кислотой, поэтому соли алюминия находятся в растворе только в присутствии избытка кислоты, а алюминаты—только в присутствии избытка щелочи. При разбавлении растворов водой эти соединения сильно гидролизованы. • Высушенный гидроксид алюминия, потерявший часть воды, не растворяется ни в кислотах, ни в щелочах и этим напоминает оксид алюминия. • Гидроксид алюминия обладает свойствами поглощать различные вещества, поэтому его применяют при очистке воды.
• Гидроксид алюминия является слабым основанием и еще более слабой кислотой, поэтому соли алюминия находятся в растворе только в присутствии избытка кислоты, а алюминаты—только в присутствии избытка щелочи. При разбавлении растворов водой эти соединения сильно гидролизованы. • Высушенный гидроксид алюминия, потерявший часть воды, не растворяется ни в кислотах, ни в щелочах и этим напоминает оксид алюминия. • Гидроксид алюминия обладает свойствами поглощать различные вещества, поэтому его применяют при очистке воды.
 Особенности металлов d-элементов К металлам - элементам d - семейства относятся 32 элемента периодической системы. Они входят в 4 - 7 -ой большие периоды. Строение внешних электронных оболочек атомов описывается общей формулой (n-1)dx nsy, где х от 1 до 10, у от 1 до 2. У атомов III - Б группы появляется первый электрон на d - орбитали (Sc - скандий - 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 1). В последующих Б группах происходит заполнение d - подуровня до 10 электронов. Отсюда и название - d - семейство.
Особенности металлов d-элементов К металлам - элементам d - семейства относятся 32 элемента периодической системы. Они входят в 4 - 7 -ой большие периоды. Строение внешних электронных оболочек атомов описывается общей формулой (n-1)dx nsy, где х от 1 до 10, у от 1 до 2. У атомов III - Б группы появляется первый электрон на d - орбитали (Sc - скандий - 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 1). В последующих Б группах происходит заполнение d - подуровня до 10 электронов. Отсюда и название - d - семейство.
 • В периодах с увеличением заряда ядра очень незначительно изменяется радиус, энергия ионизации атома. Это объясняется проникновением n. S - электронов под d - электронный слой в соответствие с принципом наименьшей энергии (лантаноидное сжатие). • В группах Б сверху вниз уменьшаются металлические свойства, хотя все d - элементы металлы, и, образуемые ими простые вещества, способны выступать в окислительно-восстановительных реакциях только восстановителями
• В периодах с увеличением заряда ядра очень незначительно изменяется радиус, энергия ионизации атома. Это объясняется проникновением n. S - электронов под d - электронный слой в соответствие с принципом наименьшей энергии (лантаноидное сжатие). • В группах Б сверху вниз уменьшаются металлические свойства, хотя все d - элементы металлы, и, образуемые ими простые вещества, способны выступать в окислительно-восстановительных реакциях только восстановителями
 • d - элементы отличаются набором разных степеней окисления элементов: Mn от +2 до +7 (+2; +3; +4; +6; +7) Ti от +2 до +4 (+2; +3; +4) Cr от +2 до +6 (+2; +3; +4; +6) • Низшая степень окисления обусловливает основные и восстановительные свойства, ей соответствует катионная форма d - элемента: Mn 2+; Mn(ОН)2; Mn+2 - 5 e → Mn+7
• d - элементы отличаются набором разных степеней окисления элементов: Mn от +2 до +7 (+2; +3; +4; +6; +7) Ti от +2 до +4 (+2; +3; +4) Cr от +2 до +6 (+2; +3; +4; +6) • Низшая степень окисления обусловливает основные и восстановительные свойства, ей соответствует катионная форма d - элемента: Mn 2+; Mn(ОН)2; Mn+2 - 5 e → Mn+7
 • С увеличением степень окисления элемента происходит усиление окислительной способности и кислотных свойств соединения. • Амфотерные свойства более типичны для соединений с промежуточными степенями окисления: Cr+2 О - основной оксид Cr 2+3 О 3 - амфотерный оксид Cr+6 О 3 - кислотный оксид
• С увеличением степень окисления элемента происходит усиление окислительной способности и кислотных свойств соединения. • Амфотерные свойства более типичны для соединений с промежуточными степенями окисления: Cr+2 О - основной оксид Cr 2+3 О 3 - амфотерный оксид Cr+6 О 3 - кислотный оксид
 В периоде с увеличением заряда ядра уменьшается устойчивость соединений с высшей степенью окисления, и одновременно возрастают их окислительные свойства. Сильными окислителями являются: (Cr+62 О 7)2 - - бихромат - ион; =+1, 33 В; (Mn+7 О 4)- - перманганат - ион; =+1, 51 В; (Fe+6 О 4)2 - - феррат - ион; =+1, 90 В; Возрастание о-в потенциала свидетельствует о возрастании окислительной способности. В группах с увеличением заряда ядра увеличивается устойчивость соединений с высшей степенью окисления, и одновременно уменьшаются их окислительные свойства.
В периоде с увеличением заряда ядра уменьшается устойчивость соединений с высшей степенью окисления, и одновременно возрастают их окислительные свойства. Сильными окислителями являются: (Cr+62 О 7)2 - - бихромат - ион; =+1, 33 В; (Mn+7 О 4)- - перманганат - ион; =+1, 51 В; (Fe+6 О 4)2 - - феррат - ион; =+1, 90 В; Возрастание о-в потенциала свидетельствует о возрастании окислительной способности. В группах с увеличением заряда ядра увеличивается устойчивость соединений с высшей степенью окисления, и одновременно уменьшаются их окислительные свойства.