Спирты альдегиды.pptx
- Количество слайдов: 41
 ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ Лекция Гидроксисоединения. Карбонильные соединения. 1. Спирты. 2. Фенолы. 3. Альдегиды и кетоны. Лектор: Ганзина Ирина Викторовна кандидат биологических наук, доцент
ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ Лекция Гидроксисоединения. Карбонильные соединения. 1. Спирты. 2. Фенолы. 3. Альдегиды и кетоны. Лектор: Ганзина Ирина Викторовна кандидат биологических наук, доцент
 Спирты • Гидроксисоединения – это вещества, которые в своем составе содержат –OH группы. К ним относят спирты, фенолы, нафтолы и др. вещества. • Спирты- это гидроксисоединения, в молекулах которых –OH группы связаны с насыщенным атомом углерода, находящимся в состоянии sp 3 -гибридизации. Общая формула спиртов R-OH
Спирты • Гидроксисоединения – это вещества, которые в своем составе содержат –OH группы. К ним относят спирты, фенолы, нафтолы и др. вещества. • Спирты- это гидроксисоединения, в молекулах которых –OH группы связаны с насыщенным атомом углерода, находящимся в состоянии sp 3 -гибридизации. Общая формула спиртов R-OH
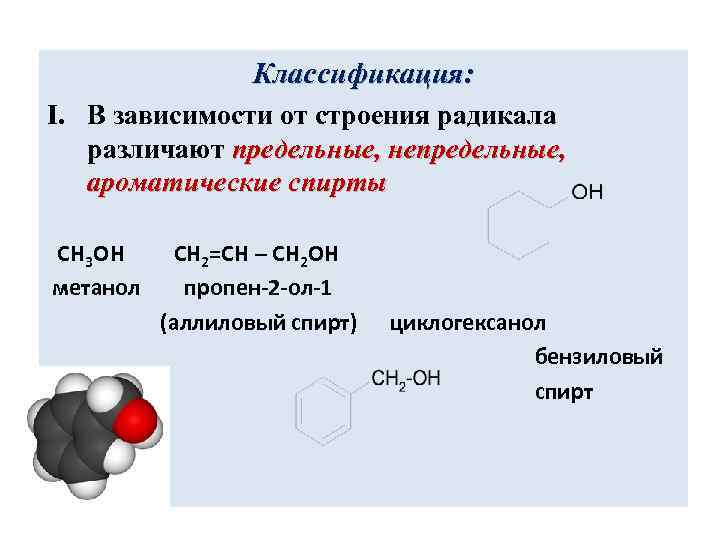 Классификация: I. В зависимости от строения радикала различают предельные, непредельные, ароматические спирты CH 3 OH метанол CH 2=CH – CH 2 OH пропен-2 -ол-1 (аллиловый спирт) циклогексанол бензиловый спирт
Классификация: I. В зависимости от строения радикала различают предельные, непредельные, ароматические спирты CH 3 OH метанол CH 2=CH – CH 2 OH пропен-2 -ол-1 (аллиловый спирт) циклогексанол бензиловый спирт
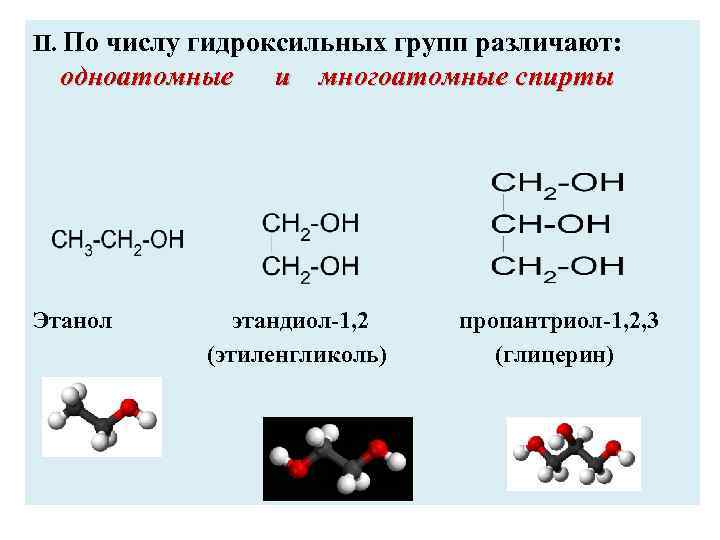 II. По числу гидроксильных групп различают: одноатомные Этанол и многоатомные спирты этандиол-1, 2 (этиленгликоль) пропантриол-1, 2, 3 (глицерин)
II. По числу гидроксильных групп различают: одноатомные Этанол и многоатомные спирты этандиол-1, 2 (этиленгликоль) пропантриол-1, 2, 3 (глицерин)
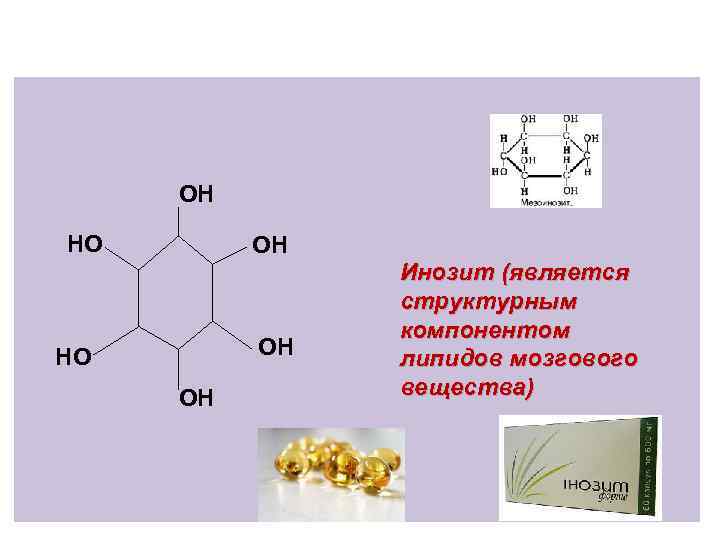 OH HO OH Инозит (является структурным компонентом липидов мозгового вещества)
OH HO OH Инозит (является структурным компонентом липидов мозгового вещества)
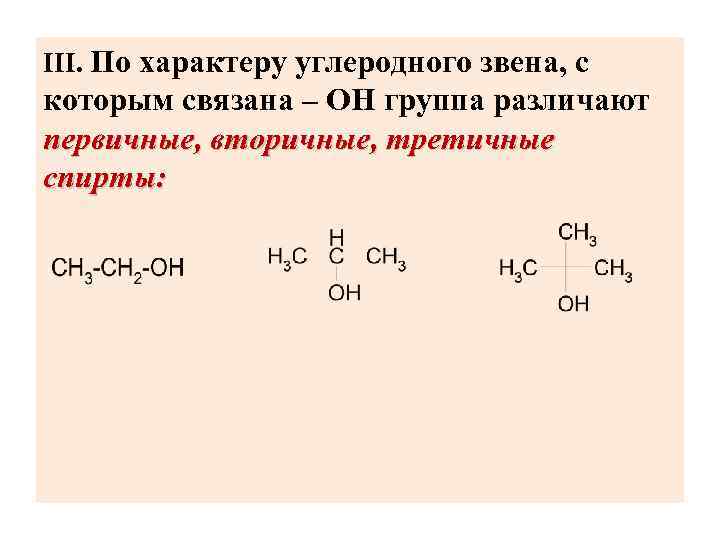 III. По характеру углеродного звена, с которым связана – ОН группа различают первичные, вторичные, третичные спирты:
III. По характеру углеродного звена, с которым связана – ОН группа различают первичные, вторичные, третичные спирты:
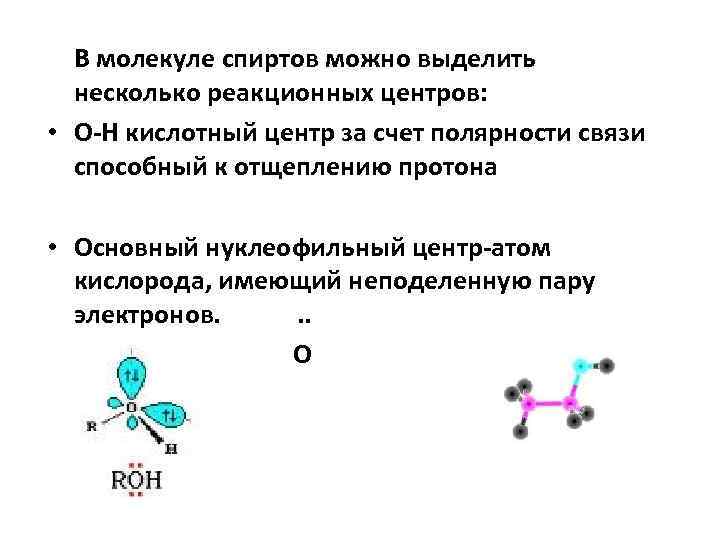 В молекуле спиртов можно выделить несколько реакционных центров: • О-Н кислотный центр за счет полярности связи способный к отщеплению протона • Основный нуклеофильный центр-атом кислорода, имеющий неподеленную пару электронов. . . О
В молекуле спиртов можно выделить несколько реакционных центров: • О-Н кислотный центр за счет полярности связи способный к отщеплению протона • Основный нуклеофильный центр-атом кислорода, имеющий неподеленную пару электронов. . . О
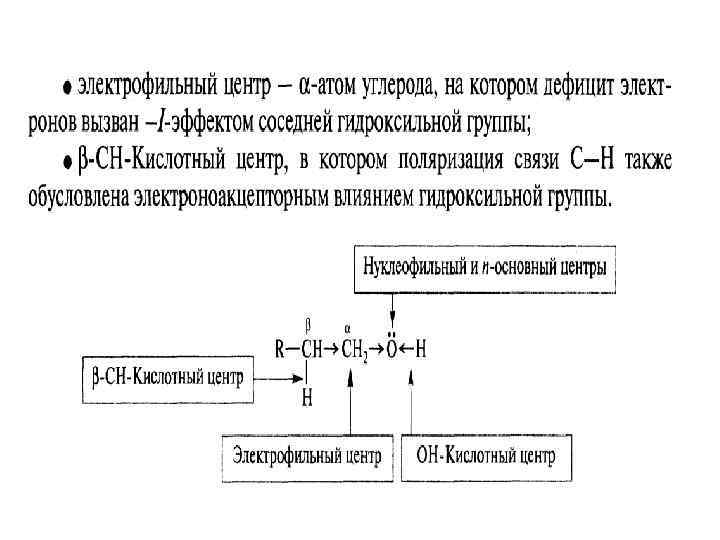
 Химические свойства спиртов I. Реакции окисления • Внутри организма (in vivo) эти реакции протекают с участием ферментов дегидрогеназ • Кофермент дегидрогеназы - НАД+ (никотинамиддинуклеотид окисленный) служит акцептором гидрид-иона (Н-) при биологическом дегидрировании субстрата. • НАД+ превращается при этом в восстановленную форму фермента-НАДН.
Химические свойства спиртов I. Реакции окисления • Внутри организма (in vivo) эти реакции протекают с участием ферментов дегидрогеназ • Кофермент дегидрогеназы - НАД+ (никотинамиддинуклеотид окисленный) служит акцептором гидрид-иона (Н-) при биологическом дегидрировании субстрата. • НАД+ превращается при этом в восстановленную форму фермента-НАДН.
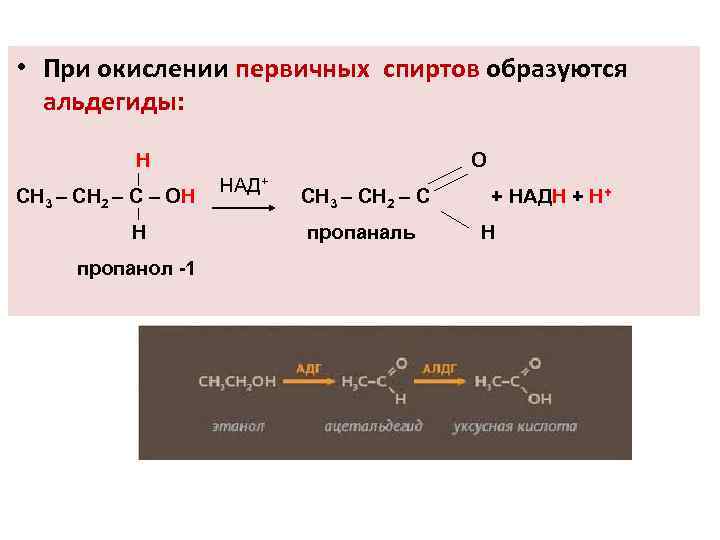 • При окислении первичных спиртов образуются альдегиды: Н СН 3 – СН 2 – С – ОН Н пропанол -1 О НАД+ СН 3 – СН 2 – С пропаналь + НАДН + Н+ Н
• При окислении первичных спиртов образуются альдегиды: Н СН 3 – СН 2 – С – ОН Н пропанол -1 О НАД+ СН 3 – СН 2 – С пропаналь + НАДН + Н+ Н
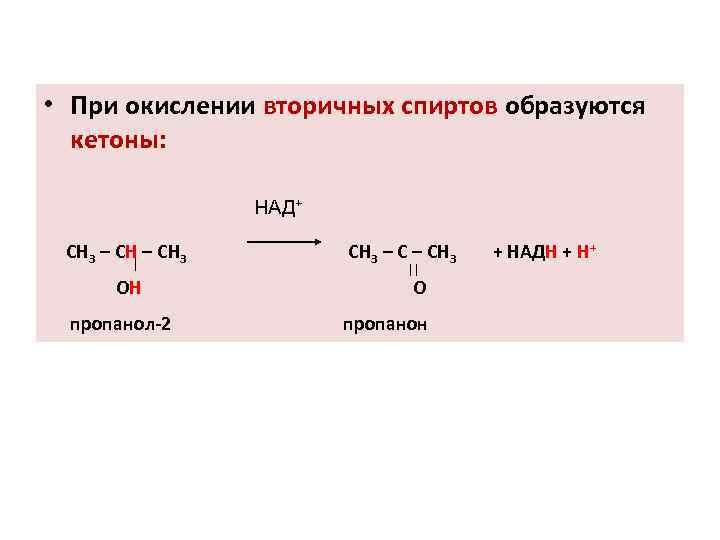 • При окислении вторичных спиртов образуются кетоны: НАД+ СН 3 – СН 3 ОН пропанол-2 СН 3 – СН 3 О пропанон + НАДН + Н+
• При окислении вторичных спиртов образуются кетоны: НАД+ СН 3 – СН 3 ОН пропанол-2 СН 3 – СН 3 О пропанон + НАДН + Н+
 2. Спирты проявляют слабые кислотные и слабые основные свойства, то есть являются амфолитами. • Спирты как кислоты реагируют со щелочными металлами, образуя алкоголяты, которые в растворах гидролизуются: 2 CH 3 CH 2 OH + 2 Na → 2 CH 3 CH 2 ONa + H 2 O → CH 3 CH 2 OH + Na. OH По кислотным свойствам спирты уступают воде.
2. Спирты проявляют слабые кислотные и слабые основные свойства, то есть являются амфолитами. • Спирты как кислоты реагируют со щелочными металлами, образуя алкоголяты, которые в растворах гидролизуются: 2 CH 3 CH 2 OH + 2 Na → 2 CH 3 CH 2 ONa + H 2 O → CH 3 CH 2 OH + Na. OH По кислотным свойствам спирты уступают воде.
 • Основные свойства спиртов обусловлены наличием на атоме кислорода гидроксильной группы неподеленной пары электронов, способной присоединять протон. R-ОН + Н+ → R- О+ Н катион ¨ l оксония Н
• Основные свойства спиртов обусловлены наличием на атоме кислорода гидроксильной группы неподеленной пары электронов, способной присоединять протон. R-ОН + Н+ → R- О+ Н катион ¨ l оксония Н
 3. Реакция нуклеофильного замещения (SN) • Реакции SN гидроксильной группы протекают по месту гетеролитического разрыва полярной связи С-ОН. • Поскольку ОН-группа является плохо уходящей группой, то прямое нуклеофильное замещение на галоген невозможно. • Поэтому ОН-группу в присутствии кислотного катализатора-ионов Н+ -переводят в оксониевую группировку, с образованием промежуточного иона алкилоксония.
3. Реакция нуклеофильного замещения (SN) • Реакции SN гидроксильной группы протекают по месту гетеролитического разрыва полярной связи С-ОН. • Поскольку ОН-группа является плохо уходящей группой, то прямое нуклеофильное замещение на галоген невозможно. • Поэтому ОН-группу в присутствии кислотного катализатора-ионов Н+ -переводят в оксониевую группировку, с образованием промежуточного иона алкилоксония.
 • Тем самым плохоуходящая группа –ОН превращается в легкоуходящую группу атомов, которая затем отделяется в виде молекулы воды (нуклеофуг). • Реагент – нуклеофил (Сl- )присодиняется к атому углерода, образуя продукт.
• Тем самым плохоуходящая группа –ОН превращается в легкоуходящую группу атомов, которая затем отделяется в виде молекулы воды (нуклеофуг). • Реагент – нуклеофил (Сl- )присодиняется к атому углерода, образуя продукт.
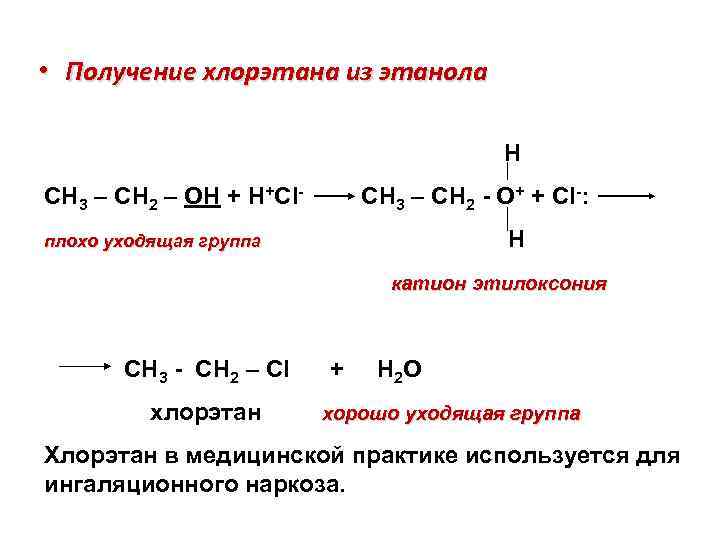 • Получение хлорэтана из этанола Н СН 3 – СН 2 – ОН + Н+Cl- CН 3 – СН 2 - О+ + Cl-: Н плохо уходящая группа катион этилоксония СН 3 - СН 2 – Сl хлорэтан + Н 2 О хорошо уходящая группа Хлорэтан в медицинской практике используется для ингаляционного наркоза.
• Получение хлорэтана из этанола Н СН 3 – СН 2 – ОН + Н+Cl- CН 3 – СН 2 - О+ + Cl-: Н плохо уходящая группа катион этилоксония СН 3 - СН 2 – Сl хлорэтан + Н 2 О хорошо уходящая группа Хлорэтан в медицинской практике используется для ингаляционного наркоза.
 4. Реакция хелатообразования • Многоатомные спирты, проявляют более выраженные кислотные свойства по сравнению с одноатомными спиртами При взаимодействии с Сu(ОН)2 в щелочной среде образуют растворимый хелатный комплекс ярко синего цвета. • Данная реакция используется для качественного обнаружения многоатомных спиртов. В реакцию при этом вступает α-диольный фрагмент структуры (две –ОН группы в соседних звеньях).
4. Реакция хелатообразования • Многоатомные спирты, проявляют более выраженные кислотные свойства по сравнению с одноатомными спиртами При взаимодействии с Сu(ОН)2 в щелочной среде образуют растворимый хелатный комплекс ярко синего цвета. • Данная реакция используется для качественного обнаружения многоатомных спиртов. В реакцию при этом вступает α-диольный фрагмент структуры (две –ОН группы в соседних звеньях).
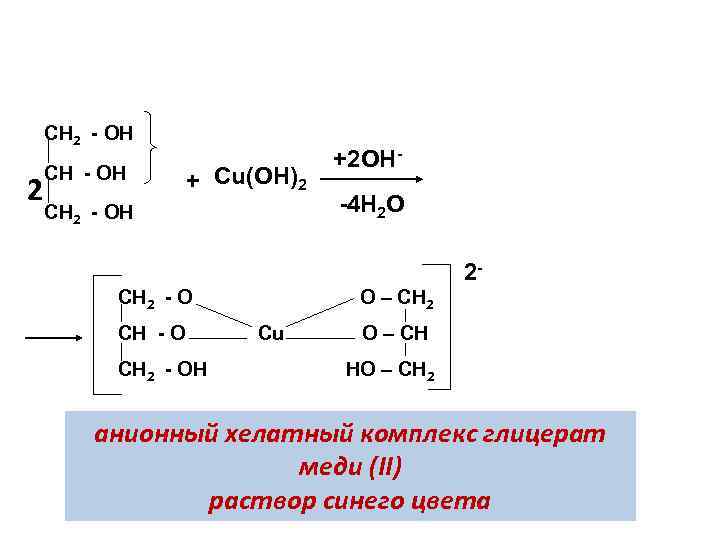 CH 2 - OH 2 CH - OH + Cu(ОН)2 CH 2 - OH +2 ОН-4 Н 2 О 2 - CH 2 - OH О – СН 2 Cu О – СН НО – СН 2 анионный хелатный комплекс глицерат меди (II) раствор синего цвета
CH 2 - OH 2 CH - OH + Cu(ОН)2 CH 2 - OH +2 ОН-4 Н 2 О 2 - CH 2 - OH О – СН 2 Cu О – СН НО – СН 2 анионный хелатный комплекс глицерат меди (II) раствор синего цвета
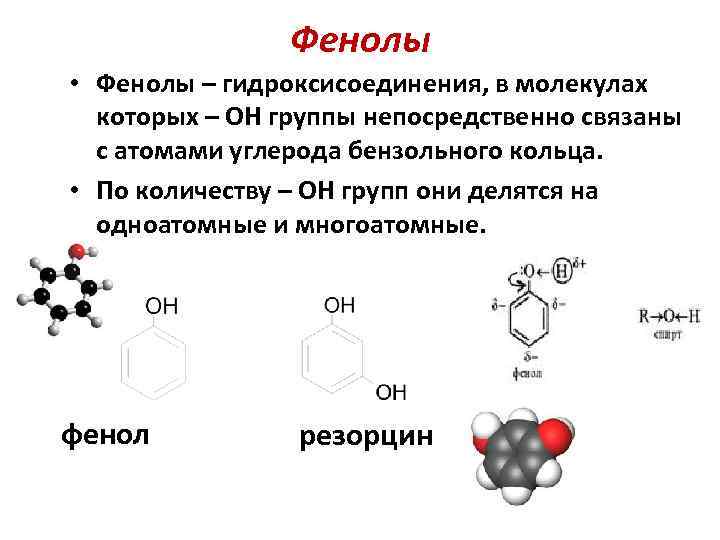 Фенолы • Фенолы – гидроксисоединения, в молекулах которых – OH группы непосредственно связаны с атомами углерода бензольного кольца. • По количеству – OH групп они делятся на одноатомные и многоатомные. фенол резорцин
Фенолы • Фенолы – гидроксисоединения, в молекулах которых – OH группы непосредственно связаны с атомами углерода бензольного кольца. • По количеству – OH групп они делятся на одноатомные и многоатомные. фенол резорцин
 • Фенол(раствор-карболовая кислота) применяется в медицине как антисептическое средство, используется для приготовления лекарственных веществ, красителей и др. • Резорцин(1, 3 дигидроксибензол) применяется в виде водных и спиртовых растворов для лечения кожных и инфекционных заболеваний. Смесь насыщенного резорцина и формалина (40% раствор) применяется в стоматологии для пломбирования корневых зубных каналов.
• Фенол(раствор-карболовая кислота) применяется в медицине как антисептическое средство, используется для приготовления лекарственных веществ, красителей и др. • Резорцин(1, 3 дигидроксибензол) применяется в виде водных и спиртовых растворов для лечения кожных и инфекционных заболеваний. Смесь насыщенного резорцина и формалина (40% раствор) применяется в стоматологии для пломбирования корневых зубных каналов.
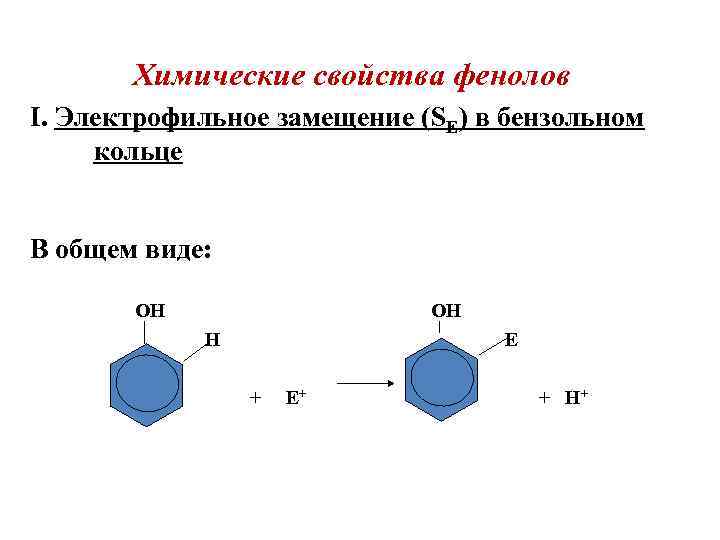 Химические свойства фенолов I. Электрофильное замещение (SЕ) в бензольном кольце В общем виде: OH OH H E + E+ + H+
Химические свойства фенолов I. Электрофильное замещение (SЕ) в бензольном кольце В общем виде: OH OH H E + E+ + H+
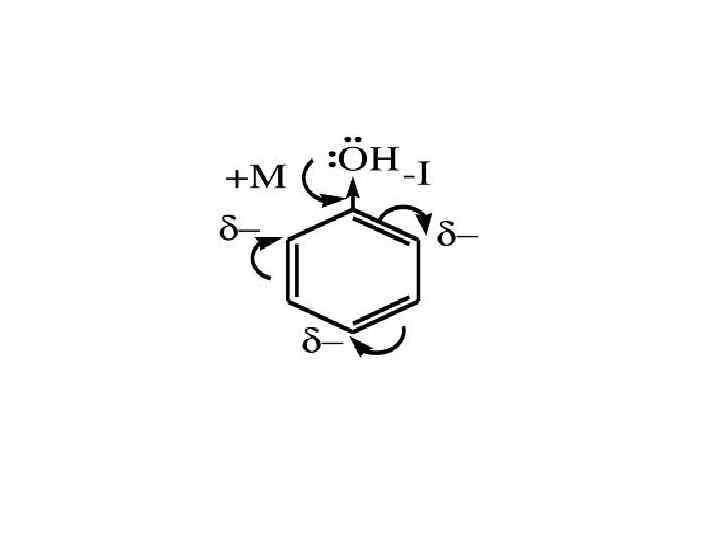
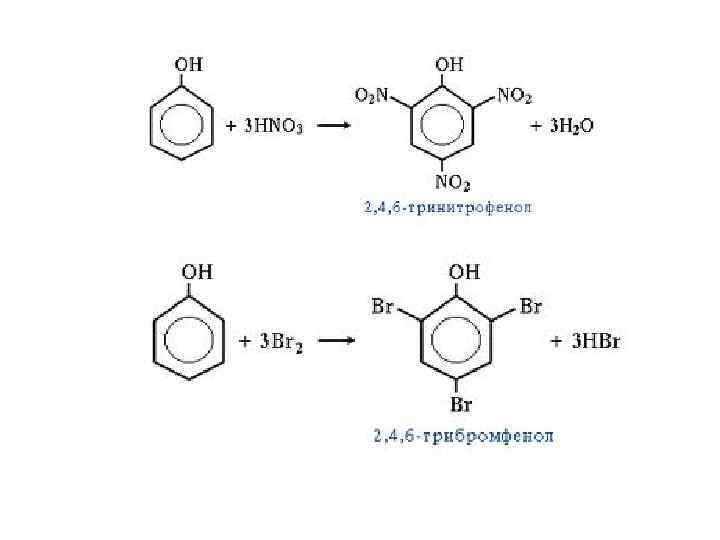
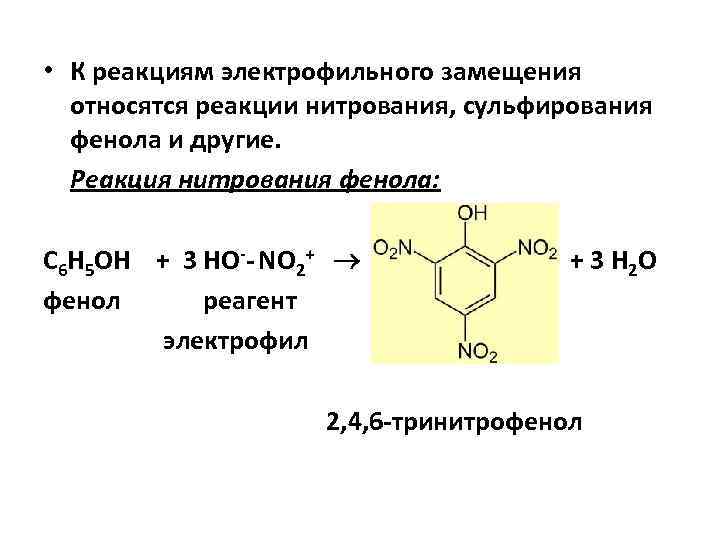 • К реакциям электрофильного замещения относятся реакции нитрования, сульфирования фенола и другие. Реакция нитрования фенола: С 6 Н 5 ОН + 3 НО-- NO 2+ фенол реагент электрофил + 3 Н 2 О 2, 4, 6 -тринитрофенол
• К реакциям электрофильного замещения относятся реакции нитрования, сульфирования фенола и другие. Реакция нитрования фенола: С 6 Н 5 ОН + 3 НО-- NO 2+ фенол реагент электрофил + 3 Н 2 О 2, 4, 6 -тринитрофенол
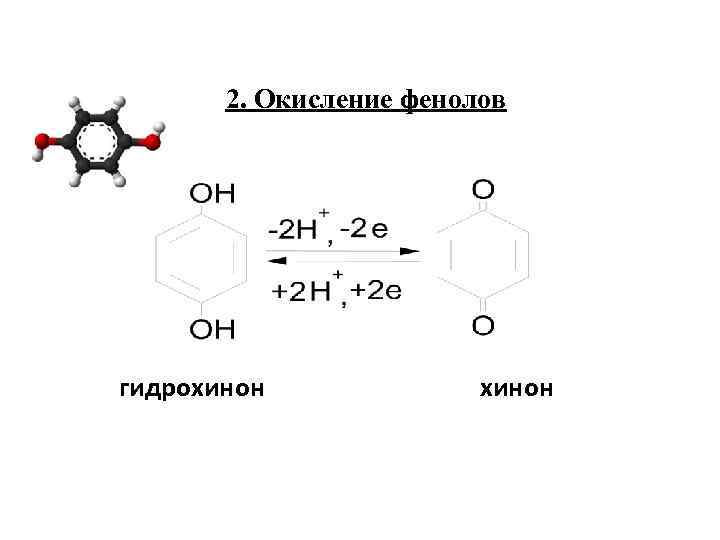 2. Окисление фенолов гидрохинон
2. Окисление фенолов гидрохинон
 • Система хинон-гидрохинон in vivo участвует в переносе электронов от субстрата к кислороду через систему цитохромов. • Хиноны широко распространены в природе и играют роль стимуляторов роста, антибиотиков.
• Система хинон-гидрохинон in vivo участвует в переносе электронов от субстрата к кислороду через систему цитохромов. • Хиноны широко распространены в природе и играют роль стимуляторов роста, антибиотиков.
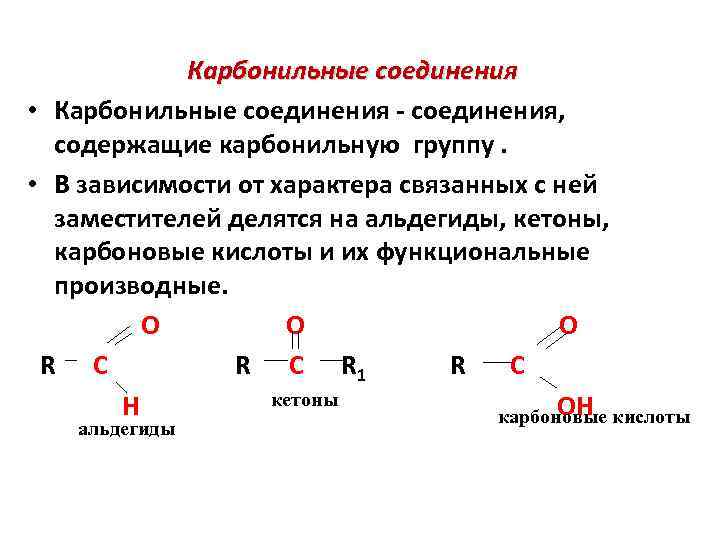 Карбонильные соединения • Карбонильные соединения - соединения, содержащие карбонильную группу. • В зависимости от характера связанных с ней заместителей делятся на альдегиды, кетоны, карбоновые кислоты и их функциональные производные. O O O R C R 1 R C кетоны H OH карбоновые кислоты альдегиды
Карбонильные соединения • Карбонильные соединения - соединения, содержащие карбонильную группу. • В зависимости от характера связанных с ней заместителей делятся на альдегиды, кетоны, карбоновые кислоты и их функциональные производные. O O O R C R 1 R C кетоны H OH карбоновые кислоты альдегиды
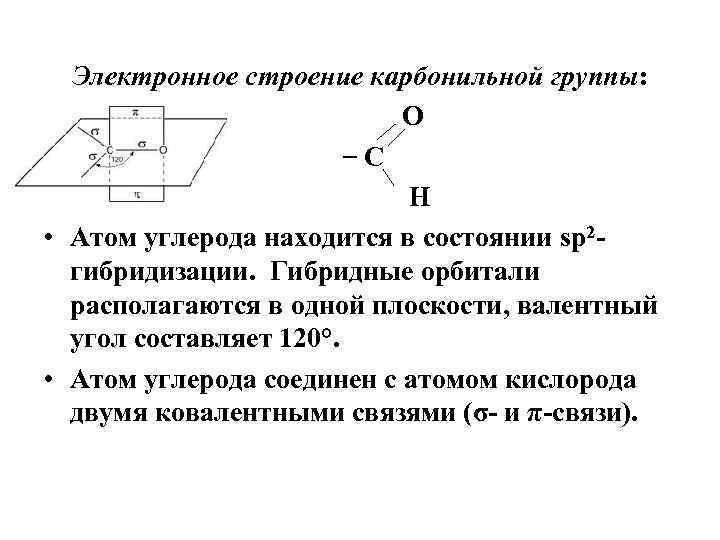 Электронное строение карбонильной группы: О С Н • Атом углерода находится в состоянии sp 2 гибридизации. Гибридные орбитали располагаются в одной плоскости, валентный угол составляет 120°. • Атом углерода соединен с атомом кислорода двумя ковалентными связями (σ- и π-связи).
Электронное строение карбонильной группы: О С Н • Атом углерода находится в состоянии sp 2 гибридизации. Гибридные орбитали располагаются в одной плоскости, валентный угол составляет 120°. • Атом углерода соединен с атомом кислорода двумя ковалентными связями (σ- и π-связи).
 • π-связь сильно поляризована, её электронная плотность смещена к более электроотрицательному атому кислороду, на котором возникает частичный отрицательный заряд. • На атоме углерода при этом наблюдается недостаток электронной плотности.
• π-связь сильно поляризована, её электронная плотность смещена к более электроотрицательному атому кислороду, на котором возникает частичный отрицательный заряд. • На атоме углерода при этом наблюдается недостаток электронной плотности.
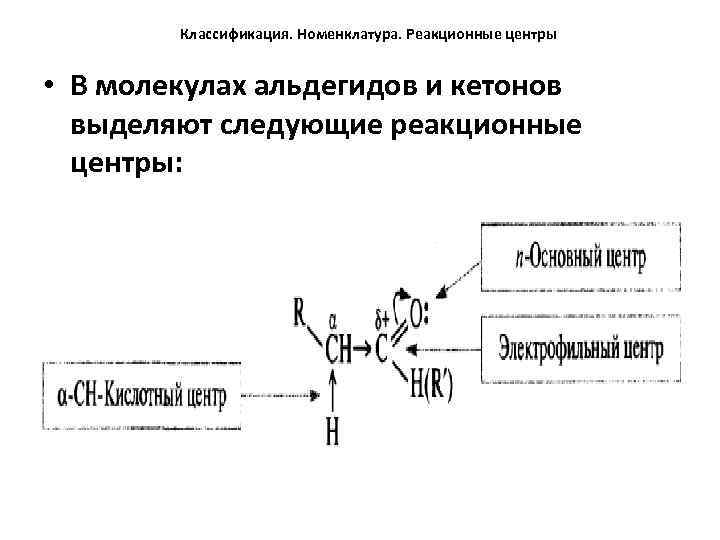 Классификация. Номенклатура. Реакционные центры • В молекулах альдегидов и кетонов выделяют следующие реакционные центры:
Классификация. Номенклатура. Реакционные центры • В молекулах альдегидов и кетонов выделяют следующие реакционные центры:
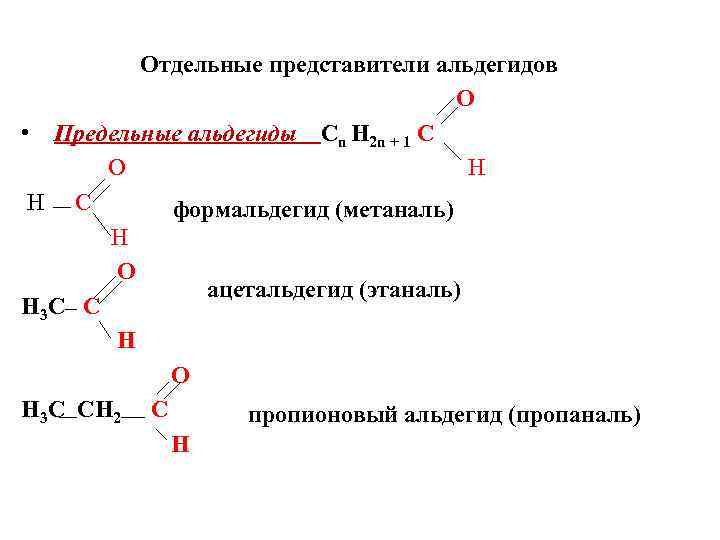 Отдельные представители альдегидов O • Предельные альдегиды Cn Н 2 n + 1 C O H H C формальдегид (метаналь) H O ацетальдегид (этаналь) H 3 C C H O H 3 C CH 2 C пропионовый альдегид (пропаналь) H
Отдельные представители альдегидов O • Предельные альдегиды Cn Н 2 n + 1 C O H H C формальдегид (метаналь) H O ацетальдегид (этаналь) H 3 C C H O H 3 C CH 2 C пропионовый альдегид (пропаналь) H
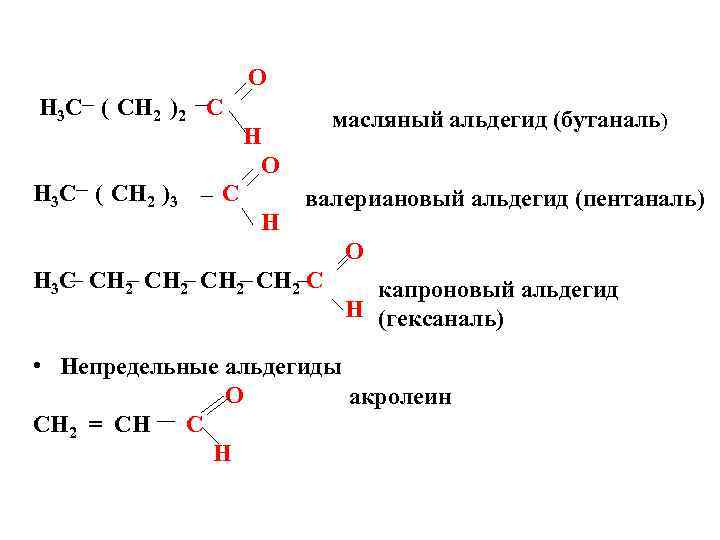 O H 3 C ( CH 2 )2 C H 3 C ( CH 2 )3 масляный альдегид (бутаналь) H O C H валериановый альдегид (пентаналь) O H 3 C CH 2 C капроновый альдегид H (гексаналь) • Непредельные альдегиды O акролеин CH 2 = CH С H
O H 3 C ( CH 2 )2 C H 3 C ( CH 2 )3 масляный альдегид (бутаналь) H O C H валериановый альдегид (пентаналь) O H 3 C CH 2 C капроновый альдегид H (гексаналь) • Непредельные альдегиды O акролеин CH 2 = CH С H
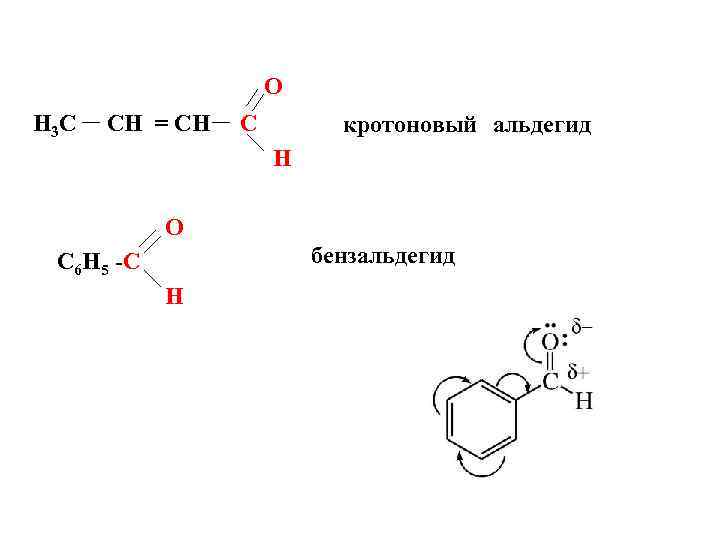 O H 3 C CH = CH C кротоновый альдегид H O бензальдегид C 6 H 5 -C H
O H 3 C CH = CH C кротоновый альдегид H O бензальдегид C 6 H 5 -C H
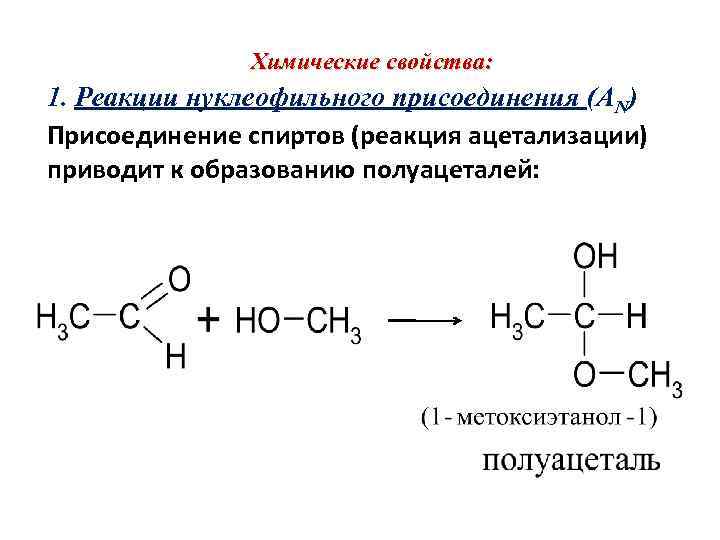 Химические свойства: 1. Реакции нуклеофильного присоединения (AN) Присоединение спиртов (реакция ацетализации) приводит к образованию полуацеталей:
Химические свойства: 1. Реакции нуклеофильного присоединения (AN) Присоединение спиртов (реакция ацетализации) приводит к образованию полуацеталей:
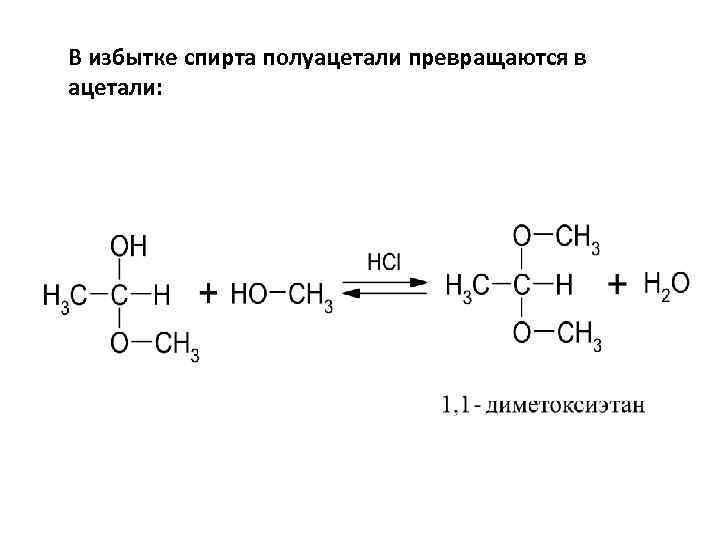 В избытке спирта полуацетали превращаются в ацетали:
В избытке спирта полуацетали превращаются в ацетали:
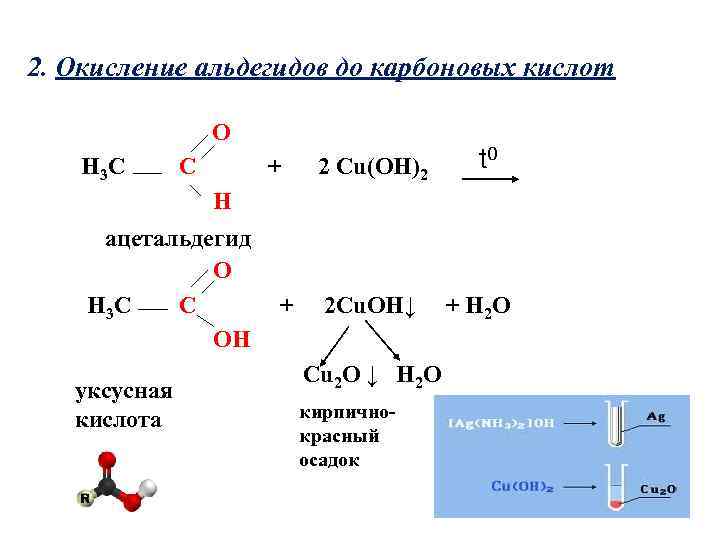 2. Окисление альдегидов до карбоновых кислот O H 3 C C + 2 Cu(OH)2 t 0 H ацетальдегид O H 3 C C OH уксусная кислота + 2 Cu. OH↓ Cu 2 O ↓ H 2 O кирпичнокрасный осадок + H 2 O
2. Окисление альдегидов до карбоновых кислот O H 3 C C + 2 Cu(OH)2 t 0 H ацетальдегид O H 3 C C OH уксусная кислота + 2 Cu. OH↓ Cu 2 O ↓ H 2 O кирпичнокрасный осадок + H 2 O
 3. Альдольная и кротоновая конденсация • Под влиянием основных катализаторов альдегиды реагируют с образованием продуктов, имеющих удвоенную молекулярную массу по сравнению с исходной молекулой. В организме реакции конденсации происходят в присутствии ферментов альдолаз по механизму AN • Некоторые кетоны тоже способны к этой реакции, только в более жестких условиях.
3. Альдольная и кротоновая конденсация • Под влиянием основных катализаторов альдегиды реагируют с образованием продуктов, имеющих удвоенную молекулярную массу по сравнению с исходной молекулой. В организме реакции конденсации происходят в присутствии ферментов альдолаз по механизму AN • Некоторые кетоны тоже способны к этой реакции, только в более жестких условиях.
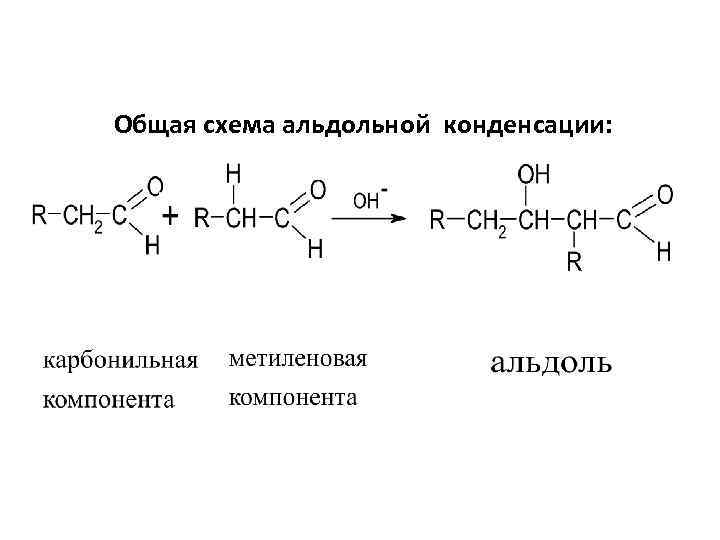 Общая схема альдольной конденсации:
Общая схема альдольной конденсации:
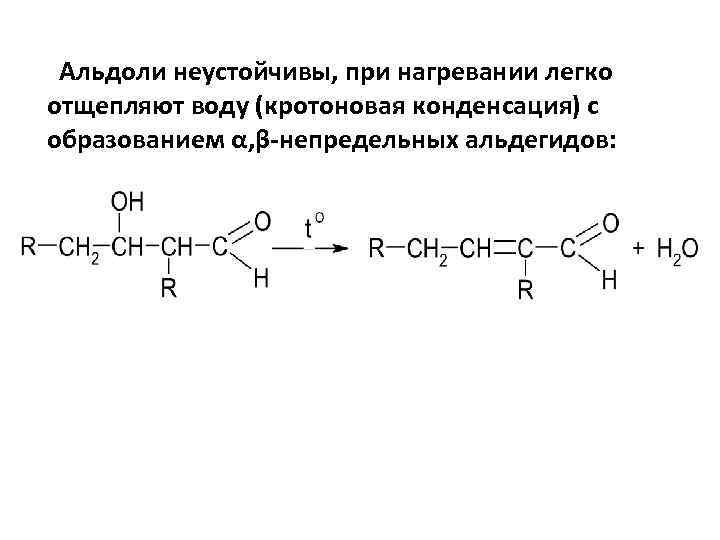 Альдоли неустойчивы, при нагревании легко отщепляют воду (кротоновая конденсация) с образованием α, β-непредельных альдегидов:
Альдоли неустойчивы, при нагревании легко отщепляют воду (кротоновая конденсация) с образованием α, β-непредельных альдегидов:
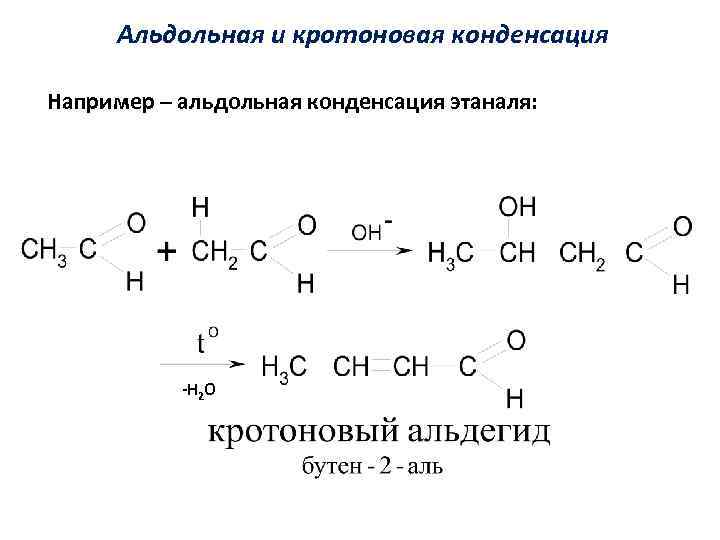 Альдольная и кротоновая конденсация Например – альдольная конденсация этаналя: -Н 2 О
Альдольная и кротоновая конденсация Например – альдольная конденсация этаналя: -Н 2 О
 БЛАГОДАРЮ ЗА ВНИМАНИЕ
БЛАГОДАРЮ ЗА ВНИМАНИЕ


