10 лекция Комплексныесоединения.ppt
- Количество слайдов: 101
 ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ Комплексные соединения 1. Строение комплексных соединений. Классификация. Номенклатура. 2. Устойчивость комплексных соединений. 3. Изомерия. 4. Комплексоны. Хелаты. Краун-эфиры. Лектор: Степанова Ирина Петровна доктор биологических наук, профессор, зав. кафедрой химии
ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ Комплексные соединения 1. Строение комплексных соединений. Классификация. Номенклатура. 2. Устойчивость комплексных соединений. 3. Изомерия. 4. Комплексоны. Хелаты. Краун-эфиры. Лектор: Степанова Ирина Петровна доктор биологических наук, профессор, зав. кафедрой химии
![Медико-биологическое значение темы [Ni(CO)4] [Fe(C 5 H 5)2] Медико-биологическое значение темы [Ni(CO)4] [Fe(C 5 H 5)2]](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-2.jpg) Медико-биологическое значение темы [Ni(CO)4] [Fe(C 5 H 5)2]
Медико-биологическое значение темы [Ni(CO)4] [Fe(C 5 H 5)2]
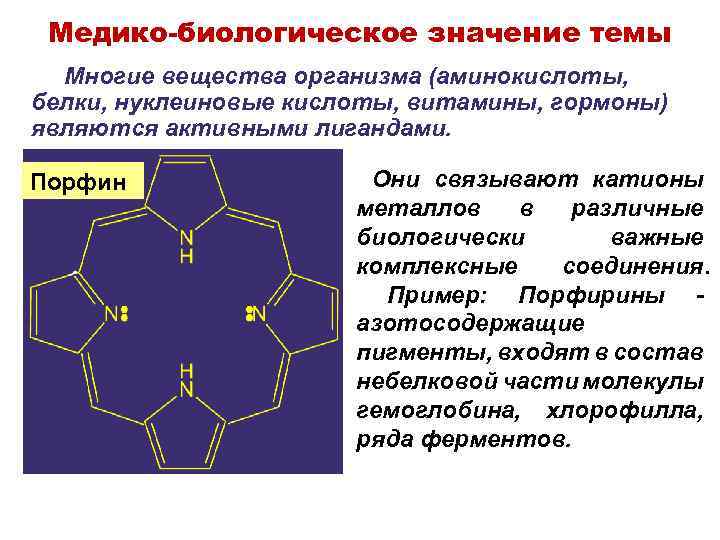 Медико-биологическое значение темы Многие вещества организма (аминокислоты, белки, нуклеиновые кислоты, витамины, гормоны) являются активными лигандами. Порфин Они связывают катионы металлов в различные биологически важные комплексные соединения. Пример: Порфирины азотосодержащие пигменты, входят в состав небелковой части молекулы гемоглобина, хлорофилла, ряда ферментов.
Медико-биологическое значение темы Многие вещества организма (аминокислоты, белки, нуклеиновые кислоты, витамины, гормоны) являются активными лигандами. Порфин Они связывают катионы металлов в различные биологически важные комплексные соединения. Пример: Порфирины азотосодержащие пигменты, входят в состав небелковой части молекулы гемоглобина, хлорофилла, ряда ферментов.
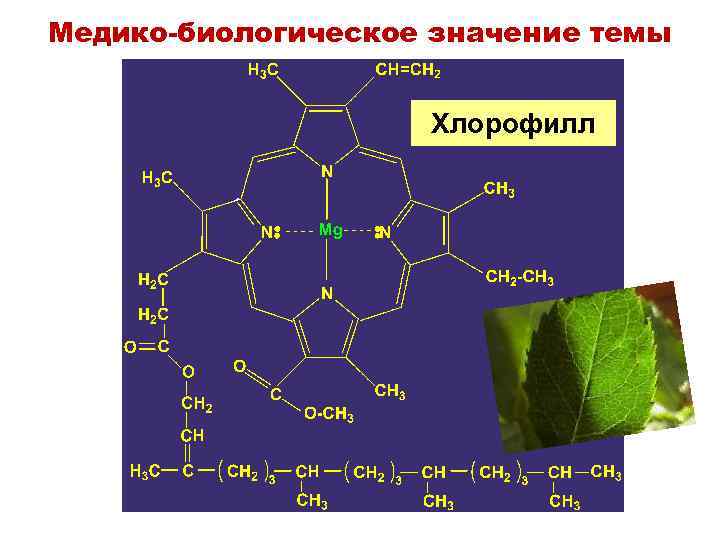 Медико-биологическое значение темы Хлорофилл
Медико-биологическое значение темы Хлорофилл
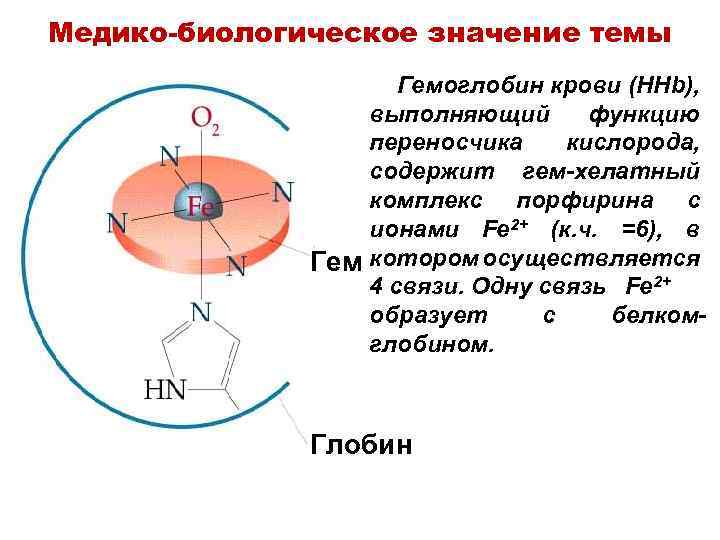 Медико-биологическое значение темы Гемоглобин крови (HHb), выполняющий функцию переносчика кислорода, содержит гем-хелатный комплекс порфирина с ионами Fe 2+ (к. ч. =6), в Гем котором осуществляется 4 связи. Одну связь Fe 2+ образует с белкомглобином. Глобин
Медико-биологическое значение темы Гемоглобин крови (HHb), выполняющий функцию переносчика кислорода, содержит гем-хелатный комплекс порфирина с ионами Fe 2+ (к. ч. =6), в Гем котором осуществляется 4 связи. Одну связь Fe 2+ образует с белкомглобином. Глобин
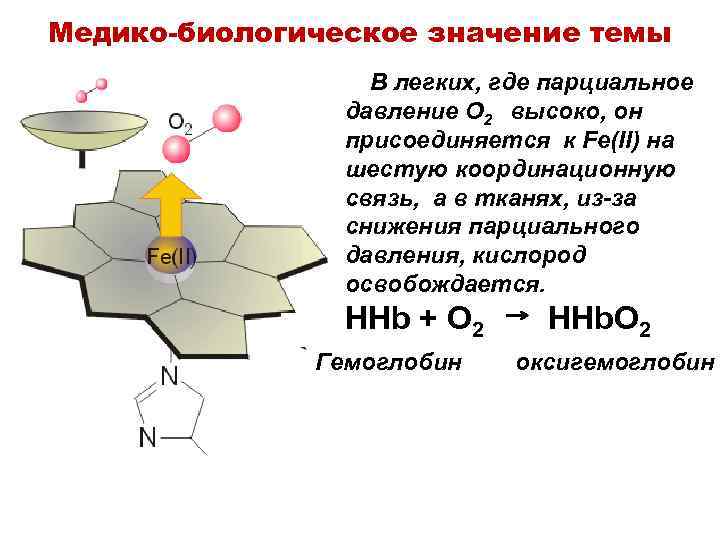 Медико-биологическое значение темы В легких, где парциальное давление O 2 высоко, он присоединяется к Fe(II) на шестую координационную связь, а в тканях, из-за снижения парциального давления, кислород освобождается. HHb + O 2 Гемоглобин HHb. O 2 оксигемоглобин
Медико-биологическое значение темы В легких, где парциальное давление O 2 высоко, он присоединяется к Fe(II) на шестую координационную связь, а в тканях, из-за снижения парциального давления, кислород освобождается. HHb + O 2 Гемоглобин HHb. O 2 оксигемоглобин
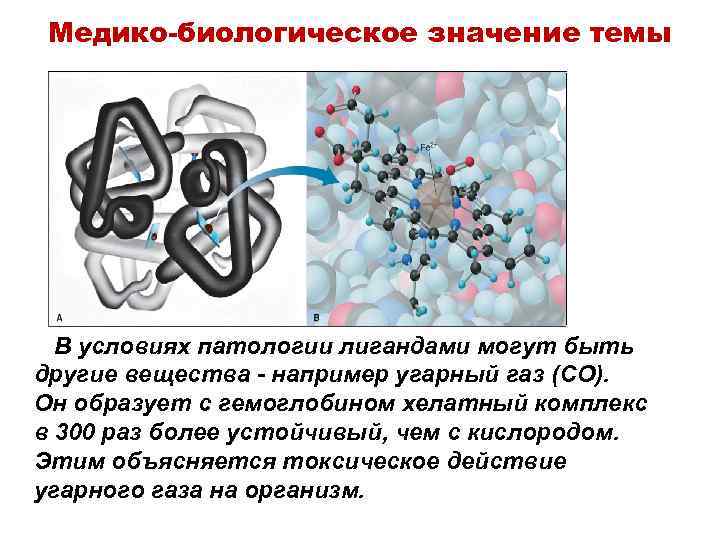 Медико-биологическое значение темы В условиях патологии лигандами могут быть другие вещества - например угарный газ (CO). Он образует с гемоглобином хелатный комплекс в 300 раз более устойчивый, чем с кислородом. Этим объясняется токсическое действие угарного газа на организм.
Медико-биологическое значение темы В условиях патологии лигандами могут быть другие вещества - например угарный газ (CO). Он образует с гемоглобином хелатный комплекс в 300 раз более устойчивый, чем с кислородом. Этим объясняется токсическое действие угарного газа на организм.
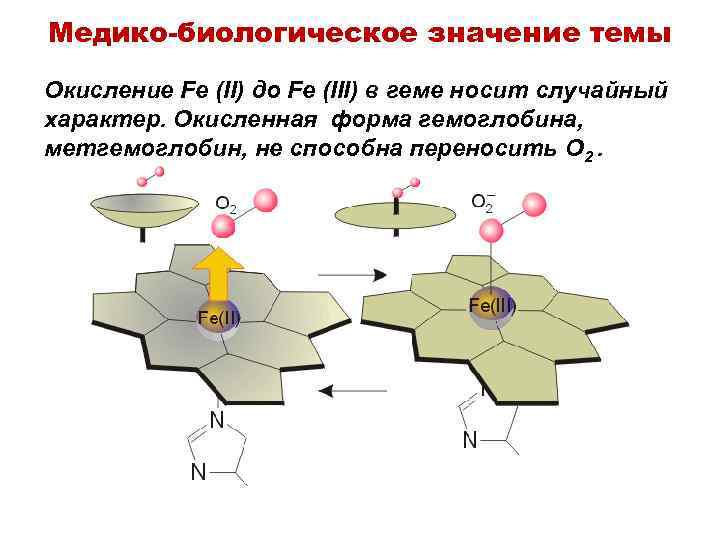 Медико-биологическое значение темы Окисление Fe (II) до Fe (III) в геме носит случайный характер. Окисленная форма гемоглобина, метгемоглобин, не способна переносить O 2.
Медико-биологическое значение темы Окисление Fe (II) до Fe (III) в геме носит случайный характер. Окисленная форма гемоглобина, метгемоглобин, не способна переносить O 2.
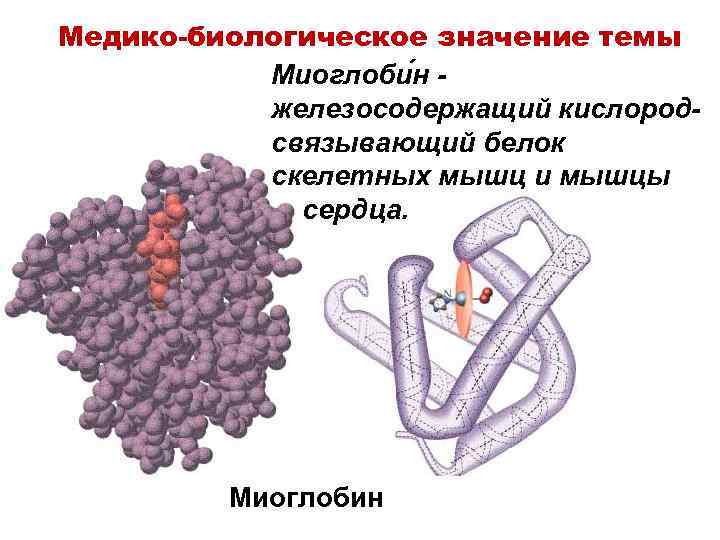 Медико-биологическое значение темы Миоглоби н железосодержащий кислородсвязывающий белок скелетных мышц и мышцы сердца. Миоглобин
Медико-биологическое значение темы Миоглоби н железосодержащий кислородсвязывающий белок скелетных мышц и мышцы сердца. Миоглобин
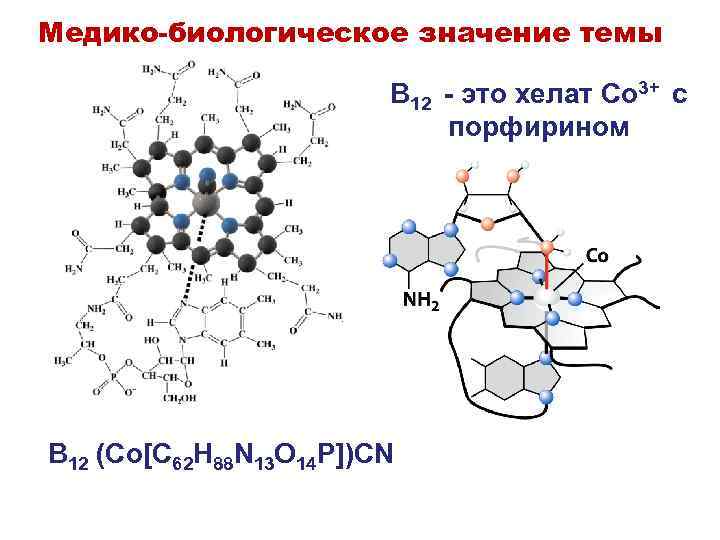 Медико-биологическое значение темы B 12 - это хелат Co 3+ c порфирином B 12 (Co[C 62 H 88 N 13 O 14 P])CN
Медико-биологическое значение темы B 12 - это хелат Co 3+ c порфирином B 12 (Co[C 62 H 88 N 13 O 14 P])CN
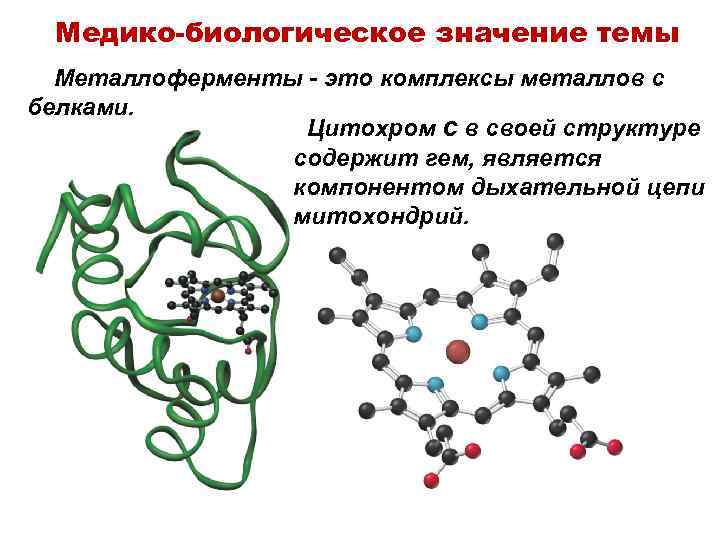 Медико-биологическое значение темы Металлоферменты - это комплексы металлов с белками. Цитохром с в своей структуре содержит гем, является компонентом дыхательной цепи митохондрий.
Медико-биологическое значение темы Металлоферменты - это комплексы металлов с белками. Цитохром с в своей структуре содержит гем, является компонентом дыхательной цепи митохондрий.
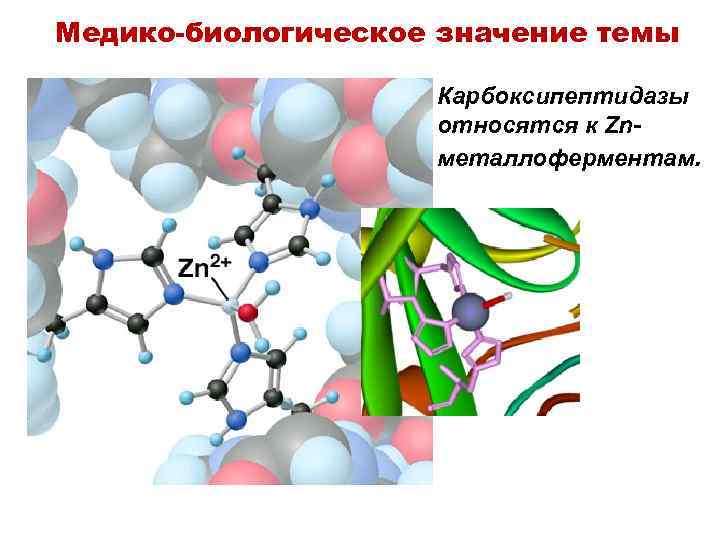 Медико-биологическое значение темы Карбоксипептидазы относятся к Znметаллоферментам.
Медико-биологическое значение темы Карбоксипептидазы относятся к Znметаллоферментам.
 Медико-биологическое значение темы Гормон инсулин - хелат Zn 2+ c белком.
Медико-биологическое значение темы Гормон инсулин - хелат Zn 2+ c белком.
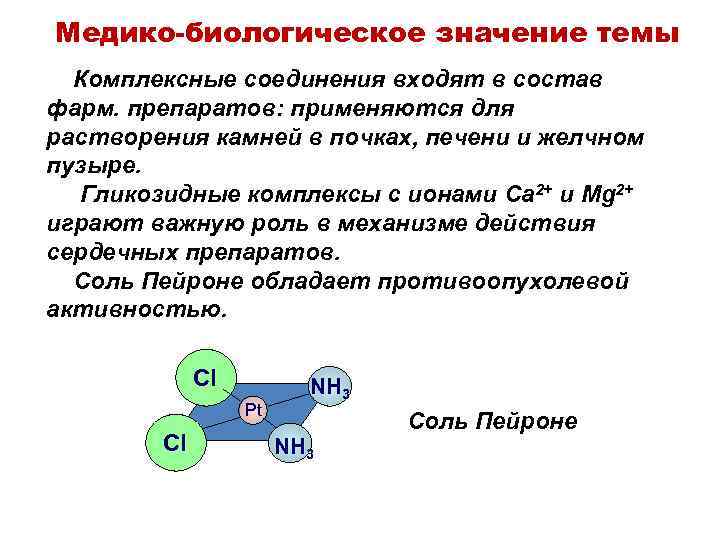 Медико-биологическое значение темы Комплексные соединения входят в состав фарм. препаратов: применяются для растворения камней в почках, печени и желчном пузыре. Гликозидные комплексы с ионами Ca 2+ и Mg 2+ играют важную роль в механизме действия сердечных препаратов. Соль Пейроне обладает противоопухолевой активностью. Cl Pt Cl NH 3 Соль Пейроне
Медико-биологическое значение темы Комплексные соединения входят в состав фарм. препаратов: применяются для растворения камней в почках, печени и желчном пузыре. Гликозидные комплексы с ионами Ca 2+ и Mg 2+ играют важную роль в механизме действия сердечных препаратов. Соль Пейроне обладает противоопухолевой активностью. Cl Pt Cl NH 3 Соль Пейроне
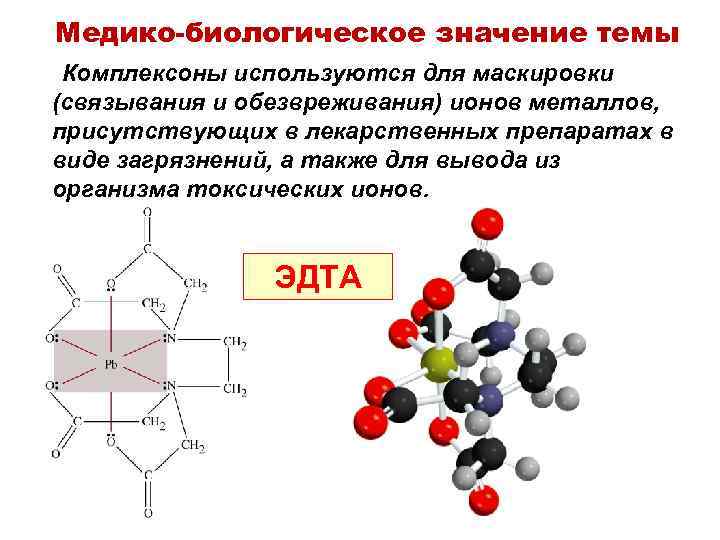 Медико-биологическое значение темы Комплексоны используются для маскировки (связывания и обезвреживания) ионов металлов, присутствующих в лекарственных препаратах в виде загрязнений, а также для вывода из организма токсических ионов. ЭДТА
Медико-биологическое значение темы Комплексоны используются для маскировки (связывания и обезвреживания) ионов металлов, присутствующих в лекарственных препаратах в виде загрязнений, а также для вывода из организма токсических ионов. ЭДТА
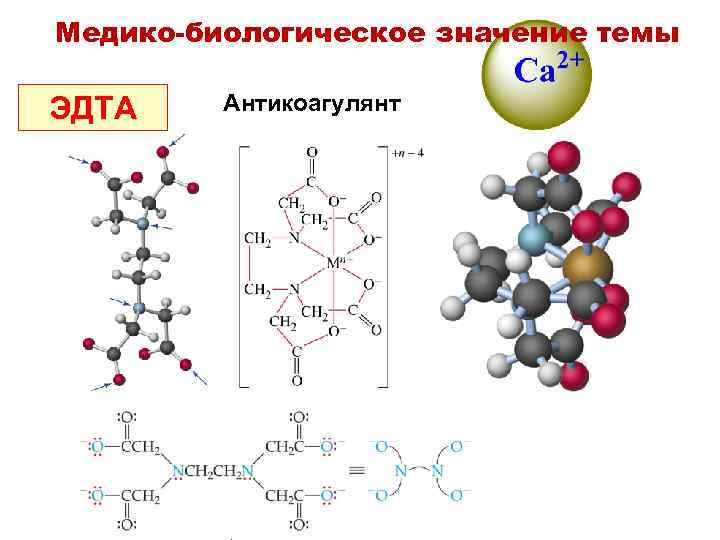 Медико-биологическое значение темы ЭДТА Антикоагулянт
Медико-биологическое значение темы ЭДТА Антикоагулянт
 Медико-биологическое значение темы Комплексные соединения часто имеют яркую окраску, поэтому их используют для проведения качественных реакций Cu. SO 4 · 5 H 2 O Ni. SO 4 · 7 H 2 O Co(NO 3)2 · 7 H 2 O
Медико-биологическое значение темы Комплексные соединения часто имеют яркую окраску, поэтому их используют для проведения качественных реакций Cu. SO 4 · 5 H 2 O Ni. SO 4 · 7 H 2 O Co(NO 3)2 · 7 H 2 O
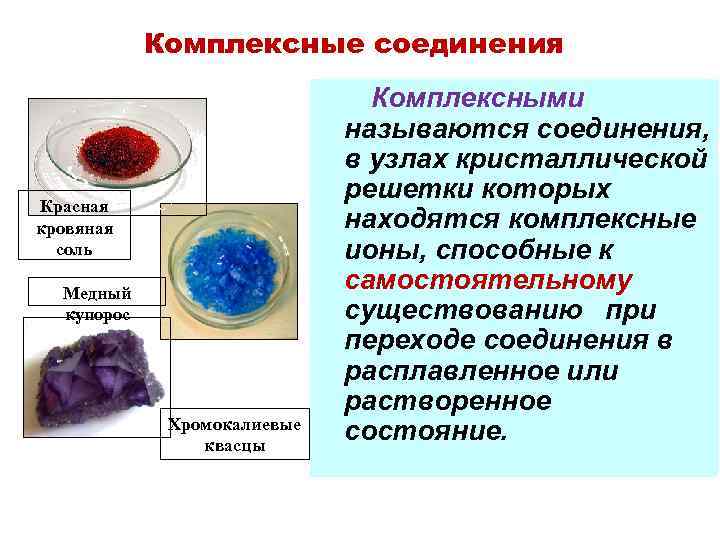 Комплексные соединения Комплексными Красная кровяная соль Медный купорос Хромокалиевые квасцы называются соединения, в узлах кристаллической решетки которых находятся комплексные ионы, способные к самостоятельному существованию при переходе соединения в расплавленное или растворенное состояние.
Комплексные соединения Комплексными Красная кровяная соль Медный купорос Хромокалиевые квасцы называются соединения, в узлах кристаллической решетки которых находятся комплексные ионы, способные к самостоятельному существованию при переходе соединения в расплавленное или растворенное состояние.
 Координационная теория А. Вернера (1893 г. ) "Меня часто охватывает экстаз пред красотой моей науки. Чем дальше я погружаюсь в ее тайны, тем более она кажется мне огромной, величественной, слишком красивой для простого смертного. " Альфред Вернер (1866 -1919), швейцарский химик
Координационная теория А. Вернера (1893 г. ) "Меня часто охватывает экстаз пред красотой моей науки. Чем дальше я погружаюсь в ее тайны, тем более она кажется мне огромной, величественной, слишком красивой для простого смертного. " Альфред Вернер (1866 -1919), швейцарский химик
![Строение комплексных соединений. Классификация. Номенклатура Внешняя сфера Внутренняя сфера K 3[Fe(CN)6] Ион. Координационное Комплексочисло Строение комплексных соединений. Классификация. Номенклатура Внешняя сфера Внутренняя сфера K 3[Fe(CN)6] Ион. Координационное Комплексочисло](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-20.jpg) Строение комплексных соединений. Классификация. Номенклатура Внешняя сфера Внутренняя сфера K 3[Fe(CN)6] Ион. Координационное Комплексочисло образователь Лиганды [Cu(NH 3)4]Cl 2 Внутренняя сфера Внешняя сфера
Строение комплексных соединений. Классификация. Номенклатура Внешняя сфера Внутренняя сфера K 3[Fe(CN)6] Ион. Координационное Комплексочисло образователь Лиганды [Cu(NH 3)4]Cl 2 Внутренняя сфера Внешняя сфера
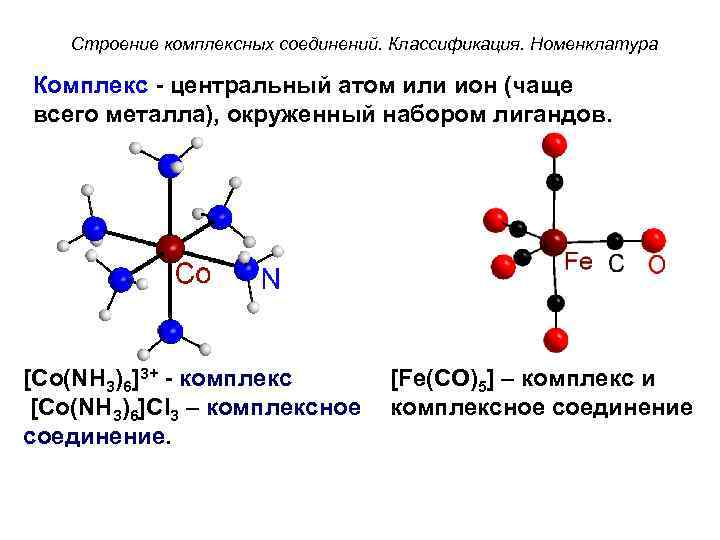 Строение комплексных соединений. Классификация. Номенклатура Комплекс - центральный атом или ион (чаще всего металла), окруженный набором лигандов. [Co(NH 3)6]3+ - комплекс [Co(NH 3)6]Cl 3 – комплексное соединение. [Fe(CO)5] – комплекс и комплексное соединение
Строение комплексных соединений. Классификация. Номенклатура Комплекс - центральный атом или ион (чаще всего металла), окруженный набором лигандов. [Co(NH 3)6]3+ - комплекс [Co(NH 3)6]Cl 3 – комплексное соединение. [Fe(CO)5] – комплекс и комплексное соединение
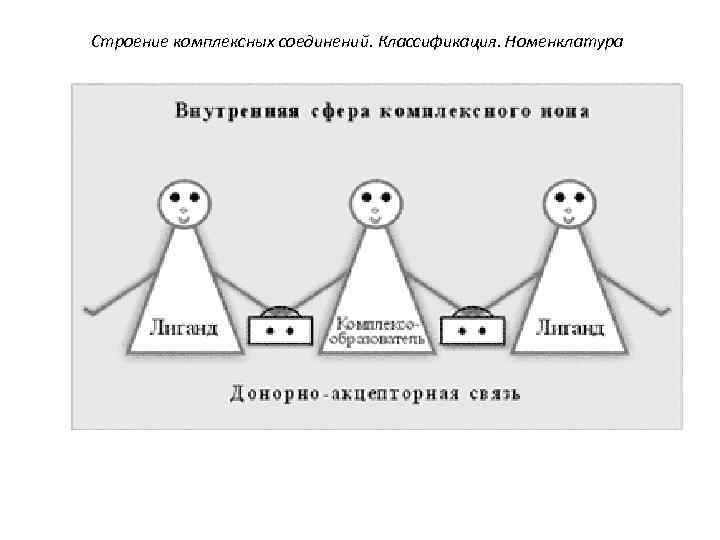
 Строение комплексных соединений. Классификация. Номенклатура 1. Внутренняя сфера комплекса включает центральный атом или ионкомплексообразователя, вокруг которого находятся связанные с ним лиганды - молекулы или ионы. При записи формул внутреннюю сферу выделяют квадратными скобками.
Строение комплексных соединений. Классификация. Номенклатура 1. Внутренняя сфера комплекса включает центральный атом или ионкомплексообразователя, вокруг которого находятся связанные с ним лиганды - молекулы или ионы. При записи формул внутреннюю сферу выделяют квадратными скобками.
 Строение комплексных соединений. Классификация. Номенклатура 2. Внешняя сфера - это совокупность ионов, непосредственно не связанных с центральным атомом комплексообразователя и удерживаемых около внутренней сферы электростатическими силами.
Строение комплексных соединений. Классификация. Номенклатура 2. Внешняя сфера - это совокупность ионов, непосредственно не связанных с центральным атомом комплексообразователя и удерживаемых около внутренней сферы электростатическими силами.
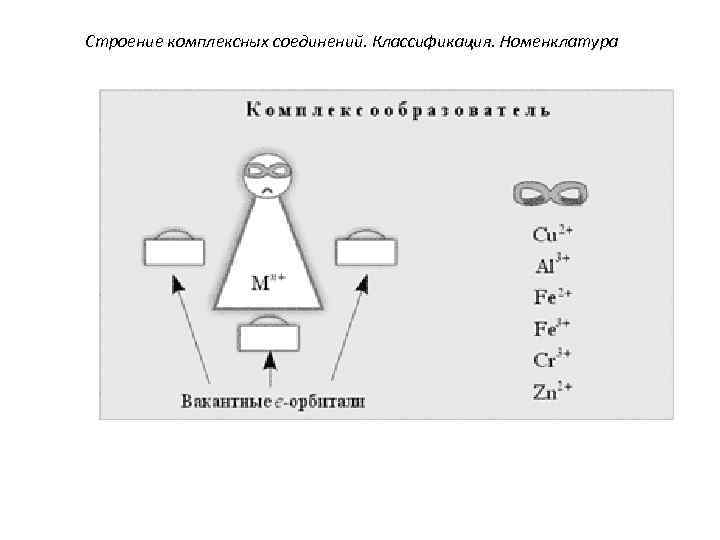
 Строение комплексных соединений. Классификация. Номенклатура 3. Комплексообразователями являются атомы или ионы металлов, имеющие свободные орбитали (чаще металлы d-элементы Co 3+, Cu 2+, Cu+, Fe 3+, Pt 2+ и др. ), т. е. они являются акцепторами электронов.
Строение комплексных соединений. Классификация. Номенклатура 3. Комплексообразователями являются атомы или ионы металлов, имеющие свободные орбитали (чаще металлы d-элементы Co 3+, Cu 2+, Cu+, Fe 3+, Pt 2+ и др. ), т. е. они являются акцепторами электронов.
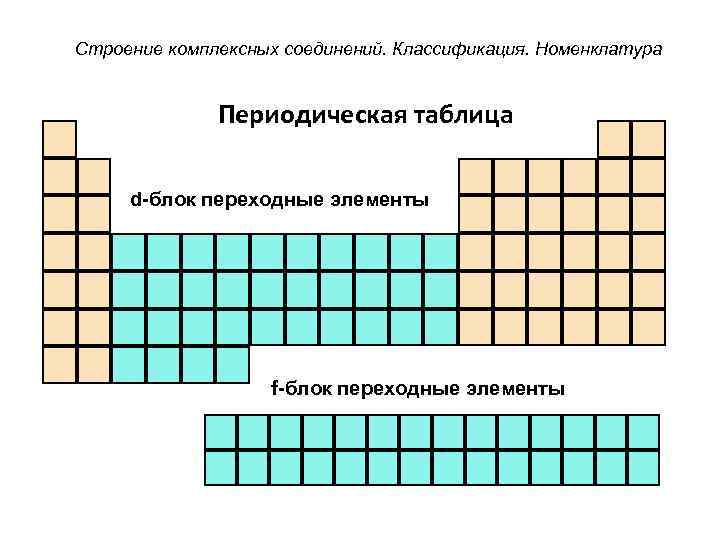 Строение комплексных соединений. Классификация. Номенклатура Периодическая таблица d-блок переходные элементы f-блок переходные элементы
Строение комплексных соединений. Классификация. Номенклатура Периодическая таблица d-блок переходные элементы f-блок переходные элементы
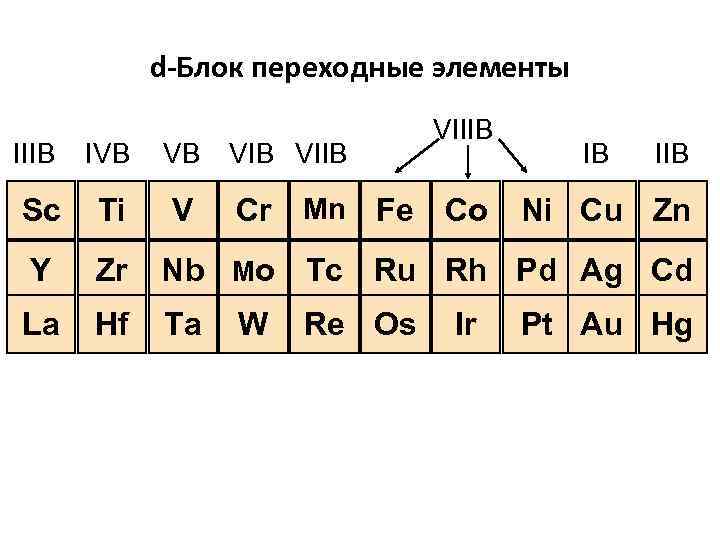 d-Блок переходные элементы VIB VIIIB IVB VB Sc Ti V Y Zr Nb Mo Tc Ru Rh Pd Ag Cd La Hf Ta Cr Mn Fe Co W Re Os Ir IB IIB Ni Cu Zn Pt Au Hg
d-Блок переходные элементы VIB VIIIB IVB VB Sc Ti V Y Zr Nb Mo Tc Ru Rh Pd Ag Cd La Hf Ta Cr Mn Fe Co W Re Os Ir IB IIB Ni Cu Zn Pt Au Hg
![Электронные конфигурации Элемент Sc Ti V Cr Mn Конфигурация [Ar]3 d 14 s 2 Электронные конфигурации Элемент Sc Ti V Cr Mn Конфигурация [Ar]3 d 14 s 2](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-27.jpg) Электронные конфигурации Элемент Sc Ti V Cr Mn Конфигурация [Ar]3 d 14 s 2 [Ar]3 d 24 s 2 [Ar]3 d 34 s 2 [Ar]3 d 54 s 1 [Ar]3 d 54 s 2 [Ar] = 1 s 22 p 63 s 23 p 6
Электронные конфигурации Элемент Sc Ti V Cr Mn Конфигурация [Ar]3 d 14 s 2 [Ar]3 d 24 s 2 [Ar]3 d 34 s 2 [Ar]3 d 54 s 1 [Ar]3 d 54 s 2 [Ar] = 1 s 22 p 63 s 23 p 6
![Электронные конфигурации Элемент Fe Co Ni Cu Zn Конфигурация [Ar] 3 d 64 s Электронные конфигурации Элемент Fe Co Ni Cu Zn Конфигурация [Ar] 3 d 64 s](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-28.jpg) Электронные конфигурации Элемент Fe Co Ni Cu Zn Конфигурация [Ar] 3 d 64 s 2 [Ar] 3 d 74 s 2 [Ar] 3 d 84 s 2 [Ar]3 d 104 s 1 [Ar]3 d 104 s 2 [Ar] = 1 s 22 p 63 s 23 p 6
Электронные конфигурации Элемент Fe Co Ni Cu Zn Конфигурация [Ar] 3 d 64 s 2 [Ar] 3 d 74 s 2 [Ar] 3 d 84 s 2 [Ar]3 d 104 s 1 [Ar]3 d 104 s 2 [Ar] = 1 s 22 p 63 s 23 p 6
 Строение комплексных соединений. Классификация. Номенклатура
Строение комплексных соединений. Классификация. Номенклатура
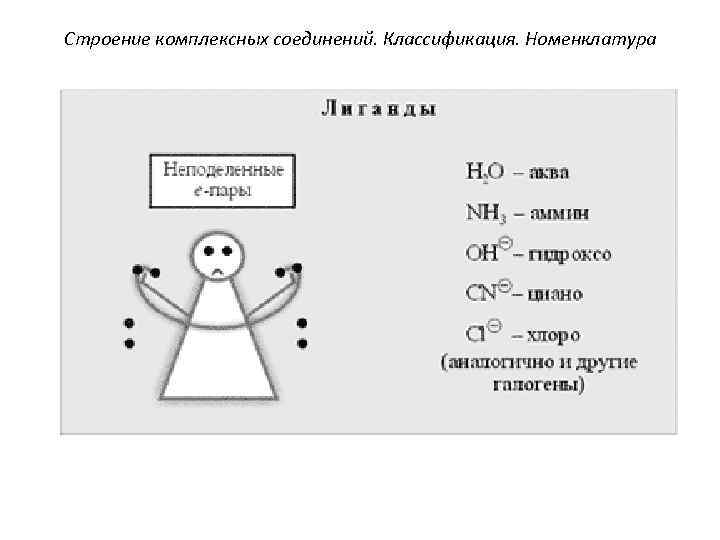
 Строение комплексных соединений. Классификация. Номенклатура 4. Лиганды (от лат. ligo – привязываю) имеют неподеленные электронные пары, т. е. являются донорами электронов(или адденами) - гидроксо-группы (OH-), кислотные остатки (Cl, Br-, J-, NO 2 -, CN, SO 42 - и др. ), а также нейтральные полярные молекулы (H 2 O, NH 3, CO и др. ).
Строение комплексных соединений. Классификация. Номенклатура 4. Лиганды (от лат. ligo – привязываю) имеют неподеленные электронные пары, т. е. являются донорами электронов(или адденами) - гидроксо-группы (OH-), кислотные остатки (Cl, Br-, J-, NO 2 -, CN, SO 42 - и др. ), а также нейтральные полярные молекулы (H 2 O, NH 3, CO и др. ).
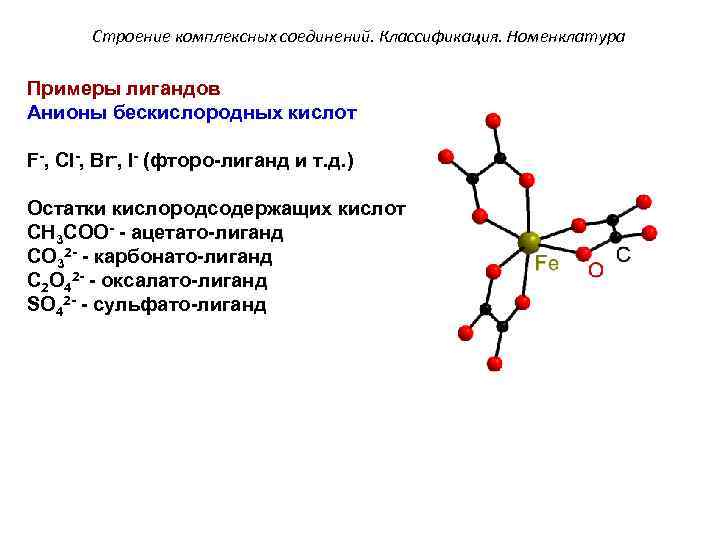 Строение комплексных соединений. Классификация. Номенклатура Примеры лигандов Анионы бескислородных кислот F-, Cl-, Br-, I- (фторо-лиганд и т. д. ) Остатки кислородсодержащих кислот CH 3 COO- - ацетато-лиганд CO 32 - - карбонато-лиганд C 2 O 42 - - оксалато-лиганд SO 42 - - сульфато-лиганд
Строение комплексных соединений. Классификация. Номенклатура Примеры лигандов Анионы бескислородных кислот F-, Cl-, Br-, I- (фторо-лиганд и т. д. ) Остатки кислородсодержащих кислот CH 3 COO- - ацетато-лиганд CO 32 - - карбонато-лиганд C 2 O 42 - - оксалато-лиганд SO 42 - - сульфато-лиганд
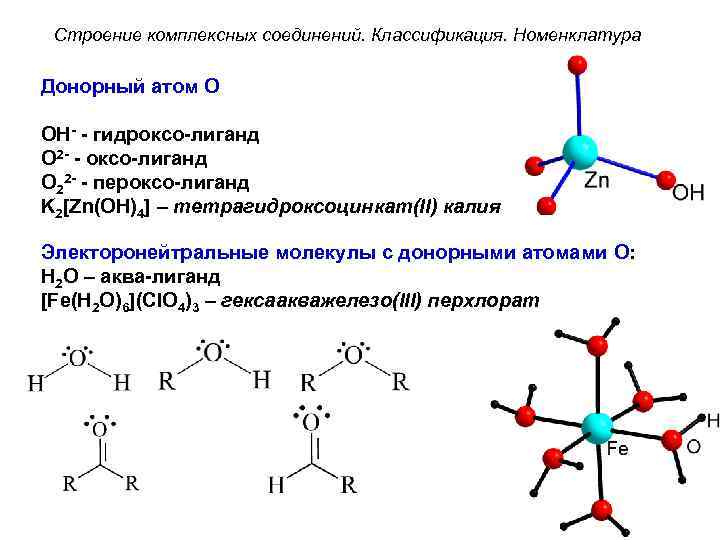 Строение комплексных соединений. Классификация. Номенклатура Донорный атом O OH- - гидроксо-лиганд O 2 - - оксо-лиганд O 22 - - пероксо-лиганд K 2[Zn(OH)4] – тетрагидроксоцинкат(II) калия Электоронейтральные молекулы с донорными атомами O: H 2 O – аква-лиганд [Fe(H 2 O)6](Cl. O 4)3 – гексаакважелезо(III) перхлорат
Строение комплексных соединений. Классификация. Номенклатура Донорный атом O OH- - гидроксо-лиганд O 2 - - оксо-лиганд O 22 - - пероксо-лиганд K 2[Zn(OH)4] – тетрагидроксоцинкат(II) калия Электоронейтральные молекулы с донорными атомами O: H 2 O – аква-лиганд [Fe(H 2 O)6](Cl. O 4)3 – гексаакважелезо(III) перхлорат
 Строение комплексных соединений. Классификация. Номенклатура
Строение комплексных соединений. Классификация. Номенклатура
 Строение комплексных соединений. Классификация. Номенклатура 5. Механизм комплексообразования связан с межионным, межмолекулярным взаимодействиями, но основной вклад в образование внутренней сферы вносит донорноакцепторное взаимодействие.
Строение комплексных соединений. Классификация. Номенклатура 5. Механизм комплексообразования связан с межионным, межмолекулярным взаимодействиями, но основной вклад в образование внутренней сферы вносит донорноакцепторное взаимодействие.
![Механизм образования комплексного иона [Al(OH)4]- Механизм образования комплексного иона [Al(OH)4]-](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-35.jpg) Механизм образования комплексного иона [Al(OH)4]-
Механизм образования комплексного иона [Al(OH)4]-
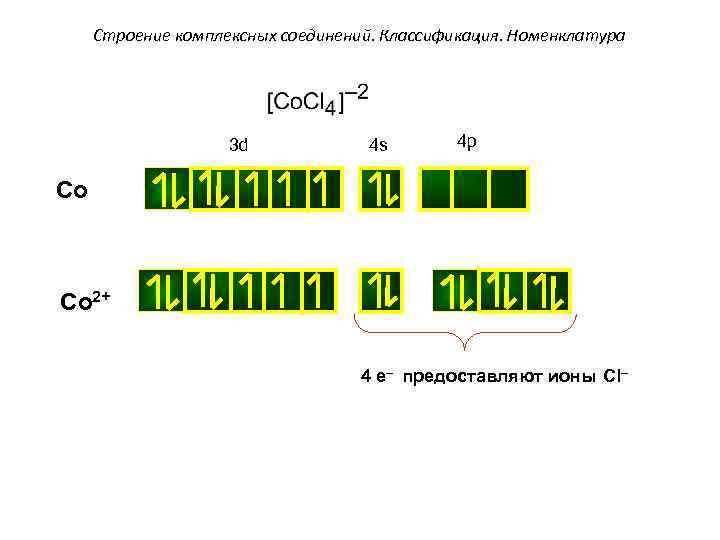 Строение комплексных соединений. Классификация. Номенклатура 3 d 4 s 4 p Co 2+ 4 e– предоставляют ионы Cl–
Строение комплексных соединений. Классификация. Номенклатура 3 d 4 s 4 p Co 2+ 4 e– предоставляют ионы Cl–
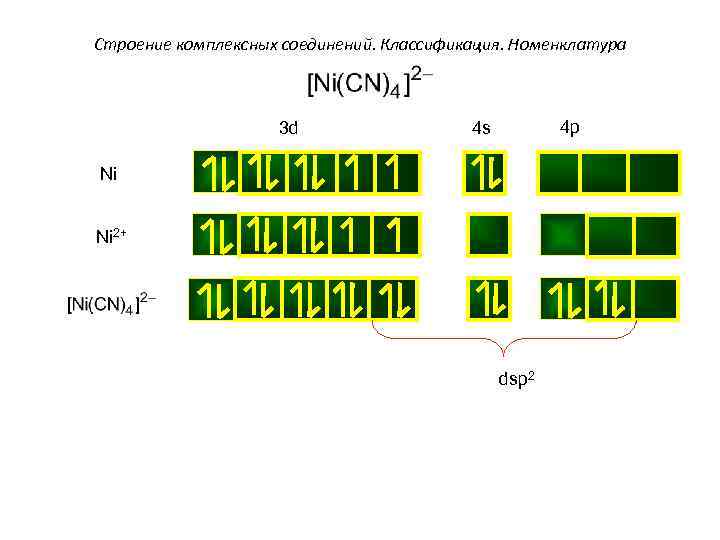 Строение комплексных соединений. Классификация. Номенклатура 3 d 4 p 4 s Ni Ni 2+ dsp 2
Строение комплексных соединений. Классификация. Номенклатура 3 d 4 p 4 s Ni Ni 2+ dsp 2
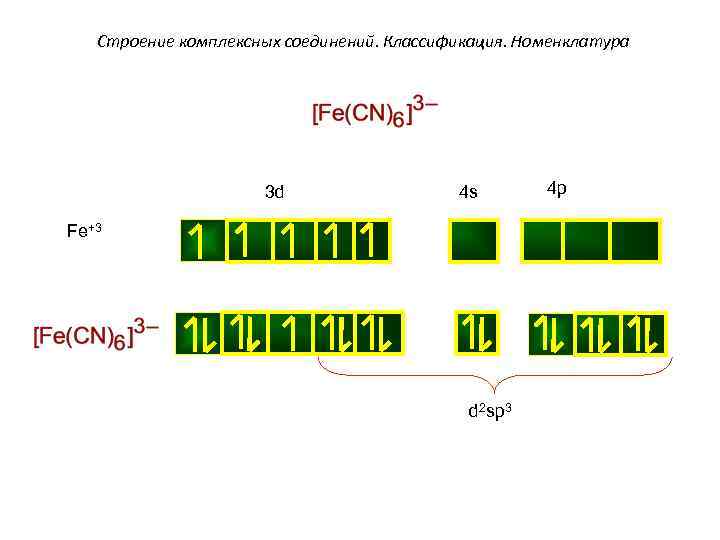 Строение комплексных соединений. Классификация. Номенклатура 3 d 4 s Fe+3 d 2 sp 3 4 p
Строение комплексных соединений. Классификация. Номенклатура 3 d 4 s Fe+3 d 2 sp 3 4 p
 Строение комплексных соединений. Классификация. Номенклатура
Строение комплексных соединений. Классификация. Номенклатура
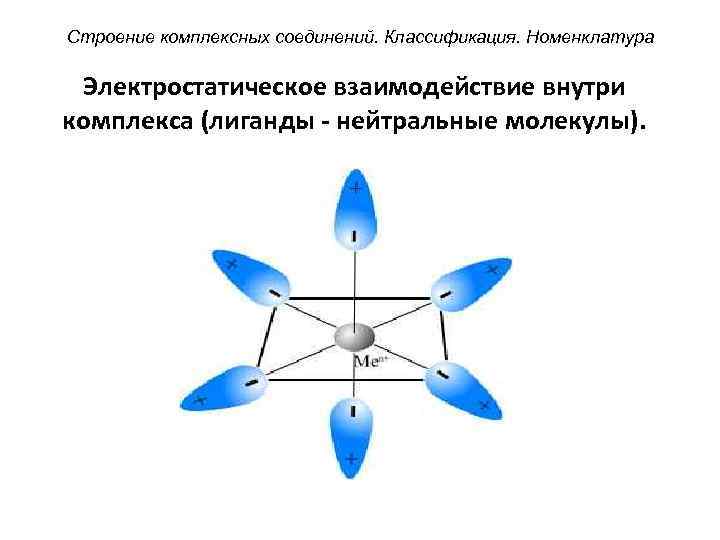 Строение комплексных соединений. Классификация. Номенклатура Электростатическое взаимодействие внутри комплекса (лиганды - нейтральные молекулы).
Строение комплексных соединений. Классификация. Номенклатура Электростатическое взаимодействие внутри комплекса (лиганды - нейтральные молекулы).
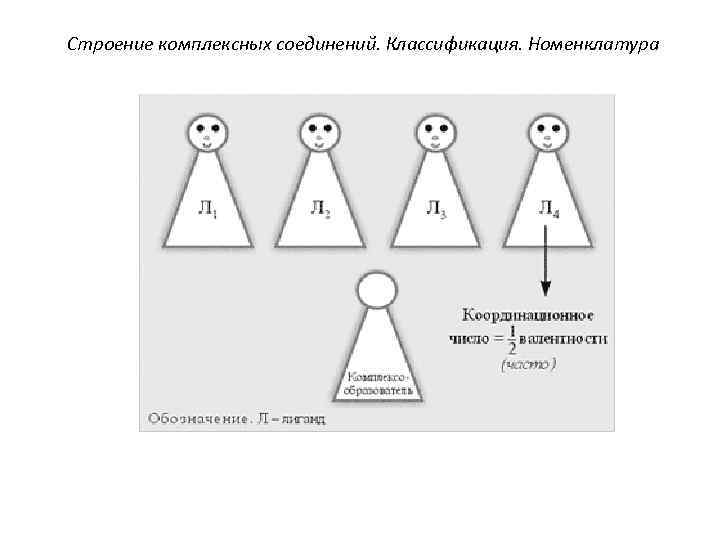
 Строение комплексных соединений. Классификация. Номенклатура 6. Координационное число (к. ч. ) комплексообразователя показывает, сколько связей образует комплексообразователь с лигандами. Величина к. ч. зависит от природы комплексообразователя, лигандов и условий комплексообразования (концентрации, р. Н, температуры и др. ).
Строение комплексных соединений. Классификация. Номенклатура 6. Координационное число (к. ч. ) комплексообразователя показывает, сколько связей образует комплексообразователь с лигандами. Величина к. ч. зависит от природы комплексообразователя, лигандов и условий комплексообразования (концентрации, р. Н, температуры и др. ).
 Строение комплексных соединений. Классификация. Номенклатура
Строение комплексных соединений. Классификация. Номенклатура
 Строение комплексных соединений. Классификация. Номенклатура Координационные числа наиболее распространенных комплексообразователей: Комплексообразователь К. ч. Ag+ , Cu+ Cu 2+ , Zn 2+, Pt 2+, Hg 2+ Fe 3+, Co 3+, Fe 2+, Ni 2+, Al 3+, Pt 4+ 2 4 6
Строение комплексных соединений. Классификация. Номенклатура Координационные числа наиболее распространенных комплексообразователей: Комплексообразователь К. ч. Ag+ , Cu+ Cu 2+ , Zn 2+, Pt 2+, Hg 2+ Fe 3+, Co 3+, Fe 2+, Ni 2+, Al 3+, Pt 4+ 2 4 6
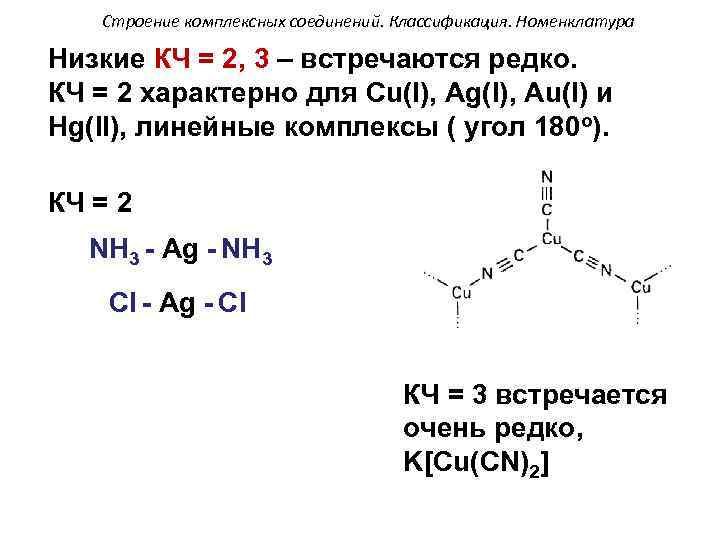 Строение комплексных соединений. Классификация. Номенклатура Низкие КЧ = 2, 3 – встречаются редко. КЧ = 2 характерно для Cu(I), Ag(I), Au(I) и Hg(II), линейные комплексы ( угол 180 о). КЧ = 2 NH 3 Cl - Ag - NH 3 Ag - Cl КЧ = 3 встречается очень редко, K[Cu(CN)2]
Строение комплексных соединений. Классификация. Номенклатура Низкие КЧ = 2, 3 – встречаются редко. КЧ = 2 характерно для Cu(I), Ag(I), Au(I) и Hg(II), линейные комплексы ( угол 180 о). КЧ = 2 NH 3 Cl - Ag - NH 3 Ag - Cl КЧ = 3 встречается очень редко, K[Cu(CN)2]
![Строение комплексных соединений. Классификация. Номенклатура КЧ = 4 (тетраэдр и плоский квадрат). [Ni(CO)4] 2+ Строение комплексных соединений. Классификация. Номенклатура КЧ = 4 (тетраэдр и плоский квадрат). [Ni(CO)4] 2+](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-45.jpg) Строение комплексных соединений. Классификация. Номенклатура КЧ = 4 (тетраэдр и плоский квадрат). [Ni(CO)4] 2+ Тетраэдр Квадратный комплекс [Pt 2+(NH 3)2 Cl 2]
Строение комплексных соединений. Классификация. Номенклатура КЧ = 4 (тетраэдр и плоский квадрат). [Ni(CO)4] 2+ Тетраэдр Квадратный комплекс [Pt 2+(NH 3)2 Cl 2]
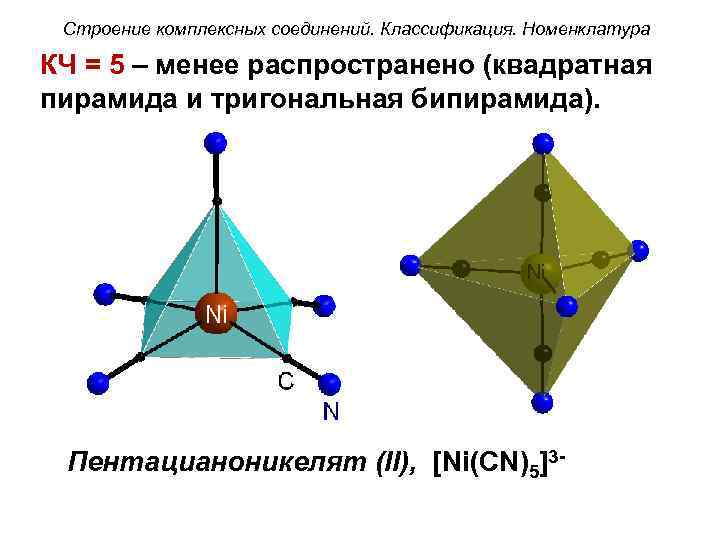 Строение комплексных соединений. Классификация. Номенклатура КЧ = 5 – менее распространено (квадратная пирамида и тригональная бипирамида). Пентацианоникелят (II), [Ni(CN)5]3 -
Строение комплексных соединений. Классификация. Номенклатура КЧ = 5 – менее распространено (квадратная пирамида и тригональная бипирамида). Пентацианоникелят (II), [Ni(CN)5]3 -
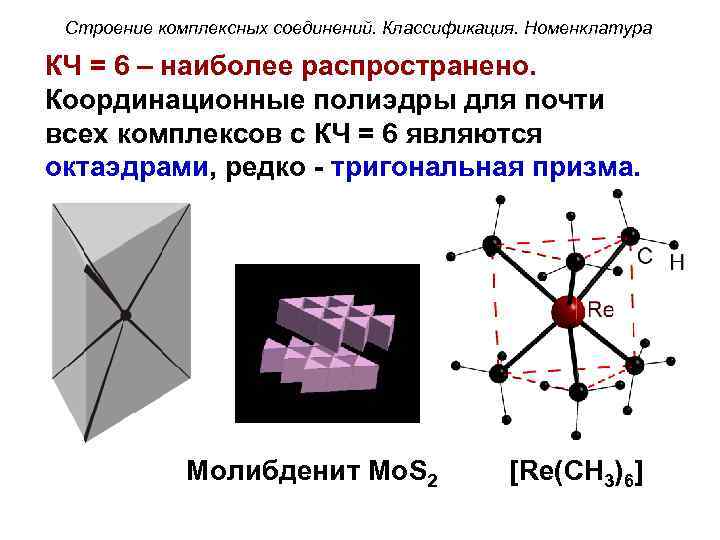 Строение комплексных соединений. Классификация. Номенклатура КЧ = 6 – наиболее распространено. Координационные полиэдры для почти всех комплексов с КЧ = 6 являются октаэдрами, редко - тригональная призма. Молибденит Mo. S 2 [Re(CH 3)6]
Строение комплексных соединений. Классификация. Номенклатура КЧ = 6 – наиболее распространено. Координационные полиэдры для почти всех комплексов с КЧ = 6 являются октаэдрами, редко - тригональная призма. Молибденит Mo. S 2 [Re(CH 3)6]
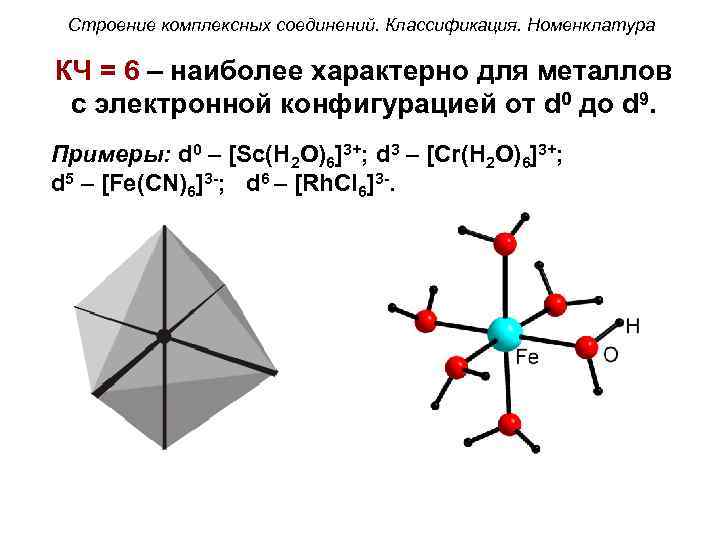 Строение комплексных соединений. Классификация. Номенклатура КЧ = 6 – наиболее характерно для металлов с электронной конфигурацией от d 0 до d 9. Примеры: d 0 – [Sc(H 2 O)6]3+; d 3 – [Cr(H 2 O)6]3+; d 5 – [Fe(CN)6]3 -; d 6 – [Rh. Cl 6]3 -.
Строение комплексных соединений. Классификация. Номенклатура КЧ = 6 – наиболее характерно для металлов с электронной конфигурацией от d 0 до d 9. Примеры: d 0 – [Sc(H 2 O)6]3+; d 3 – [Cr(H 2 O)6]3+; d 5 – [Fe(CN)6]3 -; d 6 – [Rh. Cl 6]3 -.
![Строение комплексных соединений. Классификация. Номенклатура КЧ = 7 Пентагональная бипирамида [UO 2(H 2 O)5]2+ Строение комплексных соединений. Классификация. Номенклатура КЧ = 7 Пентагональная бипирамида [UO 2(H 2 O)5]2+](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-49.jpg) Строение комплексных соединений. Классификация. Номенклатура КЧ = 7 Пентагональная бипирамида [UO 2(H 2 O)5]2+ Тригональная призма с одной шапкой [Nb. F 7]2 - Октаэдр с одной шапкой [Ta. Cl 4(PMe 3)3]
Строение комплексных соединений. Классификация. Номенклатура КЧ = 7 Пентагональная бипирамида [UO 2(H 2 O)5]2+ Тригональная призма с одной шапкой [Nb. F 7]2 - Октаэдр с одной шапкой [Ta. Cl 4(PMe 3)3]
![Строение комплексных соединений. Классификация. Номенклатура КЧ = 8 додекаэдр [Hf(ox)4]4 - квадратная антипризма [Mo(CN)8]3 Строение комплексных соединений. Классификация. Номенклатура КЧ = 8 додекаэдр [Hf(ox)4]4 - квадратная антипризма [Mo(CN)8]3](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-50.jpg) Строение комплексных соединений. Классификация. Номенклатура КЧ = 8 додекаэдр [Hf(ox)4]4 - квадратная антипризма [Mo(CN)8]3 -
Строение комплексных соединений. Классификация. Номенклатура КЧ = 8 додекаэдр [Hf(ox)4]4 - квадратная антипризма [Mo(CN)8]3 -
![Строение комплексных соединений. Классификация. Номенклатура КЧ = 8, [Сo. F 8]5 - квадратная антипризма Строение комплексных соединений. Классификация. Номенклатура КЧ = 8, [Сo. F 8]5 - квадратная антипризма](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-51.jpg) Строение комплексных соединений. Классификация. Номенклатура КЧ = 8, [Сo. F 8]5 - квадратная антипризма
Строение комплексных соединений. Классификация. Номенклатура КЧ = 8, [Сo. F 8]5 - квадратная антипризма
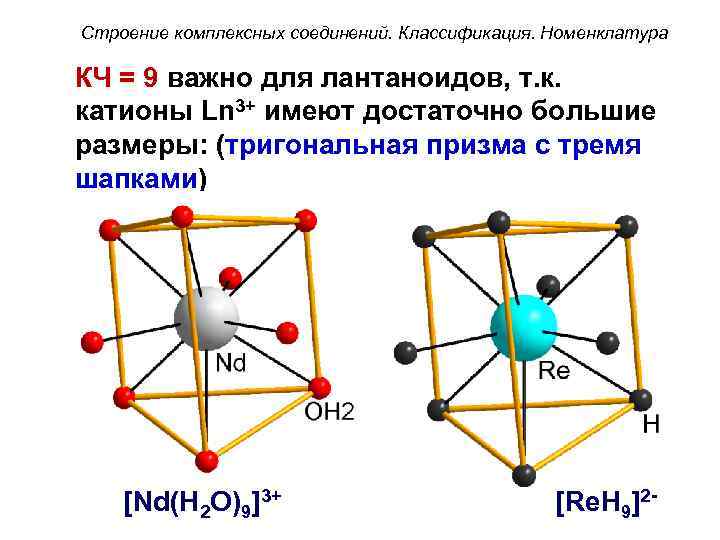 Строение комплексных соединений. Классификация. Номенклатура КЧ = 9 важно для лантаноидов, т. к. катионы Ln 3+ имеют достаточно большие размеры: (тригональная призма с тремя шапками) [Nd(H 2 O)9]3+ [Re. H 9]2 -
Строение комплексных соединений. Классификация. Номенклатура КЧ = 9 важно для лантаноидов, т. к. катионы Ln 3+ имеют достаточно большие размеры: (тригональная призма с тремя шапками) [Nd(H 2 O)9]3+ [Re. H 9]2 -
![Строение комплексных соединений. Классификация. Номенклатура КЧ = 10, 12 КЧ=12, [Ce(NO 3)6]2 - КЧ Строение комплексных соединений. Классификация. Номенклатура КЧ = 10, 12 КЧ=12, [Ce(NO 3)6]2 - КЧ](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-53.jpg) Строение комплексных соединений. Классификация. Номенклатура КЧ = 10, 12 КЧ=12, [Ce(NO 3)6]2 - КЧ = 10, [Bi(NO 3)5]2 -
Строение комплексных соединений. Классификация. Номенклатура КЧ = 10, 12 КЧ=12, [Ce(NO 3)6]2 - КЧ = 10, [Bi(NO 3)5]2 -
 Строение комплексных соединений. Классификация. Номенклатура Пример: Заряд внутренней сферы комплексного соединения Z равен алгебраической сумме зарядов комплексообразователя и лигандов.
Строение комплексных соединений. Классификация. Номенклатура Пример: Заряд внутренней сферы комплексного соединения Z равен алгебраической сумме зарядов комплексообразователя и лигандов.
 Строение комплексных соединений. Классификация. Номенклатура Пример: Комплексообразователь – Со 3+ Лиганды- Сl- , Н 2 О КЧ (Со 3+) = 6 [Со 3+ (Сl- )4(Н 2 О)2]Z=1 ·(+3)+4 ·(-1)+2 · 0=-1 Дописываем ионы внешней сферы : К + [Со 3+ (Сl- )4 (Н 2 О)2 ]-
Строение комплексных соединений. Классификация. Номенклатура Пример: Комплексообразователь – Со 3+ Лиганды- Сl- , Н 2 О КЧ (Со 3+) = 6 [Со 3+ (Сl- )4(Н 2 О)2]Z=1 ·(+3)+4 ·(-1)+2 · 0=-1 Дописываем ионы внешней сферы : К + [Со 3+ (Сl- )4 (Н 2 О)2 ]-
 Классификация и номенклатура комплексных соединений По характеру заряда внутренней сферы различают катионные, анионные и нейтральные комплексы. Например: 1) [Cu 2+(H 2 О)4]2+ - катионный комплекс 2) [Fe 3+ (CN)6]3 - - анионный комплекс 3) [Zn 2+(ОН)2(NН 3)(Н 2 О)]0 - нейтральный комплекс
Классификация и номенклатура комплексных соединений По характеру заряда внутренней сферы различают катионные, анионные и нейтральные комплексы. Например: 1) [Cu 2+(H 2 О)4]2+ - катионный комплекс 2) [Fe 3+ (CN)6]3 - - анионный комплекс 3) [Zn 2+(ОН)2(NН 3)(Н 2 О)]0 - нейтральный комплекс
 Строение комплексных соединений. Классификация. Номенклатура Название комплекса: Число лигандов – греч. числит. • 1 – (моно) • 2 – ди • 3 – три • 4 – тетра • 5 – пента • 6 – гекса • 7 – гепта … число лигандов каждого типа название лигандов название комплексообр. в нужной форме • Число сложных лигандов: бис-, трис-, тетракис-, пентакис… • [M(en)4] тетракис(этилендиамин)… • [M(SO 42 -)2] бис(сульфато-)…
Строение комплексных соединений. Классификация. Номенклатура Название комплекса: Число лигандов – греч. числит. • 1 – (моно) • 2 – ди • 3 – три • 4 – тетра • 5 – пента • 6 – гекса • 7 – гепта … число лигандов каждого типа название лигандов название комплексообр. в нужной форме • Число сложных лигандов: бис-, трис-, тетракис-, пентакис… • [M(en)4] тетракис(этилендиамин)… • [M(SO 42 -)2] бис(сульфато-)…
 I. Номенклатура катионных комплексов • Греческим числительным называют число лигандов: 1 -моно, 2 -ди, 3 -три, 4 -тетра, 5 -пента, 6 -гекса • Называют лиганды: а) нейтральные молекулы (их называют в первую очередь): Н 2 О –аква; NH 3 – аммин; СО – карбонил; NO – нитрозил. б) лиганды-анионы называют с окончанием «-о» : ОН- - гидроксо; CI- -хлоро; Br- - бромо; I- - иодо; NO 2 - - нитро; NO - - нитрато; SO 2 - - сульфато; 3 4 CN- - циано; SCN- - родано. • Называют комплексообразователь русским наименованием. • Отмечают валентность комплексообразователя римской цифрой в скобках.
I. Номенклатура катионных комплексов • Греческим числительным называют число лигандов: 1 -моно, 2 -ди, 3 -три, 4 -тетра, 5 -пента, 6 -гекса • Называют лиганды: а) нейтральные молекулы (их называют в первую очередь): Н 2 О –аква; NH 3 – аммин; СО – карбонил; NO – нитрозил. б) лиганды-анионы называют с окончанием «-о» : ОН- - гидроксо; CI- -хлоро; Br- - бромо; I- - иодо; NO 2 - - нитро; NO - - нитрато; SO 2 - - сульфато; 3 4 CN- - циано; SCN- - родано. • Называют комплексообразователь русским наименованием. • Отмечают валентность комплексообразователя римской цифрой в скобках.
![Строение комплексных соединений. Классификация. Номенклатура Примеры: II [Cu(NH 3)4]Cl 2 Хлорид тетраамминмеди(II) H 2 Строение комплексных соединений. Классификация. Номенклатура Примеры: II [Cu(NH 3)4]Cl 2 Хлорид тетраамминмеди(II) H 2](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-59.jpg) Строение комплексных соединений. Классификация. Номенклатура Примеры: II [Cu(NH 3)4]Cl 2 Хлорид тетраамминмеди(II) H 2 O – аква NH 3 – аммин Cl- – хлоро. NO 2 - - нитро CN- - циано. SCN- - родано- 1 – моно 2 – ди 3 – три 4 – тетра 5 – пента 6 – гекса
Строение комплексных соединений. Классификация. Номенклатура Примеры: II [Cu(NH 3)4]Cl 2 Хлорид тетраамминмеди(II) H 2 O – аква NH 3 – аммин Cl- – хлоро. NO 2 - - нитро CN- - циано. SCN- - родано- 1 – моно 2 – ди 3 – три 4 – тетра 5 – пента 6 – гекса
![Строение комплексных соединений. Классификация. Номенклатура Примеры: [Ag. I(NH 3)2]OH – гидроксид диамминсеребра(I); [Co. III(NH Строение комплексных соединений. Классификация. Номенклатура Примеры: [Ag. I(NH 3)2]OH – гидроксид диамминсеребра(I); [Co. III(NH](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-60.jpg) Строение комплексных соединений. Классификация. Номенклатура Примеры: [Ag. I(NH 3)2]OH – гидроксид диамминсеребра(I); [Co. III(NH 3)6]Cl 3 – хлорид гексаамминкобальта(III); [Cr 2 III(OH)(NH 3)2]Cl 4 – хлорид нонаамминдигидроксодихрома(III).
Строение комплексных соединений. Классификация. Номенклатура Примеры: [Ag. I(NH 3)2]OH – гидроксид диамминсеребра(I); [Co. III(NH 3)6]Cl 3 – хлорид гексаамминкобальта(III); [Cr 2 III(OH)(NH 3)2]Cl 4 – хлорид нонаамминдигидроксодихрома(III).
 • • II. Номенклатура анионных комплексов Греческим числительным называют число лигандов. Называют лиганды. Называют комплексообразователь латинским наименованием с окончанием «-ат» . Отмечают валентность комплексообразователя римской цифрой в скобках.
• • II. Номенклатура анионных комплексов Греческим числительным называют число лигандов. Называют лиганды. Называют комплексообразователь латинским наименованием с окончанием «-ат» . Отмечают валентность комплексообразователя римской цифрой в скобках.
![Строение комплексных соединений. Классификация. Номенклатура Примеры: III K 3[Fe(CN)6] Гексацианоферрат(III) калия H 2 O Строение комплексных соединений. Классификация. Номенклатура Примеры: III K 3[Fe(CN)6] Гексацианоферрат(III) калия H 2 O](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-62.jpg) Строение комплексных соединений. Классификация. Номенклатура Примеры: III K 3[Fe(CN)6] Гексацианоферрат(III) калия H 2 O – аква NH 3 – аммин Cl- – хлоро. NO 2 - – нитро CN- – циано. SCN- – родано- 1 – моно 2 – ди 3 – три 4 – тетра 5 – пента 6 – гекса
Строение комплексных соединений. Классификация. Номенклатура Примеры: III K 3[Fe(CN)6] Гексацианоферрат(III) калия H 2 O – аква NH 3 – аммин Cl- – хлоро. NO 2 - – нитро CN- – циано. SCN- – родано- 1 – моно 2 – ди 3 – три 4 – тетра 5 – пента 6 – гекса
![Строение комплексных соединений. Классификация. Номенклатура Примеры: Ag – аргент- [Fe(CN)6]3– – гексацианоферрат(III)ион Au – Строение комплексных соединений. Классификация. Номенклатура Примеры: Ag – аргент- [Fe(CN)6]3– – гексацианоферрат(III)ион Au –](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-63.jpg) Строение комплексных соединений. Классификация. Номенклатура Примеры: Ag – аргент- [Fe(CN)6]3– – гексацианоферрат(III)ион Au – аур- [Ag(CN)2 ион ]– – дицианоаргентат(I)- K 2[Hg. I 4] – тетраиодомеркурат(II) калия K 2[Pt. Cl 6] – гексахлороплатинат(IV) калия Cu – купр. Fe – ферр. Hg – меркур. Mn – манган. Ni – никкол. Pb – плюмб. Sb – стиб. Sn – станн-
Строение комплексных соединений. Классификация. Номенклатура Примеры: Ag – аргент- [Fe(CN)6]3– – гексацианоферрат(III)ион Au – аур- [Ag(CN)2 ион ]– – дицианоаргентат(I)- K 2[Hg. I 4] – тетраиодомеркурат(II) калия K 2[Pt. Cl 6] – гексахлороплатинат(IV) калия Cu – купр. Fe – ферр. Hg – меркур. Mn – манган. Ni – никкол. Pb – плюмб. Sb – стиб. Sn – станн-
 III. Номенклатура нейтральных комплексов • Греческим числительным называют число лигандов. • Называют лиганды. • Называют комплексообразователь русским наименованием. • Валентность комплексообразователя не указывают.
III. Номенклатура нейтральных комплексов • Греческим числительным называют число лигандов. • Называют лиганды. • Называют комплексообразователь русским наименованием. • Валентность комплексообразователя не указывают.
![Строение комплексных соединений. Классификация. Номенклатура Примеры: [Ni(CO)4] – тетракарбонилникель; [Co 2(CO)8] – октакарбонилдикобальт; [Al Строение комплексных соединений. Классификация. Номенклатура Примеры: [Ni(CO)4] – тетракарбонилникель; [Co 2(CO)8] – октакарбонилдикобальт; [Al](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-65.jpg) Строение комплексных соединений. Классификация. Номенклатура Примеры: [Ni(CO)4] – тетракарбонилникель; [Co 2(CO)8] – октакарбонилдикобальт; [Al 2 Cl 6] – гексахлородиалюминий; [Co. IIICl 3(NH 3)3] – триамминтрихлорокобальт(III); [Co. II (NO 2)2(H 2 O)4] – тетрааквадинитрокобальт(II).
Строение комплексных соединений. Классификация. Номенклатура Примеры: [Ni(CO)4] – тетракарбонилникель; [Co 2(CO)8] – октакарбонилдикобальт; [Al 2 Cl 6] – гексахлородиалюминий; [Co. IIICl 3(NH 3)3] – триамминтрихлорокобальт(III); [Co. II (NO 2)2(H 2 O)4] – тетрааквадинитрокобальт(II).
![Типы комплексных соединений 1. Аквакомплексы В водных растворах: • [Be(H 2 O)4]2+ • [Al(H Типы комплексных соединений 1. Аквакомплексы В водных растворах: • [Be(H 2 O)4]2+ • [Al(H](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-66.jpg) Типы комплексных соединений 1. Аквакомплексы В водных растворах: • [Be(H 2 O)4]2+ • [Al(H 2 O)6]3+ • [Cr(H 2 O)6]3+ … Кристаллогидраты: • [Be(H 2 O)4]SO 4 • [Al(H 2 O)6]Cl 3 • [K(H 2 O)6][Cr(H 2 O)6](SO 4)2 • [Cu(H 2 O)4]SO 4·H 2 O • [Ni(H 2 O)6]SO 4·H 2 O M : OH 2
Типы комплексных соединений 1. Аквакомплексы В водных растворах: • [Be(H 2 O)4]2+ • [Al(H 2 O)6]3+ • [Cr(H 2 O)6]3+ … Кристаллогидраты: • [Be(H 2 O)4]SO 4 • [Al(H 2 O)6]Cl 3 • [K(H 2 O)6][Cr(H 2 O)6](SO 4)2 • [Cu(H 2 O)4]SO 4·H 2 O • [Ni(H 2 O)6]SO 4·H 2 O M : OH 2
![Аквакомплексы Кристаллогидрат [Cu(H 2 O)4]SO 4·H 2 O ( «медный купорос» ) Аквакомплекс H Аквакомплексы Кристаллогидрат [Cu(H 2 O)4]SO 4·H 2 O ( «медный купорос» ) Аквакомплекс H](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-67.jpg) Аквакомплексы Кристаллогидрат [Cu(H 2 O)4]SO 4·H 2 O ( «медный купорос» ) Аквакомплекс H 2 O Cu OH 2 H O O OH 2 O S H O O
Аквакомплексы Кристаллогидрат [Cu(H 2 O)4]SO 4·H 2 O ( «медный купорос» ) Аквакомплекс H 2 O Cu OH 2 H O O OH 2 O S H O O
![Аквакомплексы Кристаллогидрат [Fe(H 2 O)6]SO 4·H 2 O ( «железный купорос» ) Аквакомплекс H Аквакомплексы Кристаллогидрат [Fe(H 2 O)6]SO 4·H 2 O ( «железный купорос» ) Аквакомплекс H](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-68.jpg) Аквакомплексы Кристаллогидрат [Fe(H 2 O)6]SO 4·H 2 O ( «железный купорос» ) Аквакомплекс H 2 O Fe OH 2 H O O OH 2 O S H O O
Аквакомплексы Кристаллогидрат [Fe(H 2 O)6]SO 4·H 2 O ( «железный купорос» ) Аквакомплекс H 2 O Fe OH 2 H O O OH 2 O S H O O
![2. Гидроксокомплексы [Zn(OH)4]2– M : OH– 2. Гидроксокомплексы [Zn(OH)4]2– M : OH–](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-69.jpg) 2. Гидроксокомплексы [Zn(OH)4]2– M : OH–
2. Гидроксокомплексы [Zn(OH)4]2– M : OH–
![3. Аммины (аммиакаты) [Ag(NH 3)2]+ [Cu(NH 3)4](OH)2 M : NH 3 [Ni(NH 3)6]Cl 2 3. Аммины (аммиакаты) [Ag(NH 3)2]+ [Cu(NH 3)4](OH)2 M : NH 3 [Ni(NH 3)6]Cl 2](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-70.jpg) 3. Аммины (аммиакаты) [Ag(NH 3)2]+ [Cu(NH 3)4](OH)2 M : NH 3 [Ni(NH 3)6]Cl 2
3. Аммины (аммиакаты) [Ag(NH 3)2]+ [Cu(NH 3)4](OH)2 M : NH 3 [Ni(NH 3)6]Cl 2
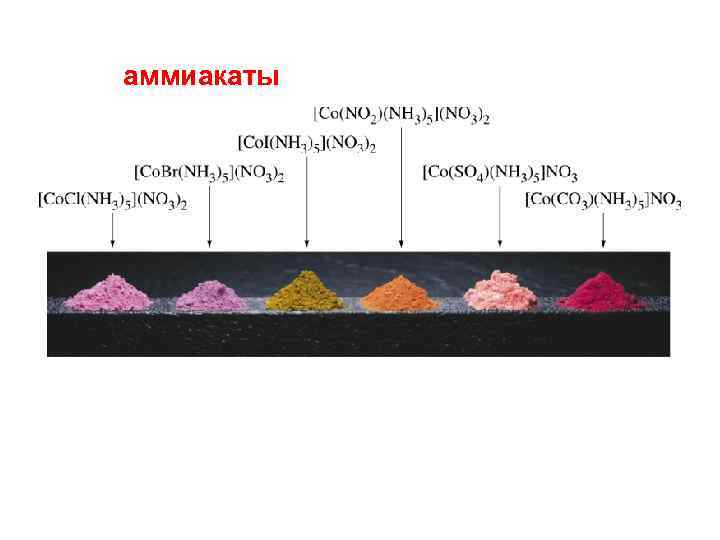 аммиакаты
аммиакаты
![4. Ацидокомплексы M : Х– [Hg. I 4]2– [Fe(NCS)6]3− Получение и разрушение тиоцианатного к-са 4. Ацидокомплексы M : Х– [Hg. I 4]2– [Fe(NCS)6]3− Получение и разрушение тиоцианатного к-са](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-72.jpg) 4. Ацидокомплексы M : Х– [Hg. I 4]2– [Fe(NCS)6]3− Получение и разрушение тиоцианатного к-са Fe(III) K 3[Fe(CN)6] K 4[Fe(CN)6]
4. Ацидокомплексы M : Х– [Hg. I 4]2– [Fe(NCS)6]3− Получение и разрушение тиоцианатного к-са Fe(III) K 3[Fe(CN)6] K 4[Fe(CN)6]
![5. Гидридокомплексы M : H– Na[BH 4] Al[BH 4]3 Li[Al. H 4] Na[BH 4] 5. Гидридокомплексы M : H– Na[BH 4] Al[BH 4]3 Li[Al. H 4] Na[BH 4]](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-73.jpg) 5. Гидридокомплексы M : H– Na[BH 4] Al[BH 4]3 Li[Al. H 4] Na[BH 4]
5. Гидридокомплексы M : H– Na[BH 4] Al[BH 4]3 Li[Al. H 4] Na[BH 4]
 Устойчивость комплексных соединений Различают первичную и вторичную диссоциацию комплексных соединений. а) Первичная диссоциация – это диссоциация комплексной соли на внутреннюю сферу и ионы внешней сферы. Идет легко по принципу сильных электролитов. [Ag(NH 3)2]Cl [Ag(NH 3)2]+ + Cl-
Устойчивость комплексных соединений Различают первичную и вторичную диссоциацию комплексных соединений. а) Первичная диссоциация – это диссоциация комплексной соли на внутреннюю сферу и ионы внешней сферы. Идет легко по принципу сильных электролитов. [Ag(NH 3)2]Cl [Ag(NH 3)2]+ + Cl-
![Устойчивость комплексных соединений б) Вторичная диссоциация – диссоциация внутренней сферы: [Ag(NH 3)2]+ [Ag(NH 3)]+ Устойчивость комплексных соединений б) Вторичная диссоциация – диссоциация внутренней сферы: [Ag(NH 3)2]+ [Ag(NH 3)]+](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-75.jpg) Устойчивость комплексных соединений б) Вторичная диссоциация – диссоциация внутренней сферы: [Ag(NH 3)2]+ [Ag(NH 3)]+ + NH 3 [Ag(NH 3)]+ Ag+ + NH 3 [Ag(NH 3)2]+ Ag+ + 2 NH 3 Она протекает незначительно.
Устойчивость комплексных соединений б) Вторичная диссоциация – диссоциация внутренней сферы: [Ag(NH 3)2]+ [Ag(NH 3)]+ + NH 3 [Ag(NH 3)]+ Ag+ + NH 3 [Ag(NH 3)2]+ Ag+ + 2 NH 3 Она протекает незначительно.
 Устойчивость комплексных соединений Устойчивость комплексных ионов характеризуется константой нестойкости (Кнест), которая определяется на основании закона действующих масс. [Ag+] [NH 3]2 KH = = 5, 89. 10 -8 = [ [Ag(NH 3)2]+
Устойчивость комплексных соединений Устойчивость комплексных ионов характеризуется константой нестойкости (Кнест), которая определяется на основании закона действующих масс. [Ag+] [NH 3]2 KH = = 5, 89. 10 -8 = [ [Ag(NH 3)2]+
![Константы нестойкости некоторых комплексов Комплексный ион [Fe(CN)6]3[Fe(CN)6]4[Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ [Zn(OH)4]2– Константа Константы нестойкости некоторых комплексов Комплексный ион [Fe(CN)6]3[Fe(CN)6]4[Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ [Zn(OH)4]2– Константа](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-77.jpg) Константы нестойкости некоторых комплексов Комплексный ион [Fe(CN)6]3[Fe(CN)6]4[Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ [Zn(OH)4]2– Константа нестойкости 1, 0. 10– 31 1, 0. 10– 36 7, 75. 10– 6 9, 31. 10– 8 2, 14. 10– 13 3, 6. 10– 16
Константы нестойкости некоторых комплексов Комплексный ион [Fe(CN)6]3[Fe(CN)6]4[Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ [Zn(OH)4]2– Константа нестойкости 1, 0. 10– 31 1, 0. 10– 36 7, 75. 10– 6 9, 31. 10– 8 2, 14. 10– 13 3, 6. 10– 16
 Устойчивость комплексных соединений Константа нестойкости характеризует термодинамическую устойчивость комплекса, которая зависит от прочности связей между центральным атомом и лигандами. Чем меньше значение, Кнест, тем более прочен комплекс, тем он устойчивее.
Устойчивость комплексных соединений Константа нестойкости характеризует термодинамическую устойчивость комплекса, которая зависит от прочности связей между центральным атомом и лигандами. Чем меньше значение, Кнест, тем более прочен комплекс, тем он устойчивее.
 Устойчивость комплексных соединений Мерой прочности комплекса является энергия разрыва связей, величина которой характеризуется изменением энергии Гиббса (∆G) в результате вторичной диссоциации. Уравнением изотермы: , где: R = 8, 314 Дж моль-1 К-1 T – температура, К ln К = 2, 303. lg. К
Устойчивость комплексных соединений Мерой прочности комплекса является энергия разрыва связей, величина которой характеризуется изменением энергии Гиббса (∆G) в результате вторичной диссоциации. Уравнением изотермы: , где: R = 8, 314 Дж моль-1 К-1 T – температура, К ln К = 2, 303. lg. К
 Изомерия комплексных соединений Для комплексных соединений характерны следующие виды изомерии: сольватная (в водных средах гидратная), ионизационная, координационная, геометрическая , оптическая (зеркальная). При изучении химиотерапии особое место занимает геометрическая изомерия или изомерия положения у комплексов, содержащих не менее двух разных лигандов.
Изомерия комплексных соединений Для комплексных соединений характерны следующие виды изомерии: сольватная (в водных средах гидратная), ионизационная, координационная, геометрическая , оптическая (зеркальная). При изучении химиотерапии особое место занимает геометрическая изомерия или изомерия положения у комплексов, содержащих не менее двух разных лигандов.
![Геометрическая изомерия цис- (cis-) cis-[Co. Cl 2(NH 3)4]+ транс- (trans-) trans-[Co. Cl 2(NH 3)4]+ Геометрическая изомерия цис- (cis-) cis-[Co. Cl 2(NH 3)4]+ транс- (trans-) trans-[Co. Cl 2(NH 3)4]+](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-81.jpg) Геометрическая изомерия цис- (cis-) cis-[Co. Cl 2(NH 3)4]+ транс- (trans-) trans-[Co. Cl 2(NH 3)4]+
Геометрическая изомерия цис- (cis-) cis-[Co. Cl 2(NH 3)4]+ транс- (trans-) trans-[Co. Cl 2(NH 3)4]+
![Геометрическая изомерия Например: [Pt. Cl 2(NH 3)2] диамминдихлороплатина Соль Пейроне Хлорид второго основания Рейзе Геометрическая изомерия Например: [Pt. Cl 2(NH 3)2] диамминдихлороплатина Соль Пейроне Хлорид второго основания Рейзе](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-82.jpg) Геометрическая изомерия Например: [Pt. Cl 2(NH 3)2] диамминдихлороплатина Соль Пейроне Хлорид второго основания Рейзе 1844 г. М. Пейроне Cl NH 3 Pt Cl Cl NH 3 Pt NH 3 Цис-изомер Оранжево-желтый Противоопухолевая активность! NH 3 Cl Транс-изомер Светло-желтый
Геометрическая изомерия Например: [Pt. Cl 2(NH 3)2] диамминдихлороплатина Соль Пейроне Хлорид второго основания Рейзе 1844 г. М. Пейроне Cl NH 3 Pt Cl Cl NH 3 Pt NH 3 Цис-изомер Оранжево-желтый Противоопухолевая активность! NH 3 Cl Транс-изомер Светло-желтый
![Сольватная изомерия [Cr(H 2 O)6]Cl 3 Фиолетовый [Cr. Cl(H 2 O)5]Cl 2 Светло-зеленый [Cr. Сольватная изомерия [Cr(H 2 O)6]Cl 3 Фиолетовый [Cr. Cl(H 2 O)5]Cl 2 Светло-зеленый [Cr.](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-83.jpg) Сольватная изомерия [Cr(H 2 O)6]Cl 3 Фиолетовый [Cr. Cl(H 2 O)5]Cl 2 Светло-зеленый [Cr. Cl 2(H 2 O)4]Cl Темно-зеленый
Сольватная изомерия [Cr(H 2 O)6]Cl 3 Фиолетовый [Cr. Cl(H 2 O)5]Cl 2 Светло-зеленый [Cr. Cl 2(H 2 O)4]Cl Темно-зеленый
![Оптическая изомерия Отражение [Co(En)2]3+ Оптическая изомерия Отражение [Co(En)2]3+](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-84.jpg) Оптическая изомерия Отражение [Co(En)2]3+
Оптическая изомерия Отражение [Co(En)2]3+
![mirror plane Пример: Энантиомерия cis-[Co(En)2 Cl 2]+ mirror plane Пример: Энантиомерия cis-[Co(En)2 Cl 2]+](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-85.jpg) mirror plane Пример: Энантиомерия cis-[Co(En)2 Cl 2]+
mirror plane Пример: Энантиомерия cis-[Co(En)2 Cl 2]+
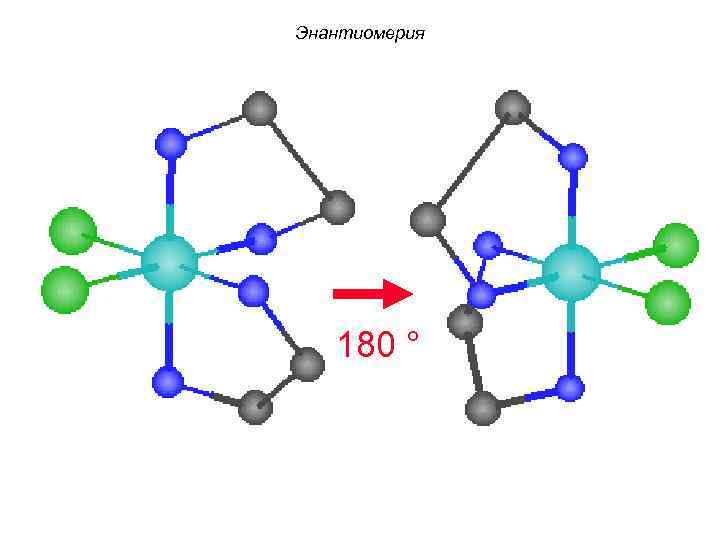 Энантиомерия 180 °
Энантиомерия 180 °
![Энантиомерия enantiome rs cis-[Co(En)2 Cl 2]+ Энантиомерия enantiome rs cis-[Co(En)2 Cl 2]+](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-87.jpg) Энантиомерия enantiome rs cis-[Co(En)2 Cl 2]+
Энантиомерия enantiome rs cis-[Co(En)2 Cl 2]+
 Хелаты. Комплексоны Лиганды могут присоединяться к комплексообразователю посредством одного или нескольких атомов, т. е. лиганды обладают координационной емкостью дентатностью. Монодентатные лиганды присоединяются к комплексообразователю одним атомом и образуют одну координационную связь. Например: H 2 O, NH 3, Cl-, CN-, OH- и др.
Хелаты. Комплексоны Лиганды могут присоединяться к комплексообразователю посредством одного или нескольких атомов, т. е. лиганды обладают координационной емкостью дентатностью. Монодентатные лиганды присоединяются к комплексообразователю одним атомом и образуют одну координационную связь. Например: H 2 O, NH 3, Cl-, CN-, OH- и др.
 Хелаты. Комплексоны. Краун-эфиры Полидентатные лиганды присоединяются к комплексообразователю посредством нескольких атомов. Например: функциональные органические соединения. Большое практическое значение имеют комплексоны – полидентатные лиганды, содержащие несколько функциональных групп и образующие прочные комплексы практически со всеми двухзарядными ионами металлов (Ca 2+, Mg 2+, Zn 2+, Cu 2+, Pt 2+…).
Хелаты. Комплексоны. Краун-эфиры Полидентатные лиганды присоединяются к комплексообразователю посредством нескольких атомов. Например: функциональные органические соединения. Большое практическое значение имеют комплексоны – полидентатные лиганды, содержащие несколько функциональных групп и образующие прочные комплексы практически со всеми двухзарядными ионами металлов (Ca 2+, Mg 2+, Zn 2+, Cu 2+, Pt 2+…).
 Хелаты. Комплексоны. Краун-эфиры Н-р, комплексон -I: Этилендиамин En содержит два атома азота. За счет электронных пар этих атомов этилендиамин присоединяется к комплексообразователю двумя координационными связями.
Хелаты. Комплексоны. Краун-эфиры Н-р, комплексон -I: Этилендиамин En содержит два атома азота. За счет электронных пар этих атомов этилендиамин присоединяется к комплексообразователю двумя координационными связями.
![Хелаты. Комплексоны. Краун-эфиры [Pt 2+(Еn)4]2+ этилендиаминплатина (II) Хелаты. Комплексоны. Краун-эфиры [Pt 2+(Еn)4]2+ этилендиаминплатина (II)](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-91.jpg) Хелаты. Комплексоны. Краун-эфиры [Pt 2+(Еn)4]2+ этилендиаминплатина (II)
Хелаты. Комплексоны. Краун-эфиры [Pt 2+(Еn)4]2+ этилендиаминплатина (II)
![Хелаты. Комплексоны. Краун-эфиры [Co 3+(Еn)4]3+ этилендиаминкобальт(II) Хелаты. Комплексоны. Краун-эфиры [Co 3+(Еn)4]3+ этилендиаминкобальт(II)](https://present5.com/presentation/3/-44888389_133772353.pdf-img/-44888389_133772353.pdf-92.jpg) Хелаты. Комплексоны. Краун-эфиры [Co 3+(Еn)4]3+ этилендиаминкобальт(II)
Хелаты. Комплексоны. Краун-эфиры [Co 3+(Еn)4]3+ этилендиаминкобальт(II)
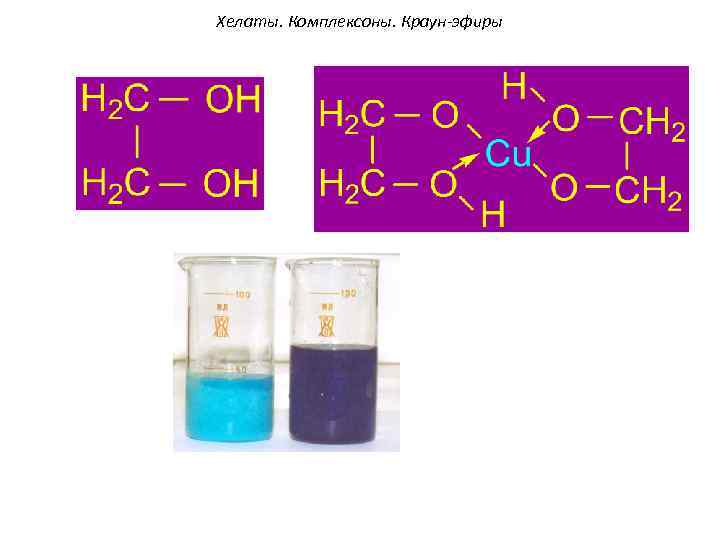
 Хелаты. Комплексоны. Краун-эфиры Для удобства координации молекулы полидентатных лигандов сворачиваются в циклы. В таких комплексах комплексообразователь зажат «клешней» лигандов. Комплексы, содержащие полидентатные лиганды, называются хелатами (от греч. chelate - клешня). Термин «хелат» , 1920 г. Морган и Дрю
Хелаты. Комплексоны. Краун-эфиры Для удобства координации молекулы полидентатных лигандов сворачиваются в циклы. В таких комплексах комплексообразователь зажат «клешней» лигандов. Комплексы, содержащие полидентатные лиганды, называются хелатами (от греч. chelate - клешня). Термин «хелат» , 1920 г. Морган и Дрю
 Хелаты. Комплексоны. Краун-эфиры
Хелаты. Комплексоны. Краун-эфиры
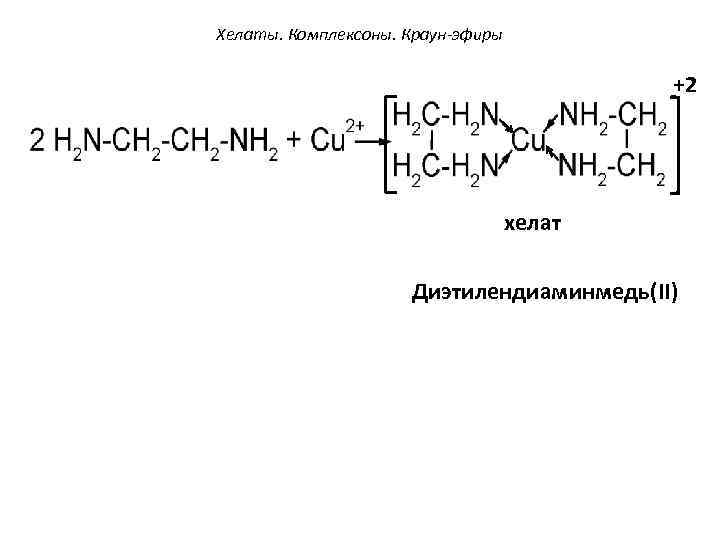 Хелаты. Комплексоны. Краун-эфиры +2 хелат Диэтилендиаминмедь(II)
Хелаты. Комплексоны. Краун-эфиры +2 хелат Диэтилендиаминмедь(II)
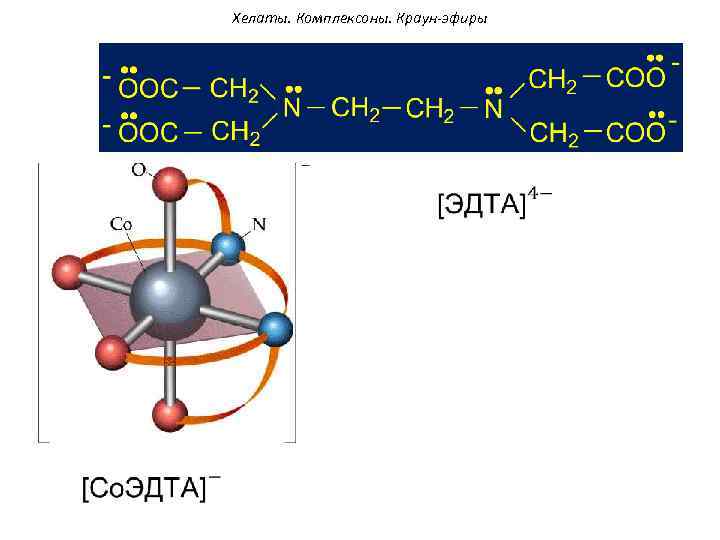
 Хелаты. Комплексоны. Краун-эфиры Обычно хелаты гораздо устойчивее комплексных соединений, содержащих монодентатные лиганды, т. к. комплексообразователь связан с лигандами несколькими донорно-акцепторными связями. Наиболее известными комплексонами высшего порядка являются: • комплексон -II этилендиаминтетрауксусная кислота (ЭДТА) • комплексон- III двузамещенная натриевая соль ЭДТА - Трилон Б: Na 2[H 2 Tr]
Хелаты. Комплексоны. Краун-эфиры Обычно хелаты гораздо устойчивее комплексных соединений, содержащих монодентатные лиганды, т. к. комплексообразователь связан с лигандами несколькими донорно-акцепторными связями. Наиболее известными комплексонами высшего порядка являются: • комплексон -II этилендиаминтетрауксусная кислота (ЭДТА) • комплексон- III двузамещенная натриевая соль ЭДТА - Трилон Б: Na 2[H 2 Tr]
 Хелаты. Комплексоны. Краун-эфиры
Хелаты. Комплексоны. Краун-эфиры
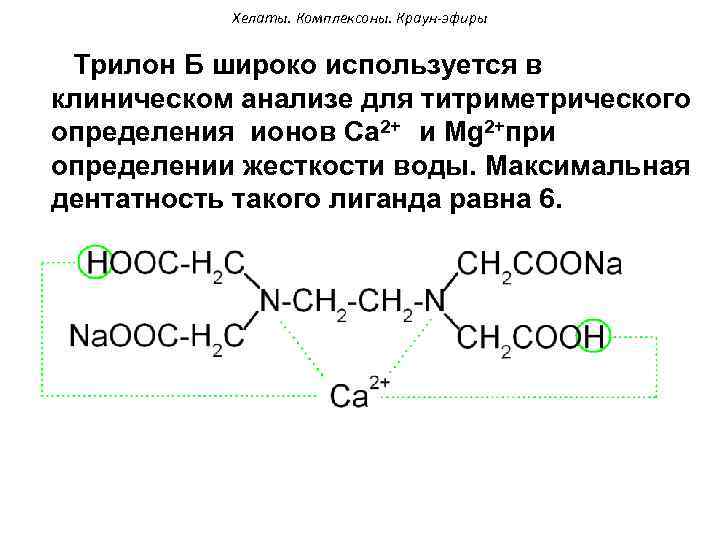 Хелаты. Комплексоны. Краун-эфиры Трилон Б широко используется в клиническом анализе для титриметрического определения ионов Са 2+ и Мg 2+при определении жесткости воды. Максимальная дентатность такого лиганда равна 6.
Хелаты. Комплексоны. Краун-эфиры Трилон Б широко используется в клиническом анализе для титриметрического определения ионов Са 2+ и Мg 2+при определении жесткости воды. Максимальная дентатность такого лиганда равна 6.
 Хелаты. Комплексоны. Краун-эфиры Особый тип полидентатных лигандов представляет собой циклические эфиры или краун-эфиры (от анг. crown - корона). В них донорные атомы кислорода заключены в плоский цикл определенного размера. Краун-эфиры содержат от 4 до 12 атомов кислорода (краун-4, краун-5 и т. д). Полости краун-эфиров имеют строго определенные размеры. Поэтому краун-эфиры могут избирательно связывать ионы металлов, размеры которых близки к размерам полости.
Хелаты. Комплексоны. Краун-эфиры Особый тип полидентатных лигандов представляет собой циклические эфиры или краун-эфиры (от анг. crown - корона). В них донорные атомы кислорода заключены в плоский цикл определенного размера. Краун-эфиры содержат от 4 до 12 атомов кислорода (краун-4, краун-5 и т. д). Полости краун-эфиров имеют строго определенные размеры. Поэтому краун-эфиры могут избирательно связывать ионы металлов, размеры которых близки к размерам полости.
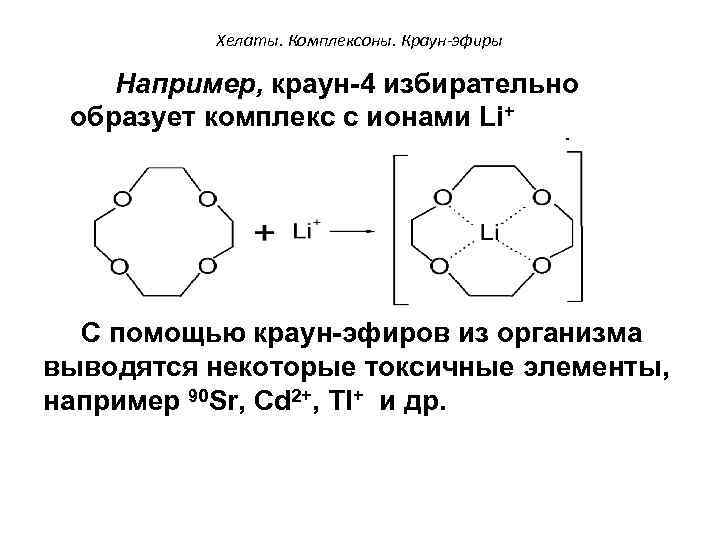 Хелаты. Комплексоны. Краун-эфиры Например, краун-4 избирательно образует комплекс с ионами Li+ + С помощью краун-эфиров из организма выводятся некоторые токсичные элементы, например 90 Sr, Cd 2+, Tl+ и др.
Хелаты. Комплексоны. Краун-эфиры Например, краун-4 избирательно образует комплекс с ионами Li+ + С помощью краун-эфиров из организма выводятся некоторые токсичные элементы, например 90 Sr, Cd 2+, Tl+ и др.
 СПАСИБО ЗА ВАШЕ ВНИМАНИЕ!
СПАСИБО ЗА ВАШЕ ВНИМАНИЕ!


