ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ











Сопряжение ароматичность фарм.pptx
- Количество слайдов: 31
 ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ ОРГАНИЧЕСКАЯ ХИМИЯ Электронное строение органических соединений 1. Виды сопряжения 2. Ароматичность 3. Электронные эффекты заместителей. Лектор: кандидат биологических наук, доцент Атавина Ольга Васильевна
ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ КАФЕДРА ХИМИИ ОРГАНИЧЕСКАЯ ХИМИЯ Электронное строение органических соединений 1. Виды сопряжения 2. Ароматичность 3. Электронные эффекты заместителей. Лектор: кандидат биологических наук, доцент Атавина Ольга Васильевна
 Виды сопряжения Сопряжение - явление выравнивания связей и зарядов в реальной молекуле по сравнению с идеальной, но несуществующей структурой. Различают 2 основных вида сопряжения: 1)π, π - сопряжение 2)p, π – сопряжение В сопряженных система возникает делокализованная связь, молекулярная орбиталь которой охватывает более двух атомов.
Виды сопряжения Сопряжение - явление выравнивания связей и зарядов в реальной молекуле по сравнению с идеальной, но несуществующей структурой. Различают 2 основных вида сопряжения: 1)π, π - сопряжение 2)p, π – сопряжение В сопряженных система возникает делокализованная связь, молекулярная орбиталь которой охватывает более двух атомов.
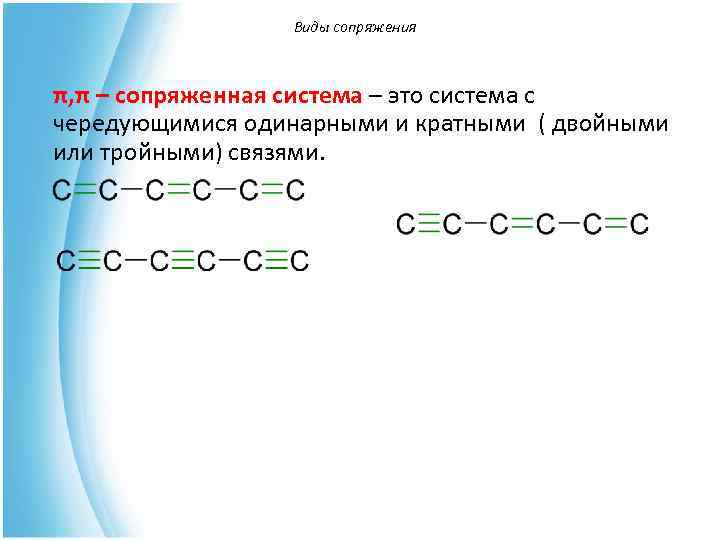
 Виды сопряжения π, π – сопряженная система – это система с чередующимися одинарными и кратными ( двойными или тройными) связями.
Виды сопряжения π, π – сопряженная система – это система с чередующимися одинарными и кратными ( двойными или тройными) связями.
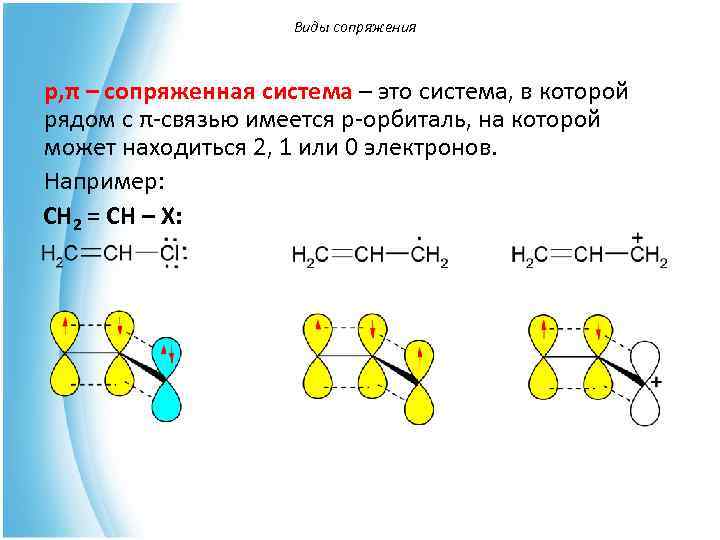
 Виды сопряжения p, π – сопряженная система – это система, в которой рядом с π-связью имеется р-орбиталь, на которой может находиться 2, 1 или 0 электронов. Например: CH 2 = CH – X:
Виды сопряжения p, π – сопряженная система – это система, в которой рядом с π-связью имеется р-орбиталь, на которой может находиться 2, 1 или 0 электронов. Например: CH 2 = CH – X:
 Виды сопряжения Сопряжённые системы бывают с открытой и замкнутой цепью сопряжения. Системы с открытой цепью сопряжения 1) π, π-cопряженная система бутадиена-1, 3 CH 2=CH-CH=CH 2 В молекуле этого вещества все атомы углерода находятся в состоянии sp 2 -гибридизации.
Виды сопряжения Сопряжённые системы бывают с открытой и замкнутой цепью сопряжения. Системы с открытой цепью сопряжения 1) π, π-cопряженная система бутадиена-1, 3 CH 2=CH-CH=CH 2 В молекуле этого вещества все атомы углерода находятся в состоянии sp 2 -гибридизации.
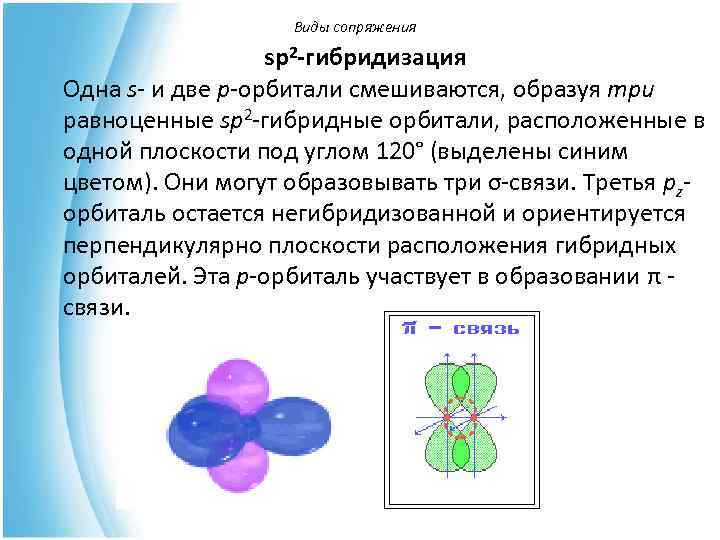
 Виды сопряжения sp 2 -гибридизация Одна s- и две p-орбитали смешиваются, образуя три равноценные sp 2 -гибридные орбитали, расположенные в одной плоскости под углом 120° (выделены синим цветом). Они могут образовывать три σ-связи. Третья рz- орбиталь остается негибридизованной и ориентируется перпендикулярно плоскости расположения гибридных орбиталей. Эта р-орбиталь участвует в образовании π - связи.
Виды сопряжения sp 2 -гибридизация Одна s- и две p-орбитали смешиваются, образуя три равноценные sp 2 -гибридные орбитали, расположенные в одной плоскости под углом 120° (выделены синим цветом). Они могут образовывать три σ-связи. Третья рz- орбиталь остается негибридизованной и ориентируется перпендикулярно плоскости расположения гибридных орбиталей. Эта р-орбиталь участвует в образовании π - связи.
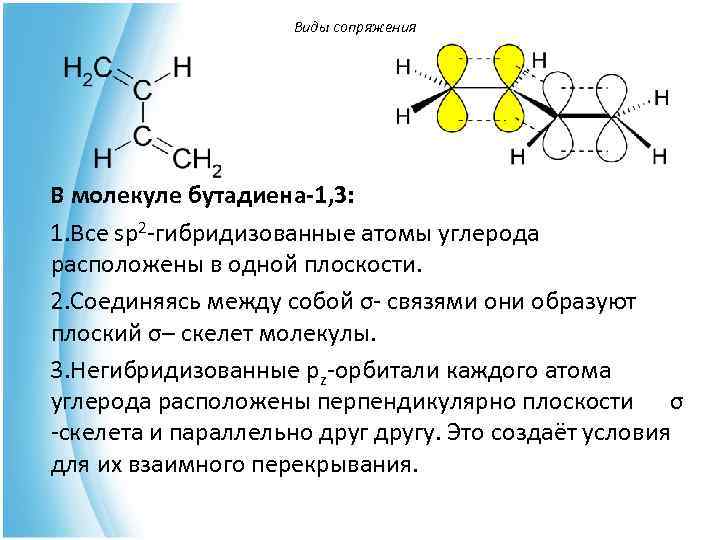
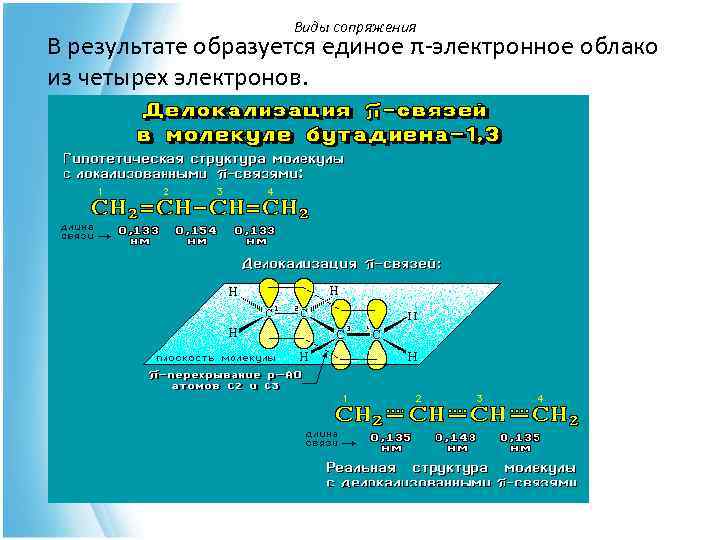
 Виды сопряжения В молекуле бутадиена-1, 3: 1. Все sp 2 -гибридизованные атомы углерода расположены в одной плоскости. 2. Соединяясь между собой σ- связями они образуют плоский σ– скелет молекулы. 3. Негибридизованные рz-орбитали каждого атома углерода расположены перпендикулярно плоскости σ -скелета и параллельно другу. Это создаёт условия для их взаимного перекрывания.
Виды сопряжения В молекуле бутадиена-1, 3: 1. Все sp 2 -гибридизованные атомы углерода расположены в одной плоскости. 2. Соединяясь между собой σ- связями они образуют плоский σ– скелет молекулы. 3. Негибридизованные рz-орбитали каждого атома углерода расположены перпендикулярно плоскости σ -скелета и параллельно другу. Это создаёт условия для их взаимного перекрывания.
 Виды сопряжения В результате образуется единое π-электронное облако из четырех электронов.
Виды сопряжения В результате образуется единое π-электронное облако из четырех электронов.
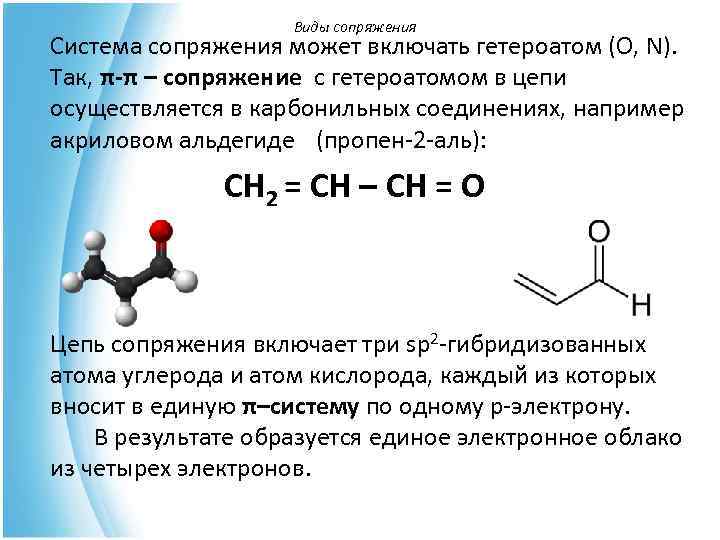
 Виды сопряжения Система сопряжения может включать гетероатом (О, N). Так, π-π – сопряжение c гетероатомом в цепи осуществляется в карбонильных соединениях, например акриловом альдегиде (пропен-2 -аль): СН 2 = СН – СН = О Цепь сопряжения включает три sp 2 -гибридизованных атома углерода и атом кислорода, каждый из которых вносит в единую π–систему по одному р-электрону. В результате образуется единое электронное облако из четырех электронов.
Виды сопряжения Система сопряжения может включать гетероатом (О, N). Так, π-π – сопряжение c гетероатомом в цепи осуществляется в карбонильных соединениях, например акриловом альдегиде (пропен-2 -аль): СН 2 = СН – СН = О Цепь сопряжения включает три sp 2 -гибридизованных атома углерода и атом кислорода, каждый из которых вносит в единую π–систему по одному р-электрону. В результате образуется единое электронное облако из четырех электронов.
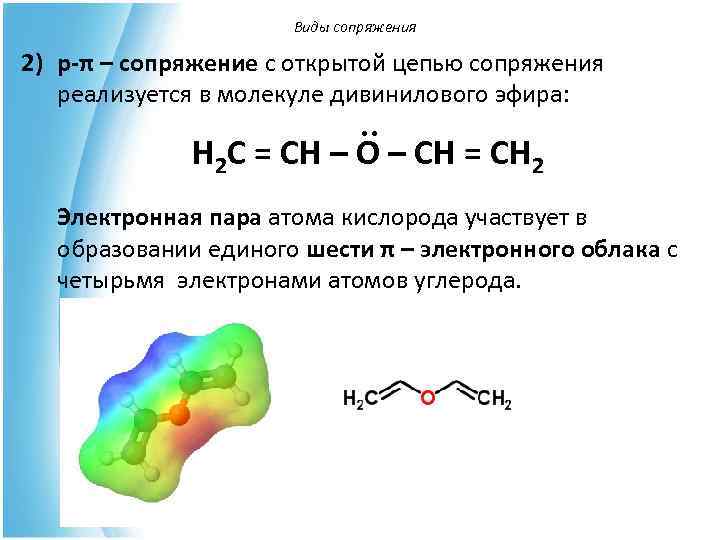
 Виды сопряжения 2) p-π – сопряжение с открытой цепью сопряжения реализуется в молекуле дивинилового эфира: . . H 2 C = CH – O – CH = CH 2 Электронная пара атома кислорода участвует в образовании единого шести π – электронного облака с четырьмя электронами атомов углерода.
Виды сопряжения 2) p-π – сопряжение с открытой цепью сопряжения реализуется в молекуле дивинилового эфира: . . H 2 C = CH – O – CH = CH 2 Электронная пара атома кислорода участвует в образовании единого шести π – электронного облака с четырьмя электронами атомов углерода.
 Устойчивость сопряженных систем О термодинамической устойчивости сопряженной системы можно судить по величине энергии сопряжения, которая выделяется при образовании сопряженной системы. Чем выше уровень энергии сопряжения, тем выше термодинамическая устойчивость соединения. С увеличением длины сопряженной цепи энергия сопряжения возрастает. Замкнутые сопряженные цепи (ароматические) более стабильны, чем открытые. Есопр. (Бутадиен-1, 3)=15 к. Дж/моль Есопр. (бензол) =150, 6 к. Дж/моль
Устойчивость сопряженных систем О термодинамической устойчивости сопряженной системы можно судить по величине энергии сопряжения, которая выделяется при образовании сопряженной системы. Чем выше уровень энергии сопряжения, тем выше термодинамическая устойчивость соединения. С увеличением длины сопряженной цепи энергия сопряжения возрастает. Замкнутые сопряженные цепи (ароматические) более стабильны, чем открытые. Есопр. (Бутадиен-1, 3)=15 к. Дж/моль Есопр. (бензол) =150, 6 к. Дж/моль
 Ароматичность Системы с замкнутой цепью сопряжения Ароматичность Ароматическими называют циклические соединения, имеющие замкнутую сопряженную систему, единое π - электронное облако в которых делокализовано на всех атомах цикла.
Ароматичность Системы с замкнутой цепью сопряжения Ароматичность Ароматическими называют циклические соединения, имеющие замкнутую сопряженную систему, единое π - электронное облако в которых делокализовано на всех атомах цикла.
 Ароматичность Критерии ароматичности (Хюккель, 1931 г. ) Эрих Арманд Артур Йозеф 1896 г. – 1980 г. 1) Молекула имеет циклическое строение 2) Все атомы цикла находятся в состоянии sp 2 –гибридизации, образуя плоский σ–скелет молекулы. Негибридные рz-орбитали располагаются перпендикулярно плоскости σ–скелета и параллельно другу, сорздавая возможность для их взаимного перекрывания. 3) Существует единая π–электронная система, охватывающая все атомы цикла и содержащая по правилу Хюккеля (4 n+2) = π – электронов , где n-натуральный ряд чисел ( 0, 1, 2 и т. д. )
Ароматичность Критерии ароматичности (Хюккель, 1931 г. ) Эрих Арманд Артур Йозеф 1896 г. – 1980 г. 1) Молекула имеет циклическое строение 2) Все атомы цикла находятся в состоянии sp 2 –гибридизации, образуя плоский σ–скелет молекулы. Негибридные рz-орбитали располагаются перпендикулярно плоскости σ–скелета и параллельно другу, сорздавая возможность для их взаимного перекрывания. 3) Существует единая π–электронная система, охватывающая все атомы цикла и содержащая по правилу Хюккеля (4 n+2) = π – электронов , где n-натуральный ряд чисел ( 0, 1, 2 и т. д. )
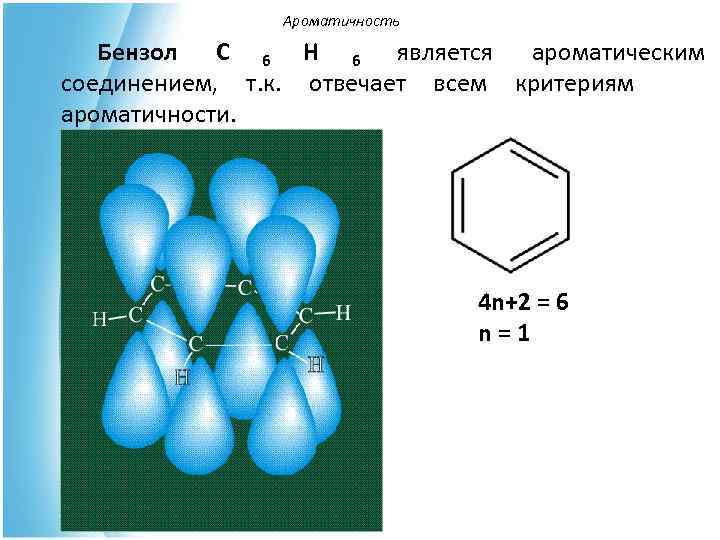
 Ароматичность Бензол С 6 Н 6 является ароматическим соединением, т. к. отвечает всем критериям ароматичности. 4 n+2 = 6 n=1
Ароматичность Бензол С 6 Н 6 является ароматическим соединением, т. к. отвечает всем критериям ароматичности. 4 n+2 = 6 n=1
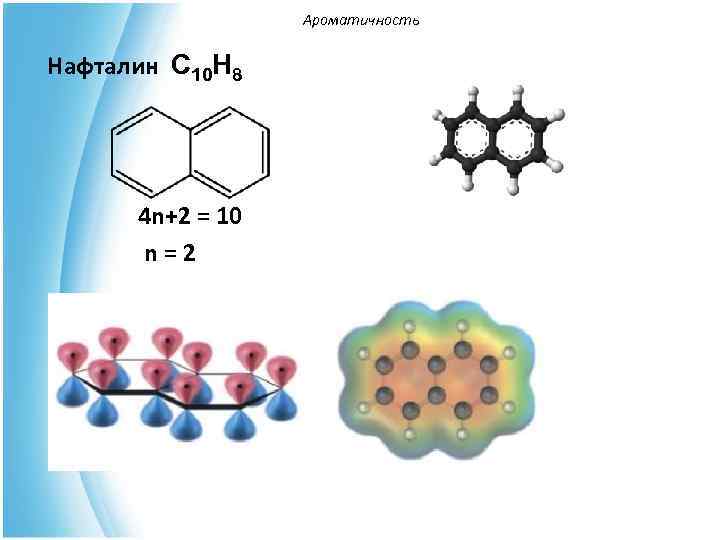
 Ароматичность Нафталин С 10 Н 8 4 n+2 = 10 n=2
Ароматичность Нафталин С 10 Н 8 4 n+2 = 10 n=2
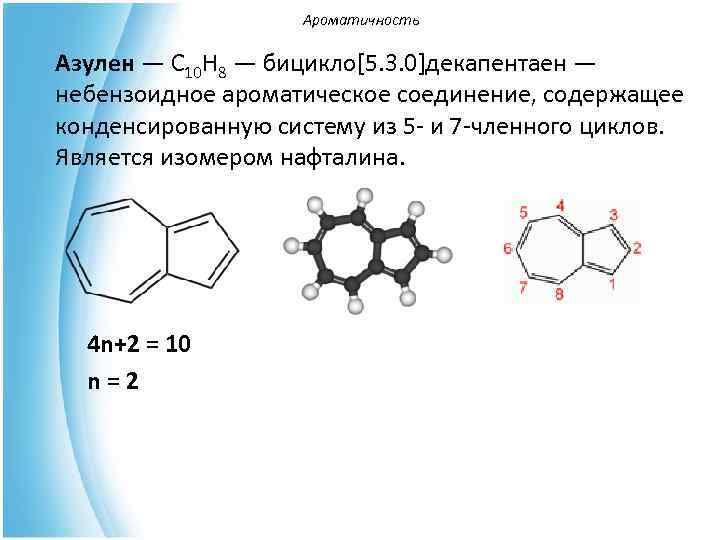
 Ароматичность Азулен — С 10 Н 8 — бицикло[5. 3. 0]декапентаен — небензоидное ароматическое соединение, содержащее конденсированную систему из 5 - и 7 -членного циклов. Является изомером нафталина. 4 n+2 = 10 n=2
Ароматичность Азулен — С 10 Н 8 — бицикло[5. 3. 0]декапентаен — небензоидное ароматическое соединение, содержащее конденсированную систему из 5 - и 7 -членного циклов. Является изомером нафталина. 4 n+2 = 10 n=2
 Ароматичность Производные азулена содержатся в эфирных маслах ряда лекарственных растений, в том числе ромашке аптечной, эвкалипте, некоторых видах полыни, с чем связывают противовоспалительное действие этих растений.
Ароматичность Производные азулена содержатся в эфирных маслах ряда лекарственных растений, в том числе ромашке аптечной, эвкалипте, некоторых видах полыни, с чем связывают противовоспалительное действие этих растений.
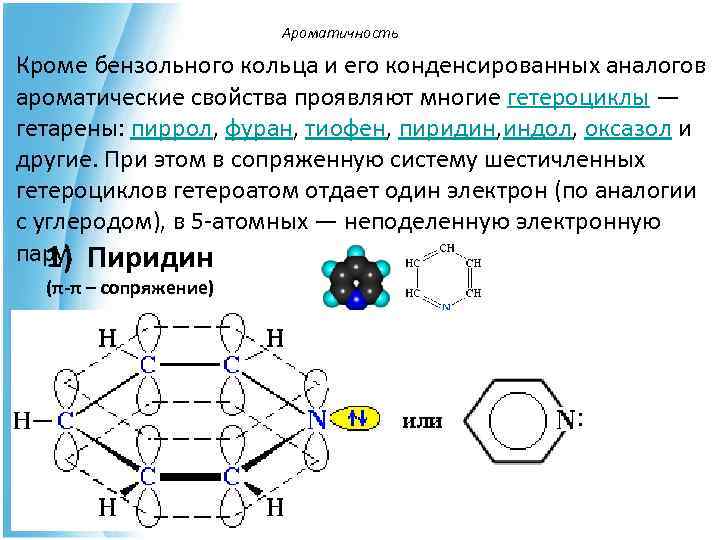
 Ароматичность Кроме бензольного кольца и его конденсированных аналогов ароматические свойства проявляют многие гетероциклы — гетарены: пиррол, фуран, тиофен, пиридин, индол, оксазол и другие. При этом в сопряженную систему шестичленных гетероциклов гетероатом отдает один электрон (по аналогии с углеродом), в 5 -атомных — неподеленную электронную пару. Пиридин 1) (π-π – сопряжение)
Ароматичность Кроме бензольного кольца и его конденсированных аналогов ароматические свойства проявляют многие гетероциклы — гетарены: пиррол, фуран, тиофен, пиридин, индол, оксазол и другие. При этом в сопряженную систему шестичленных гетероциклов гетероатом отдает один электрон (по аналогии с углеродом), в 5 -атомных — неподеленную электронную пару. Пиридин 1) (π-π – сопряжение)
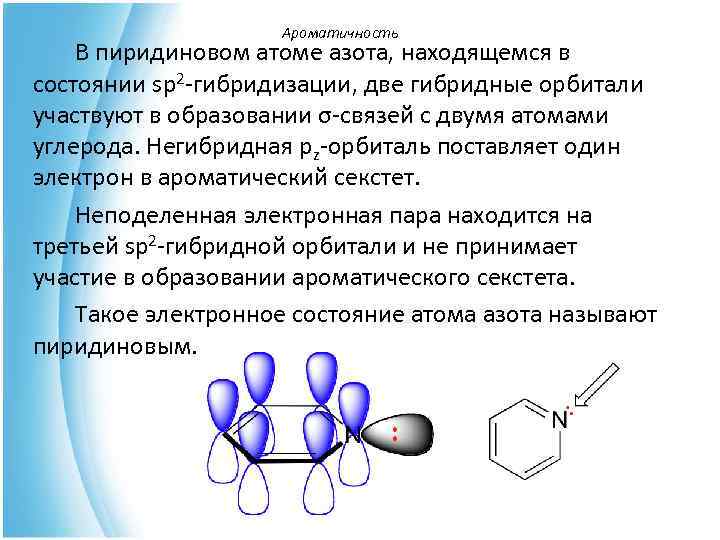
 Ароматичность В пиридиновом атоме азота, находящемся в состоянии sp 2 -гибридизации, две гибридные орбитали участвуют в образовании σ-связей с двумя атомами углерода. Негибридная рz-орбиталь поставляет один электрон в ароматический секстет. Неподеленная электронная пара находится на третьей sp 2 -гибридной орбитали и не принимает участие в образовании ароматического секстета. Такое электронное состояние атома азота называют пиридиновым.
Ароматичность В пиридиновом атоме азота, находящемся в состоянии sp 2 -гибридизации, две гибридные орбитали участвуют в образовании σ-связей с двумя атомами углерода. Негибридная рz-орбиталь поставляет один электрон в ароматический секстет. Неподеленная электронная пара находится на третьей sp 2 -гибридной орбитали и не принимает участие в образовании ароматического секстета. Такое электронное состояние атома азота называют пиридиновым.
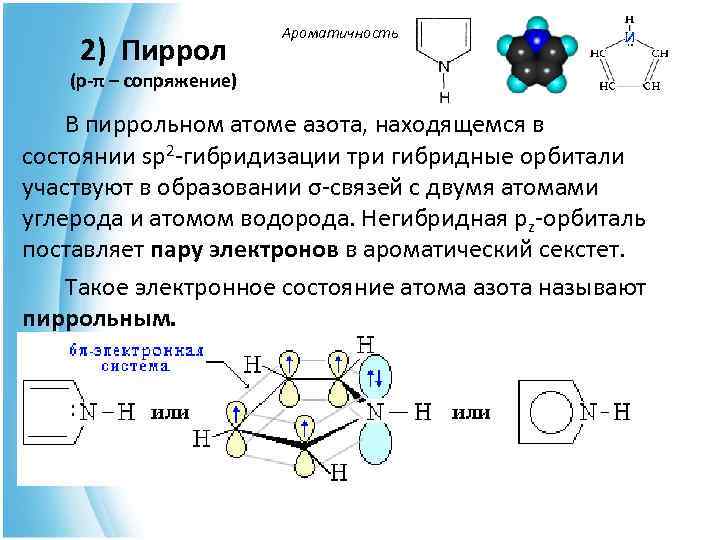
 Ароматичность 2) Пиррол (p-π – сопряжение) В пиррольном атоме азота, находящемся в состоянии sp 2 -гибридизации три гибридные орбитали участвуют в образовании σ-связей с двумя атомами углерода и атомом водорода. Негибридная рz-орбиталь поставляет пару электронов в ароматический секстет. Такое электронное состояние атома азота называют пиррольным.
Ароматичность 2) Пиррол (p-π – сопряжение) В пиррольном атоме азота, находящемся в состоянии sp 2 -гибридизации три гибридные орбитали участвуют в образовании σ-связей с двумя атомами углерода и атомом водорода. Негибридная рz-орбиталь поставляет пару электронов в ароматический секстет. Такое электронное состояние атома азота называют пиррольным.
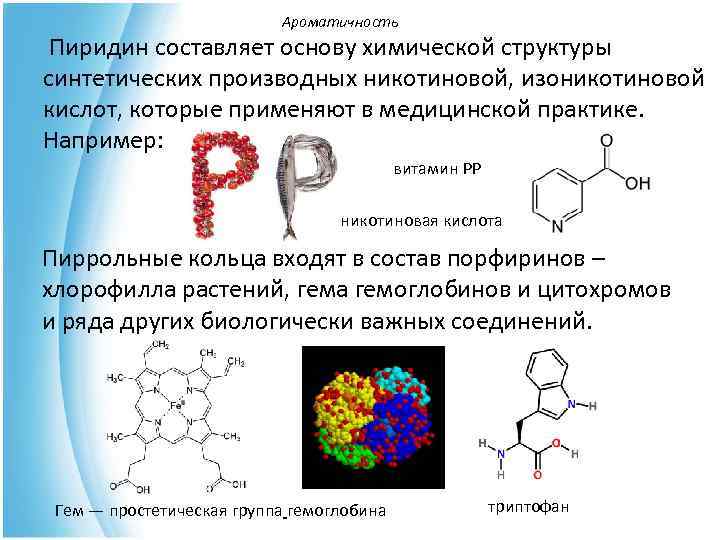
 Ароматичность Пиридин составляет основу химической структуры синтетических производных никотиновой, изоникотиновой кислот, которые применяют в медицинской практике. Например: витамин PP никотиновая кислота Пиррольные кольца входят в состав порфиринов – хлорофилла растений, гема гемоглобинов и цитохромов и ряда других биологически важных соединений. Гем — простетическая группа гемоглобина триптофан
Ароматичность Пиридин составляет основу химической структуры синтетических производных никотиновой, изоникотиновой кислот, которые применяют в медицинской практике. Например: витамин PP никотиновая кислота Пиррольные кольца входят в состав порфиринов – хлорофилла растений, гема гемоглобинов и цитохромов и ряда других биологически важных соединений. Гем — простетическая группа гемоглобина триптофан
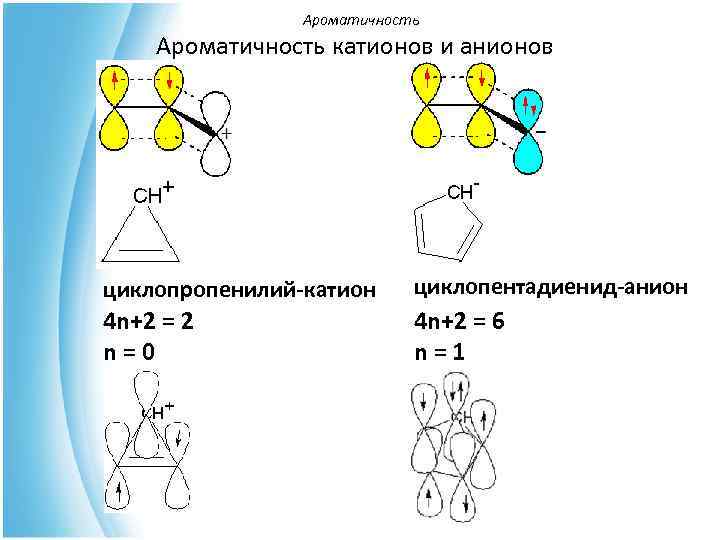
 Ароматичность катионов и анионов циклопропенилий-катион циклопентадиенид-анион 4 n+2 = 2 4 n+2 = 6 n=0 n=1
Ароматичность катионов и анионов циклопропенилий-катион циклопентадиенид-анион 4 n+2 = 2 4 n+2 = 6 n=0 n=1
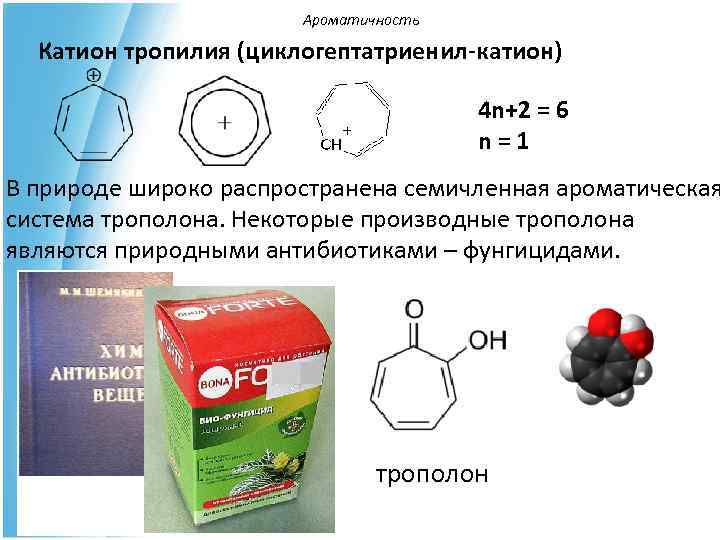
 Ароматичность Катион тропилия (циклогептатриенил-катион) 4 n+2 = 6 n=1 В природе широко распространена семичленная ароматическая система трополона. Некоторые производные трополона являются природными антибиотиками – фунгицидами. трополон
Ароматичность Катион тропилия (циклогептатриенил-катион) 4 n+2 = 6 n=1 В природе широко распространена семичленная ароматическая система трополона. Некоторые производные трополона являются природными антибиотиками – фунгицидами. трополон
 Электронные эффекты заместителей ИНДУКТИВНЫЙ ЭФФЕКТ - это передача электронного влияния заместителя по цепи сигма – связей. Индуктивный эффект обозначают буквой I и графически изображают стрелкой, остриё которой направлено в сторону более электроотрицательного элемента. Действие индуктивного эффекта наиболее сильно проявляется на двух ближайших атомах углерода, а через 3 -4 связи он затухает:
Электронные эффекты заместителей ИНДУКТИВНЫЙ ЭФФЕКТ - это передача электронного влияния заместителя по цепи сигма – связей. Индуктивный эффект обозначают буквой I и графически изображают стрелкой, остриё которой направлено в сторону более электроотрицательного элемента. Действие индуктивного эффекта наиболее сильно проявляется на двух ближайших атомах углерода, а через 3 -4 связи он затухает:
 Электронные эффекты заместителей Заместители, смещающие электронную плотность по цепи сигма – связей в свою сторону, проявляют отрицательный индуктивный эффект (-I). Это электроноакцепторные заместители (ЭА). Они снижают электронную плотность в углеродной цепи. (-ОН; -NН 2; -СООН; -СНО; галогены) Например: СН 3 -СН 2→ОН -ОН: (- I ) ЭА этанол Заместители, смещающие электронную плотность от себя в сторону углеродной цепи, проявляют положительный индуктивный эффект (+I). Это электронодонорные (ЭД) заместители, например, радикалы метил и этил (-CH 3, -C 2 H 5), металлы(-Mg-, -Li и др. )
Электронные эффекты заместителей Заместители, смещающие электронную плотность по цепи сигма – связей в свою сторону, проявляют отрицательный индуктивный эффект (-I). Это электроноакцепторные заместители (ЭА). Они снижают электронную плотность в углеродной цепи. (-ОН; -NН 2; -СООН; -СНО; галогены) Например: СН 3 -СН 2→ОН -ОН: (- I ) ЭА этанол Заместители, смещающие электронную плотность от себя в сторону углеродной цепи, проявляют положительный индуктивный эффект (+I). Это электронодонорные (ЭД) заместители, например, радикалы метил и этил (-CH 3, -C 2 H 5), металлы(-Mg-, -Li и др. )
 Электронные эффекты заместителей Мезомерный эффект – это передача электронного влияния заместителя по сопряжённой системе. Действие мезомерного эффекта заместителей проявляется как в открытых, так и замкнутых системах.
Электронные эффекты заместителей Мезомерный эффект – это передача электронного влияния заместителя по сопряжённой системе. Действие мезомерного эффекта заместителей проявляется как в открытых, так и замкнутых системах.
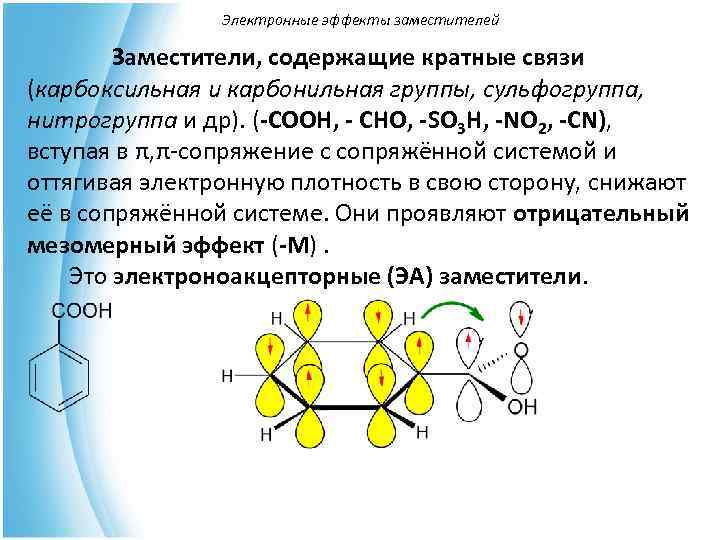
 Электронные эффекты заместителей Заместители, содержащие кратные связи (карбоксильная и карбонильная группы, сульфогруппа, нитрогруппа и др). (-COOH, - CHO, -SO 3 H, -NO 2, -CN), вступая в π, π-сопряжение с сопряжённой системой и оттягивая электронную плотность в свою сторону, снижают её в сопряжённой системе. Они проявляют отрицательный мезомерный эффект (-М). Это электроноакцепторные (ЭА) заместители.
Электронные эффекты заместителей Заместители, содержащие кратные связи (карбоксильная и карбонильная группы, сульфогруппа, нитрогруппа и др). (-COOH, - CHO, -SO 3 H, -NO 2, -CN), вступая в π, π-сопряжение с сопряжённой системой и оттягивая электронную плотность в свою сторону, снижают её в сопряжённой системе. Они проявляют отрицательный мезомерный эффект (-М). Это электроноакцепторные (ЭА) заместители.
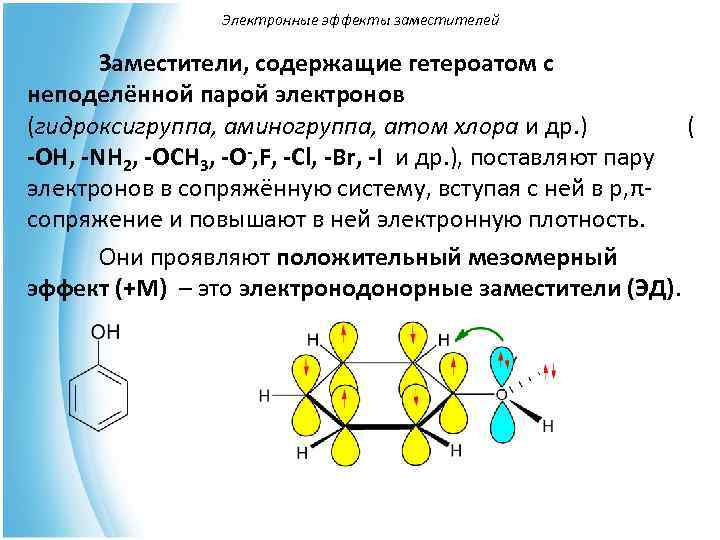
 Электронные эффекты заместителей Заместители, содержащие гетероатом с неподелённой парой электронов (гидроксигруппа, аминогруппа, атом хлора и др. ) ( -OH, -NH 2, -OCH 3, -O-, F, -Cl, -Br, -I и др. ), поставляют пару электронов в сопряжённую систему, вступая с ней в р, π- сопряжение и повышают в ней электронную плотность. Они проявляют положительный мезомерный эффект (+М) – это электронодонорные заместители (ЭД).
Электронные эффекты заместителей Заместители, содержащие гетероатом с неподелённой парой электронов (гидроксигруппа, аминогруппа, атом хлора и др. ) ( -OH, -NH 2, -OCH 3, -O-, F, -Cl, -Br, -I и др. ), поставляют пару электронов в сопряжённую систему, вступая с ней в р, π- сопряжение и повышают в ней электронную плотность. Они проявляют положительный мезомерный эффект (+М) – это электронодонорные заместители (ЭД).
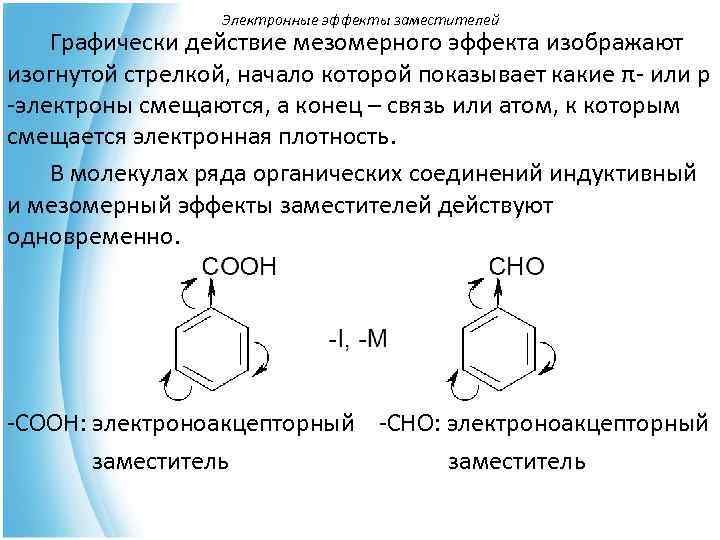
 Электронные эффекты заместителей Графически действие мезомерного эффекта изображают изогнутой стрелкой, начало которой показывает какие π- или р -электроны смещаются, а конец – связь или атом, к которым смещается электронная плотность. В молекулах ряда органических соединений индуктивный и мезомерный эффекты заместителей действуют одновременно. -СООН: электроноакцепторный -СНО: электроноакцепторный заместитель
Электронные эффекты заместителей Графически действие мезомерного эффекта изображают изогнутой стрелкой, начало которой показывает какие π- или р -электроны смещаются, а конец – связь или атом, к которым смещается электронная плотность. В молекулах ряда органических соединений индуктивный и мезомерный эффекты заместителей действуют одновременно. -СООН: электроноакцепторный -СНО: электроноакцепторный заместитель
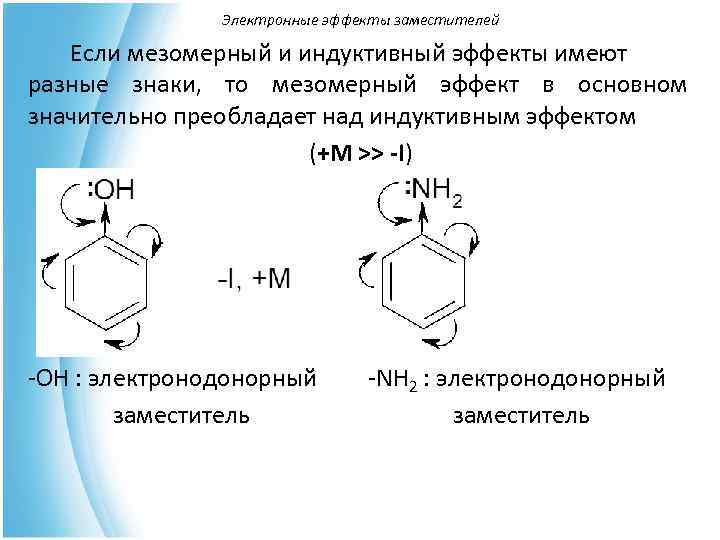
 Электронные эффекты заместителей Если мезомерный и индуктивный эффекты имеют разные знаки, то мезомерный эффект в основном значительно преобладает над индуктивным эффектом (+M >> -I) -ОН : электронодонорный -NH 2 : электронодонорный заместитель
Электронные эффекты заместителей Если мезомерный и индуктивный эффекты имеют разные знаки, то мезомерный эффект в основном значительно преобладает над индуктивным эффектом (+M >> -I) -ОН : электронодонорный -NH 2 : электронодонорный заместитель
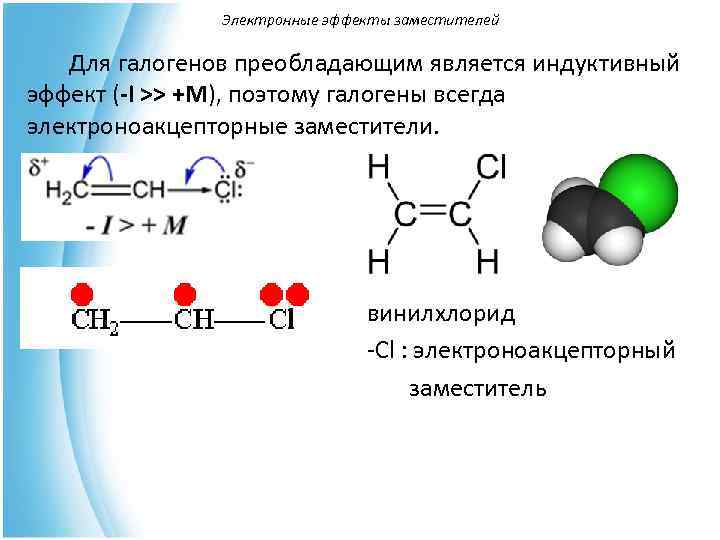
 Электронные эффекты заместителей Для галогенов преобладающим является индуктивный эффект (-I >> +M), поэтому галогены всегда электроноакцепторные заместители. винилхлорид -Сl : электроноакцепторный заместитель
Электронные эффекты заместителей Для галогенов преобладающим является индуктивный эффект (-I >> +M), поэтому галогены всегда электроноакцепторные заместители. винилхлорид -Сl : электроноакцепторный заместитель

