7d7bd622bad9436683e3f15687a08fd1.ppt
- Количество слайдов: 34

 Олимпиадные задачи по органической химии
Олимпиадные задачи по органической химии
 Задача № 5 (10 класс) Восстановление ароматических соединений под действием щелочных металлов в жидких безводных алкиламинах (реакция Бенкезера) позволяет в зависимости от условий проведения реакции получать различные соединения. Например, реакция нафталина с литием в этиламине при – 78°С дает смесь двух изомерных соединений (А и В). Каждый из продуктов (А и В) легко реагируют с бромом, образуя продукты C и D, содержащие по 53, 98% Br (по массе). Озонирование А и В дает изомерные продукты Е и F, соответственно. Взаимодействие 0, 1346 г вещества F с аммиачным раствором оксида серебра приводит к выделению 0, 1726 г серебра. Вещество Е с аммиачным раствором оксида серебра не реагирует. 1. Установите строение соединений A – F. 2. Напишите схемы указанных в задаче превращений. 3. Какой из продуктов (А или В) образуется в большем количестве и почему? 4. Почему, по Вашему мнению, введение алкильных заместителей в молекулу нафталина приводит к снижению скорости реакции? 5. С какой целью при проведении озонирования в реакционную смесь добавляют какой-нибудь восстановитель?
Задача № 5 (10 класс) Восстановление ароматических соединений под действием щелочных металлов в жидких безводных алкиламинах (реакция Бенкезера) позволяет в зависимости от условий проведения реакции получать различные соединения. Например, реакция нафталина с литием в этиламине при – 78°С дает смесь двух изомерных соединений (А и В). Каждый из продуктов (А и В) легко реагируют с бромом, образуя продукты C и D, содержащие по 53, 98% Br (по массе). Озонирование А и В дает изомерные продукты Е и F, соответственно. Взаимодействие 0, 1346 г вещества F с аммиачным раствором оксида серебра приводит к выделению 0, 1726 г серебра. Вещество Е с аммиачным раствором оксида серебра не реагирует. 1. Установите строение соединений A – F. 2. Напишите схемы указанных в задаче превращений. 3. Какой из продуктов (А или В) образуется в большем количестве и почему? 4. Почему, по Вашему мнению, введение алкильных заместителей в молекулу нафталина приводит к снижению скорости реакции? 5. С какой целью при проведении озонирования в реакционную смесь добавляют какой-нибудь восстановитель?
 Решение Способность продуктов А и В взаимодействовать с бромом и озоном указывает на их непредельный характер. Молярная масса C и D может быть вычислена из данных по содержанию брома: M(C) = M(D) = n. M(Br): ω(Br), где n – число атомов брома в молекуле. При n = 2 M(C) = M(D) =2· 79, 90: 0, 5398 = 296, 04. Эта молярная масса соответствует соединениям с формулой C 10 H 16 Br 2. Очевидно, что соединения А и В имеют формулу C 10 H 16 и содержат одну двойную связь. Таких изомерных углеводородов может быть 4: Их озонирование приводит к соответствующим дикарбонильным соединениям:
Решение Способность продуктов А и В взаимодействовать с бромом и озоном указывает на их непредельный характер. Молярная масса C и D может быть вычислена из данных по содержанию брома: M(C) = M(D) = n. M(Br): ω(Br), где n – число атомов брома в молекуле. При n = 2 M(C) = M(D) =2· 79, 90: 0, 5398 = 296, 04. Эта молярная масса соответствует соединениям с формулой C 10 H 16 Br 2. Очевидно, что соединения А и В имеют формулу C 10 H 16 и содержат одну двойную связь. Таких изомерных углеводородов может быть 4: Их озонирование приводит к соответствующим дикарбонильным соединениям:
![Решение Реакция альдегидов с реактивом Толленса идет согласно уравнению: R-CHO + 2[Ag(NH 3)2]OH = Решение Реакция альдегидов с реактивом Толленса идет согласно уравнению: R-CHO + 2[Ag(NH 3)2]OH =](https://present5.com/presentation/7d7bd622bad9436683e3f15687a08fd1/image-5.jpg) Решение Реакция альдегидов с реактивом Толленса идет согласно уравнению: R-CHO + 2[Ag(NH 3)2]OH = R-COO– NH 4+ + 2 Ag + 3 NH 3 + H 2 O, то есть на каждую альдегидную группу выделяется 2 атома серебра. В реакцию вступило 0, 1346: 168, 24 = 0, 0008 моль вещества F, а выделилось 0, 1726: 107, 87 = 0, 0016 моль серебра. Следовательно, в соединении F содержится только одна альдегидная группа, то есть F – это первый из представленных изомеров. Вещество Е не имеет альдегидных групп, это – последний изомер.
Решение Реакция альдегидов с реактивом Толленса идет согласно уравнению: R-CHO + 2[Ag(NH 3)2]OH = R-COO– NH 4+ + 2 Ag + 3 NH 3 + H 2 O, то есть на каждую альдегидную группу выделяется 2 атома серебра. В реакцию вступило 0, 1346: 168, 24 = 0, 0008 моль вещества F, а выделилось 0, 1726: 107, 87 = 0, 0016 моль серебра. Следовательно, в соединении F содержится только одна альдегидная группа, то есть F – это первый из представленных изомеров. Вещество Е не имеет альдегидных групп, это – последний изомер.
 Решение Описанные в задаче превращения могут быть описаны схемой: Изомер А должен образовываться в несколько большем количестве, так как он является наиболее замещенным алкеном из всех возможных октагидронафталинов, а следовательно, наиболее устойчивым.
Решение Описанные в задаче превращения могут быть описаны схемой: Изомер А должен образовываться в несколько большем количестве, так как он является наиболее замещенным алкеном из всех возможных октагидронафталинов, а следовательно, наиболее устойчивым.
 Решение На начальной стадии реакции литий передает свой электрон на молекулу нафталина. Введение алкильных заместителей, обладающих +I-эффектами, повышает электронную плотность в ароматическом ядре нафталина, что затрудняет передачу электрона от восстановителя и уменьшает скорость реакции. При озонировании выделяется перекись водорода, которая может окислять альдегидв и искажать результаты эксперимента. Поэтому ее разрушают подходящим восстановителем (Me 2 S, Bu 3 P, Zn и т. д. ).
Решение На начальной стадии реакции литий передает свой электрон на молекулу нафталина. Введение алкильных заместителей, обладающих +I-эффектами, повышает электронную плотность в ароматическом ядре нафталина, что затрудняет передачу электрона от восстановителя и уменьшает скорость реакции. При озонировании выделяется перекись водорода, которая может окислять альдегидв и искажать результаты эксперимента. Поэтому ее разрушают подходящим восстановителем (Me 2 S, Bu 3 P, Zn и т. д. ).
 Задача № 6 (10 класс) Смесь паров веществ X и Y в соотношении 1: 3 (по объему) имеет плотность по водороду 33, 25, а в соотношении 3: 1 – 45, 75. Эмульсию 4, 78 г сополимера Z, образованного веществами X и Y, обработали раствором брома в четыреххлористом углероде. При этом в реакцию вступило 8, 00 г брома. Вычислите соотношение звеньев X и Y в Z. l В результате длительного нагревания X и Y в толуоле образуется соединение A, при дегидрировании которого можно получить углеводород B с массовой долей углерода 93, 51%. l Изобразите структурные формулы A, B, X, Y. l
Задача № 6 (10 класс) Смесь паров веществ X и Y в соотношении 1: 3 (по объему) имеет плотность по водороду 33, 25, а в соотношении 3: 1 – 45, 75. Эмульсию 4, 78 г сополимера Z, образованного веществами X и Y, обработали раствором брома в четыреххлористом углероде. При этом в реакцию вступило 8, 00 г брома. Вычислите соотношение звеньев X и Y в Z. l В результате длительного нагревания X и Y в толуоле образуется соединение A, при дегидрировании которого можно получить углеводород B с массовой долей углерода 93, 51%. l Изобразите структурные формулы A, B, X, Y. l
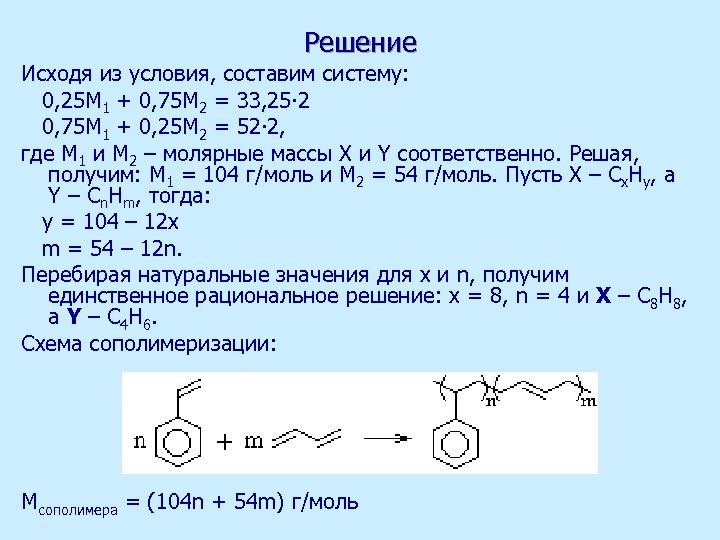 Решение Исходя из условия, составим систему: 0, 25 M 1 + 0, 75 M 2 = 33, 25∙ 2 0, 75 M 1 + 0, 25 M 2 = 52∙ 2, где M 1 и M 2 – молярные массы X и Y соответственно. Решая, получим: M 1 = 104 г/моль и M 2 = 54 г/моль. Пусть X – Cx. Hy, а Y – Cn. Hm, тогда: y = 104 – 12 x m = 54 – 12 n. Перебирая натуральные значения для x и n, получим единственное рациональное решение: x = 8, n = 4 и X – C 8 H 8, а Y – C 4 H 6. Схема сополимеризации: Mсополимера = (104 n + 54 m) г/моль
Решение Исходя из условия, составим систему: 0, 25 M 1 + 0, 75 M 2 = 33, 25∙ 2 0, 75 M 1 + 0, 25 M 2 = 52∙ 2, где M 1 и M 2 – молярные массы X и Y соответственно. Решая, получим: M 1 = 104 г/моль и M 2 = 54 г/моль. Пусть X – Cx. Hy, а Y – Cn. Hm, тогда: y = 104 – 12 x m = 54 – 12 n. Перебирая натуральные значения для x и n, получим единственное рациональное решение: x = 8, n = 4 и X – C 8 H 8, а Y – C 4 H 6. Схема сополимеризации: Mсополимера = (104 n + 54 m) г/моль
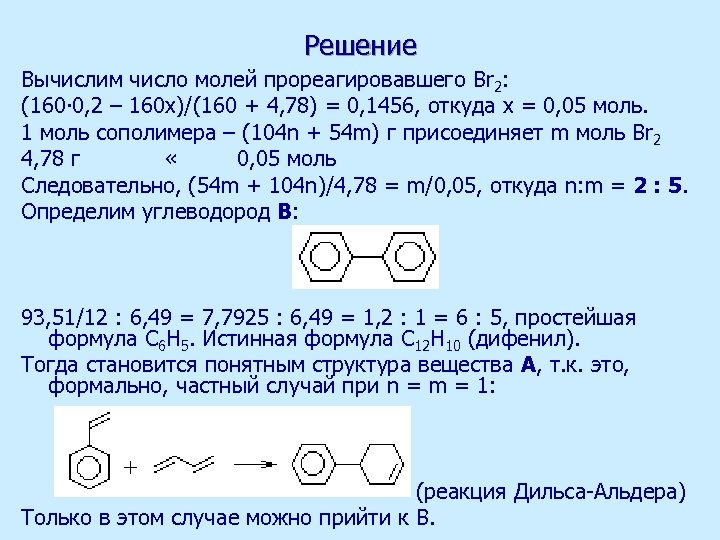 Решение Вычислим число молей прореагировавшего Br 2: (160∙ 0, 2 – 160 x)/(160 + 4, 78) = 0, 1456, откуда x = 0, 05 моль. 1 моль сополимера – (104 n + 54 m) г присоединяет m моль Br 2 4, 78 г « 0, 05 моль Следовательно, (54 m + 104 n)/4, 78 = m/0, 05, откуда n: m = 2 : 5. Определим углеводород B: 93, 51/12 : 6, 49 = 7, 7925 : 6, 49 = 1, 2 : 1 = 6 : 5, простейшая формула C 6 H 5. Истинная формула C 12 H 10 (дифенил). Тогда становится понятным структура вещества A, т. к. это, формально, частный случай при n = m = 1: (реакция Дильса-Альдера) Только в этом случае можно прийти к B.
Решение Вычислим число молей прореагировавшего Br 2: (160∙ 0, 2 – 160 x)/(160 + 4, 78) = 0, 1456, откуда x = 0, 05 моль. 1 моль сополимера – (104 n + 54 m) г присоединяет m моль Br 2 4, 78 г « 0, 05 моль Следовательно, (54 m + 104 n)/4, 78 = m/0, 05, откуда n: m = 2 : 5. Определим углеводород B: 93, 51/12 : 6, 49 = 7, 7925 : 6, 49 = 1, 2 : 1 = 6 : 5, простейшая формула C 6 H 5. Истинная формула C 12 H 10 (дифенил). Тогда становится понятным структура вещества A, т. к. это, формально, частный случай при n = m = 1: (реакция Дильса-Альдера) Только в этом случае можно прийти к B.
 Задача № 7 (10 класс) Смесь алкана и алкена с равным числом атомов водорода в молекулах общим объемом 3, 92 л (н. у. ) пропустили последовательно через склянки со слабощелочным раствором перманганата калия и с бромной водой. Масса первой склянки увеличилась на 0, 7 г, а второй – на 1, 4 г. Относительная плотность по водороду смеси газов на выходе из второй склянки составила 18. Вычислите массовые доли углеводородов в исходной смеси.
Задача № 7 (10 класс) Смесь алкана и алкена с равным числом атомов водорода в молекулах общим объемом 3, 92 л (н. у. ) пропустили последовательно через склянки со слабощелочным раствором перманганата калия и с бромной водой. Масса первой склянки увеличилась на 0, 7 г, а второй – на 1, 4 г. Относительная плотность по водороду смеси газов на выходе из второй склянки составила 18. Вычислите массовые доли углеводородов в исходной смеси.
 Решение Исходные углеводороды имеют формулы: Cn. H 2 n + 2; Cn+1 H 2 n+2. Их общее количество в смеси: (смеси) = 3, 92 / 22, 4 = 0, 175(моль) При пропускании исходной смеси через склянки с растворами KMn. O 4 (OH‒); Br 2 (H 2 O) в реакцию вступает только алкен с образованием веществ, находящихся в жидком состоянии: Cn+1 H 2 n+2(ОН)2 и Cn+1 H 2 n+2 Br 2. Масса, вступившего алкена в реакцию, равна (0, 7 + 1, 4) = 2, 1 (г). После реакций остались газообразные вещества с относительной плотностью по водороду 18. Их молярная масса равна: М = 18 · 2 = 36 (г/моль). (D = M/M(H 2)) Алкана с такой молярной массой нет. Вывод: алкен вступил в реакции не полностью, смесь состоит из исходного алкана и оставшегося алкена. В состав исходной смеси могут входить только С 2 Н 6 и С 3 Н 8. М(С 2 Н 6) = 30 г/моль, М(С 3 Н 6) = 42 г/моль. Только эта смесь газов может иметь молярную массу 36 г/моль.
Решение Исходные углеводороды имеют формулы: Cn. H 2 n + 2; Cn+1 H 2 n+2. Их общее количество в смеси: (смеси) = 3, 92 / 22, 4 = 0, 175(моль) При пропускании исходной смеси через склянки с растворами KMn. O 4 (OH‒); Br 2 (H 2 O) в реакцию вступает только алкен с образованием веществ, находящихся в жидком состоянии: Cn+1 H 2 n+2(ОН)2 и Cn+1 H 2 n+2 Br 2. Масса, вступившего алкена в реакцию, равна (0, 7 + 1, 4) = 2, 1 (г). После реакций остались газообразные вещества с относительной плотностью по водороду 18. Их молярная масса равна: М = 18 · 2 = 36 (г/моль). (D = M/M(H 2)) Алкана с такой молярной массой нет. Вывод: алкен вступил в реакции не полностью, смесь состоит из исходного алкана и оставшегося алкена. В состав исходной смеси могут входить только С 2 Н 6 и С 3 Н 8. М(С 2 Н 6) = 30 г/моль, М(С 3 Н 6) = 42 г/моль. Только эта смесь газов может иметь молярную массу 36 г/моль.
 Решение Определяем объемный состав смеси газов после реакции. ν(смеси) = 1 моль, ν(С 2 Н 6) = х моль, ν(С 3 Н 6) = (1 – х) моль 30 х + 42(1 – х) = 36, х = 0, 5 φ(С 3 Н 6) = 50% после реакции. Определяем ν(С 3 Н 6) вступившего в реакции: ν(С 3 Н 6) = 2, 1 / 42 = 0, 05 (моль). ν(С 2 Н 6, С 3 Н 6) осталось после реакций = (0, 175 – 0, 05) = 0, 125 (моль) Мольный состав этой смеси 50%, следовательно, ν(С 2 Н 6) = 0, 0625 моль, ν(С 3 Н 6) = 0, 0625 моль ν(С 3 Н 6) = (0, 0625 + 0, 05) = 0, 1125 (моль) всего в исходной смеси газов. Находим их массы и процентный состав. m(С 2 Н 6) = 0, 0625· 30 = 1, 875 (г), m(C 3 H 6) = 0, 1125· 42 = 4, 725. m(смеси) = 6, 6 г ω(С 2 Н 6) = 1, 875 / 6, 6 · 100% = 28, 41%, ω(С 3 Н 6) = 71, 59%.
Решение Определяем объемный состав смеси газов после реакции. ν(смеси) = 1 моль, ν(С 2 Н 6) = х моль, ν(С 3 Н 6) = (1 – х) моль 30 х + 42(1 – х) = 36, х = 0, 5 φ(С 3 Н 6) = 50% после реакции. Определяем ν(С 3 Н 6) вступившего в реакции: ν(С 3 Н 6) = 2, 1 / 42 = 0, 05 (моль). ν(С 2 Н 6, С 3 Н 6) осталось после реакций = (0, 175 – 0, 05) = 0, 125 (моль) Мольный состав этой смеси 50%, следовательно, ν(С 2 Н 6) = 0, 0625 моль, ν(С 3 Н 6) = 0, 0625 моль ν(С 3 Н 6) = (0, 0625 + 0, 05) = 0, 1125 (моль) всего в исходной смеси газов. Находим их массы и процентный состав. m(С 2 Н 6) = 0, 0625· 30 = 1, 875 (г), m(C 3 H 6) = 0, 1125· 42 = 4, 725. m(смеси) = 6, 6 г ω(С 2 Н 6) = 1, 875 / 6, 6 · 100% = 28, 41%, ω(С 3 Н 6) = 71, 59%.
 Задача № 4 (11 класс) В органическом синтезе важное значение имеют доступные высокоактивные реагенты. К ним относится вещество Х, легко получаемое при взаимодействии метилового эфира муравьиной кислоты и пентахлорида фосфора. Х вступает в реакции со многими органическими веществами. Некоторые реакции и свойства образующихся органических продуктов приведены в таблице. 1. Какой реагент обозначен буквой Х? Предложите еще один способ его синтеза. 2. Какие вещества обозначены буквами A–D? Напишите схемы соответствующих превращений. 3. Какова предположительная структура продукта взаимодействия Х с C 6 H 6 до взаимодействия с Н 2 О? 4. Объясните химическую основу пробы Бейльштейна. Примечание. Проба Бейльштейна: медная проволочка, смоченная веществом, вносится в пламя горелки. Проба положительна, если пламя окрашивается в голубовато-зеленый цвет.
Задача № 4 (11 класс) В органическом синтезе важное значение имеют доступные высокоактивные реагенты. К ним относится вещество Х, легко получаемое при взаимодействии метилового эфира муравьиной кислоты и пентахлорида фосфора. Х вступает в реакции со многими органическими веществами. Некоторые реакции и свойства образующихся органических продуктов приведены в таблице. 1. Какой реагент обозначен буквой Х? Предложите еще один способ его синтеза. 2. Какие вещества обозначены буквами A–D? Напишите схемы соответствующих превращений. 3. Какова предположительная структура продукта взаимодействия Х с C 6 H 6 до взаимодействия с Н 2 О? 4. Объясните химическую основу пробы Бейльштейна. Примечание. Проба Бейльштейна: медная проволочка, смоченная веществом, вносится в пламя горелки. Проба положительна, если пламя окрашивается в голубовато-зеленый цвет.
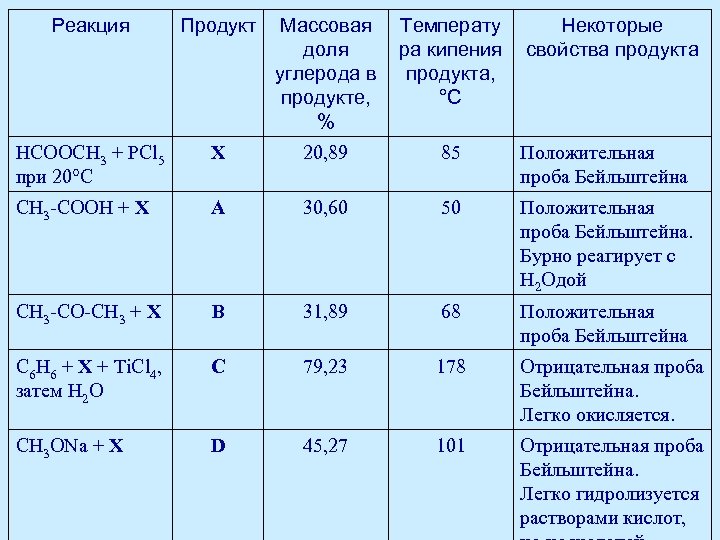 Реакция Продукт Массовая доля углерода в продукте, % Температу ра кипения продукта, °С Некоторые свойства продукта HCOOCH 3 + PCl 5 при 20°С Х 20, 89 85 Положительная проба Бейльштейна CH 3 -COOH + X A 30, 60 50 Положительная проба Бейльштейна. Бурно реагирует с Н 2 Одой CH 3 -CO-CH 3 + X B 31, 89 68 Положительная проба Бейльштейна C 6 H 6 + X + Ti. Cl 4, затем Н 2 О C 79, 23 178 Отрицательная проба Бейльштейна. Легко окисляется. CH 3 ONa + X D 45, 27 101 Отрицательная проба Бейльштейна. Легко гидролизуется растворами кислот,
Реакция Продукт Массовая доля углерода в продукте, % Температу ра кипения продукта, °С Некоторые свойства продукта HCOOCH 3 + PCl 5 при 20°С Х 20, 89 85 Положительная проба Бейльштейна CH 3 -COOH + X A 30, 60 50 Положительная проба Бейльштейна. Бурно реагирует с Н 2 Одой CH 3 -CO-CH 3 + X B 31, 89 68 Положительная проба Бейльштейна C 6 H 6 + X + Ti. Cl 4, затем Н 2 О C 79, 23 178 Отрицательная проба Бейльштейна. Легко окисляется. CH 3 ONa + X D 45, 27 101 Отрицательная проба Бейльштейна. Легко гидролизуется растворами кислот,
 Решение Положительные результаты пробы Бейльштейна указывают на то, что в молекулах соединений Х, А и В содержатся атомы хлора. Низкие температуры кипения продуктов (кроме С) указывают на их небольшие молекулярные массы. Вещество Х: M(Х) = n. M(C): ω(C), где n – число атомов углерода в молекуле. При n=1 M(Х) = 12, 01: 0, 2089 = 57, 49, что соответствует формуле СН 10 Cl. Это невозможно. При n=2 M(Х) = 114, 98. Молекула Х может содержать 1 или 2 атома Cl, но при одном атоме хлора молекулярная масса не может быть целочисленной. Значит, имеем варианты: С 2 H 20 Cl 2, С 2 H 4 OCl 2. Первая формула невозможна, а вторая соответствует метилформиату, в котором один атом кислорода замещен двумя атомами хлора: Cl 2 CHOCH 3. Это – α, α-дихлордиметиловый эфир. α, α-Дихлордиметиловый эфир можно получить также прямым хлорированием диметилового эфира: СH 3 -O-CH 3 Cl 2 CH-O-CH 3
Решение Положительные результаты пробы Бейльштейна указывают на то, что в молекулах соединений Х, А и В содержатся атомы хлора. Низкие температуры кипения продуктов (кроме С) указывают на их небольшие молекулярные массы. Вещество Х: M(Х) = n. M(C): ω(C), где n – число атомов углерода в молекуле. При n=1 M(Х) = 12, 01: 0, 2089 = 57, 49, что соответствует формуле СН 10 Cl. Это невозможно. При n=2 M(Х) = 114, 98. Молекула Х может содержать 1 или 2 атома Cl, но при одном атоме хлора молекулярная масса не может быть целочисленной. Значит, имеем варианты: С 2 H 20 Cl 2, С 2 H 4 OCl 2. Первая формула невозможна, а вторая соответствует метилформиату, в котором один атом кислорода замещен двумя атомами хлора: Cl 2 CHOCH 3. Это – α, α-дихлордиметиловый эфир. α, α-Дихлордиметиловый эфир можно получить также прямым хлорированием диметилового эфира: СH 3 -O-CH 3 Cl 2 CH-O-CH 3
 Решение Вещество А: При n=1 M(А) = 12, 01: 0, 3060 = 39, 25, что невозможно, так как молекула содержит хлор. При n=2 M(А) = 78, 50. Единственная разумная формула – С 2 Н 3 ОCl. Это – хлорангидрид уксусной кислоты, CH 3 -COCl. Вещество B: При п=1 M(B) = 12, 01: 0, 3189 = 37, 66. Разумным является вариант с n=3 и M(А) = 112, 98. Целочисленная молекулярная масса соответствует наличию двух атомов хлора в молекуле. Из возможных брутто формул реальной является С 3 Н 6 Cl 2. Это – 2, 2 -дихлорпропан, CH 3 -CCl 2 -СН 3. Вещество D: При n=1 M(D) = 12, 01: 0, 4527 = 26, 53. Так как атомов хлора в молекуле нет, то молекулярная масса должна быть целочисленной и четной. Это возможно только при n=4, тогда M(D) = 106, 12. Тогда соответствующая брутто-формула С 4 Н 10 О 3. Чтобы определить строение D, нужно обратить внимание на то, что по сравнению с Х в D отсутствуют два атома хлора, но добавились 2 атома углерода и 6 атомов водорода, то есть две группы ОСН 3. Очевидно, что прошла реакция замещения с образованием НС(ОСН 3)3. Это – триметилортоформиат.
Решение Вещество А: При n=1 M(А) = 12, 01: 0, 3060 = 39, 25, что невозможно, так как молекула содержит хлор. При n=2 M(А) = 78, 50. Единственная разумная формула – С 2 Н 3 ОCl. Это – хлорангидрид уксусной кислоты, CH 3 -COCl. Вещество B: При п=1 M(B) = 12, 01: 0, 3189 = 37, 66. Разумным является вариант с n=3 и M(А) = 112, 98. Целочисленная молекулярная масса соответствует наличию двух атомов хлора в молекуле. Из возможных брутто формул реальной является С 3 Н 6 Cl 2. Это – 2, 2 -дихлорпропан, CH 3 -CCl 2 -СН 3. Вещество D: При n=1 M(D) = 12, 01: 0, 4527 = 26, 53. Так как атомов хлора в молекуле нет, то молекулярная масса должна быть целочисленной и четной. Это возможно только при n=4, тогда M(D) = 106, 12. Тогда соответствующая брутто-формула С 4 Н 10 О 3. Чтобы определить строение D, нужно обратить внимание на то, что по сравнению с Х в D отсутствуют два атома хлора, но добавились 2 атома углерода и 6 атомов водорода, то есть две группы ОСН 3. Очевидно, что прошла реакция замещения с образованием НС(ОСН 3)3. Это – триметилортоформиат.
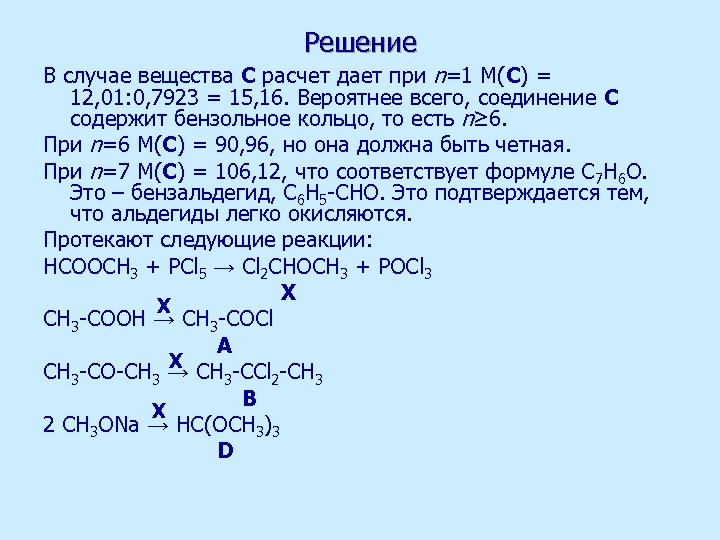 Решение В случае вещества С расчет дает при n=1 M(С) = 12, 01: 0, 7923 = 15, 16. Вероятнее всего, соединение С содержит бензольное кольцо, то есть n≥ 6. При n=6 M(С) = 90, 96, но она должна быть четная. При n=7 M(С) = 106, 12, что соответствует формуле С 7 Н 6 О. Это – бензальдегид, С 6 Н 5 -СНО. Это подтверждается тем, что альдегиды легко окисляются. Протекают следующие реакции: HCOOCH 3 + PCl 5 → Cl 2 CHOCH 3 + POCl 3 X X CH 3 -COOH → CH 3 -COCl A X CH 3 -CO-CH 3 → CH 3 -CCl 2 -CH 3 B X 2 CH 3 ONa → НС(ОСН 3)3 D
Решение В случае вещества С расчет дает при n=1 M(С) = 12, 01: 0, 7923 = 15, 16. Вероятнее всего, соединение С содержит бензольное кольцо, то есть n≥ 6. При n=6 M(С) = 90, 96, но она должна быть четная. При n=7 M(С) = 106, 12, что соответствует формуле С 7 Н 6 О. Это – бензальдегид, С 6 Н 5 -СНО. Это подтверждается тем, что альдегиды легко окисляются. Протекают следующие реакции: HCOOCH 3 + PCl 5 → Cl 2 CHOCH 3 + POCl 3 X X CH 3 -COOH → CH 3 -COCl A X CH 3 -CO-CH 3 → CH 3 -CCl 2 -CH 3 B X 2 CH 3 ONa → НС(ОСН 3)3 D
 Решение 1) X, Ti. Cl 4 2) H 2 O C 6 H 6 → C 6 H 5 -CHO C Весьма вероятно, что эта реакция протекает аналогично обычному алкилированию по Фриделю–Крафтсу, где Ti. Cl 4 выступает в роли катализатора – кислоты Льюиса. Тогда на первой стадии процесса должен образоваться C 6 H 5 -CHCl-OCH 3, который затем гидролизуется водой, отщепляя HCl и СН 3 ОН, с образованием бензальдегида. Галогенорганические соединения, сгорая в пламени горелки, выделяют галогеноводород, который в окислительной части пламени взаимодействует с медью, образуя достаточно летучий Cu. Cl 2. Летучие соединения меди окрашивают пламя в зеленый цвет.
Решение 1) X, Ti. Cl 4 2) H 2 O C 6 H 6 → C 6 H 5 -CHO C Весьма вероятно, что эта реакция протекает аналогично обычному алкилированию по Фриделю–Крафтсу, где Ti. Cl 4 выступает в роли катализатора – кислоты Льюиса. Тогда на первой стадии процесса должен образоваться C 6 H 5 -CHCl-OCH 3, который затем гидролизуется водой, отщепляя HCl и СН 3 ОН, с образованием бензальдегида. Галогенорганические соединения, сгорая в пламени горелки, выделяют галогеноводород, который в окислительной части пламени взаимодействует с медью, образуя достаточно летучий Cu. Cl 2. Летучие соединения меди окрашивают пламя в зеленый цвет.
 Задача № 5 (11 класс) Алкилсульфаты являются важными поверхностно-активными веществами, но их широкое использование приводит к загрязнению окружающей среды. Основным процессом их разрушения в природе является гидролиз, исследование которого представляет большой интерес. Для исследования зависимости кинетики гидролиза от р. Н среды был выбран неопентилсульфат калия, (CH 3)3 CCH 2 OSO 3 K (I). Результаты исследования оказались достаточно неожиданными. Во-первых, если при гидролизе в кислой среде образовывался ожидаемый неопентиловый спирт, то в нейтральной или щелочной – изомерный продукт (II). При небольшом нагревании с водным раствором серной кислоты II образует газообразный продукт III, озонирование которого дает смесь IV и V, причем IV является популярным растворителем. Во-вторых, наблюдаемая константа скорости реакции гидролиза I зависела от р. Н и имела значение kнабл=2, 3· 10– 1 с ++2, 7· 10– 6 с– 1. Н
Задача № 5 (11 класс) Алкилсульфаты являются важными поверхностно-активными веществами, но их широкое использование приводит к загрязнению окружающей среды. Основным процессом их разрушения в природе является гидролиз, исследование которого представляет большой интерес. Для исследования зависимости кинетики гидролиза от р. Н среды был выбран неопентилсульфат калия, (CH 3)3 CCH 2 OSO 3 K (I). Результаты исследования оказались достаточно неожиданными. Во-первых, если при гидролизе в кислой среде образовывался ожидаемый неопентиловый спирт, то в нейтральной или щелочной – изомерный продукт (II). При небольшом нагревании с водным раствором серной кислоты II образует газообразный продукт III, озонирование которого дает смесь IV и V, причем IV является популярным растворителем. Во-вторых, наблюдаемая константа скорости реакции гидролиза I зависела от р. Н и имела значение kнабл=2, 3· 10– 1 с ++2, 7· 10– 6 с– 1. Н
 Задача № 5 (11 класс) 1. Определите строение продукта гидролиза I в нейтральных и щелочных средах. Напишите уравнения всех упомянутых в задаче превращений. 2. Постройте график зависимости lgkнабл от р. Н в диапазоне от 2 до 10, объясните его вид. 3. Напишите кинетические уравнения для гидролиза I в неопентиловый спирт, соединение II и суммарное кинетическое уравнение гидролиза I. Определите соотношение неопентилового спирта и продукта II при р. Н 5. 4. Объясните, почему попадание некоторых бактерий в почву резко ускоряет разложение присутствующих в почве алкилсульфатов.
Задача № 5 (11 класс) 1. Определите строение продукта гидролиза I в нейтральных и щелочных средах. Напишите уравнения всех упомянутых в задаче превращений. 2. Постройте график зависимости lgkнабл от р. Н в диапазоне от 2 до 10, объясните его вид. 3. Напишите кинетические уравнения для гидролиза I в неопентиловый спирт, соединение II и суммарное кинетическое уравнение гидролиза I. Определите соотношение неопентилового спирта и продукта II при р. Н 5. 4. Объясните, почему попадание некоторых бактерий в почву резко ускоряет разложение присутствующих в почве алкилсульфатов.
 Решение Легкая дегидратация II под действием кислоты указывает на то, что это – третичный спирт. Образовавшийся алкен при озонировании образует ацетон – важный растворитель. H+ (CH 3)2 C(OH)CH 2 CH 3 → (CH 3)2 C=CHCH 3 II III O 3 (CH 3)2 C=CH 2 CH 3 → (CH 3)2 C=О + СH 3 CHO + H 2 O 2 III IV V Реакции гидролиза в кислой и щелочной средах: (CH 3)3 CCH 2 OSO 3 K + Н 2 О = (CH 3)3 CCH 2 OН + КНSO 4 (кислота – катализатор) (CH 3)3 CCH 2 OSO 3 K + КОН + = (CH 3)2 C(ОН)CH 3 + К 2 SO 4
Решение Легкая дегидратация II под действием кислоты указывает на то, что это – третичный спирт. Образовавшийся алкен при озонировании образует ацетон – важный растворитель. H+ (CH 3)2 C(OH)CH 2 CH 3 → (CH 3)2 C=CHCH 3 II III O 3 (CH 3)2 C=CH 2 CH 3 → (CH 3)2 C=О + СH 3 CHO + H 2 O 2 III IV V Реакции гидролиза в кислой и щелочной средах: (CH 3)3 CCH 2 OSO 3 K + Н 2 О = (CH 3)3 CCH 2 OН + КНSO 4 (кислота – катализатор) (CH 3)3 CCH 2 OSO 3 K + КОН + = (CH 3)2 C(ОН)CH 3 + К 2 SO 4
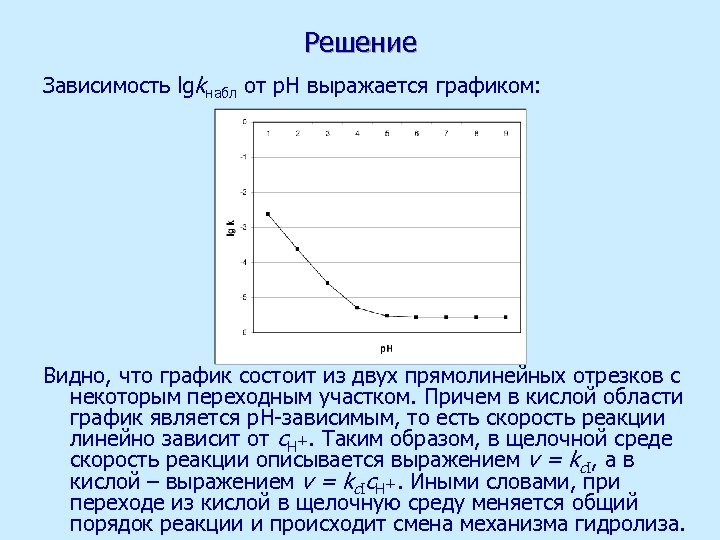 Решение Зависимость lgkнабл от р. Н выражается графиком: Видно, что график состоит из двух прямолинейных отрезков с некоторым переходным участком. Причем в кислой области график является р. Н-зависимым, то есть скорость реакции линейно зависит от с. Н+. Таким образом, в щелочной среде скорость реакции описывается выражением v = kc. I, а в кислой – выражением v = kc. Iс. Н+. Иными словами, при переходе из кислой в щелочную среду меняется общий порядок реакции и происходит смена механизма гидролиза.
Решение Зависимость lgkнабл от р. Н выражается графиком: Видно, что график состоит из двух прямолинейных отрезков с некоторым переходным участком. Причем в кислой области график является р. Н-зависимым, то есть скорость реакции линейно зависит от с. Н+. Таким образом, в щелочной среде скорость реакции описывается выражением v = kc. I, а в кислой – выражением v = kc. Iс. Н+. Иными словами, при переходе из кислой в щелочную среду меняется общий порядок реакции и происходит смена механизма гидролиза.
 Решение Видно, что график состоит из двух прямолинейных отрезков с некоторым переходным участком. Причем в кислой области график является р. Н-зависимым, то есть скорость реакции линейно зависит от с. Н+. Таким образом, в щелочной среде скорость реакции описывается выражением v = kc. I, а в кислой – выражением v = kc. Iс. Н+. Иными словами, при переходе из кислой в щелочную среду меняется общий порядок реакции и происходит смена механизма гидролиза. При р. Н = 5 реализуются оба механизма гидролиза. Если значение р. Н поддерживается постоянным, то в кислой среде реакция имеет псевдопервый порядок и значение k = 2, 3· 10– 1·с. Н+ = 2, 3· 10– 6 с– 1. В этом случае то есть при р. Н 5 продукт содержит 46% неопентанола и 54% трет-пентанола. Ускорение гидролиза алкилсульфатов в присутствии бактерий, несомненно, связано с ферментативными процессами. Действительно, многие бактерии содержат фермент сульфатазу, которая увеличивает скорость гидролиза более чем на 20 порядков.
Решение Видно, что график состоит из двух прямолинейных отрезков с некоторым переходным участком. Причем в кислой области график является р. Н-зависимым, то есть скорость реакции линейно зависит от с. Н+. Таким образом, в щелочной среде скорость реакции описывается выражением v = kc. I, а в кислой – выражением v = kc. Iс. Н+. Иными словами, при переходе из кислой в щелочную среду меняется общий порядок реакции и происходит смена механизма гидролиза. При р. Н = 5 реализуются оба механизма гидролиза. Если значение р. Н поддерживается постоянным, то в кислой среде реакция имеет псевдопервый порядок и значение k = 2, 3· 10– 1·с. Н+ = 2, 3· 10– 6 с– 1. В этом случае то есть при р. Н 5 продукт содержит 46% неопентанола и 54% трет-пентанола. Ускорение гидролиза алкилсульфатов в присутствии бактерий, несомненно, связано с ферментативными процессами. Действительно, многие бактерии содержат фермент сульфатазу, которая увеличивает скорость гидролиза более чем на 20 порядков.
 Задача № 6 (11 класс) В рамках программы поиска интересных для парфюмерной промышленности соединений был синтезирован о-эвгенол (F) – изомер природного эвгенола. Синтез был осуществлен по схеме: Вещества A, B, D, F дают характерное окрашивание при взаимодействии с раствором Fe. Cl 3, вещества С и Е – нет. Соединения Е и F являются изомерами с молекулярной формулой С 10 Н 12 О 2. Для установления точной структурной формулы о-эвгенола его обработали сначала безводным хлористым водородом, а образовавшееся производное (G) – спиртовым раствором КОН. Образовавшийся продукт (H) имеет молекулярную формулу С 10 Н 12 О 2 и не взаимодействует с раствором Fe. Cl 3.
Задача № 6 (11 класс) В рамках программы поиска интересных для парфюмерной промышленности соединений был синтезирован о-эвгенол (F) – изомер природного эвгенола. Синтез был осуществлен по схеме: Вещества A, B, D, F дают характерное окрашивание при взаимодействии с раствором Fe. Cl 3, вещества С и Е – нет. Соединения Е и F являются изомерами с молекулярной формулой С 10 Н 12 О 2. Для установления точной структурной формулы о-эвгенола его обработали сначала безводным хлористым водородом, а образовавшееся производное (G) – спиртовым раствором КОН. Образовавшийся продукт (H) имеет молекулярную формулу С 10 Н 12 О 2 и не взаимодействует с раствором Fe. Cl 3.
 Задача № 6 (11 класс) 1. Установите строение о-эвгенола и соединений В–Е и G –Н. 2. Рассчитайте общий выход о-эвгенола. 3. Почему при добавлении раствора Fe. Cl 3 к некоторым веществам образуются окрашенные растворы?
Задача № 6 (11 класс) 1. Установите строение о-эвгенола и соединений В–Е и G –Н. 2. Рассчитайте общий выход о-эвгенола. 3. Почему при добавлении раствора Fe. Cl 3 к некоторым веществам образуются окрашенные растворы?
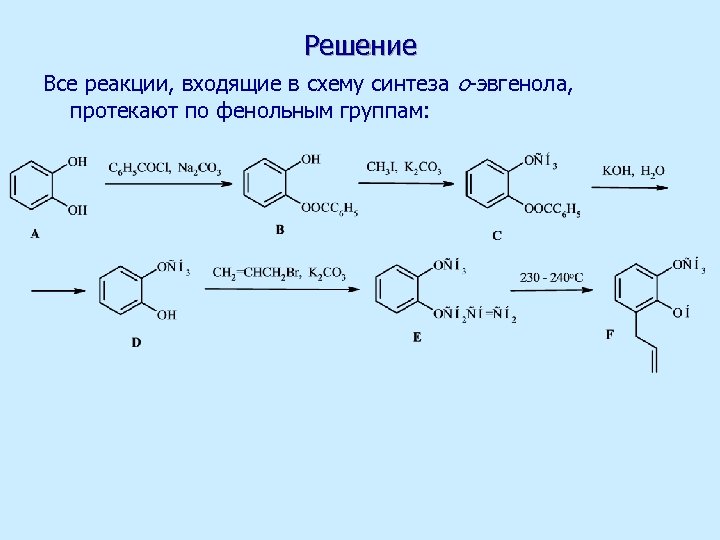 Решение Все реакции, входящие в схему синтеза о-эвгенола, протекают по фенольным группам:
Решение Все реакции, входящие в схему синтеза о-эвгенола, протекают по фенольным группам:
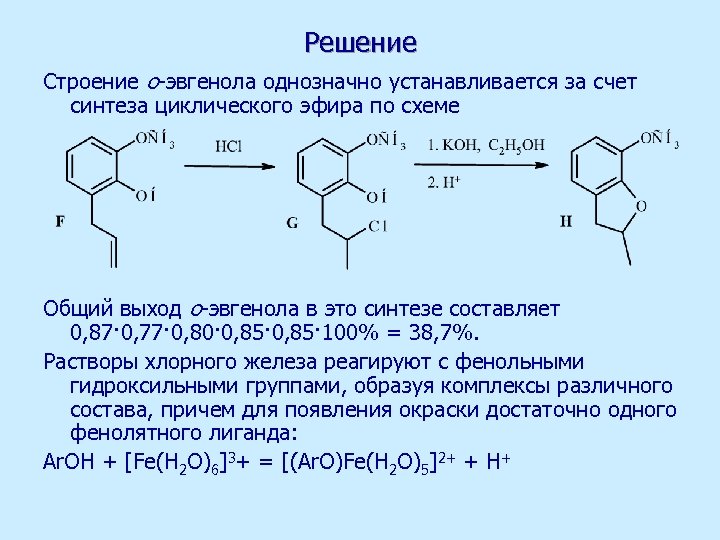 Решение Строение о-эвгенола однозначно устанавливается за счет синтеза циклического эфира по схеме Общий выход о-эвгенола в это синтезе составляет 0, 87· 0, 77· 0, 80· 0, 85· 100% = 38, 7%. Растворы хлорного железа реагируют с фенольными гидроксильными группами, образуя комплексы различного состава, причем для появления окраски достаточно одного фенолятного лиганда: Ar. OH + [Fe(H 2 O)6]3+ = [(Ar. O)Fe(H 2 O)5]2+ + H+
Решение Строение о-эвгенола однозначно устанавливается за счет синтеза циклического эфира по схеме Общий выход о-эвгенола в это синтезе составляет 0, 87· 0, 77· 0, 80· 0, 85· 100% = 38, 7%. Растворы хлорного железа реагируют с фенольными гидроксильными группами, образуя комплексы различного состава, причем для появления окраски достаточно одного фенолятного лиганда: Ar. OH + [Fe(H 2 O)6]3+ = [(Ar. O)Fe(H 2 O)5]2+ + H+
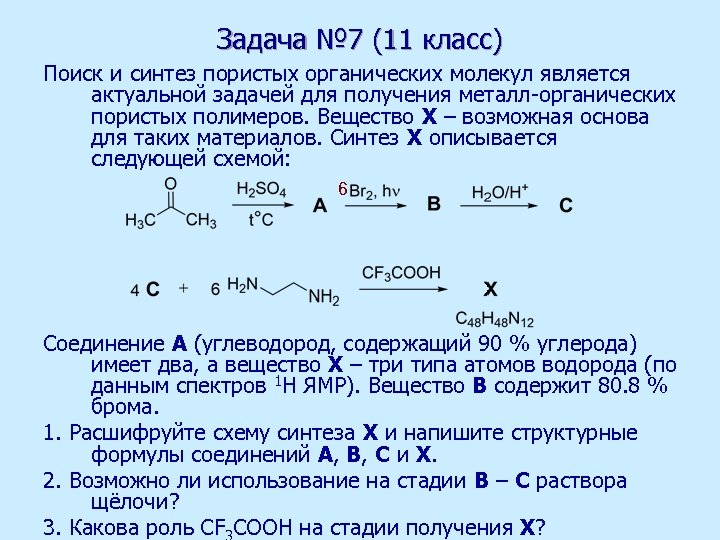 Задача № 7 (11 класс) Поиск и синтез пористых органических молекул является актуальной задачей для получения металл-органических пористых полимеров. Вещество Х – возможная основа для таких материалов. Синтез Х описывается следующей схемой: 6 Соединение A (углеводород, содержащий 90 % углерода) имеет два, а вещество Х – три типа атомов водорода (по данным спектров 1 Н ЯМР). Вещество В содержит 80. 8 % брома. 1. Расшифруйте схему синтеза Х и напишите структурные формулы соединений А, В, С и X. 2. Возможно ли использование на стадии B – C раствора щёлочи? 3. Какова роль СF COOH на стадии получения Х?
Задача № 7 (11 класс) Поиск и синтез пористых органических молекул является актуальной задачей для получения металл-органических пористых полимеров. Вещество Х – возможная основа для таких материалов. Синтез Х описывается следующей схемой: 6 Соединение A (углеводород, содержащий 90 % углерода) имеет два, а вещество Х – три типа атомов водорода (по данным спектров 1 Н ЯМР). Вещество В содержит 80. 8 % брома. 1. Расшифруйте схему синтеза Х и напишите структурные формулы соединений А, В, С и X. 2. Возможно ли использование на стадии B – C раствора щёлочи? 3. Какова роль СF COOH на стадии получения Х?
 Решение Рассчитаем состав углеводорода А. ν(С): ν(Н) = (90/12): (10/1) = 7, 5: 10 = 3: 4. Отсюда формула А – (С 3 Н 4)n. Так как в А кислорода не обнаруживается, то при действии серной кислоты на ацетон можно предположить выделение воды – это кротоновая конденсация. Однако при первом рассмотрении в случае образования ациклического соединения кислород должен сохраняться (соединения 1, 2, 3): Нужный результат (вещество А – мезитилен, С 9 Н 12) даёт внутримолекулярная кротоновая конденсация соединения 3. Наличие только двух типов атомов водорода в А также удовлетворяет условию задачи.
Решение Рассчитаем состав углеводорода А. ν(С): ν(Н) = (90/12): (10/1) = 7, 5: 10 = 3: 4. Отсюда формула А – (С 3 Н 4)n. Так как в А кислорода не обнаруживается, то при действии серной кислоты на ацетон можно предположить выделение воды – это кротоновая конденсация. Однако при первом рассмотрении в случае образования ациклического соединения кислород должен сохраняться (соединения 1, 2, 3): Нужный результат (вещество А – мезитилен, С 9 Н 12) даёт внутримолекулярная кротоновая конденсация соединения 3. Наличие только двух типов атомов водорода в А также удовлетворяет условию задачи.
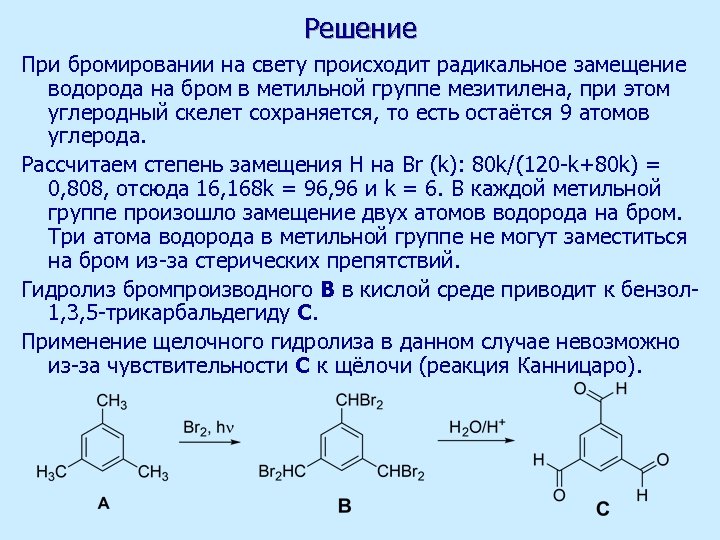 Решение При бромировании на свету происходит радикальное замещение водорода на бром в метильной группе мезитилена, при этом углеродный скелет сохраняется, то есть остаётся 9 атомов углерода. Рассчитаем степень замещения Н на Вr (k): 80 k/(120 -k+80 k) = 0, 808, отсюда 16, 168 k = 96, 96 и k = 6. В каждой метильной группе произошло замещение двух атомов водорода на бром. Три атома водорода в метильной группе не могут заместиться на бром из-за стерических препятствий. Гидролиз бромпроизводного B в кислой среде приводит к бензол 1, 3, 5 -трикарбальдегиду С. Применение щелочного гидролиза в данном случае невозможно из-за чувствительности С к щёлочи (реакция Канницаро).
Решение При бромировании на свету происходит радикальное замещение водорода на бром в метильной группе мезитилена, при этом углеродный скелет сохраняется, то есть остаётся 9 атомов углерода. Рассчитаем степень замещения Н на Вr (k): 80 k/(120 -k+80 k) = 0, 808, отсюда 16, 168 k = 96, 96 и k = 6. В каждой метильной группе произошло замещение двух атомов водорода на бром. Три атома водорода в метильной группе не могут заместиться на бром из-за стерических препятствий. Гидролиз бромпроизводного B в кислой среде приводит к бензол 1, 3, 5 -трикарбальдегиду С. Применение щелочного гидролиза в данном случае невозможно из-за чувствительности С к щёлочи (реакция Канницаро).
 Решение Реакция альдегидов и кетонов с первичными аминами приводит к образованию иминов (соединений со связью С=N) с выделением молекулы воды. Сумма атомов исходных веществ (4 молекулы альдегида и 6 молекул этилендиамина) – С 48 Н 72 N 12 О 12. При сравнении с брутто-формулой Х С 48 Н 48 N 12 видно, что в результате реакции выделяется 12 молекул воды. Наличие только трёх типов атомов водорода в Х свидетельствует о высокой симметрии этой молекулы. Из-за наличия трёх альдегидных групп в С и двух аминогрупп в этилендиамине происходит сшивка с образованием Х, имеющего полость внутри. Трифторуксусная кислота используется в качестве катализатора, активирующего альдегидную группу для присоединения атома азота этилендиамина.
Решение Реакция альдегидов и кетонов с первичными аминами приводит к образованию иминов (соединений со связью С=N) с выделением молекулы воды. Сумма атомов исходных веществ (4 молекулы альдегида и 6 молекул этилендиамина) – С 48 Н 72 N 12 О 12. При сравнении с брутто-формулой Х С 48 Н 48 N 12 видно, что в результате реакции выделяется 12 молекул воды. Наличие только трёх типов атомов водорода в Х свидетельствует о высокой симметрии этой молекулы. Из-за наличия трёх альдегидных групп в С и двух аминогрупп в этилендиамине происходит сшивка с образованием Х, имеющего полость внутри. Трифторуксусная кислота используется в качестве катализатора, активирующего альдегидную группу для присоединения атома азота этилендиамина.
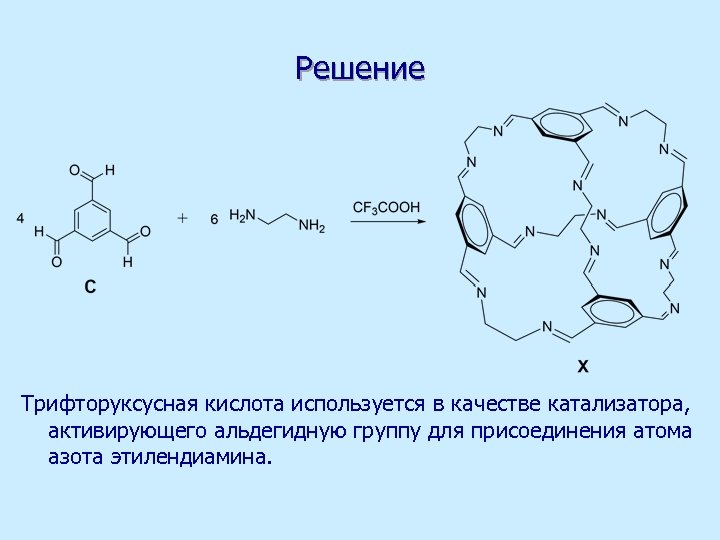 Решение Трифторуксусная кислота используется в качестве катализатора, активирующего альдегидную группу для присоединения атома азота этилендиамина.
Решение Трифторуксусная кислота используется в качестве катализатора, активирующего альдегидную группу для присоединения атома азота этилендиамина.



