13 спирты.ppt
- Количество слайдов: 24
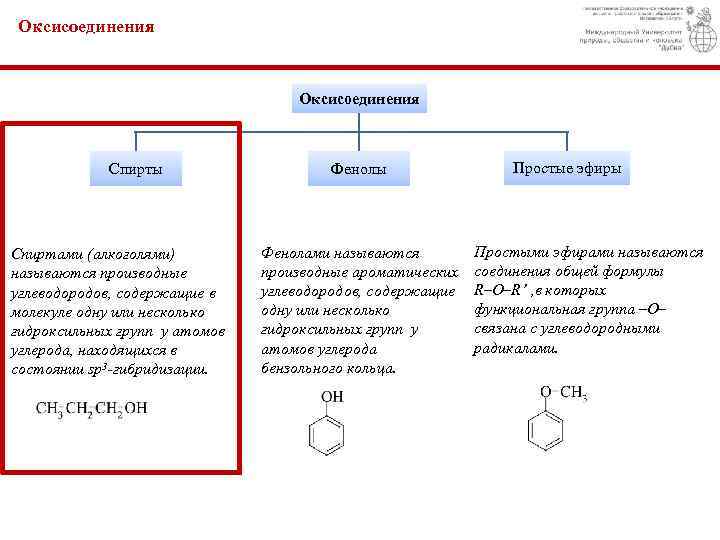 Оксисоединения Спирты Спиртами (алкоголями) называются производные углеводородов, содержащие в молекуле одну или несколько гидроксильных групп у атомов углерода, находящихся в состоянии sp 3 -гибридизации. Фенолы Фенолами называются производные ароматических углеводородов, содержащие одну или несколько гидроксильных групп у атомов углерода бензольного кольца. Простые эфиры Простыми эфирами называются соединения общей формулы R–O–R’ , в которых функциональная группа –O– связана с углеводородными радикалами.
Оксисоединения Спирты Спиртами (алкоголями) называются производные углеводородов, содержащие в молекуле одну или несколько гидроксильных групп у атомов углерода, находящихся в состоянии sp 3 -гибридизации. Фенолы Фенолами называются производные ароматических углеводородов, содержащие одну или несколько гидроксильных групп у атомов углерода бензольного кольца. Простые эфиры Простыми эфирами называются соединения общей формулы R–O–R’ , в которых функциональная группа –O– связана с углеводородными радикалами.
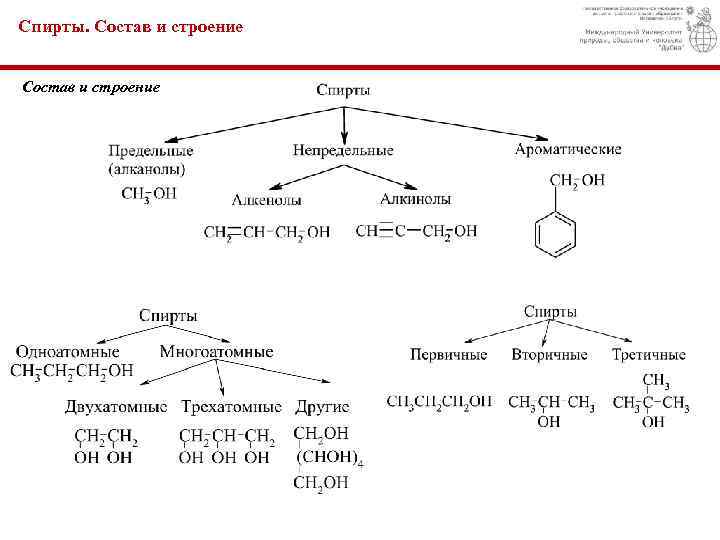 Спирты. Состав и строение
Спирты. Состав и строение
 Спирты. Изомерия и номенклатура Изомерия Одноатомным спиртам присущи следующие типы изомерии: — Изомерия цепи. — Изомерия положения гидроксильной группы. — Межклассовая изомерия. Спирты изомерны простым эфирам: Номенклатура 1. Выбирают в молекуле самую длинную неразветвленную (главную) цепь атомов углерода, содержащую гидроксильную группу. 2. Нумеруют атомы углерода главной цепи таким образом, чтобы атом, связанный с гидроксильной группой, имел наименьший номер. 3. Указывают положения заместителей и дают название углеводороду, соответствующему главной цепи. 4. Обозначают гидроксильную группу суффиксом -ол. 5. Цифрой указывают положение гидроксильной группы.
Спирты. Изомерия и номенклатура Изомерия Одноатомным спиртам присущи следующие типы изомерии: — Изомерия цепи. — Изомерия положения гидроксильной группы. — Межклассовая изомерия. Спирты изомерны простым эфирам: Номенклатура 1. Выбирают в молекуле самую длинную неразветвленную (главную) цепь атомов углерода, содержащую гидроксильную группу. 2. Нумеруют атомы углерода главной цепи таким образом, чтобы атом, связанный с гидроксильной группой, имел наименьший номер. 3. Указывают положения заместителей и дают название углеводороду, соответствующему главной цепи. 4. Обозначают гидроксильную группу суффиксом -ол. 5. Цифрой указывают положение гидроксильной группы.
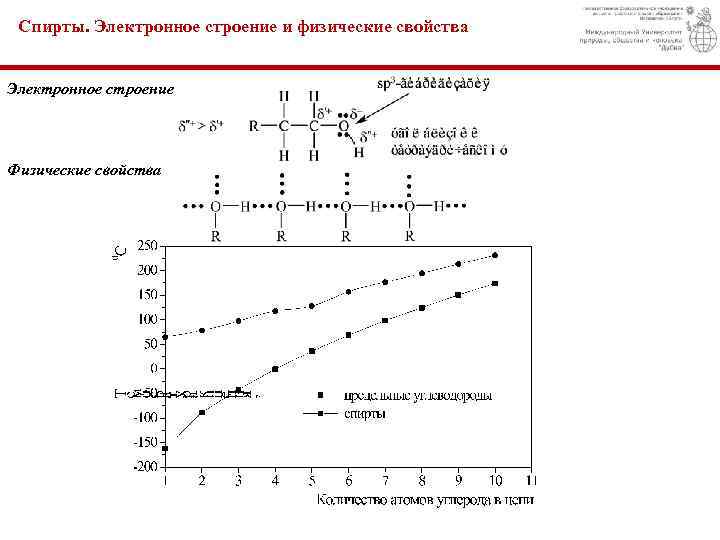 Спирты. Электронное строение и физические свойства Электронное строение Физические свойства
Спирты. Электронное строение и физические свойства Электронное строение Физические свойства
 Спирты. Способы получения 1. Гидратация алкенов. 2. Взаимодействие алкенов с серной кислотой 3. Гидролиз галогенпроизводных. 4. Восстановление альдегидов и кетонов. Восстановители: H 2 (Ni, Pd, Pt), Na. BH 4(спирт), Li. Al. H 4 (абсолютный эфир).
Спирты. Способы получения 1. Гидратация алкенов. 2. Взаимодействие алкенов с серной кислотой 3. Гидролиз галогенпроизводных. 4. Восстановление альдегидов и кетонов. Восстановители: H 2 (Ni, Pd, Pt), Na. BH 4(спирт), Li. Al. H 4 (абсолютный эфир).
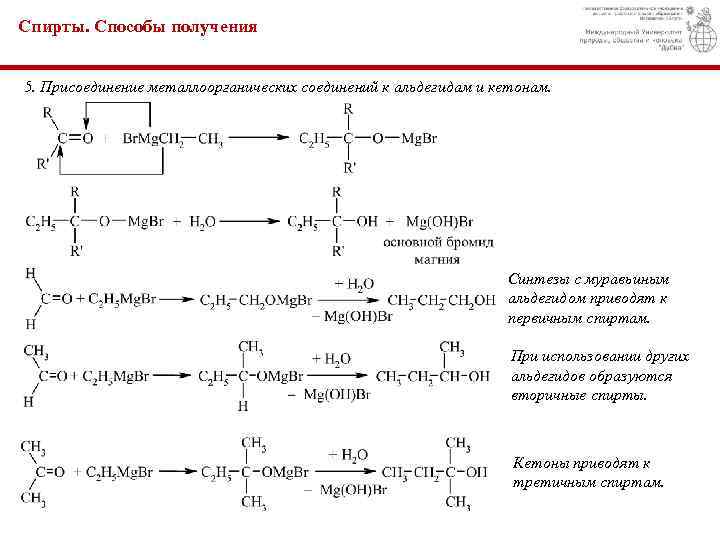 Спирты. Способы получения 5. Присоединение металлоорганических соединений к альдегидам и кетонам. Синтезы с муравьиным альдегидом приводят к первичным спиртам. При использовании других альдегидов образуются вторичные спирты. Кетоны приводят к третичным спиртам.
Спирты. Способы получения 5. Присоединение металлоорганических соединений к альдегидам и кетонам. Синтезы с муравьиным альдегидом приводят к первичным спиртам. При использовании других альдегидов образуются вторичные спирты. Кетоны приводят к третичным спиртам.
 Спирты. Способы получения 6. Оксимеркурирование алкенов. 7. Гидроборирование алкенов. 8. Восстановление карбоновых кислот и их производных. Восстановление сложных эфиров по Буво-Блану:
Спирты. Способы получения 6. Оксимеркурирование алкенов. 7. Гидроборирование алкенов. 8. Восстановление карбоновых кислот и их производных. Восстановление сложных эфиров по Буво-Блану:
 Спирты. Способы получения 9. Специфические методы получения метанола и этанола. 10. Методы получения многоатомных спиртов. Многоатомные спирты могут быть получены аналогично одноатомным спиртам или другими способами. Важнейшие из них: а. Гидролиз дигалогенпроизводных или хлоргидринов: б. гидратация эпоксисоединений: в. гидроксилирование алкенов
Спирты. Способы получения 9. Специфические методы получения метанола и этанола. 10. Методы получения многоатомных спиртов. Многоатомные спирты могут быть получены аналогично одноатомным спиртам или другими способами. Важнейшие из них: а. Гидролиз дигалогенпроизводных или хлоргидринов: б. гидратация эпоксисоединений: в. гидроксилирование алкенов
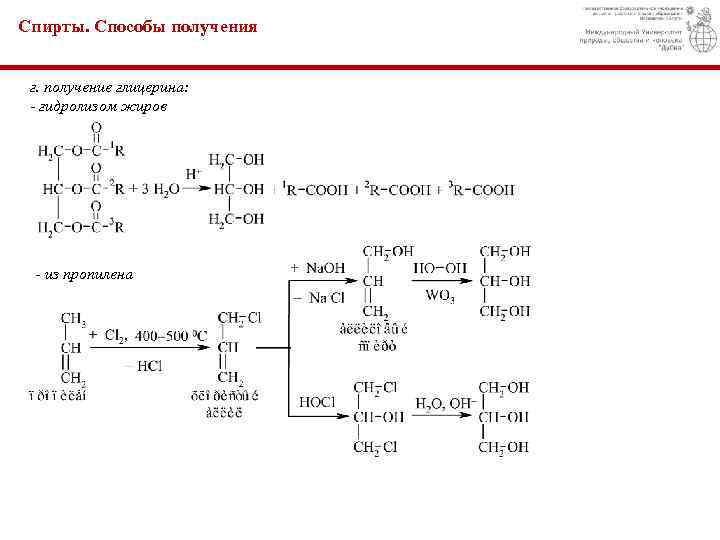 Спирты. Способы получения г. получение глицерина: - гидролизом жиров - из пропилена
Спирты. Способы получения г. получение глицерина: - гидролизом жиров - из пропилена
 Спирты. Химические свойства 1. Кислотно-основные свойства: а. алкоголяты металлов: - взаимодействие со щелочными металлами - взаимодействие с гидридом натрия - взаимодействие с металлоорганическими соединениями - обменные реакции Кислотные свойства: чем выше способность к делокализации отрицательного заряда в алкоголяте, тем выше кислотность: - первичные>вторичные>третичные; - электроноакцепторные заместители в радикале увеличивают кислотность. Гидролиз алкоголятов: Спиртовые растворы щелочей более сильные основания, чем их водные растворы
Спирты. Химические свойства 1. Кислотно-основные свойства: а. алкоголяты металлов: - взаимодействие со щелочными металлами - взаимодействие с гидридом натрия - взаимодействие с металлоорганическими соединениями - обменные реакции Кислотные свойства: чем выше способность к делокализации отрицательного заряда в алкоголяте, тем выше кислотность: - первичные>вторичные>третичные; - электроноакцепторные заместители в радикале увеличивают кислотность. Гидролиз алкоголятов: Спиртовые растворы щелочей более сильные основания, чем их водные растворы
 Спирты. Химические свойства б. взаимодействие с сильными кислотами 2. Спирты и алкоголяты как нуклеофильные реагенты. 2. 1. Получение простых эфиров (синтез Вильямсона) 2. 2. Получение сложных эфиров
Спирты. Химические свойства б. взаимодействие с сильными кислотами 2. Спирты и алкоголяты как нуклеофильные реагенты. 2. 1. Получение простых эфиров (синтез Вильямсона) 2. 2. Получение сложных эфиров
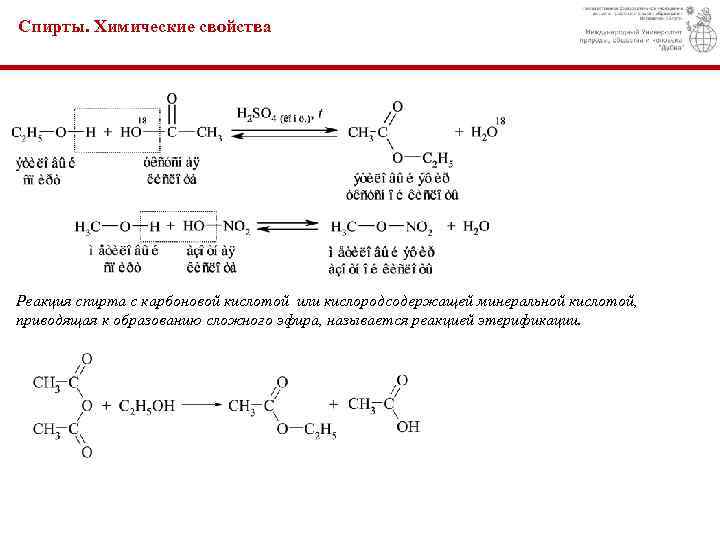 Спирты. Химические свойства Реакция спирта с карбоновой кислотой или кислородсодержащей минеральной кислотой, приводящая к образованию сложного эфира, называется реакцией этерификации.
Спирты. Химические свойства Реакция спирта с карбоновой кислотой или кислородсодержащей минеральной кислотой, приводящая к образованию сложного эфира, называется реакцией этерификации.
 Спирты. Химические свойства 3. Дегидратация. а. Пропусканием паров спиртов над нагретой окисью алюминия. б. Под действием минеральных кислот (H 3 PO 4 или H 2 SO 4, например) или карбоновых кислот (щавелевой, фталевой) при нагревании. Вторичные и третичные спирты дегидратируются в соответствии с правилом Зайцева, образуя термодинамически более устойчивый алкен.
Спирты. Химические свойства 3. Дегидратация. а. Пропусканием паров спиртов над нагретой окисью алюминия. б. Под действием минеральных кислот (H 3 PO 4 или H 2 SO 4, например) или карбоновых кислот (щавелевой, фталевой) при нагревании. Вторичные и третичные спирты дегидратируются в соответствии с правилом Зайцева, образуя термодинамически более устойчивый алкен.
 Спирты. Химические свойства 4. Замещение гидроксильной группы. Большинство реакций протекает в присутствии кислот, протонных или Льюиса. Роль протонной кислоты состоит с превращении плохой уходящей группы ОН– в хорошую – Н 2 О. а. Галогеном. Реакция с галогеноводородами (HI ˃ HBr ˃ HCl – ряд активности галогеноводородов). S N 1 вторичные и третичные спирты S N 2 метанол и первичные спирты
Спирты. Химические свойства 4. Замещение гидроксильной группы. Большинство реакций протекает в присутствии кислот, протонных или Льюиса. Роль протонной кислоты состоит с превращении плохой уходящей группы ОН– в хорошую – Н 2 О. а. Галогеном. Реакция с галогеноводородами (HI ˃ HBr ˃ HCl – ряд активности галогеноводородов). S N 1 вторичные и третичные спирты S N 2 метанол и первичные спирты
 Спирты. Химические свойства Реакции спиртов с галогеноводородами сопровождаются перегруппировками: – гидридный сдвиг – перенос алкильной группы
Спирты. Химические свойства Реакции спиртов с галогеноводородами сопровождаются перегруппировками: – гидридный сдвиг – перенос алкильной группы
 Спирты. Химические свойства – аллильная перегруппировка Реагент Лукаса – смесь концентрированной соляной кислоты и хлорида цинка. Применяется как для анализа спиртов, так и для препаративного получения хлоралканов.
Спирты. Химические свойства – аллильная перегруппировка Реагент Лукаса – смесь концентрированной соляной кислоты и хлорида цинка. Применяется как для анализа спиртов, так и для препаративного получения хлоралканов.
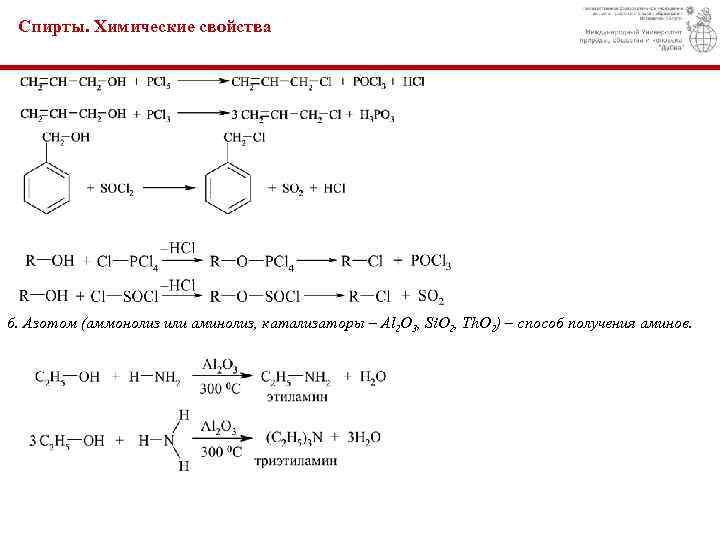 Спирты. Химические свойства б. Азотом (аммонолиз или аминолиз, катализаторы – Al 2 O 3, Si. O 2, Th. O 2) – способ получения аминов.
Спирты. Химические свойства б. Азотом (аммонолиз или аминолиз, катализаторы – Al 2 O 3, Si. O 2, Th. O 2) – способ получения аминов.
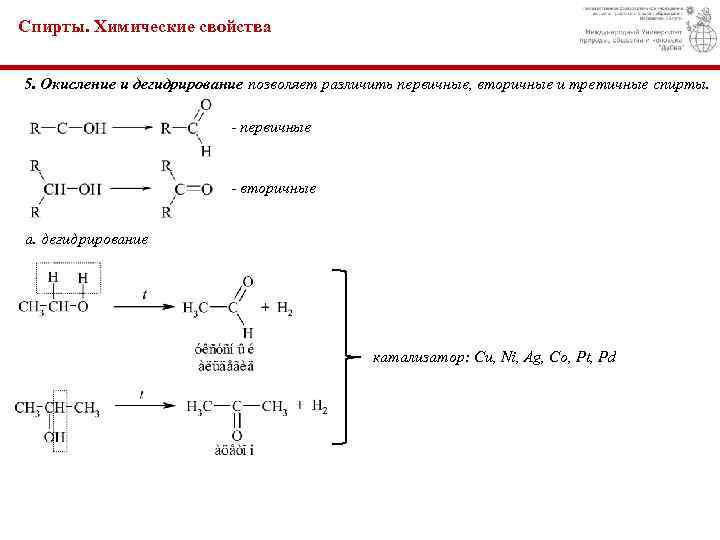 Спирты. Химические свойства 5. Окисление и дегидрирование позволяет различить первичные, вторичные и третичные спирты. - первичные - вторичные а. дегидрирование катализатор: Cu, Ni, Ag, Co, Pt, Pd
Спирты. Химические свойства 5. Окисление и дегидрирование позволяет различить первичные, вторичные и третичные спирты. - первичные - вторичные а. дегидрирование катализатор: Cu, Ni, Ag, Co, Pt, Pd
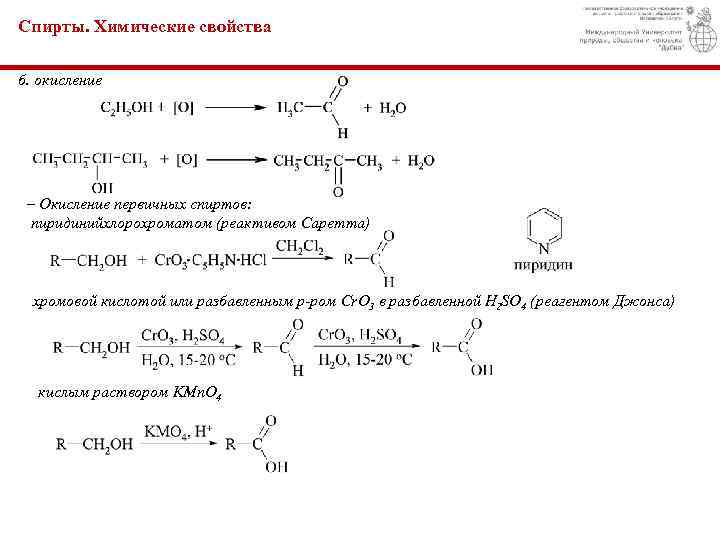 Спирты. Химические свойства б. окисление – Окисление первичных спиртов: пиридинийхлорохроматом (реактивом Саретта) хромовой кислотой или разбавленным р-ром Cr. O 3 в разбавленной H 2 SO 4 (реагентом Джонса) кислым раствором KMn. O 4
Спирты. Химические свойства б. окисление – Окисление первичных спиртов: пиридинийхлорохроматом (реактивом Саретта) хромовой кислотой или разбавленным р-ром Cr. O 3 в разбавленной H 2 SO 4 (реагентом Джонса) кислым раствором KMn. O 4
 Спирты. Химические свойства окисление аллиловых спиртов свежеосажденным Mn. O 2 – Окисление вторичных спиртов: р-ром бихромата калия в разбавленной серной кислоте или хромовым ангидридом в уксусной кислоте. кислым раствором KMn. O 4
Спирты. Химические свойства окисление аллиловых спиртов свежеосажденным Mn. O 2 – Окисление вторичных спиртов: р-ром бихромата калия в разбавленной серной кислоте или хромовым ангидридом в уксусной кислоте. кислым раствором KMn. O 4
 Спирты. Химические свойства – Окисление третичных спиртов. Среди третичных спиртов окислению подвержены только те, которые способны дегидратироваться.
Спирты. Химические свойства – Окисление третичных спиртов. Среди третичных спиртов окислению подвержены только те, которые способны дегидратироваться.
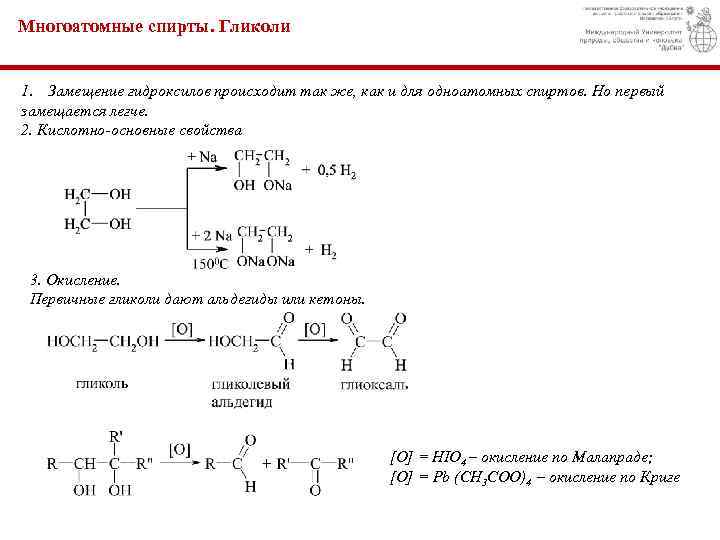 Многоатомные спирты. Гликоли 1. Замещение гидроксилов происходит так же, как и для одноатомных спиртов. Но первый замещается легче. 2. Кислотно-основные свойства 3. Окисление. Первичные гликоли дают альдегиды или кетоны. [O] = HIO 4 – окисление по Малапраде; [O] = Pb (CH 3 COO)4 – окисление по Криге
Многоатомные спирты. Гликоли 1. Замещение гидроксилов происходит так же, как и для одноатомных спиртов. Но первый замещается легче. 2. Кислотно-основные свойства 3. Окисление. Первичные гликоли дают альдегиды или кетоны. [O] = HIO 4 – окисление по Малапраде; [O] = Pb (CH 3 COO)4 – окисление по Криге
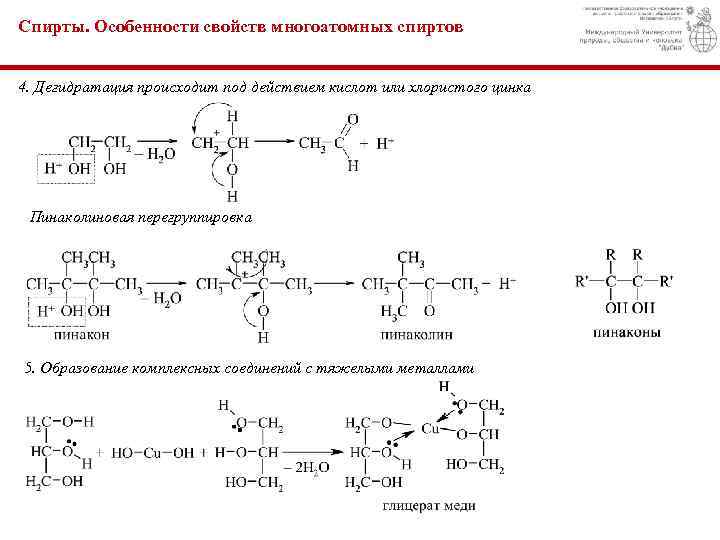 Спирты. Особенности свойств многоатомных спиртов 4. Дегидратация происходит под действием кислот или хлористого цинка Пинаколиновая перегруппировка 5. Образование комплексных соединений с тяжелыми металлами
Спирты. Особенности свойств многоатомных спиртов 4. Дегидратация происходит под действием кислот или хлористого цинка Пинаколиновая перегруппировка 5. Образование комплексных соединений с тяжелыми металлами
 Спирты. Особенности свойств многоатомных спиртов 6. Этерификация
Спирты. Особенности свойств многоатомных спиртов 6. Этерификация


