Галогени 2.ppt
- Количество слайдов: 35

Оксигенвмісні сполуки галогенів

Галогени з киснем безпосередньо не взаємодіють, всі сполуки галогенів з оксигеном отримують непрямим шляхом F 2 + H 2 O → 4 HF + O 2 2 F 2 + 2 Na. OH → OF 2 + 2 Na. F + H 2 O OF 2 – фторид оксигену
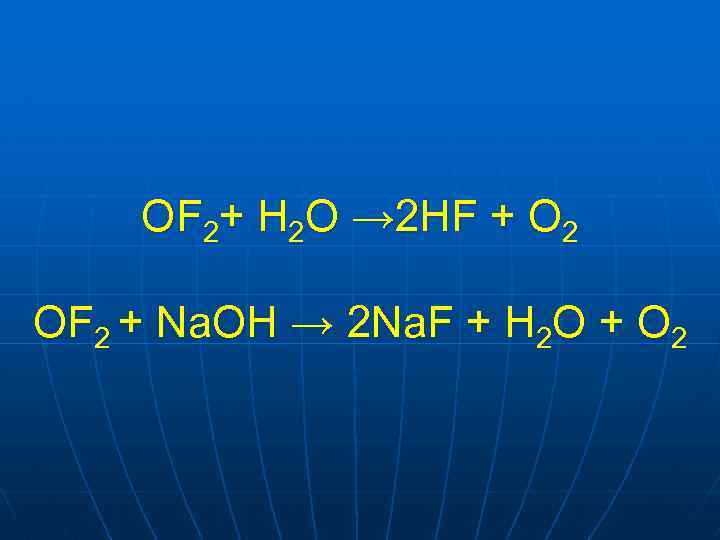
OF 2+ H 2 O → 2 HF + O 2 OF 2 + Na. OH → 2 Na. F + H 2 O + O 2
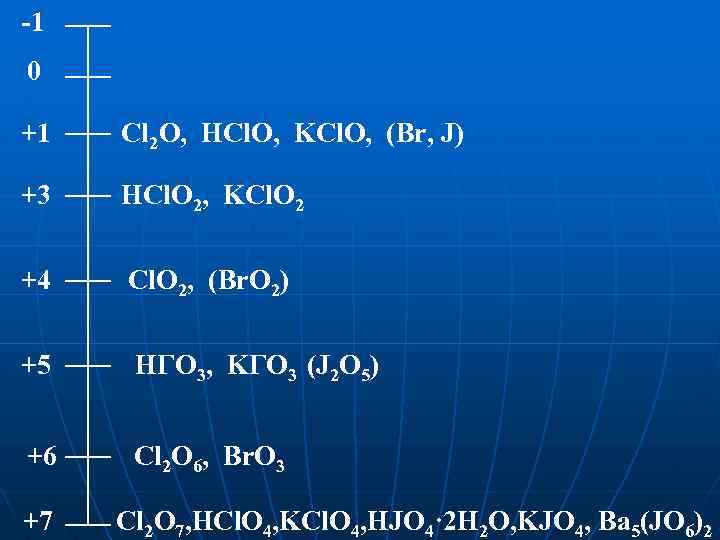
-1 0 +1 Cl 2 O, HCl. O, KCl. O, (Br, J) +3 HCl. O 2, KCl. O 2 +4 Cl. O 2, (Br. O 2) +5 HГO 3, KГO 3 (J 2 O 5) +6 Cl 2 O 6, Br. O 3 +7 Cl 2 O 7, HCl. O 4, KCl. O 4, HJO 4· 2 H 2 O, KJO 4, Ba 5(JO 6)2

-1 +1 Cl 2 + H 2 O ⇆ HCl + HCl. O Br 2 + H 2 O ⇆ HBr + HBr. O J 2 + H 2 O ⇆ H J + H J O Ступінь взаємодії з Н 2 О зменшується, оскільки зменшуються окислювальні властивості
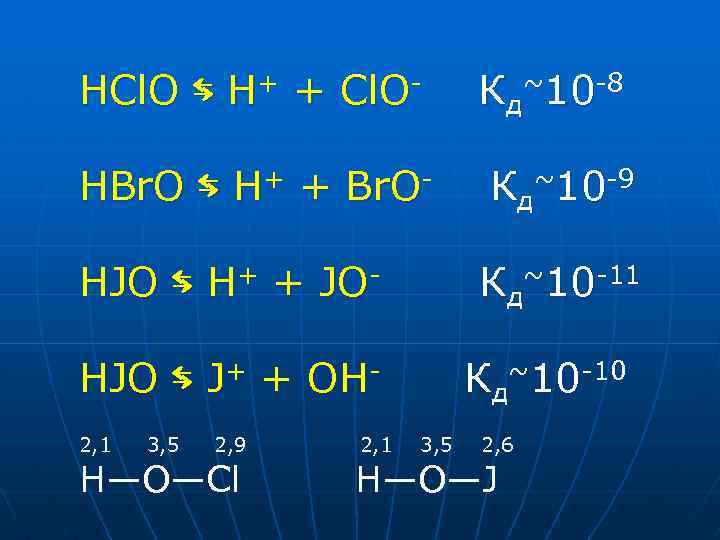
HCl. O ⇆ H+ + Cl. O- Кд~10 -8 HBr. O ⇆ H+ + Br. O- Кд~10 -9 HJO ⇆ H+ + JO- Кд~10 -11 HJO ⇆ J+ + OH 2, 1 3, 5 2, 9 H—O—Cl 2, 1 Кд~10 -10 3, 5 2, 6 H—O—J

Розклад 1) HCl. O HCl + O 2) 2 HCl. O → H 2 O + Cl 2 O 3) 3 HCl. O 3 + 2 HCl

1 й тип розкладу HCl. O HBr. O HJO окисні властивості слабшають 2 й тип розкладу (під дією водовіднімаючих речовин, Ca. Cl 2) Cl 2 + Hg. O → Hg. Cl 2 + Cl 2 O I 2 O майже не існує Br 2 O дуже нестійкий(-100 С)
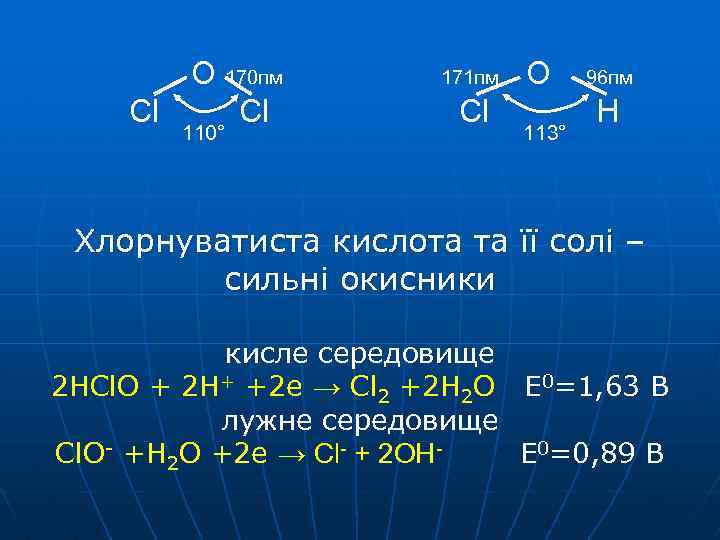
Cl O 170 пм Cl 110° 171 пм Cl O 113° 96 пм H Хлорнуватиста кислота та її солі – сильні окисники кисле середовище 2 HCl. O + 2 H+ +2 e → Cl 2 +2 H 2 O E 0=1, 63 B лужне середовище Cl. O- +H 2 O +2 e → Cl- + 2 OHE 0=0, 89 B
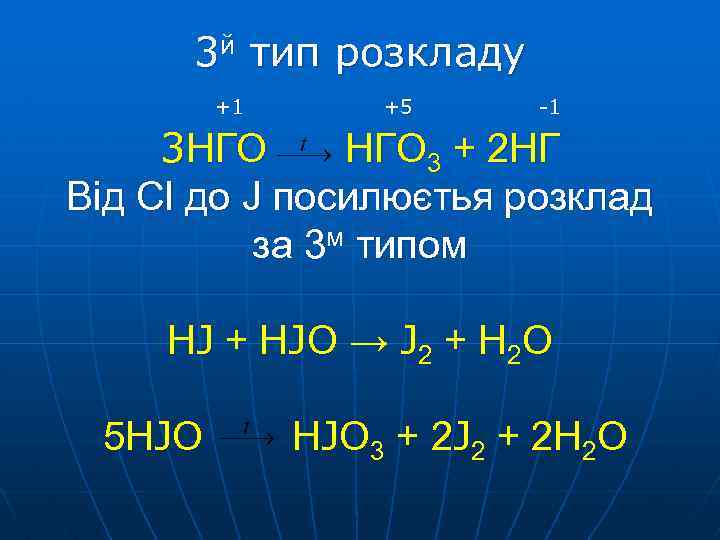
3 й тип розкладу +1 +5 -1 3 НГО 3 + 2 НГ Від Cl до J посилюєтья розклад за 3 м типом H J + H J O → J 2 + H 2 O 5 HJO 3 + 2 J 2 + 2 H 2 O

Cl 2 + 2 KOH → KCl + KCl. O + H 2 O Cl 2 + Ca(OH)2 → Ca(Cl. O)Cl + H 2 O Ca. OCl 2 3 HCl. O 3 + 2 HCl 3 Cl 2 + 6 KOH → 5 KCl + KCl. O 3 + 3 H 2 O KCl. O 3 – хлорат калію, сіль хлорнуватої кислоти HCl. O 3, менш розчинний, ніж KCl

Хлорнувата кислота HCl. O 3 (сильна, існує в розчинах) +5 Ba(Cl. O 3)2 + H 2 SO 4 → Ba. SO 4↓ + 2 HCl. O 3 Для J +5 найстійкіший ступінь окиснення 2 Br 2 + 5 Cl 2 + 6 H 2 O → 10 HCl + 2 HBr. O 3 3 J 2 + 10 HNO 3 → 6 HJO 3 + 10 NO + 2 H 2 O

НCl. O 3, НBr. O 3 існують тільки в розчинах, а НJO 3 – кристалічна речовина, стійка за температури 250 о 2 HJO 3 HCl. O 3 J 2 O 5 + H 2 O HBr. O 3 H JO 3 кислотні властивості послаблюються
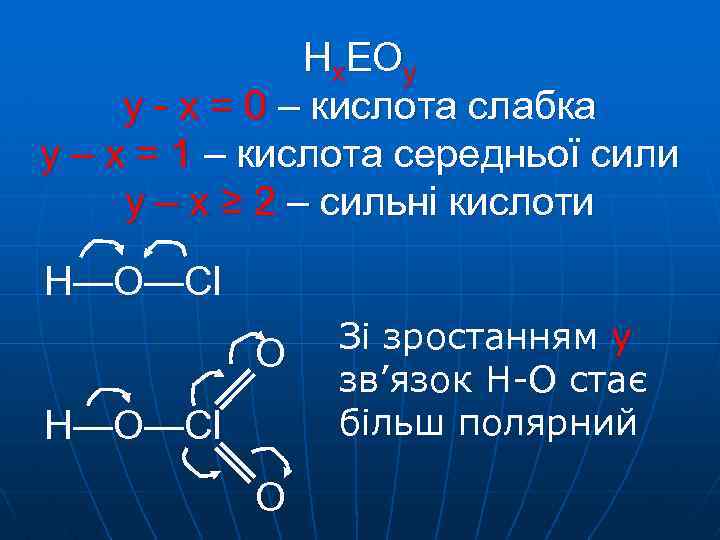
Нx. EOy y - x = 0 – кислота слабка y – x = 1 – кислота середньої сили y – x ≥ 2 – сильні кислоти H—O—Cl O Зі зростанням y зв’язок Н-О стає більш полярний

Сполуки галогенів +5 – сильні окисники Cl. O 3 - кисле середовище + 8 H+ +6 e → Cl- +3 H 2 O E 0=1, 45 B лужне середовище +3 H 2 O +6 e → Cl- + 6 OH- E 0=0, 63 B 2 KCl. O 3 2 KCl + 3 O 2 4 KCl. O 3 KCl + 3 KCl. O 4 KCl. O 3 + Cr 2 O 3+ 4 KOH→ 2 K 2 Cr. O 4 + KCl + 2 H 2 O

2 KCl. O 3+H 2 C 2 O 4→ 2 Cl. O 2+CO 2+K 2 CO 3+ H 2 O 2 KCl. O 3 + H 2 C 2 O 4→ 2 Cl. O 2 + 2 KHCO 3 2 KCl. O 3 + SO 2 → K 2 SO 4 + 2 Cl. O 2 – зеленкувато-жовтий газ з різким запахом (отруйний, вибухонезпечний)
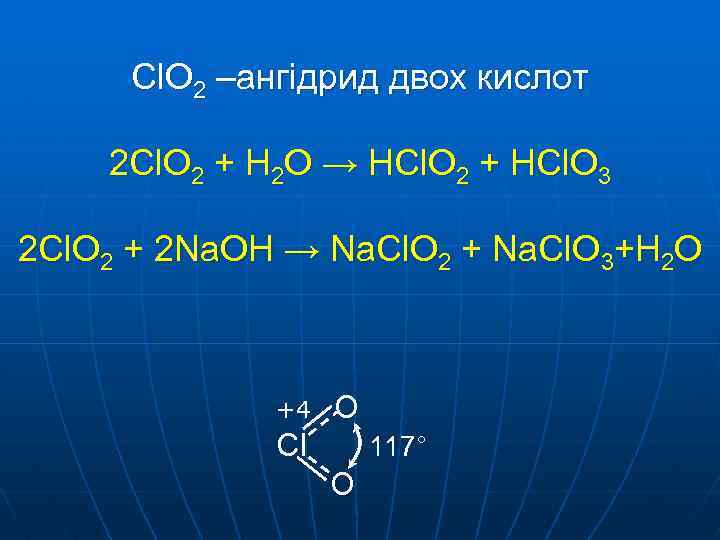
Cl. O 2 –ангідрид двох кислот 2 Cl. O 2 + H 2 O → HCl. O 2 + HCl. O 3 2 Cl. O 2 + 2 Na. OH → Na. Cl. O 2 + Na. Cl. O 3+Н 2 О +4 O Cl 117° O

Добування HCl. O 2 + Ba. O 2 → Ba(Cl. O 2)2 + O 2 Ba(Cl. O 2)2 + H 2 SO 4→ 2 HCl. O 2 + Ba. SO 4 HCl. O 2 ↔ H+ + Cl. O 2 - К = 10 -2 кисле середовище 2 HCl. O 2 + 2 H+ +2 e →HCl. O +H 2 O лужне середовище Cl. O 2 - +H 2 O +2 e → Cl. O- + 2 OH- E 0=1, 64 B E 0=0, 66 B
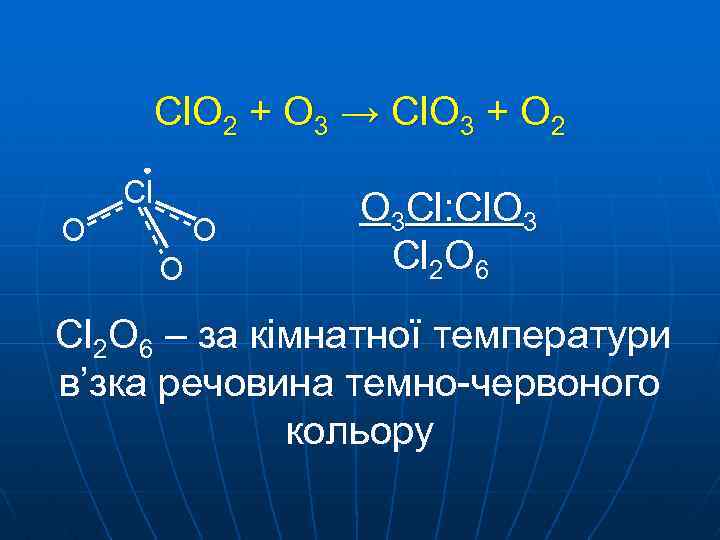
Cl. O 2 + O 3 → Cl. O 3 + O 2 Cl O O 3 Cl: Cl. O 3 Cl 2 O 6 – за кімнатної температури в’зка речовина темно-червоного кольору

Cl 2 O 6 + H 2 O → HCl. O 3 + HCl. O 4 хлорна Cl 2 O 6 + 2 KOH → KCl. O 3 + KCl. O 4+H 2 O перхлорат В промисловості хлорну кислоту добувають анодним окисленням Na. Cl. O 3 К(-) 2 HOH + 2 e → H 2 + 2 OHА(+) Cl. O 3 - – 2 e+H 2 O → Cl. O 4 -+2 H+ KCl. O 4 + H 2 SO 4 → KHSO 4 + HCl. O 4
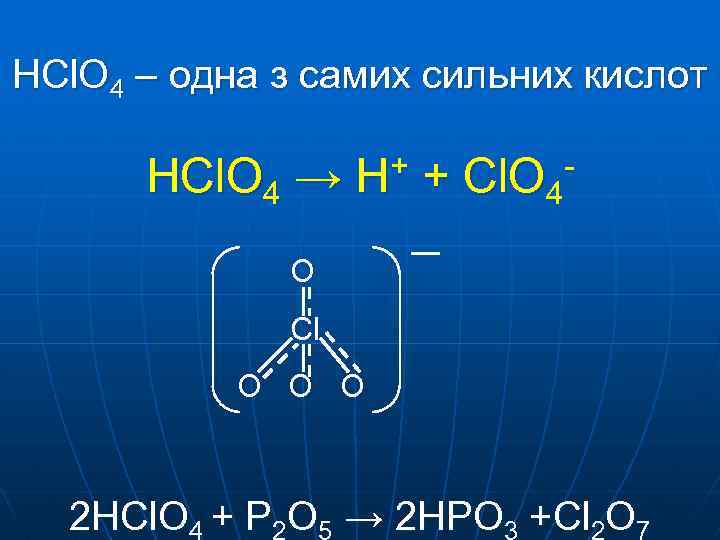
HCl. O 4 – одна з самих сильних кислот HCl. O 4 → H+ + Cl. O 4 O Cl O O O 2 HCl. O 4 + P 2 O 5 → 2 HPO 3 +Cl 2 O 7
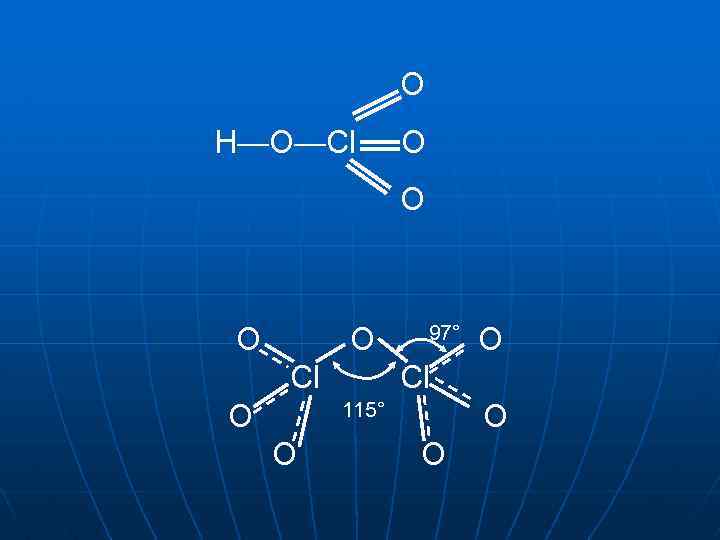
O H—O—Cl O O Cl O 97° Cl O 115° O O O

кисле середовище Cl. O 4 - + 8 H+ + 8 e → Cl- +4 H 2 O E 0=1, 38 B лужне середовище Cl. O 4 - +4 H 2 O + 8 e → Cl- + 8 OHE 0=0, 56 B
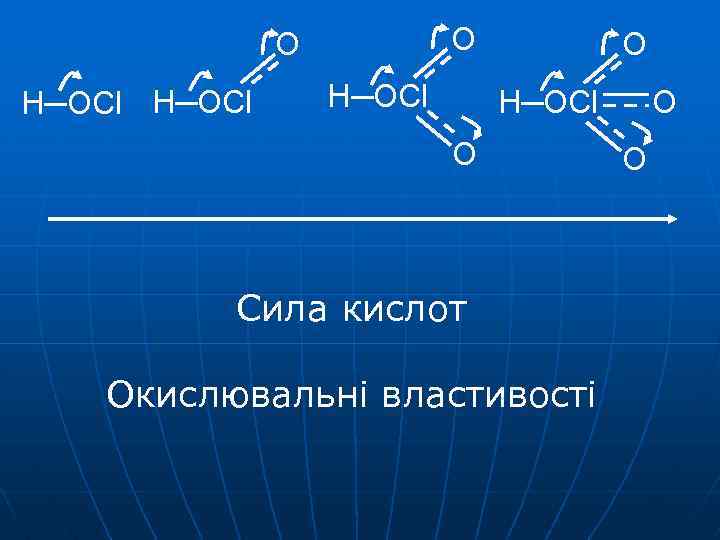
O O H─OCl O Сила кислот Окислювальні властивості O O

2 HCl. O + 2 H+ +2 e → Cl 2 +2 H 2 O E 0=1, 63 B 2 HCl. O 2 + 2 H+ +2 e →HCl. O +H 2 O E 0=1, 64 B Cl. O 3 - + 8 H+ + 6 e → Cl- +3 H 2 O E 0=1, 45 B Cl. O 4 - + 8 H+ + 8 e → Cl- +4 H 2 O E 0=1, 38 B

Br+7 – нестійка H 2 O + Na. Br. O 3 + Xe. F 2 → Na. Br. O 4 + Xe + 2 HF J+7 KJO 3 + Cl 2 + 3 KOH → K 2 H 3 JO 6 + 2 KCl H 5 JO 6 п’ятиосновна кислота середньої сили за І і ІІ стадіями, тому неможливо отримати К 5 JO 6 в розчині
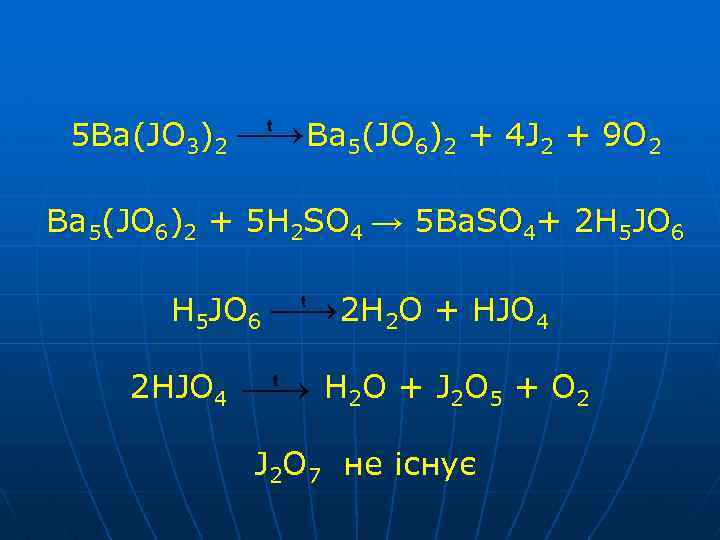
5 Ba(JO 3)2 Ba 5(JO 6)2 + 4 J 2 + 9 O 2 Ba 5(JO 6)2 + 5 H 2 SO 4 → 5 Ba. SO 4+ 2 H 5 JO 6 2 HJO 4 2 H 2 O + HJO 4 H 2 O + J 2 O 5 + O 2 J 2 O 7 не існує
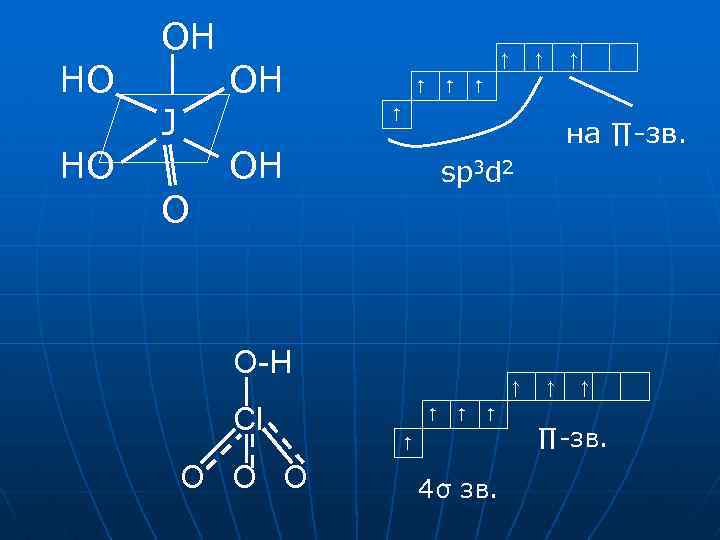
HO HO OH J ↑ OH ↑ ↑ O на ∏-зв. OH sp 3 d 2 O-H Cl O O O ↑ 4σ зв. ↑ ↑ ∏-зв.

HCl. O 4 HBr. O 4 H 5 JO 6 зільшується радіус атомів, тому зменшується стійкість sp 3 і збільшується стійкість sp 3 d 2 сила кислот окисні властивості

- + 8 H+ + 8 e ⇆ Cl- + 4 H O E 0=1, 38 B Cl. O 4 2 - → Cl Cl. O 4 2 E 0=1, 34 B - + 2 H+ +2 e ⇆ Br. O - + H O E 0=1, 76 B Br. O 4 3 2 H 5 JO 6 + H+ + 2 e ⇆ JO 3 - + 3 H 2 O E 0=1, 60 B JO 4 - + 2 H+ + 2 e ⇆ JO 3 - + H 2 O E 0=1, 65 B H 5 J O 6 + 7 H+ - + 6 H O E 0=1, 24 B + 8 e → J 2

Огляд оксигенвмісних сполук галогенів
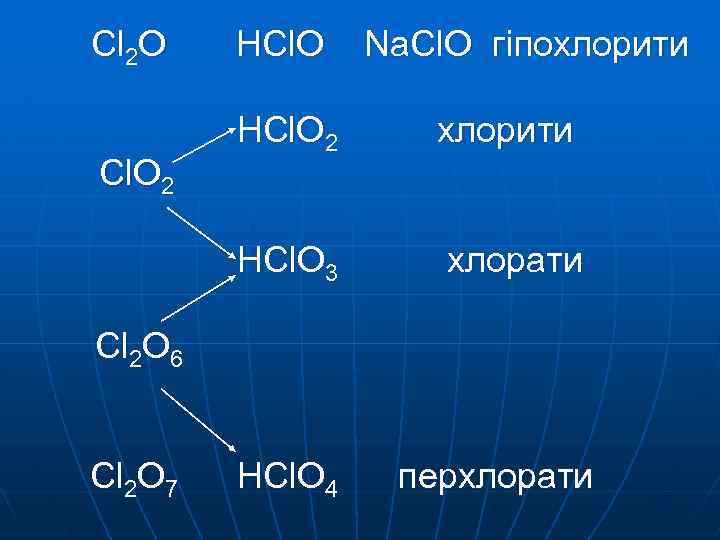
Cl 2 O Cl. O 2 HCl. O 2 Na. Cl. O гіпохлорити. HCl. O 3 хлорати Cl 2 O 6 Cl 2 O 7 . HCl. O 4 перхлорати .
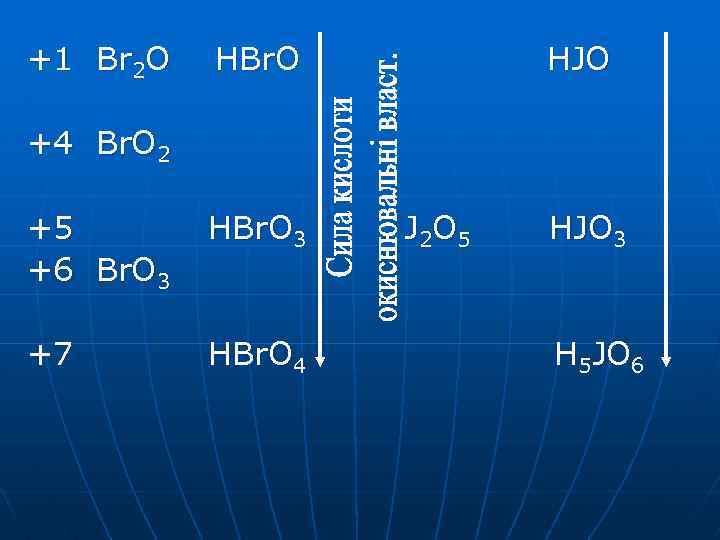
+1 Br 2 O HBr. O HJO +4 Br. O 2 +5 +6 Br. O 3 HBr. O 3 +7 HBr. O 4 J 2 O 5 HJO 3 H 5 JO 6

Всі оксиди Br існують за дуже низьких температур H 5 JO 6 і HJO 3 – кристалічні реч. HСІO 3 – рідина Ці речовино отримують непрямим шляхом

HCl. O — HBr. O — HJO HCl. O 3 — HBr. O 3 — HJO 3 зменшується сила кислот и окисні властивості HCl. O 4 HBr. O 4 сильні H 5 JO 6 сер. Сили Br+7 – самий сильний окисник
Галогени 2.ppt