Оксиды углерода Вспомним изученное – Подберите


Оксиды углерода

Вспомним изученное – Подберите названия к иллюстрациям

3
4

5

7

8

9

Задачи урока: • Рассмотреть строение, получение, химические свойства и применение оксидов углерода; • Выявить биологическое действие изучаемых веществ на живые организмы.

Угарный газ Оксид углерода (II) монооксид углерода, С=О окись углерода 2 s 2 p 1 s 2 p 2 s 1 s

Угарный газ – ядовитое вещество! ПДК (СО) = 20 мг/м 3 Способы получения: 2 С + О 2 = 2 СО СО 2 + С = 2 СО

Физические свойства: Мr(СО) = 28 Цвета, запаха не имеет. Мr(возд. ) = 29 В воде нерастворим. Химические свойства: 2 СО + О 2 = 2 СО 2 СО – сильный восстановитель!
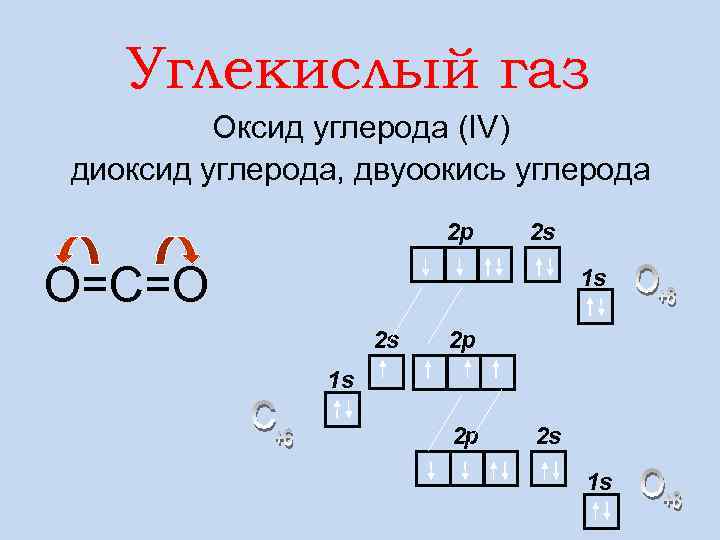
Углекислый газ Оксид углерода (IV) диоксид углерода, двуоокись углерода 2 p 2 s О=С=О 1 s 2 s 2 p 1 s 2 p 2 s 1 s

Углекислый газ — условно ядовитое вещество ПДК (СО 2) = 30 мг/м 3 Способы получения: С + О 2 = СО 2 2 СО + О 2 = 2 СО 2 Са. СО 3 = СО 2 + Са. О Са. СО 3 + 2 HCl = H 2 О + СО 2 + Са. Cl 2

Физические свойства: Мr(СО 2) = 44 Мr(возд. ) = 29 Цвета, запаха не имеет. Хорошо растворяется в воде. Способы распознавания: Не поддерживает горение Вызывает помутнение известковой воды
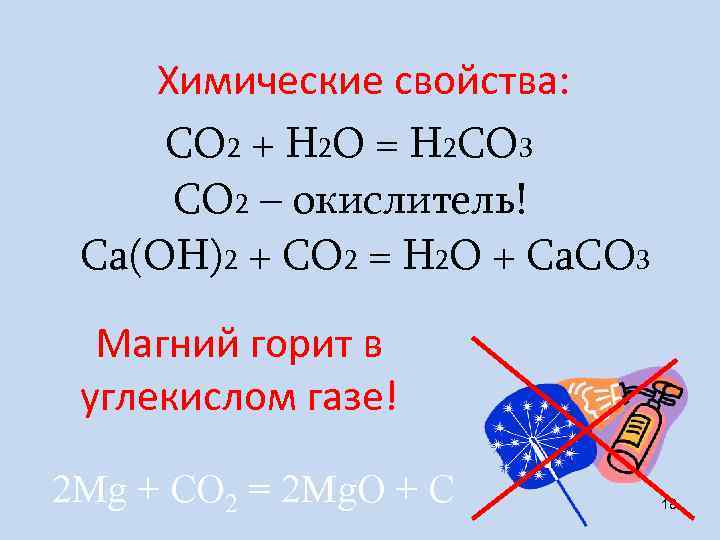
Химические свойства: СО 2 + H 2 О = H 2 СО 3 СО 2 – окислитель! Са(ОН)2 + СО 2 = H 2 О + Са. СО 3 Магний горит в углекислом газе! 2 Мg + CO 2 = 2 Mg. O + C 18

Химический диктант 1 вариант 2 вариант Фамилия: _______ Углекислый газ Угарный газ . . . 1 2 3 4 5 6 7

Оксид углерода (IV)

СO

Окислитель

Не имеет запаха

Растворим в воде

СO 2

Восстановитель

Домашнее задание § 29 , упр. 1 -4
Оксиды углероды.ppt
- Количество слайдов: 25

