оксиды.ppt
- Количество слайдов: 21
 ОКСИДЫ
ОКСИДЫ
 Применение оксидов Са(ОН)2 – гашеная известь- основной строительный продукт оксид цинка Zn. O – вещество белого цвета, поэтому используется для приготовления белой масляной краски (цинковые белила). оксид титана (IV) – Ti. O 2. Он тоже имеет красивый белый цвет и применяется для изготовления титановых белил. «Зелёная хромовая» Cr 2 O 3 – пигмент оливково – зелёной краски.
Применение оксидов Са(ОН)2 – гашеная известь- основной строительный продукт оксид цинка Zn. O – вещество белого цвета, поэтому используется для приготовления белой масляной краски (цинковые белила). оксид титана (IV) – Ti. O 2. Он тоже имеет красивый белый цвет и применяется для изготовления титановых белил. «Зелёная хромовая» Cr 2 O 3 – пигмент оливково – зелёной краски.
 Углекислый газ (CO 2) → Песок (Оксид кремния (IV)Si. O 2) Fe 2 O 3, Si. O 2, Al 2 O 3 (смесь) красная охра.
Углекислый газ (CO 2) → Песок (Оксид кремния (IV)Si. O 2) Fe 2 O 3, Si. O 2, Al 2 O 3 (смесь) красная охра.
 Al 2 O 3 Оксид алюминия Боксит (глина), рубин, сапфир, корунд Cr 2 О 3 как пигмент используют для типографской краски
Al 2 O 3 Оксид алюминия Боксит (глина), рубин, сапфир, корунд Cr 2 О 3 как пигмент используют для типографской краски
 Получение оксидов. Окисление кислородом простых веществ 2 Mg +O 2=2 Mg. O сложных веществ 2 H 2 S+3 O 2=2 H 2 O+2 S O 2 Разложение нагреванием солей нагреванием оснований Сa. CO 3=Ca. O+CO 2 Cu (OH)2=Cu. O+H 20 нагреванием H 2 SO 3=H 2 O+SO 2 кислородсодержащих кислот нагреванием высших 4 Cr. O 3=2 Cr 2 O 3+3 O 2 оксидов Окисление низших оксидов 4 Fe. O+O 2=2 Fe 2 O 3 Вытеснение летучего оксида менее летучим Na 2 CO 3+Si. O 2=Na 2 Si. O 3+CO 2
Получение оксидов. Окисление кислородом простых веществ 2 Mg +O 2=2 Mg. O сложных веществ 2 H 2 S+3 O 2=2 H 2 O+2 S O 2 Разложение нагреванием солей нагреванием оснований Сa. CO 3=Ca. O+CO 2 Cu (OH)2=Cu. O+H 20 нагреванием H 2 SO 3=H 2 O+SO 2 кислородсодержащих кислот нагреванием высших 4 Cr. O 3=2 Cr 2 O 3+3 O 2 оксидов Окисление низших оксидов 4 Fe. O+O 2=2 Fe 2 O 3 Вытеснение летучего оксида менее летучим Na 2 CO 3+Si. O 2=Na 2 Si. O 3+CO 2
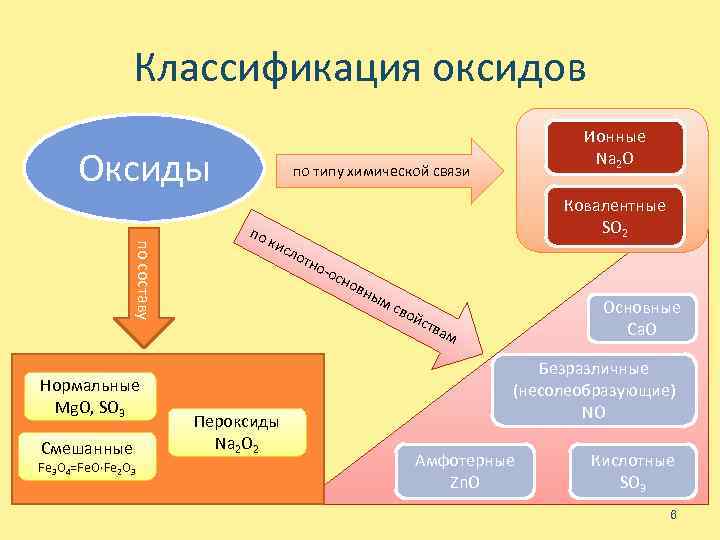 Классификация оксидов Оксиды по составу Нормальные Mg. O, SO 3 Смешанные Fe 3 O 4=Fe. O∙Fe 2 O 3 Ионные Na 2 O по типу химической связи по кис Ковалентные SO 2 Пероксиды Na 2 O 2 лот но- осн овн ым сво Основные Ca. O йст в ам Безразличные (несолеобразующие) NO Амфотерные Zn. O Кислотные SO 3 6
Классификация оксидов Оксиды по составу Нормальные Mg. O, SO 3 Смешанные Fe 3 O 4=Fe. O∙Fe 2 O 3 Ионные Na 2 O по типу химической связи по кис Ковалентные SO 2 Пероксиды Na 2 O 2 лот но- осн овн ым сво Основные Ca. O йст в ам Безразличные (несолеобразующие) NO Амфотерные Zn. O Кислотные SO 3 6
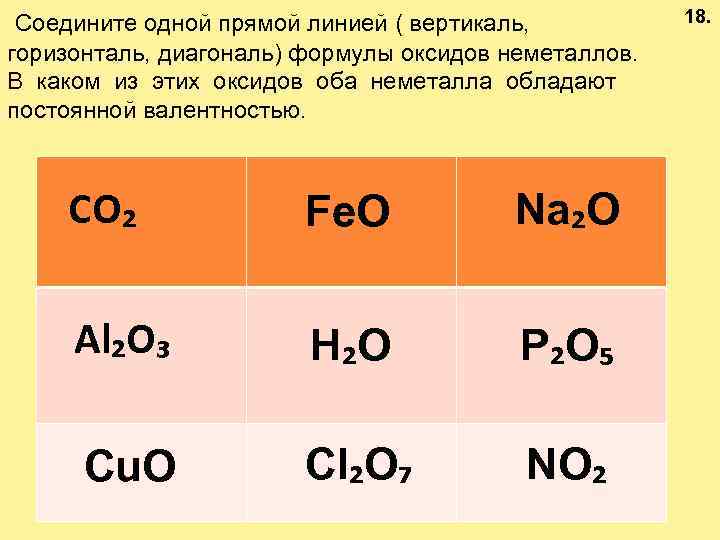 Соедините одной прямой линией ( вертикаль, горизонталь, диагональ) формулы оксидов неметаллов. В каком из этих оксидов оба неметалла обладают постоянной валентностью. CO₂ Fe. O Na₂O Al₂O₃ H₂O P₂O₅ Cu. O Cl₂O₇ NO₂ 18.
Соедините одной прямой линией ( вертикаль, горизонталь, диагональ) формулы оксидов неметаллов. В каком из этих оксидов оба неметалла обладают постоянной валентностью. CO₂ Fe. O Na₂O Al₂O₃ H₂O P₂O₅ Cu. O Cl₂O₇ NO₂ 18.
 С повышением степени окисления атомов элемента, образующего оксиды, увеличиваются кислотные свойства его оксидов и гидроксидов. Неметаллы образуют кислотные оксиды ( исключение несолеобразующие оксиды). Металлы Степени окисления Характер оксидов +1, +2 Основные оксиды (исключение Be. O, Zn. O, Sn. O, Pb. O +3, +4 Амфотерные оксиды и Be. O, Zn. O, Sn. O, Pb. O +5 и выше Кислотные оксиды
С повышением степени окисления атомов элемента, образующего оксиды, увеличиваются кислотные свойства его оксидов и гидроксидов. Неметаллы образуют кислотные оксиды ( исключение несолеобразующие оксиды). Металлы Степени окисления Характер оксидов +1, +2 Основные оксиды (исключение Be. O, Zn. O, Sn. O, Pb. O +3, +4 Амфотерные оксиды и Be. O, Zn. O, Sn. O, Pb. O +5 и выше Кислотные оксиды
 Химические свойства оксидов Основные Кислотные 1. Взаимодействие с водой(оксиды щелочных и 1. Большинство щелочноземельных металлов. ) взаимодействуют с водой Ca. O+H 2 O=Ca(OH)2 SO 3+H 2 O=H 2 SO 4 2. Все с кислотами AI 2 O 3+6 HCl=2 Al. Cl 3+3 H 2 O При избытке многоосновной кислоты образуется кислая соль. При избытке оксида, которому соответствует многоосновное основание, образуется основная соль. В этих случаях вода может не выделяться или даже поглощаться. 2. Со щелочами Na. OH+Si. O 2=Na 2 Si. O 3+H 2 O При избытке кислотного оксида, которому соответствует многоосновная кислота, образуется кислая соль. При избытке многокислотного основания образуется основная соль.
Химические свойства оксидов Основные Кислотные 1. Взаимодействие с водой(оксиды щелочных и 1. Большинство щелочноземельных металлов. ) взаимодействуют с водой Ca. O+H 2 O=Ca(OH)2 SO 3+H 2 O=H 2 SO 4 2. Все с кислотами AI 2 O 3+6 HCl=2 Al. Cl 3+3 H 2 O При избытке многоосновной кислоты образуется кислая соль. При избытке оксида, которому соответствует многоосновное основание, образуется основная соль. В этих случаях вода может не выделяться или даже поглощаться. 2. Со щелочами Na. OH+Si. O 2=Na 2 Si. O 3+H 2 O При избытке кислотного оксида, которому соответствует многоосновная кислота, образуется кислая соль. При избытке многокислотного основания образуется основная соль.
 3. С кислотными и амфотерными оксидами Ca. O+CO 2=Ca. CO 3 Li 2 O+Al 2 O 3=2 Li. Al. O 2 3. С основными и амфотерными оксидами Si. O 2+Ca. O=Ca. Si. O 3 Al 2 O 3+3 SO 3=Al 2(SO 4)3 4. Основный оксид и амфотерный гидроксид (при температуре) Li 2 O + 2 Al(OН)3=2 Li. Al. O 2 + 3 Н 2 О 4. Кислотный оксид (нелетучий) и соль, образованная кислотой, которой соответствует летучий оксид Si. O 2 + Na 2 СO 3 = СO 2 + +Na 2 Si. O 3
3. С кислотными и амфотерными оксидами Ca. O+CO 2=Ca. CO 3 Li 2 O+Al 2 O 3=2 Li. Al. O 2 3. С основными и амфотерными оксидами Si. O 2+Ca. O=Ca. Si. O 3 Al 2 O 3+3 SO 3=Al 2(SO 4)3 4. Основный оксид и амфотерный гидроксид (при температуре) Li 2 O + 2 Al(OН)3=2 Li. Al. O 2 + 3 Н 2 О 4. Кислотный оксид (нелетучий) и соль, образованная кислотой, которой соответствует летучий оксид Si. O 2 + Na 2 СO 3 = СO 2 + +Na 2 Si. O 3
 5. Получение металлов из их оксидов при высокой температуре с помощью восстановителей: С, СО, Н 2, металлов (чаще AL. Mg) – пирометаллургический способ получения металлов. Cu 2 O + C = 2 Cu + CO Cr 2 O 3 + 2 AL = 2 Cr + Al 2 O 3 4. СО 2 реагирует с гидроксидом Be, Zn, Pb(II), Cu(II), c образованием основных солей.
5. Получение металлов из их оксидов при высокой температуре с помощью восстановителей: С, СО, Н 2, металлов (чаще AL. Mg) – пирометаллургический способ получения металлов. Cu 2 O + C = 2 Cu + CO Cr 2 O 3 + 2 AL = 2 Cr + Al 2 O 3 4. СО 2 реагирует с гидроксидом Be, Zn, Pb(II), Cu(II), c образованием основных солей.

 Свойства амфотерных оксидов Амфотерность – двойственность свойств 1. Реагируют с кислотами, проявляя свойства основных оксидов: Al 2 O 3 + 6 HCl = 2 Al. Cl 3 + 3 H 2 O При избытке многоосновной кислоты образуется кислая соль. При избытке оксида – основная соль. 2. Реагируют со щелочами, проявляя свойства кислотных оксидов: Al 2 O 3 + 2 Na. OH + 3 H 2 O= 2 Na[Al(OH)4] (растворе) Al 2 O 3 + 2 Na. OH = 2 Na. Al. O 2 + H 2 O (при сплавлении) Fe 2 O 3 и Сr 2 O 3 взаимодействуют со щелочами только при сплавлении.
Свойства амфотерных оксидов Амфотерность – двойственность свойств 1. Реагируют с кислотами, проявляя свойства основных оксидов: Al 2 O 3 + 6 HCl = 2 Al. Cl 3 + 3 H 2 O При избытке многоосновной кислоты образуется кислая соль. При избытке оксида – основная соль. 2. Реагируют со щелочами, проявляя свойства кислотных оксидов: Al 2 O 3 + 2 Na. OH + 3 H 2 O= 2 Na[Al(OH)4] (растворе) Al 2 O 3 + 2 Na. OH = 2 Na. Al. O 2 + H 2 O (при сплавлении) Fe 2 O 3 и Сr 2 O 3 взаимодействуют со щелочами только при сплавлении.
 Свойства амфотерных оксидов 3. Амфотерный оксид + кислотный оксид (основный оксид) = соль ( при нагревании)
Свойства амфотерных оксидов 3. Амфотерный оксид + кислотный оксид (основный оксид) = соль ( при нагревании)
 Оксидами являются оба вещества в паре 1)Mg. O и H 2 O 2 2)Na 2 O 2 и Ba. O 3)Mn 2 О 7 и N 2 O 3 4)F 2 О и P 2 O 5
Оксидами являются оба вещества в паре 1)Mg. O и H 2 O 2 2)Na 2 O 2 и Ba. O 3)Mn 2 О 7 и N 2 O 3 4)F 2 О и P 2 O 5
 С водой реагируют оксиды: 1)Ba. O и Si. O 2 2)Сu. O и SO 3 3)Ba. O и SO 3 4)Fe. O и СО 2
С водой реагируют оксиды: 1)Ba. O и Si. O 2 2)Сu. O и SO 3 3)Ba. O и SO 3 4)Fe. O и СО 2
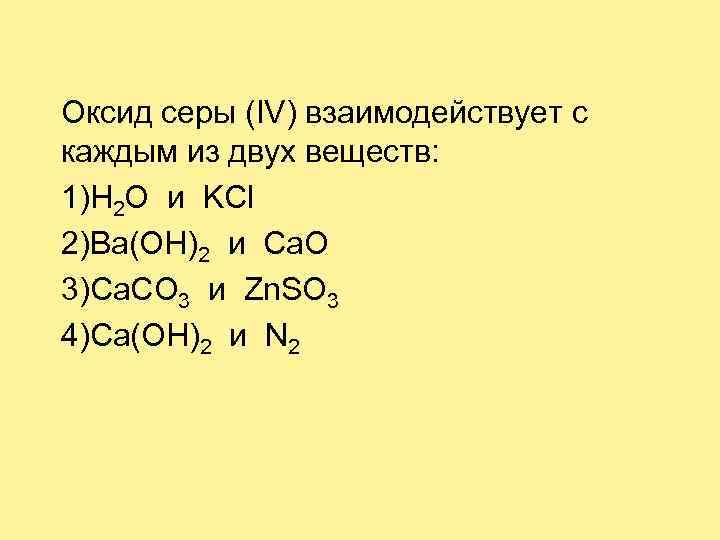 Оксид серы (IV) взаимодействует с каждым из двух веществ: 1)H 2 O и KCl 2)Ba(OH)2 и Ca. O 3)Ca. CO 3 и Zn. SO 3 4)Ca(OH)2 и N 2
Оксид серы (IV) взаимодействует с каждым из двух веществ: 1)H 2 O и KCl 2)Ba(OH)2 и Ca. O 3)Ca. CO 3 и Zn. SO 3 4)Ca(OH)2 и N 2
 С соляной кислотой реагируют каждый из двух оксидов 1)K 2 O и SO 3 2)Al 2 O 3 и Ca. O 3)CO 2 и Zn. O 4)Cr. O 3 и Na 2 O
С соляной кислотой реагируют каждый из двух оксидов 1)K 2 O и SO 3 2)Al 2 O 3 и Ca. O 3)CO 2 и Zn. O 4)Cr. O 3 и Na 2 O
 И с раствором гидроксида натрия и с серной кислотой реагирует 1)Ва. O 2) Cr 2 O 3 3) Si. O 2 4) Mg. O
И с раствором гидроксида натрия и с серной кислотой реагирует 1)Ва. O 2) Cr 2 O 3 3) Si. O 2 4) Mg. O
 Применение оксидов: CO 2 – оксид углерода (IV), углекислый газ. Твердый оксид углерода – сухой лед. Для изготовления соды, сахара, газированных напитков, в жидком виде в огнетушителях. Si. O 2 – оксид кремния (IV) – твердое, тугоплавкое вещество в природе в двух видах: 1) кристаллический кремнезем – в виде минерала кварца и его разновидностей: горный хрусталь, халцедон, агат, яшма, кремень – используют в силикатной промышленности, строительстве. 2) аморфный кремнезем Si. O 2 ∙ n. H 2 O – минерал опал. Применяют соединения оксида кремния в ювелирном деле, изготовлении химической посуды, кварцевых ламп. Для создания цветных стекол используют следующие оксиды: Cо 2 O 3 – синий цвет , Cr 2 O 3 – зеленый цвет, Mn. O 2 – розовый цвет.
Применение оксидов: CO 2 – оксид углерода (IV), углекислый газ. Твердый оксид углерода – сухой лед. Для изготовления соды, сахара, газированных напитков, в жидком виде в огнетушителях. Si. O 2 – оксид кремния (IV) – твердое, тугоплавкое вещество в природе в двух видах: 1) кристаллический кремнезем – в виде минерала кварца и его разновидностей: горный хрусталь, халцедон, агат, яшма, кремень – используют в силикатной промышленности, строительстве. 2) аморфный кремнезем Si. O 2 ∙ n. H 2 O – минерал опал. Применяют соединения оксида кремния в ювелирном деле, изготовлении химической посуды, кварцевых ламп. Для создания цветных стекол используют следующие оксиды: Cо 2 O 3 – синий цвет , Cr 2 O 3 – зеленый цвет, Mn. O 2 – розовый цвет.
 Применение оксидов: Fe 2 O 3 – оксид железа (III) – темно-красного цвета – гематит или красный железняк – для изготовления красок. Fe 3 O 4 – оксид железа (II, III) – минерал магнетит или магнитный железняк, хороший проводник электричества – для получения и изготовления электродов. Ca. O – оксид кальция (II) – порошок белого цвета – «негашеная» известь, используют в строительстве. Al 2 O 3 – оксид алюминия (III) – минерал твердый корунд – как полирующее средство. SO 2 – оксид серы (IV) или сернистый газ – бесцветный газ, имеющий удушливый запах, убивает микроорганизмы, плесневые грибки – окуривают подвалы, погреба, при перевозке и хранении фруктов и ягод.
Применение оксидов: Fe 2 O 3 – оксид железа (III) – темно-красного цвета – гематит или красный железняк – для изготовления красок. Fe 3 O 4 – оксид железа (II, III) – минерал магнетит или магнитный железняк, хороший проводник электричества – для получения и изготовления электродов. Ca. O – оксид кальция (II) – порошок белого цвета – «негашеная» известь, используют в строительстве. Al 2 O 3 – оксид алюминия (III) – минерал твердый корунд – как полирующее средство. SO 2 – оксид серы (IV) или сернистый газ – бесцветный газ, имеющий удушливый запах, убивает микроорганизмы, плесневые грибки – окуривают подвалы, погреба, при перевозке и хранении фруктов и ягод.


