 Оксиды Презентацию выполнили Скопина Татьяна, Стороженко Яна, Четвериков Николай, Цапаев Никита, Братухина Марина, Слобожанинова Полина
Оксиды Презентацию выполнили Скопина Татьяна, Стороженко Яна, Четвериков Николай, Цапаев Никита, Братухина Марина, Слобожанинова Полина
 Определение и факты Оксид — бинарное соединение химического элемента с кислородом в степени окисления − 2, в котором сам кислород связан только с менее электроотрицательным элементом. Весьма распространённый тип соединений, содержащихся в земной коре и во Вселенной вообще. Оксидами называется класс минералов, представляющих собой соединения металла с кислородом
Определение и факты Оксид — бинарное соединение химического элемента с кислородом в степени окисления − 2, в котором сам кислород связан только с менее электроотрицательным элементом. Весьма распространённый тип соединений, содержащихся в земной коре и во Вселенной вообще. Оксидами называется класс минералов, представляющих собой соединения металла с кислородом
 Определение и факты Примерами таких соединений являются ржавчина, вода, песок, углекислый газ, ряд красителей. Ржавчина - Fe(OН)3 Песок - Si. O 2 Вода - H 2 O
Определение и факты Примерами таких соединений являются ржавчина, вода, песок, углекислый газ, ряд красителей. Ржавчина - Fe(OН)3 Песок - Si. O 2 Вода - H 2 O
 Номенклатура Оксиды называют словом «оксид» , после которого следует наименование химического элемента в родительном падеже, например: Na 2 O — оксид натрия, Al 2 O 3 — оксид алюминия. Если элемент имеет переменную степень окисления, то в названии оксида указывается его степень окисления римской цифрой в скобках сразу после названия, например, Cu 2 О — оксид меди(I), Cu. O — оксид меди(II). Также распространены исторически сложившиеся (тривиальные) названия оксидов, например угарный газ CO, серный ангидрид SO 3 и т. д.
Номенклатура Оксиды называют словом «оксид» , после которого следует наименование химического элемента в родительном падеже, например: Na 2 O — оксид натрия, Al 2 O 3 — оксид алюминия. Если элемент имеет переменную степень окисления, то в названии оксида указывается его степень окисления римской цифрой в скобках сразу после названия, например, Cu 2 О — оксид меди(I), Cu. O — оксид меди(II). Также распространены исторически сложившиеся (тривиальные) названия оксидов, например угарный газ CO, серный ангидрид SO 3 и т. д.
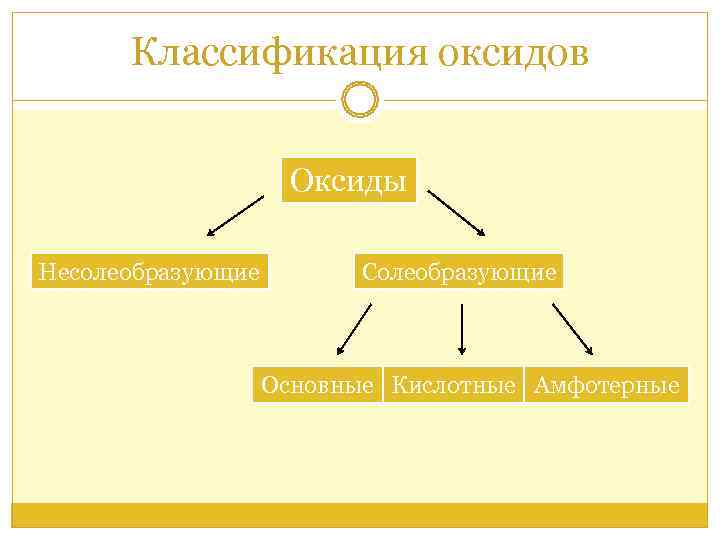 Классификация оксидов Оксиды Несолеобразующие Солеобразующие Основные Кислотные Амфотерные
Классификация оксидов Оксиды Несолеобразующие Солеобразующие Основные Кислотные Амфотерные
 Способы получения оксидов Взаимодействие простых веществ (за исключением инертных газов, золота и платины) с кислородом: 2 H 2 + O 2 = 2 H 2 O 2 Cu + O 2 = 2 Cu. O При горении в кислороде щелочных металлов (кроме лития), а также стронция и бария образуются пероксиды инад пероксиды: 2 Na + O 2 = Na 2 O 2 K + O 2 = KO 2
Способы получения оксидов Взаимодействие простых веществ (за исключением инертных газов, золота и платины) с кислородом: 2 H 2 + O 2 = 2 H 2 O 2 Cu + O 2 = 2 Cu. O При горении в кислороде щелочных металлов (кроме лития), а также стронция и бария образуются пероксиды инад пероксиды: 2 Na + O 2 = Na 2 O 2 K + O 2 = KO 2
 Способы получения оксидов Обжиг или горение бинарных соединений в кислороде: 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 Cs 2 + 3 O 2 = CO 2 + SO 2 2 PH 3 + 4 O 2 = P 2 O 5 + 3 H 2 O Термическое разложение солей: Ca. CO 3 = Ca. O + CO 2 2 Fe. SO 4 = Fe 2 O 3 + SO 2 + SO 3 Термическое разложение оснований или кислот: 2 Al(OH)3 = Al 2 O 3 + 3 H 2 O 4 HNO 3 = 4 NO 2 + 2 H 2 O
Способы получения оксидов Обжиг или горение бинарных соединений в кислороде: 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 Cs 2 + 3 O 2 = CO 2 + SO 2 2 PH 3 + 4 O 2 = P 2 O 5 + 3 H 2 O Термическое разложение солей: Ca. CO 3 = Ca. O + CO 2 2 Fe. SO 4 = Fe 2 O 3 + SO 2 + SO 3 Термическое разложение оснований или кислот: 2 Al(OH)3 = Al 2 O 3 + 3 H 2 O 4 HNO 3 = 4 NO 2 + 2 H 2 O
 Способы получения оксидов Окисление низших оксидов в высшие и восстановление высших в низшие: 4 Fe. O + O 2 = 2 Fe 2 O 3 Взаимодействие некоторых металлов с водой при высокой температуре: Zn + H 2 O = Zn. O + H 2 Взаимодействие солей с кислотными оксидами при сжигании кокса с выделением летучего оксида: Ca 3(PO 4)2 + 3 Si. O 2 + 5 C = 3 Ca. Si. O 3 + 2 P + 5 Ca
Способы получения оксидов Окисление низших оксидов в высшие и восстановление высших в низшие: 4 Fe. O + O 2 = 2 Fe 2 O 3 Взаимодействие некоторых металлов с водой при высокой температуре: Zn + H 2 O = Zn. O + H 2 Взаимодействие солей с кислотными оксидами при сжигании кокса с выделением летучего оксида: Ca 3(PO 4)2 + 3 Si. O 2 + 5 C = 3 Ca. Si. O 3 + 2 P + 5 Ca
 Способы получения оксидов Взаимодействие металлов с кислотами- оксилителями: Zn + 4 HNO 3 = Zn(NO 3)2 + 2 NO 2↑ + 2 H 2 O При действии водоотнимающих веществ на кислоты и соли: 2 KCl. O 4 + H 2 SO 4 = K 2 SO 4 + Cl 2 O 7 + H 2 O Взаимодействие солей слабых неустойчивых кислот с более сильными кислотами: Na. HCO 3 + HCl = Na. Cl + H 2 O + CO 2↑
Способы получения оксидов Взаимодействие металлов с кислотами- оксилителями: Zn + 4 HNO 3 = Zn(NO 3)2 + 2 NO 2↑ + 2 H 2 O При действии водоотнимающих веществ на кислоты и соли: 2 KCl. O 4 + H 2 SO 4 = K 2 SO 4 + Cl 2 O 7 + H 2 O Взаимодействие солей слабых неустойчивых кислот с более сильными кислотами: Na. HCO 3 + HCl = Na. Cl + H 2 O + CO 2↑
 Спасибо за внимание!
Спасибо за внимание!





















