Оксиды.ppt
- Количество слайдов: 13

Оксиды

План Определение оксидов Примеры Классификация Солеобразующие оксиды Номенклатура Химические свойства основных оксидов Химические свойства кислотных оксидов Химические свойства амфотерных оксидов Получение

Определение Окси д (о кисел, о кись) — бинарное соединение химического элемента с кислородом в степени окисления − 2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все соединения химических элементов с кислородом. К исключениям относятся, например, дифторид кислорода OF 2.

Примеры оксидов Ржавчина Вода Песок Углекислый газ Различные красители… Оксид хрома (III) Оксид свинца
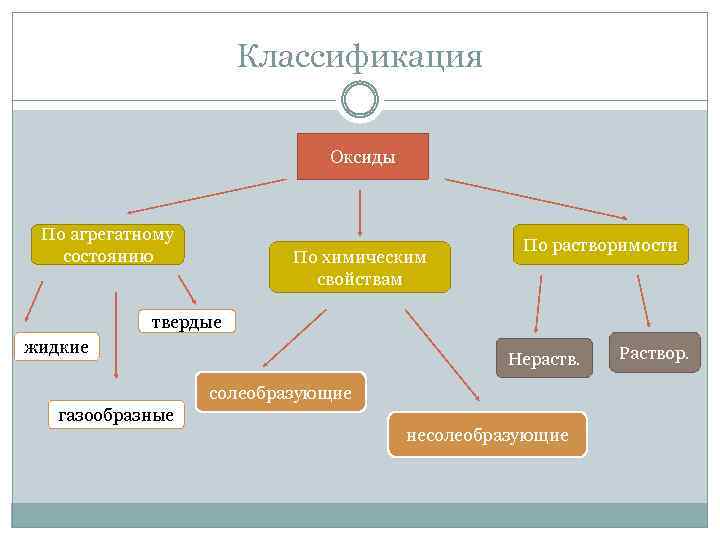
Классификация Оксиды По агрегатному состоянию По химическим свойствам По растворимости твердые жидкие Нераств. солеобразующие газообразные несолеобразующие Раствор.

Солеобразующие оксиды Основные (оксиды металлов, степень окисления которых I-II). Например, Na 2 O, Cu. O… Кислотные (оксиды металлов со степенью окисления V-VII и оксиды неметаллов). Например, Cr. O 3, Mg 2 O 7… Амфотерные (оксиды металлов со степенью окисления III-IV и исключения – Sn. O, Be. O, Zn. O, Pb. O)

Номенклатура В соответствии с номенклатурой ИЮПАК, оксиды называют словом «оксид» , после которого следует наименование химического элемента в родительном падеже. Если элемент имеет переменную степень окисления, то в названии оксида указывается его степень окисления римской цифрой в скобках сразу после названия. Часто используют и другие наименования оксидов по числу атомов кислорода: если оксид содержит только один атом кислорода, то его называют монооксидом, моноокисью или закисью, если два — диоксидом или двуокисью, если три — то триоксидом или триокисью и т. д. Также распространены исторически сложившиеся (тривиальные) названия оксидов, например угарный газ CO, серный ангидрид SO 3 и т. д. В начале XIX века и ранее тугоплавкие, практически не растворимые в воде оксиды химики называли «землями»

Химические свойства основных оксидов Активные металлы взаимодействуют с водой с образованием щелочи. (сильноосновный оксид!) K 2 O + H 2 O = 2 KOH Реагируют с кислотными оксидами с образованием соли при нагревании: 1)Активный металл: K 2 O + CO 2 = K 2 CO 3 2)Неактивный мет. : Fe. O + SO 3 (только жидкий или твердый) = Fe 2 So 4

Химические свойства основных оксидов Реагируют с кислотами с образованием соли и воды: K 2 O + HNO 3 = KNO 3 + H 2 O Реагируют с водородом с образованием металла и воды (металл должен быть менее активен, чем алюминий): Cu. O + H 2 = Cu + H 2 O Реагируют при нагревании с амфотерными оксидами с образованием соли: Na 2 O + Zn. O = H 2 Zn. O 2

Химические свойства кислотных оксидов Взаимодействуют с водой с образованием кислоты: P 2 O 5 + 3 H 2 O = 2 H 3 PO 4 ( при t) (Si. O 2 в реакцию не вступает!) Реагируют с основными оксидами с образованием соли. Реагируют с щелочами с образованием соли и воды: CO 2 + 2 KOH = K 2 CO 3 + H 2 O Реагируют при нагревании с амфотерными с образованием соли: Al 2 O 3 + 3 SO 3 = Al 2(SO 4)3 (при t)

Химические свойства амфотерных оксидов Не реагируют с водой! Реагируют с основными оксидами с образованием соли. Реагируют с щелочами с образованием соли и воды: Al 2 O 3 + 2 KOH = 2 KAl. O 2 + H 2 O Реагируют с кислотными оксидами с образованием соли. Реагируют с кислотами с образованием соли и воды: Zn. O + H 2 SO 4 = Zn. SO 4 + H 2 O

Получение Взаимодействие простых веществ (за исключением инертных газов, золота и платины) с кислородом: 2 H 2 + O 2 → 2 H 2 O 2 Cu + O 2 → 2 Cu. O При горении в кислороде щелочных металлов (кроме лития), а также стронция и бария образуются пероксиды и надпероксиды: 2 Na + O 2 → Na 2 O 2 K + O 2 → KO 2 Обжиг или горение бинарных соединений в кислороде: 4 Fe. S 2 + 11 O 2 → 2 Fe 2 O 3 + 8 SO 2↑ CS 2 + 3 O 2 → CO 2 + 2 SO 2 2 PH 3 + 4 O 2 → P 2 O 5 + 3 H 2 O Термическое разложение солей: Ca. CO 3 → Ca. O + CO 2↑ 2 Fe. SO 4 → Fe 2 O 3 + SO 2↑ + SO 3↑ Термическое разложение оснований или кислот: 2 Al(OH)3 → Al 2 O 3 + 3 H 2 O↑ 4 HNO 3 → 4 NO 2↑ + 2 H 2 O

Получение Окисление низших оксидов в высшие и восстановление высших в низшие: 4 Fe. O + O 2 → 2 Fe 2 O 3 + CO → 2 Fe. O + CO 2↑ Взаимодействие некоторых металлов с водой при высокой температуре: Zn + H 2 O → Zn. O + H 2↑ Взаимодействие солей с кислотными оксидами при сжигании кокса с выделением летучего оксида: Ca 3(PO 4)2 + 3 Si. O 2 + 5 C(кокс) → 3 Ca. Si. O 3 + 2 P+5 CO↑ Взаимодействие металлов с кислотами-оксилителями: Zn + 4 HNO 3(конц. ) → Zn(NO 3)2 + 2 NO 2↑ + 2 H 2 O При действии водоотнимающих веществ на кислоты и соли: 2 KCl. O 4 + H 2 SO 4(конц) → K 2 SO 4 + Cl 2 O 7 + H 2 O Взаимодействие солей слабых неустойчивых кислот с более сильными кислотами: Na. HCO 3 + HCl → Na. Cl + H 2 O + CO 2↑
Оксиды.ppt