оксиды азота.ppt
- Количество слайдов: 14

Оксиды азота.

Азот способен проявлять положительные степени окисления от +1 до +5. Известны несколько оксидов азота. +1 +2 +3 +4 +5 N 2 O NO N 2 O 5 N 2 O 3 NO 2 Солеобразующие: N 2 O 3 NO 2 N 2 O 4 N 2 O 5 димер оксида азота(IV) Несолеобразующие: N 2 O NO Все оксиды азота, кроме N 2 O, ядовитые вещества.

Азот образует ряд оксидов, формально отвечающих всем возможным степеням окисления от +1 до +5: N 2 O, NО, N 2 O 3, NO 2, N 2 O 5, однако всего два из них — оксид азота(II) и оксид азота(IV) — не только устойчивы при обычных условиях, но и активно задействованы в природном и промышленном круговоротах азота.

N 2 O оксид азота (I) II IV II N=N=O +2 2 N=N=O степень окисления распределяется на два атома азота и равна для обоих +2, а для одного +1 Молекула линейна Получение: NH 4 NO 3 = N 2 O + 2 Н 2 O Бесцветный газ со слабым запахом и сладковатым вкусом, хорошо растворим в воде, но не взаимодействует с ней. В смеси с кислородом используется в медицине для слабого наркоза. ( «веселящий» газ)

Проявляет окислительные свойства, в нем, как и в кислороде, вспыхивает тлеющая лучина и ярко горит сера. При нагревании выше 600 °С разлагается со взрывом: 2 N 2 O = 2 N 2 + O 2. Взаимодействует с водородом: N 2 O + H 2 = N 2 + H 2 O. При поджигании смеси оксида азота (I) и аммиака происходит взрыв: 3 N 2 O + 2 NH 3 = 4 N 2 + 3 H 2 O. При взаимодействии с сильными окислителями проявляет восстановительные свойства: 5 N 2 O + 2 KMn. O 4 + 3 H 2 SO 4 = 10 NO + 2 Mn. SO 4 + K 2 SO 4 + 3 H 2 O.

NO оксид азота (II) II N=О молекула линейна, имеет неспаренный электрон, поэтому является радикалом, используется как донор электронов. Окислительно-восстановительная двойственность Восстановитель: Окислитель: так как радикал, очень легко подвергается окислению Нитрозный способ получения серной кислоты 2 NO + O 2 = 2 NO 2 (легко!) 2 NO + 2 SO 2 = 2 SO 3 + N 2 Бесцветный газ, не имеет запаха. В воде малорастворим. Образуется из азота и кислорода при сильных электрических разрядах (например, во время грозы в воздухе) или при высокой температуре: N 2 + O 2 2 NO В лаборатории: 3 Сu +8 HNO 3 ==3 Cu(NO 3)2 +2 NO +4 H 2 O разб.


N 2 O 3 оксид азота (III) Это соединение очень неустойчиво и существует только при низких температурах. В твердом и жидком состоянии (tпл = -100 °С) это вещество окрашено в ярко-синий цвет; выше О °С оно разлагается: N 203=N 0 + N 02 Кислотный оксид: N 2 O 3 + H 2 O = 2 HNO 2 N 2 O 3 + 2 KOH = 2 KNO 2 + H 2 O жидкость, темно – синего цвета, неустойчива при низких температурах и разлагается: N 2 O 3 = NO + NO 2

Оксид азота (IV) II III II O=N N=O Условно кислотный оксид: +3 +5 2 NO 2 + H 2 O = HNO 2 + HNO 3 При температуре выше 0 °С реакция протекает по другому: 3 NO 2 + H 2 O = 2 HNO 3 + NO. 2 NO 2 + 2 Na. OH = Na. NO 3 + Na. NO 2 + H 2 O Ниже 22 С молекулы оксида азота(IV) легко 2 NO 2 = N 2 O 4 соединяются попарно и образуют бесцветную жидкость состава N 2 O 4 , которая при охлаждении до 10, 2 С превращается в бесцветные кристаллы «Лисий хвост» Ядовитый газ бурого цвета, имеет характерный запах. Хорошо растворяется в воде.

Диоксид азота – сильный окислитель, Сильный окислитель, в его атмосфере горят углерод и сера: С + 2 NO 2 = CO 2 + 2 NO; S + 2 NO 2 = SO 2 + 2 NO.

Оксид азота (V) Кислотный оксид: N 2 O 5 + H 2 O = 2 HNO 3 Легко разлагается (при нагревании – со взрывом): 2 N 2 O 5 = 4 NO 2 + O 2 Бесцветные прозрачные кристаллы, хорошо растворяющиеся в воде с образованием азотной кислоты : N 2 O 5 + H 2 O = 2 HNO 3 Нестойкие кристаллы: 2 N 2 O 5 =4 NO 2 + O 2 Как и оксид азота(III) практического значения не имеет

При растворении N 205 в воде образуется азотная кислота. Высший оксид азота является сильным окислителем, например: N 205 + I 2 = I 205 + N 2 В безводных кислотах (серной, азотной, ортофосфорной, хлорной) N 205 рас падается, образуя катион нитрония N 02: N 2 O 5 + НСl. O 4= NO 2 +Cl O 4 + HNO 3 Соли нитрония являются сильными окислителями. При попадании в воду они гид ролизуются: NO 2 +Cl. O 4 + Н 2 O = HNO 3 + НСl. O 4

Обобщающие задания. 1. Имеются три закрытых цилиндра: с оксидом азота (IV), с азотом, с аммиаком. Как проще всего узнать, в каком цилиндре какой газ содержится? В каких цилиндрах и как изменится окраска влажной фиолетовой лакмусовой бумажки? NH 3 NO 2
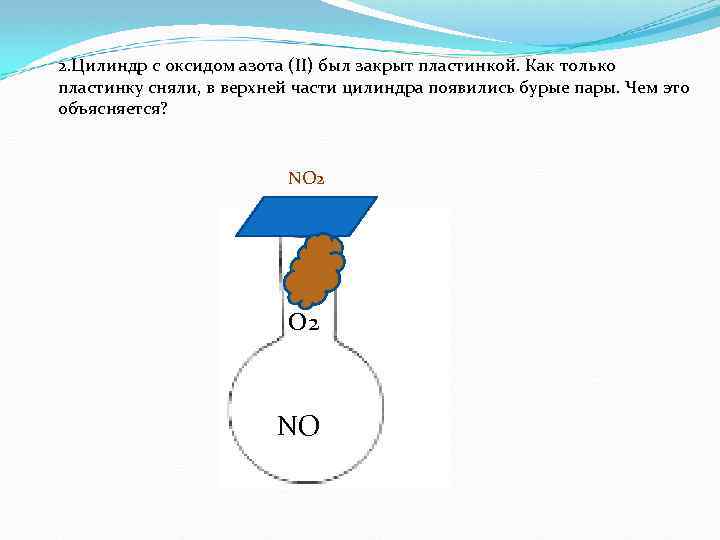
2. Цилиндр с оксидом азота (II) был закрыт пластинкой. Как только пластинку сняли, в верхней части цилиндра появились бурые пары. Чем это объясняется? NO 2 NO
оксиды азота.ppt