Оксидоредуктазы ОФ.ppt++.pptказ.ppt
- Количество слайдов: 45
 ОКСИДОРЕДУКТАЗАЛАР
ОКСИДОРЕДУКТАЗАЛАР
 ОСПАРЫ: , ДӘРІС Ж ЖІКТЕЛУІ Р, УКТАЗАЛА ЕД ОКСИДОР Ы 1. ҚҰРЫЛЫС ӨЛІ ГИЯЛЫҚ Р 2. БИОЛО.
ОСПАРЫ: , ДӘРІС Ж ЖІКТЕЛУІ Р, УКТАЗАЛА ЕД ОКСИДОР Ы 1. ҚҰРЫЛЫС ӨЛІ ГИЯЛЫҚ Р 2. БИОЛО.
 ОКСИДОРЕДУКТАЗАЛАР–ТОТЫҒУ– ТОТЫҚСЫЗДАНУ РЕАКЦИЯЛАРЫН ТЕЗДЕТЕДІ. ОЛАР 2 КОМПОНЕНТТІ. ЖАСУША ІШІЛІК ФЕРМЕНТТЕР. ТОТЫҒУ ТҮРІНЕ ҚАРАЙ 4 ТОПҚА БӨЛЕДІ: 1) 2) 3) 4) ДЕГИДРОГЕНАЗАЛАР(анаэробты, аэробты) ЦИТОХРОМДАР КАТАЛАЗА МЕН ПЕРОКСИДАЗАЛАР ОКСИГЕНАЗАЛАР
ОКСИДОРЕДУКТАЗАЛАР–ТОТЫҒУ– ТОТЫҚСЫЗДАНУ РЕАКЦИЯЛАРЫН ТЕЗДЕТЕДІ. ОЛАР 2 КОМПОНЕНТТІ. ЖАСУША ІШІЛІК ФЕРМЕНТТЕР. ТОТЫҒУ ТҮРІНЕ ҚАРАЙ 4 ТОПҚА БӨЛЕДІ: 1) 2) 3) 4) ДЕГИДРОГЕНАЗАЛАР(анаэробты, аэробты) ЦИТОХРОМДАР КАТАЛАЗА МЕН ПЕРОКСИДАЗАЛАР ОКСИГЕНАЗАЛАР
 ДЕГИДРОГЕНАЗАЛАР–субстратты дегидрлеу, яғни сутек атомын (Н) бөліп алу арқылы тотықтырады. Өкілдері: 1) пиридин ферменттер (ПФ); 2) флавин ферменттер (ФП); 3) кофермент Q немесе убихинон (Ко. Q)
ДЕГИДРОГЕНАЗАЛАР–субстратты дегидрлеу, яғни сутек атомын (Н) бөліп алу арқылы тотықтырады. Өкілдері: 1) пиридин ферменттер (ПФ); 2) флавин ферменттер (ФП); 3) кофермент Q немесе убихинон (Ко. Q)
 ПИРИДИН ФЕРМЕНТ (ПФ) 2 КОМПОНЕНТТІ. КОФЕРМЕНТТЕРІ: НАД , НАДФ ( никотинамидадениндинуклеотид) (никотинамидадениндинуклеоти дфосфат)
ПИРИДИН ФЕРМЕНТ (ПФ) 2 КОМПОНЕНТТІ. КОФЕРМЕНТТЕРІ: НАД , НАДФ ( никотинамидадениндинуклеотид) (никотинамидадениндинуклеоти дфосфат)
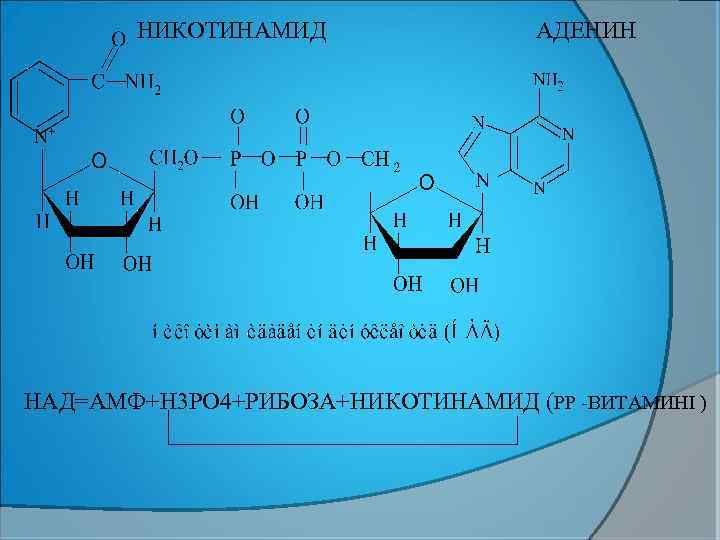 НИКОТИНАМИД АДЕНИН НАД=АМФ+Н 3 РО 4+РИБОЗА+НИКОТИНАМИД (РР -ВИТАМИНІ )
НИКОТИНАМИД АДЕНИН НАД=АМФ+Н 3 РО 4+РИБОЗА+НИКОТИНАМИД (РР -ВИТАМИНІ )
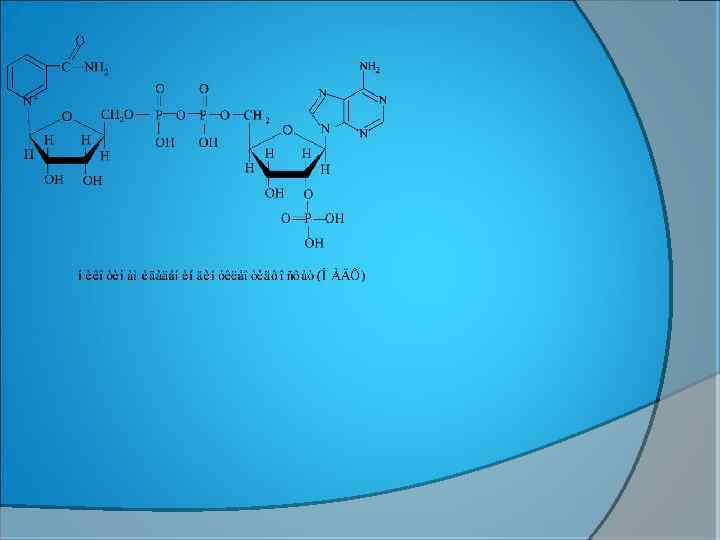
 ПФ СУБСТРАТТЫ ДЕГИДРЛЕНУ ЖОЛЫМЕН ТОТЫҚТЫРАДЫ. ТОТЫҒУ-ТОТЫҚСЫЗДАНУ РЕАКЦИЯСЫНА КОФЕРМЕНТТІҢ ТЕК НИКОТИНАМИД БӨЛІГІ ҚАТЫСАДЫ.
ПФ СУБСТРАТТЫ ДЕГИДРЛЕНУ ЖОЛЫМЕН ТОТЫҚТЫРАДЫ. ТОТЫҒУ-ТОТЫҚСЫЗДАНУ РЕАКЦИЯСЫНА КОФЕРМЕНТТІҢ ТЕК НИКОТИНАМИД БӨЛІГІ ҚАТЫСАДЫ.
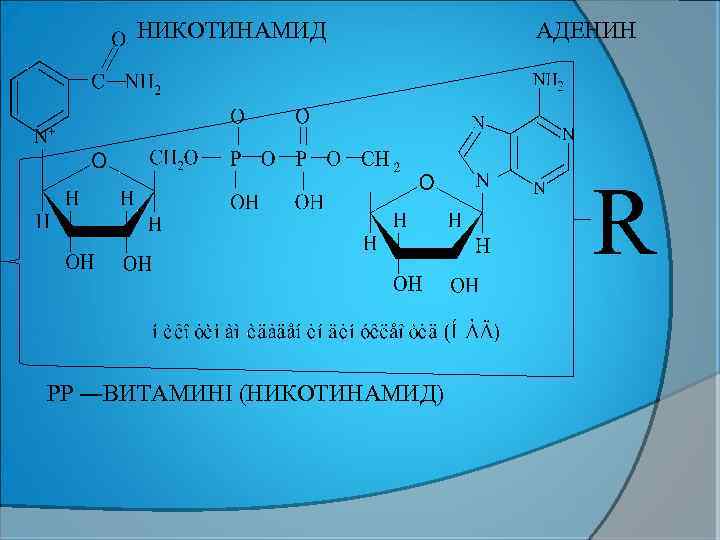 НИКОТИНАМИД АДЕНИН R РР ―ВИТАМИНІ (НИКОТИНАМИД)
НИКОТИНАМИД АДЕНИН R РР ―ВИТАМИНІ (НИКОТИНАМИД)
 Мысалы: коферменті НАД болатын ЛДГ ЛАКТАТ ПИРУВАТ Н+ +ē ТОТЫҚҚАН ТОТЫҚСЫЗДАНҒАН
Мысалы: коферменті НАД болатын ЛДГ ЛАКТАТ ПИРУВАТ Н+ +ē ТОТЫҚҚАН ТОТЫҚСЫЗДАНҒАН
 ЛАКТАТТАН 2 Н АТОМЫ БӨЛІНЕДІ: БІР СУТЕК АТОМЫ НИКОТИНАМИДТЕГІ С-4 ОРНЫНА ҚОСЫЛАДЫ, АЛ ЕКІНШІ Н 0→Н++е. ЫДЫРАЙДЫ. е- БІРІНШІ ОРЫНДАҒЫ АЗОТҚА ҚОСЫЛЫП, АЗОТ НЕЙТРАЛ КҮЙГЕ АЙНАЛАДЫ. АПОФЕРМЕНТ КОФЕРМЕНТТЕН БӨЛІНІП КЕТЕДІ. ПРОТОН ЕРТІНДІДЕ ҚАЛАДЫ. НИКОТИНАМИДТЕГІ 3 ҚОС БАЙЛАНЫС 2 БАЙЛАНЫСҚА АЙНАЛАДЫ. НАДН 2 Н/Е НАДФН 2 ТОТЫҚСЫЗДАНАДЫ, НАДН 2 ФП(ФМН)- МЕН ТОТЫҒАДЫ.
ЛАКТАТТАН 2 Н АТОМЫ БӨЛІНЕДІ: БІР СУТЕК АТОМЫ НИКОТИНАМИДТЕГІ С-4 ОРНЫНА ҚОСЫЛАДЫ, АЛ ЕКІНШІ Н 0→Н++е. ЫДЫРАЙДЫ. е- БІРІНШІ ОРЫНДАҒЫ АЗОТҚА ҚОСЫЛЫП, АЗОТ НЕЙТРАЛ КҮЙГЕ АЙНАЛАДЫ. АПОФЕРМЕНТ КОФЕРМЕНТТЕН БӨЛІНІП КЕТЕДІ. ПРОТОН ЕРТІНДІДЕ ҚАЛАДЫ. НИКОТИНАМИДТЕГІ 3 ҚОС БАЙЛАНЫС 2 БАЙЛАНЫСҚА АЙНАЛАДЫ. НАДН 2 Н/Е НАДФН 2 ТОТЫҚСЫЗДАНАДЫ, НАДН 2 ФП(ФМН)- МЕН ТОТЫҒАДЫ.
 ПФ - БІРІНШІ РЕТТІК ДЕГИДРОГЕНАЗАЛАР , СЕБЕБІ СУБСТРАТПЕН ТІКЕЛЕЙ ӘРЕКЕТТЕСІП ОЛАРДАН СУТЕГІН БӨЛІП АЛАДЫ.
ПФ - БІРІНШІ РЕТТІК ДЕГИДРОГЕНАЗАЛАР , СЕБЕБІ СУБСТРАТПЕН ТІКЕЛЕЙ ӘРЕКЕТТЕСІП ОЛАРДАН СУТЕГІН БӨЛІП АЛАДЫ.
 НАД- ПЕН НАДФ- ТІҢ БІРІНЕН АЙЫРМАШЫЛЫҒЫ: vҚҰРЫЛЫСЫНДА (НАДФ-ТЕ АМФ ҚҰРАМЫНДАҒЫ РИБОЗАНЫҢ 2´―ОН ТОБЫНА ФОСФОР ҚЫШҚЫЛЫ БАЙЛАНЫСҚАН) v. БИОЛОГИЯЛЫҚ ФУНКЦИЯСЫНДА v. КЕЗДЕСЕТІН ОРНЫНДА
НАД- ПЕН НАДФ- ТІҢ БІРІНЕН АЙЫРМАШЫЛЫҒЫ: vҚҰРЫЛЫСЫНДА (НАДФ-ТЕ АМФ ҚҰРАМЫНДАҒЫ РИБОЗАНЫҢ 2´―ОН ТОБЫНА ФОСФОР ҚЫШҚЫЛЫ БАЙЛАНЫСҚАН) v. БИОЛОГИЯЛЫҚ ФУНКЦИЯСЫНДА v. КЕЗДЕСЕТІН ОРНЫНДА
 ФЛАВИНФЕРМЕНТІ (ФП) 2 КОМПОНЕНТТІ. КОФЕРМЕНТТЕРІ: ФМН ФАД (ФЛАВИНМОНОНУКЛЕОТИД) (ФЛАВИНАДЕНИНДИ Д)
ФЛАВИНФЕРМЕНТІ (ФП) 2 КОМПОНЕНТТІ. КОФЕРМЕНТТЕРІ: ФМН ФАД (ФЛАВИНМОНОНУКЛЕОТИД) (ФЛАВИНАДЕНИНДИ Д)
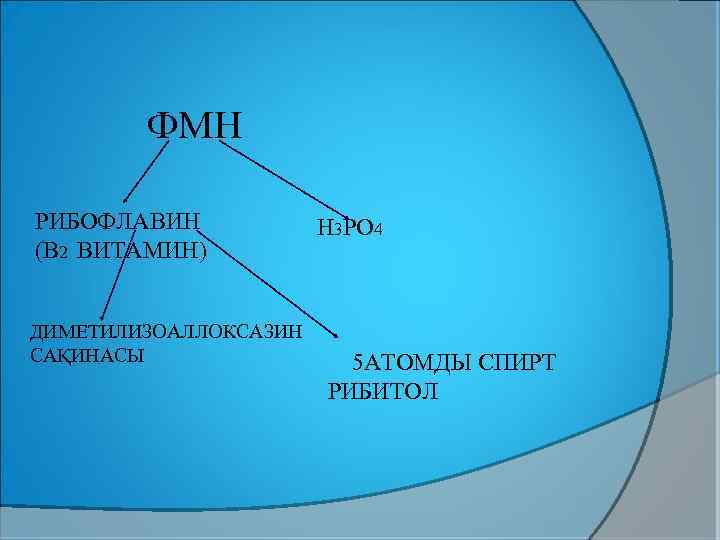 ФМН РИБОФЛАВИН (В 2 ВИТАМИН) ДИМЕТИЛИЗОАЛЛОКСАЗИН САҚИНАСЫ Н 3 РО 4 5 АТОМДЫ СПИРТ РИБИТОЛ
ФМН РИБОФЛАВИН (В 2 ВИТАМИН) ДИМЕТИЛИЗОАЛЛОКСАЗИН САҚИНАСЫ Н 3 РО 4 5 АТОМДЫ СПИРТ РИБИТОЛ
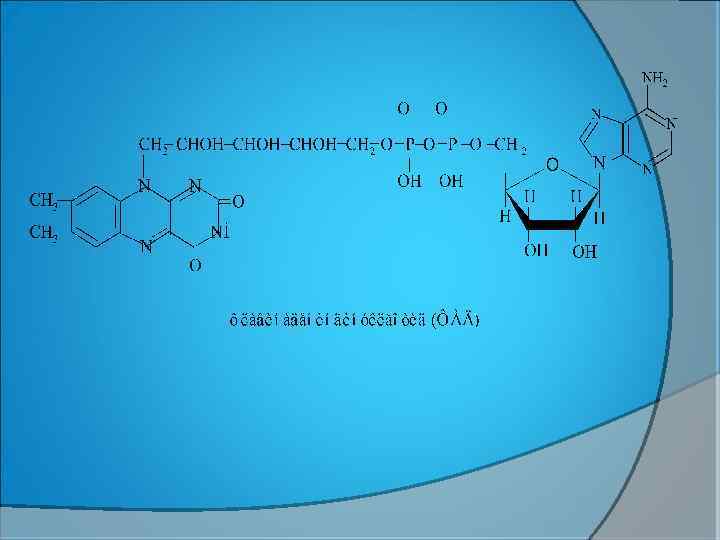
 ИЗОАЛЛОКСАЗИН РИБИТОЛ 1 10 ФАД=ФМН+АМФ
ИЗОАЛЛОКСАЗИН РИБИТОЛ 1 10 ФАД=ФМН+АМФ
 ФП СУБСТРАТТЫ ДЕГИДРЛЕНУ ЖОЛЫМЕН ТОТЫҚТЫРАДЫ. ТОТЫҒУ ־ ТОТЫҚСЫЗДАНУ РЕАКЦИЯСЫНА ТЕК ИЗОАЛЛОКСАЗИН САҚИНАСЫ ҚАТЫСАДЫ.
ФП СУБСТРАТТЫ ДЕГИДРЛЕНУ ЖОЛЫМЕН ТОТЫҚТЫРАДЫ. ТОТЫҒУ ־ ТОТЫҚСЫЗДАНУ РЕАКЦИЯСЫНА ТЕК ИЗОАЛЛОКСАЗИН САҚИНАСЫ ҚАТЫСАДЫ.
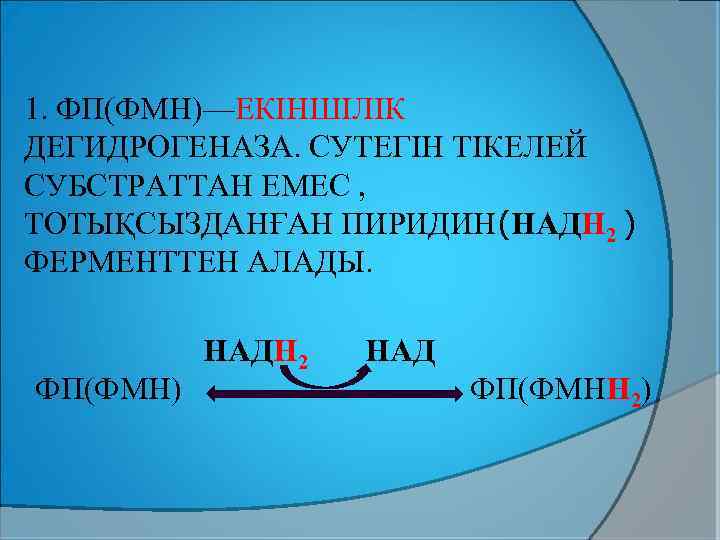 1. ФП(ФМН)—ЕКІНШІЛІК ДЕГИДРОГЕНАЗА. СУТЕГІН ТІКЕЛЕЙ СУБСТРАТТАН ЕМЕС , ТОТЫҚСЫЗДАНҒАН ПИРИДИН(НАДН 2 ) ФЕРМЕНТТЕН АЛАДЫ. ФП(ФМН) НАДН 2 НАД ФП(ФМНН 2)
1. ФП(ФМН)—ЕКІНШІЛІК ДЕГИДРОГЕНАЗА. СУТЕГІН ТІКЕЛЕЙ СУБСТРАТТАН ЕМЕС , ТОТЫҚСЫЗДАНҒАН ПИРИДИН(НАДН 2 ) ФЕРМЕНТТЕН АЛАДЫ. ФП(ФМН) НАДН 2 НАД ФП(ФМНН 2)
 СУБСТРАТТАН БӨЛІНГЕН СУТЕГІНІҢ БІР АТОМЫ ИЗОАЛЛОКСАЗИН САҚИНАСЫНДАҒЫ N— 1, АЛ, 2 - ші сутек N— 10 қосылады. НӘТИЖЕСІНДЕ ИЗОАЛЛОКСАЗИНДЕГІ— 1, 10 ОРЫНДАҒЫ ҚОС БАЙЛАНЫСТАР ҮЗІЛІП ОНЫҢ ОРНЫНА БІР ҚОС БАЙЛАНЫС ПАЙДА БОЛАДЫ. ФП ТОТЫҚСЫЗДАНАДЫ
СУБСТРАТТАН БӨЛІНГЕН СУТЕГІНІҢ БІР АТОМЫ ИЗОАЛЛОКСАЗИН САҚИНАСЫНДАҒЫ N— 1, АЛ, 2 - ші сутек N— 10 қосылады. НӘТИЖЕСІНДЕ ИЗОАЛЛОКСАЗИНДЕГІ— 1, 10 ОРЫНДАҒЫ ҚОС БАЙЛАНЫСТАР ҮЗІЛІП ОНЫҢ ОРНЫНА БІР ҚОС БАЙЛАНЫС ПАЙДА БОЛАДЫ. ФП ТОТЫҚСЫЗДАНАДЫ
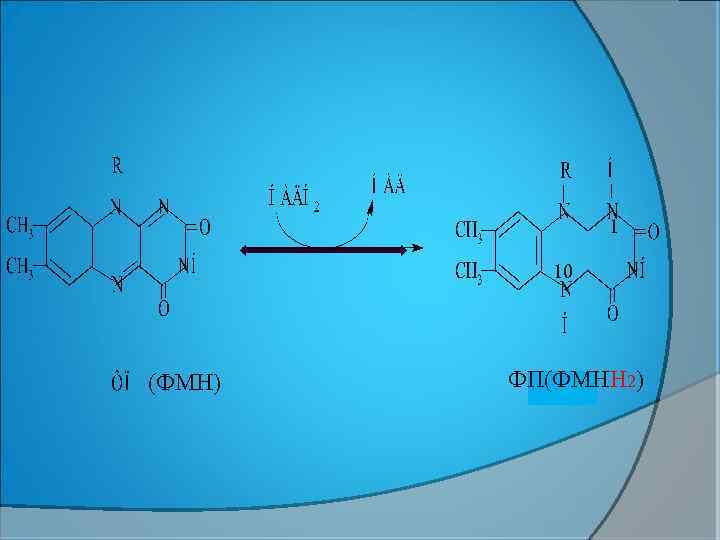 1 10 (ФМН) ФП(ФМНН 2)
1 10 (ФМН) ФП(ФМНН 2)
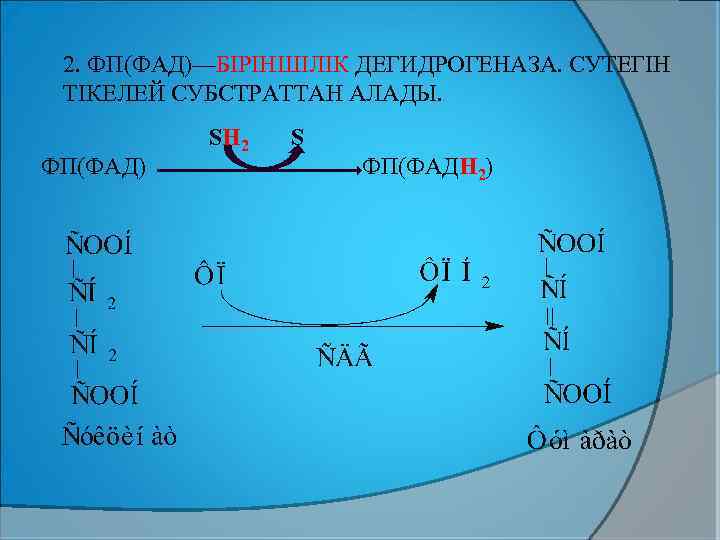 2. ФП(ФАД)—БІРІНШІЛІК ДЕГИДРОГЕНАЗА. СУТЕГІН ТІКЕЛЕЙ СУБСТРАТТАН АЛАДЫ. ФП(ФАД) SН 2 S ФП(ФАДН 2)
2. ФП(ФАД)—БІРІНШІЛІК ДЕГИДРОГЕНАЗА. СУТЕГІН ТІКЕЛЕЙ СУБСТРАТТАН АЛАДЫ. ФП(ФАД) SН 2 S ФП(ФАДН 2)
 ФП(ФАД) СУБСТРАТПЕН ТІКЕЛЕЙ ӘРЕКЕТТЕСІП 2 СУТЕГІН ҚОСЫП АЛЫП ТОТТЫҚҚАН САРЫ ТҮСТЕН ТОТЫҚСЫЗДАНҒАН ФП(ФАДН 2) ТҮССІЗ КҮЙГЕ ӨТЕДІ. СУБСТРАТ ТОТЫҒАДЫ.
ФП(ФАД) СУБСТРАТПЕН ТІКЕЛЕЙ ӘРЕКЕТТЕСІП 2 СУТЕГІН ҚОСЫП АЛЫП ТОТТЫҚҚАН САРЫ ТҮСТЕН ТОТЫҚСЫЗДАНҒАН ФП(ФАДН 2) ТҮССІЗ КҮЙГЕ ӨТЕДІ. СУБСТРАТ ТОТЫҒАДЫ.
 ФП(ФАДН 2) МЕН ФП(ФМНН 2) ӨЗІНДЕГІ СУТЕГІН Ко. Q-ға БЕРІП ТОТЫҒАДЫ. КЕЙДЕ ФПН 2 ТІКЕЛЕЙ ОТТЕКПЕН ТОТЫҒУЫ ДА МҮМКІН. ФПН 2 + О 2 ФП+ Н 2 О 2 Реакция дегидрлену емес оттекпен тотығу болғандықтан оларды оксидазалар деп атайды. М/лы, моноаминооксидаза МАО, диаминоксидаза, ксантиноксидаза т. б
ФП(ФАДН 2) МЕН ФП(ФМНН 2) ӨЗІНДЕГІ СУТЕГІН Ко. Q-ға БЕРІП ТОТЫҒАДЫ. КЕЙДЕ ФПН 2 ТІКЕЛЕЙ ОТТЕКПЕН ТОТЫҒУЫ ДА МҮМКІН. ФПН 2 + О 2 ФП+ Н 2 О 2 Реакция дегидрлену емес оттекпен тотығу болғандықтан оларды оксидазалар деп атайды. М/лы, моноаминооксидаза МАО, диаминоксидаза, ксантиноксидаза т. б
 • Убихинон(Ko. Q), Кофермент Q немесе убихинон Ол – изопреннің қалдығымен (10 молекуласы) байланысқан бензохинонның туындысы. Убихинонның апоферменті жоқ. Убихинонның формуласы:
• Убихинон(Ko. Q), Кофермент Q немесе убихинон Ол – изопреннің қалдығымен (10 молекуласы) байланысқан бензохинонның туындысы. Убихинонның апоферменті жоқ. Убихинонның формуласы:
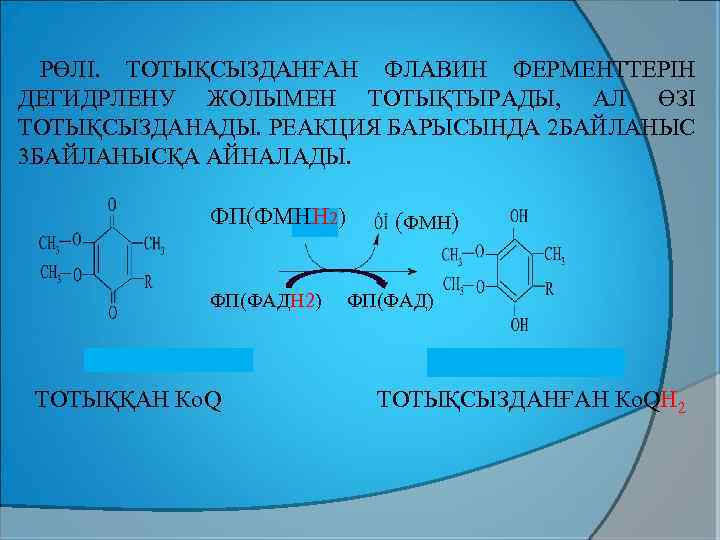 РӨЛІ. ТОТЫҚСЫЗДАНҒАН ФЛАВИН ФЕРМЕНТТЕРІН ДЕГИДРЛЕНУ ЖОЛЫМЕН ТОТЫҚТЫРАДЫ, АЛ ӨЗІ ТОТЫҚСЫЗДАНАДЫ. РЕАКЦИЯ БАРЫСЫНДА 2 БАЙЛАНЫС 3 БАЙЛАНЫСҚА АЙНАЛАДЫ. ФП(ФМНН 2) ФП(ФАДН 2) ТОТЫҚҚАН Ко. Q (ФМН) ФП(ФАД) ТОТЫҚСЫЗДАНҒАН Ко. QН 2
РӨЛІ. ТОТЫҚСЫЗДАНҒАН ФЛАВИН ФЕРМЕНТТЕРІН ДЕГИДРЛЕНУ ЖОЛЫМЕН ТОТЫҚТЫРАДЫ, АЛ ӨЗІ ТОТЫҚСЫЗДАНАДЫ. РЕАКЦИЯ БАРЫСЫНДА 2 БАЙЛАНЫС 3 БАЙЛАНЫСҚА АЙНАЛАДЫ. ФП(ФМНН 2) ФП(ФАДН 2) ТОТЫҚҚАН Ко. Q (ФМН) ФП(ФАД) ТОТЫҚСЫЗДАНҒАН Ко. QН 2
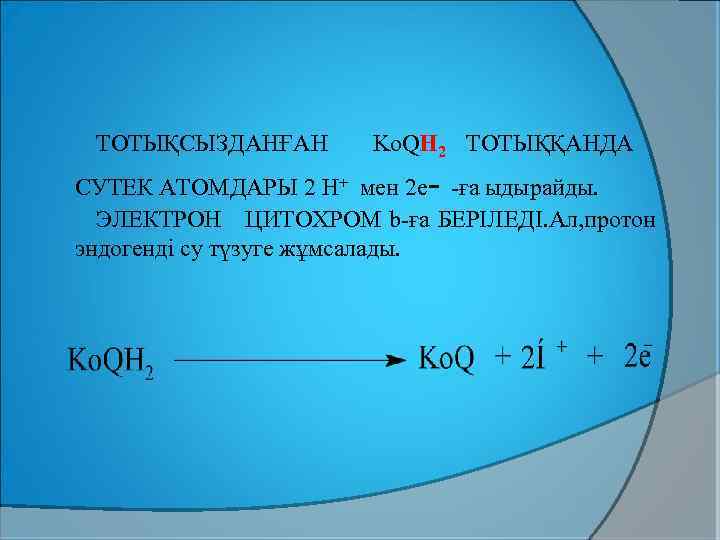 ТОТЫҚСЫЗДАНҒАН Ko. QН 2 ТОТЫҚҚАНДА - СУТЕК АТОМДАРЫ 2 Н+ мен 2 e -ға ыдырайды. ЭЛЕКТРОН ЦИТОХРОМ b-ға БЕРІЛЕДІ. Ал, протон эндогенді су түзуге жұмсалады.
ТОТЫҚСЫЗДАНҒАН Ko. QН 2 ТОТЫҚҚАНДА - СУТЕК АТОМДАРЫ 2 Н+ мен 2 e -ға ыдырайды. ЭЛЕКТРОН ЦИТОХРОМ b-ға БЕРІЛЕДІ. Ал, протон эндогенді су түзуге жұмсалады.
 ЦИТОХРОМДАР (Цх) Екі компонентті, коферменттері әртүрлі құрлыстағы гемдер. ЦХ-дар гемдерінің табиғатына байланысты 4 топқа бөлінеді: Бір топтағы ферменттердің апоферменттері әр түрлі, коферменттері бірдей
ЦИТОХРОМДАР (Цх) Екі компонентті, коферменттері әртүрлі құрлыстағы гемдер. ЦХ-дар гемдерінің табиғатына байланысты 4 топқа бөлінеді: Бір топтағы ферменттердің апоферменттері әр түрлі, коферменттері бірдей
 Цитохромдар электрондарды (e—) тасымалдау жолымен субстратты тотықтырады. Цх маңызы: e— тотықсызданған Ко. Q Н 2 ден ОТТЕККЕ тасымалдау. Ол кезде цх геміндегі Fе валенттігі өзгереді.
Цитохромдар электрондарды (e—) тасымалдау жолымен субстратты тотықтырады. Цх маңызы: e— тотықсызданған Ко. Q Н 2 ден ОТТЕККЕ тасымалдау. Ол кезде цх геміндегі Fе валенттігі өзгереді.
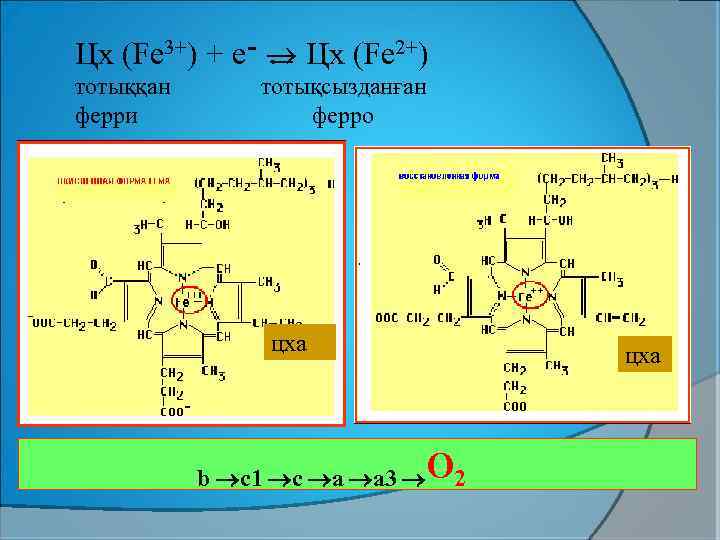 Цх (Fe 3+) + e ־ Цх (Fe 2+) тотыққан ферри тотықсызданған ферро цха b c 1 c a a 3 О 2 цха
Цх (Fe 3+) + e ־ Цх (Fe 2+) тотыққан ферри тотықсызданған ферро цха b c 1 c a a 3 О 2 цха
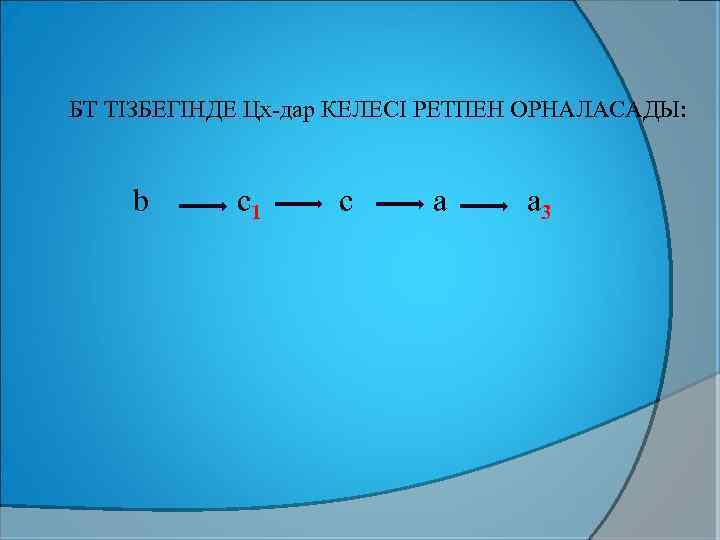 БТ ТІЗБЕГІНДЕ Цх-дар КЕЛЕСІ РЕТПЕН ОРНАЛАСАДЫ: b с1 c a a 3
БТ ТІЗБЕГІНДЕ Цх-дар КЕЛЕСІ РЕТПЕН ОРНАЛАСАДЫ: b с1 c a a 3
 Цитохром В Өкілдері: цхb және цхb 5. Цхb 5 ксенобиотиктердің метаболизміне қатысады, ал цхb БТ тізбегіне eтасымалдауға қатысады. цхb екі компонентті, коферменті гем. Рационалды аты: 1, 3, 5, 8 - тетраметил, -2, 4 -дивинил, 6, 7 - дипропион қышқылының темір порфині. Гемнің құрылысы гемоглобин мен миоглобиндікіндей.
Цитохром В Өкілдері: цхb және цхb 5. Цхb 5 ксенобиотиктердің метаболизміне қатысады, ал цхb БТ тізбегіне eтасымалдауға қатысады. цхb екі компонентті, коферменті гем. Рационалды аты: 1, 3, 5, 8 - тетраметил, -2, 4 -дивинил, 6, 7 - дипропион қышқылының темір порфині. Гемнің құрылысы гемоглобин мен миоглобиндікіндей.
 Цхb-ның рөлі e- тотықсызданған Ko. QН 2 ден алып цхс1 -ге береді. Ко. Q тотығады, цхb тотықсызданады. Ko. QН 2 2 цхb(Fe 3+) Ко. Q+ 2 H++ 2 е ־ 2 цхb(Fe 2+)
Цхb-ның рөлі e- тотықсызданған Ko. QН 2 ден алып цхс1 -ге береді. Ко. Q тотығады, цхb тотықсызданады. Ko. QН 2 2 цхb(Fe 3+) Ко. Q+ 2 H++ 2 е ־ 2 цхb(Fe 2+)
 Цитохром С Өкілдері: цхс ж/е цхс1 екі компонентті. Коферменттері бірдей, апоферменттері әртүрлі. Гемі: -1, 3, 5, 8 - тетраметил, -2, 4 -диэтил, -6, 7 - дипропион қышқылының темір порфині.
Цитохром С Өкілдері: цхс ж/е цхс1 екі компонентті. Коферменттері бірдей, апоферменттері әртүрлі. Гемі: -1, 3, 5, 8 - тетраметил, -2, 4 -диэтил, -6, 7 - дипропион қышқылының темір порфині.
 цхс1–дің рөлі: ферро цхb-ны тотықтырады, цхс -ні тотықсыздандырады: 2 e- цхс–нің рөлі: ферро цхс1 -ді тотықтырады, цхa-ні тотықсыздандырады: 2 e-
цхс1–дің рөлі: ферро цхb-ны тотықтырады, цхс -ні тотықсыздандырады: 2 e- цхс–нің рөлі: ферро цхс1 -ді тотықтырады, цхa-ні тотықсыздандырады: 2 e-
 Цитохром А Өкілдері: цха және цха 3. Коферменттері бірдей, апоферменттері әртүрлі. Гемі: С 1, С 3 , С 5 орындарда метил тобы, С 2 -15 көміртек атомдарынан тұратын радикал, С 4 -ші винил тобы, С 6 мен С 7 орындарда пропион қышқылының қалдықтары, С 8 -ші орында формил тобы орналасқан.
Цитохром А Өкілдері: цха және цха 3. Коферменттері бірдей, апоферменттері әртүрлі. Гемі: С 1, С 3 , С 5 орындарда метил тобы, С 2 -15 көміртек атомдарынан тұратын радикал, С 4 -ші винил тобы, С 6 мен С 7 орындарда пропион қышқылының қалдықтары, С 8 -ші орында формил тобы орналасқан.
 цха мен цха 3 цитохромоксидаза (ЦХО) комплексін түзеді. ол 2 цха+4 цха 3+6 Сu тұрады. ЦХО-дағы мыстың валентілігі ауыспалы, сондықтан электрон көзі бола алады.
цха мен цха 3 цитохромоксидаза (ЦХО) комплексін түзеді. ол 2 цха+4 цха 3+6 Сu тұрады. ЦХО-дағы мыстың валентілігі ауыспалы, сондықтан электрон көзі бола алады.
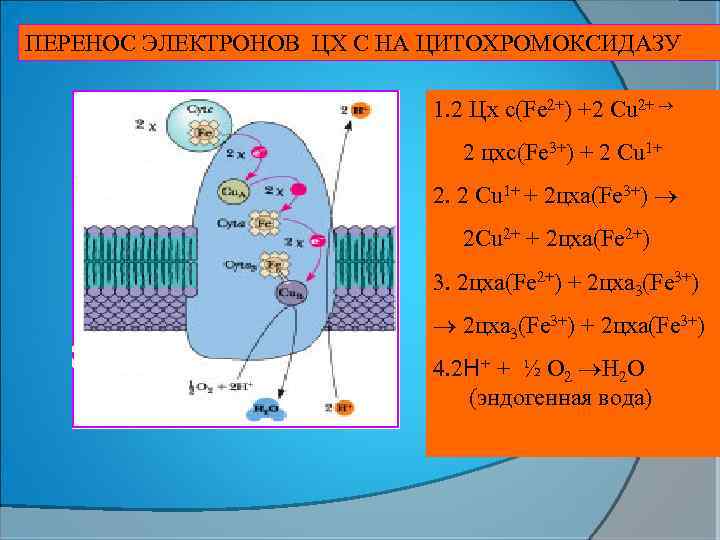 ПЕРЕНОС ЭЛЕКТРОНОВ ЦХ С НА ЦИТОХРОМОКСИДАЗУ 1. 2 Цх с(Fe 2+) +2 Cu 2+ 2 цхс(Fe 3+) + 2 Cu 1+ 2. 2 Cu 1+ + 2 цха(Fe 3+) 2 Сu 2+ + 2 цха(Fe 2+) 3. 2 цха(Fe 2+) + 2 цха 3(Fe 3+) + 2 цха(Fe 3+) 4. 2 Н+ + ½ O 2 H 2 O (эндогенная вода)
ПЕРЕНОС ЭЛЕКТРОНОВ ЦХ С НА ЦИТОХРОМОКСИДАЗУ 1. 2 Цх с(Fe 2+) +2 Cu 2+ 2 цхс(Fe 3+) + 2 Cu 1+ 2. 2 Cu 1+ + 2 цха(Fe 3+) 2 Сu 2+ + 2 цха(Fe 2+) 3. 2 цха(Fe 2+) + 2 цха 3(Fe 3+) + 2 цха(Fe 3+) 4. 2 Н+ + ½ O 2 H 2 O (эндогенная вода)
 Цитохромоксидаза(ЦХО) рөлі: цха ферро цхс- дан e-- ды алып цха 3 - КЕ тасымалдайды; ал цха 3 қосып алған электронды оттекке беріп оны Оттектің активті түріне айналдырады. Бір оттек атомын тотықсыздандыру үшін 2 e-, ал молекулалық О 2 иондау үшін 4 e- керек. Әр ионданған активті оттек Ko. QН 2 ТОТЫҚҚАНДА ЕРТІНДІДЕ ҚАЛҒАН ПРОТОНМЕН (Н+) ӘРЕКЕТТЕСІП ЭНДОГЕНДІ СУ ТҮЗЕДІ.
Цитохромоксидаза(ЦХО) рөлі: цха ферро цхс- дан e-- ды алып цха 3 - КЕ тасымалдайды; ал цха 3 қосып алған электронды оттекке беріп оны Оттектің активті түріне айналдырады. Бір оттек атомын тотықсыздандыру үшін 2 e-, ал молекулалық О 2 иондау үшін 4 e- керек. Әр ионданған активті оттек Ko. QН 2 ТОТЫҚҚАНДА ЕРТІНДІДЕ ҚАЛҒАН ПРОТОНМЕН (Н+) ӘРЕКЕТТЕСІП ЭНДОГЕНДІ СУ ТҮЗЕДІ.
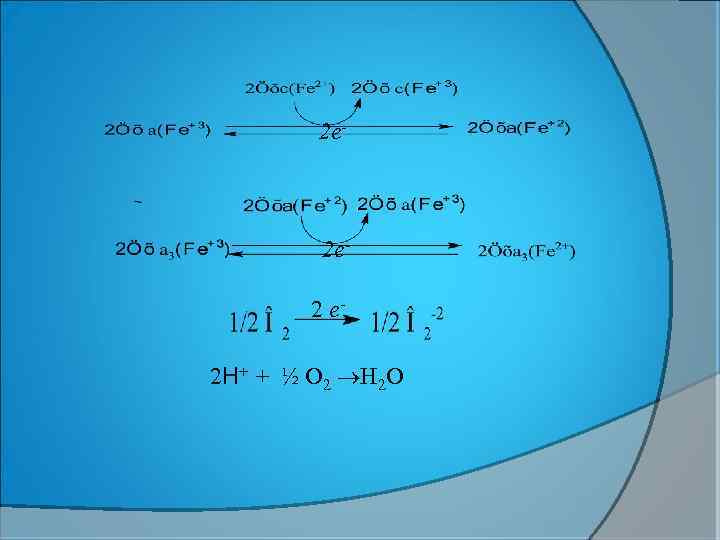 2 e- 2 e 2 e 2 Н+ + ½ O 2 H 2 O
2 e- 2 e 2 e 2 Н+ + ½ O 2 H 2 O
 Оксидоредуктаза ферменттерінің орналасу тәртібі олардың тотығутотықсыздану потенциалдарының(ТТП) өсуіне байланысты. ТТП жоғарысы өзінің алдындағы ферментті тотықтырады, кейінгісін тотықсыздандырады. SН 2 НАДН 2 ФПН 2 Ко. QН 2 b c 1 c a a 3 О 2
Оксидоредуктаза ферменттерінің орналасу тәртібі олардың тотығутотықсыздану потенциалдарының(ТТП) өсуіне байланысты. ТТП жоғарысы өзінің алдындағы ферментті тотықтырады, кейінгісін тотықсыздандырады. SН 2 НАДН 2 ФПН 2 Ко. QН 2 b c 1 c a a 3 О 2
 • Каталаза мен пероксидазалар. Каталаза мен пероксидаза БТ-ға тікелей қатыспайды. Каталаза 2 компонентті коферменті 4 гем , бірақ геміндегі Fe 3+. Қанда, сүйек кемігінде, шырышты қабаттардың мембранасында, бүйрек, бауырда кездеседі. Каталаза сутек пероксидін су мен молекулалық оттекке ыдыратады: 2 Н 2 О 2 2 Н 2 О + О 2 Каталаза жасушаларды пероксидтік тотығудан қорғайды. АКАТАЛАЗЕМИЯ
• Каталаза мен пероксидазалар. Каталаза мен пероксидаза БТ-ға тікелей қатыспайды. Каталаза 2 компонентті коферменті 4 гем , бірақ геміндегі Fe 3+. Қанда, сүйек кемігінде, шырышты қабаттардың мембранасында, бүйрек, бауырда кездеседі. Каталаза сутек пероксидін су мен молекулалық оттекке ыдыратады: 2 Н 2 О 2 2 Н 2 О + О 2 Каталаза жасушаларды пероксидтік тотығудан қорғайды. АКАТАЛАЗЕМИЯ
 Пероксидаза 2 компонентті коферменті бір гем. Пероксидаза өсімдіктерде, лейкоциттерде, тромбоциттерде, сүтте кездеседі. Пероксидаза сутек пероксидін су мен атомдық оттекке дейін ыдыратады: Н 2 О 2 Н 2 О + О Атомдық оттек өте күшті тотықтырғыштық қасиет көрсетеді. Бұл ферменттер ароматты қосылыстарды тотықтыруға қатысады Цхb, гемоглобин, миоглобин, каталаза, пероксидазанің гемдері бірдей.
Пероксидаза 2 компонентті коферменті бір гем. Пероксидаза өсімдіктерде, лейкоциттерде, тромбоциттерде, сүтте кездеседі. Пероксидаза сутек пероксидін су мен атомдық оттекке дейін ыдыратады: Н 2 О 2 Н 2 О + О Атомдық оттек өте күшті тотықтырғыштық қасиет көрсетеді. Бұл ферменттер ароматты қосылыстарды тотықтыруға қатысады Цхb, гемоглобин, миоглобин, каталаза, пероксидазанің гемдері бірдей.
 ОКСИГЕНАЗАЛАР Стероидтар, ксенобиотиктер және басқа да циклді қосылыстардың алмасуында маңызды рөл атқарады. Екі компонентті, коферментінің құрамында С витамині бар ферменттер. ОКСИГЕНАЗАЛАР: монооксигеназалар мен диоксигеназалар. Олар оттегін субстратқа қосушы ферменттер депте аталады. Диоксигеназалар молекулалық оттектің 2 атомын субстратқа тікелей қосады: R + О 2 → RО 2
ОКСИГЕНАЗАЛАР Стероидтар, ксенобиотиктер және басқа да циклді қосылыстардың алмасуында маңызды рөл атқарады. Екі компонентті, коферментінің құрамында С витамині бар ферменттер. ОКСИГЕНАЗАЛАР: монооксигеназалар мен диоксигеназалар. Олар оттегін субстратқа қосушы ферменттер депте аталады. Диоксигеназалар молекулалық оттектің 2 атомын субстратқа тікелей қосады: R + О 2 → RО 2
 Монооксигеназалар ( гидроксилазалар) молекулалық оттектің 1 атомын ғана субстратқа қосады, ал екінші оттек атомы суға дейін тотықсызданады. Сутегінің доноры рөлін НАДФН 2 атқарады. RH + O 2 + HADФН 2 → ROH + Н 2 О + НАДФ+ Ксенобиотиктерді зиянсыздандырудың бірінші сатысына монооксигеназа қатысады. Гидроксилазалар холестерин мен адреналиннің, стероидты гормондардың синтезіне де қатысады. Бұл ферменттер цитоплазмада, эндоплазмалық ретикулм жүйесінде, митохондрияларда және микросомаларда кездеседі.
Монооксигеназалар ( гидроксилазалар) молекулалық оттектің 1 атомын ғана субстратқа қосады, ал екінші оттек атомы суға дейін тотықсызданады. Сутегінің доноры рөлін НАДФН 2 атқарады. RH + O 2 + HADФН 2 → ROH + Н 2 О + НАДФ+ Ксенобиотиктерді зиянсыздандырудың бірінші сатысына монооксигеназа қатысады. Гидроксилазалар холестерин мен адреналиннің, стероидты гормондардың синтезіне де қатысады. Бұл ферменттер цитоплазмада, эндоплазмалық ретикулм жүйесінде, митохондрияларда және микросомаларда кездеседі.


