гот.pptm [Автосохраненный].pptx
- Количество слайдов: 24
 Оксидлашу – кайтарылу реакцияләре Химия, 11 класс
Оксидлашу – кайтарылу реакцияләре Химия, 11 класс
 Дәреснең максаты: Атомнарның оксидлашу дәрәҗәләре үзгәрүне анализлау Оксидлашу-кай тарылу реакцияләрендә оксидлаштыручыны һәм кайтаручыны ачыклау. Оксидлашу-кайтарылу реакцияләрен төзегәндә электрон баланс методы буенча коэффициентлар кую.
Дәреснең максаты: Атомнарның оксидлашу дәрәҗәләре үзгәрүне анализлау Оксидлашу-кай тарылу реакцияләрендә оксидлаштыручыны һәм кайтаручыны ачыклау. Оксидлашу-кайтарылу реакцияләрен төзегәндә электрон баланс методы буенча коэффициентлар кую.
 1. Ca. CO 3 → Ca. O + CO 2 2. KCIO 3 + P → P 2 O 5 +KCI 3. H 2 SO 4 +Ba. CI 2 → Ba. SO 4 + HCI
1. Ca. CO 3 → Ca. O + CO 2 2. KCIO 3 + P → P 2 O 5 +KCI 3. H 2 SO 4 +Ba. CI 2 → Ba. SO 4 + HCI
 Установите соответствие между схемой реакции и степенью окисления восстановителя Схема реакции -3 + - +2 +2 0 0 + -2 + А) N H 4 CI +Cu. O →N 2 +Cu +H 2 O +HCI -3 + 0 0 Б) N 2 +H 2 → N H 3 Степень окисления 1. 2. 3 Б 4. 6 2 +5 5. В -3 +4 6. А +2 3. +2 -2 0 +4 -2 В) N O +O 2 → N O 2 + -2 + + +5 -2 ++3 -2 +4 -2 Г) N O 2 +Na. O H →Na N O 3 +Na. N O 2 +3 0 Г 5
Установите соответствие между схемой реакции и степенью окисления восстановителя Схема реакции -3 + - +2 +2 0 0 + -2 + А) N H 4 CI +Cu. O →N 2 +Cu +H 2 O +HCI -3 + 0 0 Б) N 2 +H 2 → N H 3 Степень окисления 1. 2. 3 Б 4. 6 2 +5 5. В -3 +4 6. А +2 3. +2 -2 0 +4 -2 В) N O +O 2 → N O 2 + -2 + + +5 -2 ++3 -2 +4 -2 Г) N O 2 +Na. O H →Na N O 3 +Na. N O 2 +3 0 Г 5
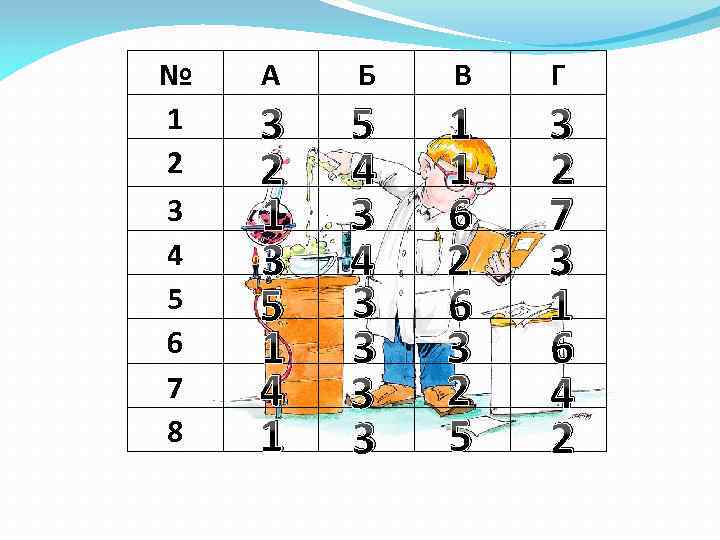 № 1 2 3 4 5 6 7 8 A Б В Г 3 2 1 3 5 1 4 1 5 4 3 3 3 3 1 1 6 2 6 3 2 5 3 2 7 3 1 6 4 2
№ 1 2 3 4 5 6 7 8 A Б В Г 3 2 1 3 5 1 4 1 5 4 3 3 3 3 1 1 6 2 6 3 2 5 3 2 7 3 1 6 4 2
 Оксидлашу – кайтарылу реакцияләен ахыргача язу кагыйдәләре ЮОД –югары оксидлашу дәрәҗәсе ТОД – тубэн оксидлашу дәрәҗәсе АОД – арадаш оксидлашу дәрәҗәсе ЮОД – төркем саны белән билгеләнә. Эгэр элемент атомы ЮОД дә икән, ул бары тик оксидлаштыручы гына була. Эгэр элемент атомы ТОД да икән, ул бары тик кайтаручы гына була. Мәсәлән, ЮОД (N)+5, ТОД (N)-3. -3< АОД (N)<+5. Эгэр элемент атомы АОД да икән, реакция шартына карап, ул я оксидлаштыручы, я кайтаручы булла.
Оксидлашу – кайтарылу реакцияләен ахыргача язу кагыйдәләре ЮОД –югары оксидлашу дәрәҗәсе ТОД – тубэн оксидлашу дәрәҗәсе АОД – арадаш оксидлашу дәрәҗәсе ЮОД – төркем саны белән билгеләнә. Эгэр элемент атомы ЮОД дә икән, ул бары тик оксидлаштыручы гына була. Эгэр элемент атомы ТОД да икән, ул бары тик кайтаручы гына була. Мәсәлән, ЮОД (N)+5, ТОД (N)-3. -3< АОД (N)<+5. Эгэр элемент атомы АОД да икән, реакция шартына карап, ул я оксидлаштыручы, я кайтаручы булла.
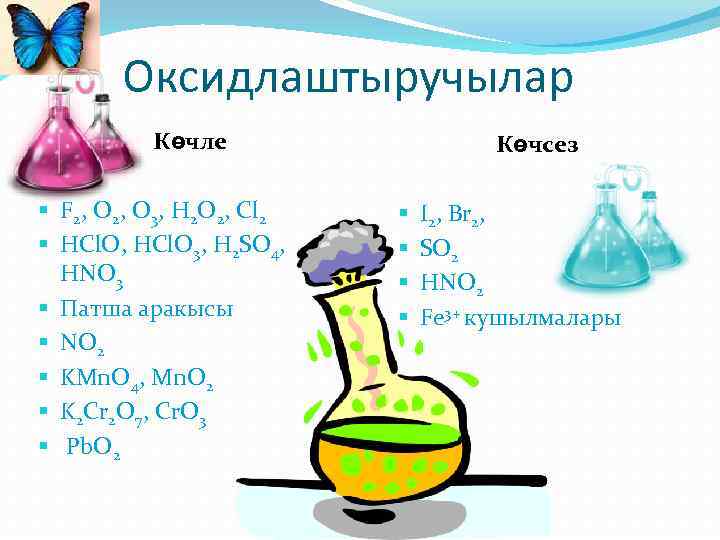 Оксидлаштыручылар Көчле § F 2, O 3, H 2 O 2, Cl 2 § HCl. O, HCl. O 3, H 2 SO 4, HNO 3 § Патша аракысы § NO 2 § KMn. O 4, Mn. O 2 § K 2 Cr 2 O 7, Cr. O 3 § Pb. O 2 Көчсез § § I 2, Br 2, SO 2 HNO 2 Fe 3+ кушылмалары
Оксидлаштыручылар Көчле § F 2, O 3, H 2 O 2, Cl 2 § HCl. O, HCl. O 3, H 2 SO 4, HNO 3 § Патша аракысы § NO 2 § KMn. O 4, Mn. O 2 § K 2 Cr 2 O 7, Cr. O 3 § Pb. O 2 Көчсез § § I 2, Br 2, SO 2 HNO 2 Fe 3+ кушылмалары
 Кайтаручылар § § § § Көчле Селтеле металлар Mg, Al, H 2 HI и йодидлар HBr и бромидлар H 2 S и сульфидлар NH 3, PH 3, H 3 PO 3 C, CO Fe 2+, Cr 2+ кушылмалары § § § Көчсез металлар(Pb, Cu, Ag, Hg) HCl SO 2 HNO 2 Альдегидлар, спиртлар, кырмыска кислотасы, кузгалак кислота, глюкоза
Кайтаручылар § § § § Көчле Селтеле металлар Mg, Al, H 2 HI и йодидлар HBr и бромидлар H 2 S и сульфидлар NH 3, PH 3, H 3 PO 3 C, CO Fe 2+, Cr 2+ кушылмалары § § § Көчсез металлар(Pb, Cu, Ag, Hg) HCl SO 2 HNO 2 Альдегидлар, спиртлар, кырмыска кислотасы, кузгалак кислота, глюкоза
 Оксидлашу – кайтарылу реакцияләре тигеләмәләрен төзү Электрон баланс методы Ионлы-электронлы баланс методы (метод полуреакций)
Оксидлашу – кайтарылу реакцияләре тигеләмәләрен төзү Электрон баланс методы Ионлы-электронлы баланс методы (метод полуреакций)
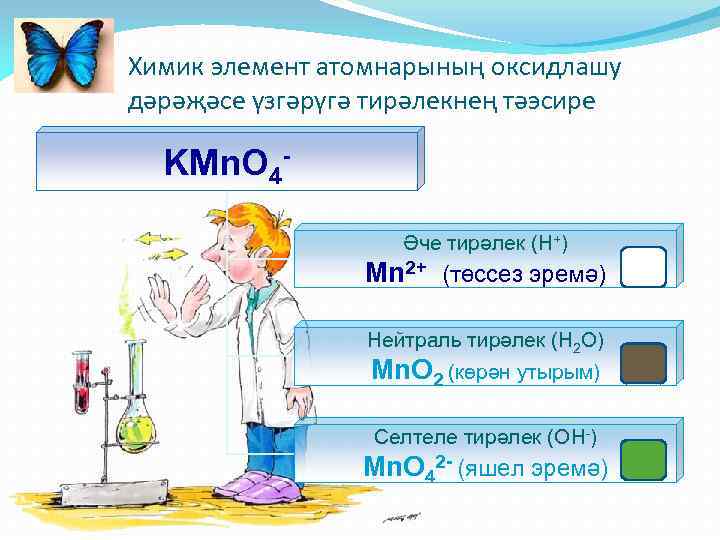 Химик элемент атомнарының оксидлашу дәрәҗәсе үзгәрүгә тирәлекнең тәэсире KMn. O 4Әче тирәлек (Н+) Mn 2+ (төссез эремә) Нейтраль тирәлек (Н 2 О) Mn. O 2 (көрән утырым) Селтеле тирәлек (ОН-) Mn. O 42 - (яшел эремә)
Химик элемент атомнарының оксидлашу дәрәҗәсе үзгәрүгә тирәлекнең тәэсире KMn. O 4Әче тирәлек (Н+) Mn 2+ (төссез эремә) Нейтраль тирәлек (Н 2 О) Mn. O 2 (көрән утырым) Селтеле тирәлек (ОН-) Mn. O 42 - (яшел эремә)
 Калий перманганатының әче тирәлектә кайтарылуы KMn. O 4 + KI + H 2 SO 4 Mn+7 + 5 e 2 I-1 - 2 e- Mn. SO 4 + I 2 + K 2 SO 4 + H 2 O Mn+2 2 кайтарыла оксидлаштыручы I 20 5 оксидлаша кайтаручы Молекуляр тигезләмә: KMn. O 4 + KI + H 2 SO 4 = Mn. SO 4 + I 2+ K 2 SO 4+ H 2 O
Калий перманганатының әче тирәлектә кайтарылуы KMn. O 4 + KI + H 2 SO 4 Mn+7 + 5 e 2 I-1 - 2 e- Mn. SO 4 + I 2 + K 2 SO 4 + H 2 O Mn+2 2 кайтарыла оксидлаштыручы I 20 5 оксидлаша кайтаручы Молекуляр тигезләмә: KMn. O 4 + KI + H 2 SO 4 = Mn. SO 4 + I 2+ K 2 SO 4+ H 2 O
 Калий перманганатының нейтраль тирәлектә кайтарылуы KMn. O 4 + K 2 SO 3 + H 2 O Mn. O 2 + K 2 SO 4 + KOH Mn+7 + 3 e- Mn+4 2 кайтарыла оксидлаштыручы S+4 – 2 e- S+6 оксидлаша кайтаручы 3 Молекуляр тигезләмә: KMn. O 4 + K 2 SO 3 + H 2 O = K 2 SO 4 + Mn. O 2 + KOH
Калий перманганатының нейтраль тирәлектә кайтарылуы KMn. O 4 + K 2 SO 3 + H 2 O Mn. O 2 + K 2 SO 4 + KOH Mn+7 + 3 e- Mn+4 2 кайтарыла оксидлаштыручы S+4 – 2 e- S+6 оксидлаша кайтаручы 3 Молекуляр тигезләмә: KMn. O 4 + K 2 SO 3 + H 2 O = K 2 SO 4 + Mn. O 2 + KOH
 Калий перманганатының селтеле тирәлектә кайтарылуы KMn. O 4 + K 2 SO 3 + KOH K 2 Mn. O 4 + K 2 SO 4 +H 2 O Mn+7 +1 e- Mn+6 2 кайтарыла оксидлаштыручы S+4 -2 e- S+6 1 оксидлаша кайтаручы Молекуляр тигезләмә: KMn. O 4 + K 2 SO 3 + KOH = K 2 Mn. O 4 + K 2 SO 4 + H 2 O
Калий перманганатының селтеле тирәлектә кайтарылуы KMn. O 4 + K 2 SO 3 + KOH K 2 Mn. O 4 + K 2 SO 4 +H 2 O Mn+7 +1 e- Mn+6 2 кайтарыла оксидлаштыручы S+4 -2 e- S+6 1 оксидлаша кайтаручы Молекуляр тигезләмә: KMn. O 4 + K 2 SO 3 + KOH = K 2 Mn. O 4 + K 2 SO 4 + H 2 O
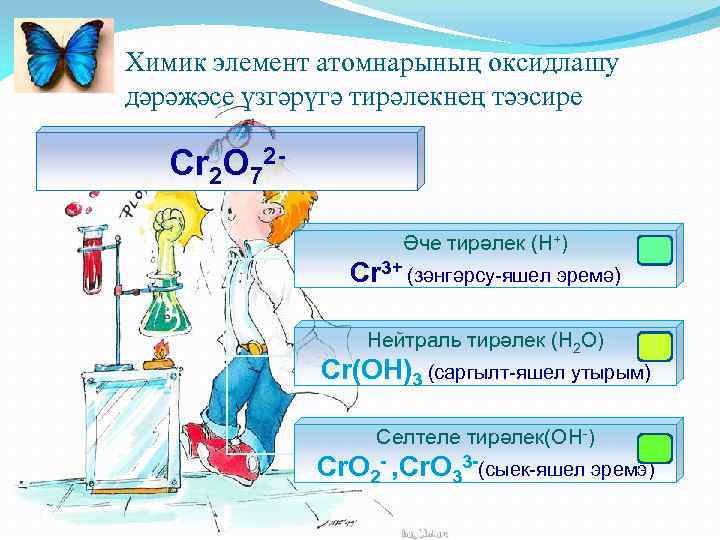 Химик элемент атомнарының оксидлашу дәрәҗәсе үзгәрүгә тирәлекнең тәэсире Cr 2 O 72Әче тирәлек (Н+) Cr 3+ (зәнгәрсу-яшел эремә) Нейтраль тирәлек (Н 2 О) Cr(OH)3 (саргылт-яшел утырым) Селтеле тирәлек(ОН-) Cr. O 2 - , Cr. O 33 -(сыек-яшел эремэ)
Химик элемент атомнарының оксидлашу дәрәҗәсе үзгәрүгә тирәлекнең тәэсире Cr 2 O 72Әче тирәлек (Н+) Cr 3+ (зәнгәрсу-яшел эремә) Нейтраль тирәлек (Н 2 О) Cr(OH)3 (саргылт-яшел утырым) Селтеле тирәлек(ОН-) Cr. O 2 - , Cr. O 33 -(сыек-яшел эремэ)
 Калий дихроматының әче тирәлектә кайтарылуы K 2 Cr 2 O 7 + Fe. SO 4 +H 2 SO 4 Fe 2(SO 4)3 + K 2 SO 4 + Cr 2(SO 4)3 + H 2 O 2 Cr+6 + 6 e Cr+32 1 кайтарыла оксидлаштыручы Fe+2 Fe+3 кайтаручы -1 e 6 оксидлаша Молекуляр тигезләмә: K 2 Cr 2 O 7 + Fe. SO 4+ H 2 SO 4 → Fe 2(SO 4)3 +K 2 SO 4+Cr 2(SO 4)3+ H 2 O
Калий дихроматының әче тирәлектә кайтарылуы K 2 Cr 2 O 7 + Fe. SO 4 +H 2 SO 4 Fe 2(SO 4)3 + K 2 SO 4 + Cr 2(SO 4)3 + H 2 O 2 Cr+6 + 6 e Cr+32 1 кайтарыла оксидлаштыручы Fe+2 Fe+3 кайтаручы -1 e 6 оксидлаша Молекуляр тигезләмә: K 2 Cr 2 O 7 + Fe. SO 4+ H 2 SO 4 → Fe 2(SO 4)3 +K 2 SO 4+Cr 2(SO 4)3+ H 2 O
 Хром селтеле тирәлектә оксидлаша KCr O 2 + Br 2 +KOH Cr+3 -3 e Cr+6 Br 02 +2 e 2 Br- K 2 Cr. O 4 + KBr + H 2 O 2 оксидлаша 3 кайтарыла кайтаручы оксидлаштыручы Молекуляр тигезләмә: KCr. O 2 + Br 2 + KOH → K 2 Cr. O 4 + KBr+ H 2 O
Хром селтеле тирәлектә оксидлаша KCr O 2 + Br 2 +KOH Cr+3 -3 e Cr+6 Br 02 +2 e 2 Br- K 2 Cr. O 4 + KBr + H 2 O 2 оксидлаша 3 кайтарыла кайтаручы оксидлаштыручы Молекуляр тигезләмә: KCr. O 2 + Br 2 + KOH → K 2 Cr. O 4 + KBr+ H 2 O
 Калий хроматының нейтраль тирәлектә кайтарылуы K 2 Cr. O 4 +H 2 S +H 2 O Cr+6 +3 e S-2 -2 e Cr+3 2 S 0 3 Cr(OH)3 +S +KOH кайтарыла оксидлаштыручы оксидлаша кайтаручы Молекуляр тигезләмә: K 2 Cr. O 4 + H 2 S + H 2 O → Cr(OH)3 + S + KOH
Калий хроматының нейтраль тирәлектә кайтарылуы K 2 Cr. O 4 +H 2 S +H 2 O Cr+6 +3 e S-2 -2 e Cr+3 2 S 0 3 Cr(OH)3 +S +KOH кайтарыла оксидлаштыручы оксидлаша кайтаручы Молекуляр тигезләмә: K 2 Cr. O 4 + H 2 S + H 2 O → Cr(OH)3 + S + KOH
 Галогеннарнын кислородлы кислоталары һәм аларның тозлары галогеноводородларга яки металл галогенидларына кадәр кайтарыла. KCIO 3 +KOH +Mn. O 2 CI+5 +6 e Mn+4 -2 e CIMn+6 K 2 Mn. O 4 + KCI +H 2 O 1 кайтарыла оксидлаштыручы 3 оксидлаша кайтаручы Молекуляр тигезләмә: KCIO 3 + KOH+ Mn. O 2 → K 2 Mn. O 4 + KCI + H 2 O
Галогеннарнын кислородлы кислоталары һәм аларның тозлары галогеноводородларга яки металл галогенидларына кадәр кайтарыла. KCIO 3 +KOH +Mn. O 2 CI+5 +6 e Mn+4 -2 e CIMn+6 K 2 Mn. O 4 + KCI +H 2 O 1 кайтарыла оксидлаштыручы 3 оксидлаша кайтаручы Молекуляр тигезләмә: KCIO 3 + KOH+ Mn. O 2 → K 2 Mn. O 4 + KCI + H 2 O
 Галогенид – ионнар (CI-, Br-, I-) һәрвакыт кайтаручылар гына була, һәм алар галогенга кадәр оксидлаша HBr+H 2 SO 4 2 Br- -2 e S+6 +2 e Br 02 S+4 Br 2 +SO 2 + H 2 O оксидлаша кайтаручы кайтарыла оксидлаштыручы Молекуляр тигезләмә: HBr +H 2 SO 4 → Br 2 +SO 2+ H 2 O
Галогенид – ионнар (CI-, Br-, I-) һәрвакыт кайтаручылар гына була, һәм алар галогенга кадәр оксидлаша HBr+H 2 SO 4 2 Br- -2 e S+6 +2 e Br 02 S+4 Br 2 +SO 2 + H 2 O оксидлаша кайтаручы кайтарыла оксидлаштыручы Молекуляр тигезләмә: HBr +H 2 SO 4 → Br 2 +SO 2+ H 2 O
 Pb. S + H 2 O 2 → Pb. SO 4 +H 2 O S-2 S+6 1 оксидлаша кайтаручы -8 e O 2 -1 +2 e 2 O-2 4 кайтарыла оксидлаштыручы Молекуляр тигезләмә: Pb. S + H 2 O 2 → Pb. SO 4+ H 2 O
Pb. S + H 2 O 2 → Pb. SO 4 +H 2 O S-2 S+6 1 оксидлаша кайтаручы -8 e O 2 -1 +2 e 2 O-2 4 кайтарыла оксидлаштыручы Молекуляр тигезләмә: Pb. S + H 2 O 2 → Pb. SO 4+ H 2 O
 KMn O 4 +H 2 O 2 +H 2 SO 4 → Mn SO 4 +K 2 SO 4 +O 2 + H 2 O Mn+7 +5 e Mn+2 2 кайтарыла оксидлаштыручы 2 O-1 -2 e O 0 2 5 оксидлаша кайтаручы Молекуляр тигезләмә: KMn. O 4 + H 2 O 2 + H 2 SO 4 → Mn. SO 4 +K 2 SO 4 + O 2 + H 2 O
KMn O 4 +H 2 O 2 +H 2 SO 4 → Mn SO 4 +K 2 SO 4 +O 2 + H 2 O Mn+7 +5 e Mn+2 2 кайтарыла оксидлаштыручы 2 O-1 -2 e O 0 2 5 оксидлаша кайтаручы Молекуляр тигезләмә: KMn. O 4 + H 2 O 2 + H 2 SO 4 → Mn. SO 4 +K 2 SO 4 + O 2 + H 2 O
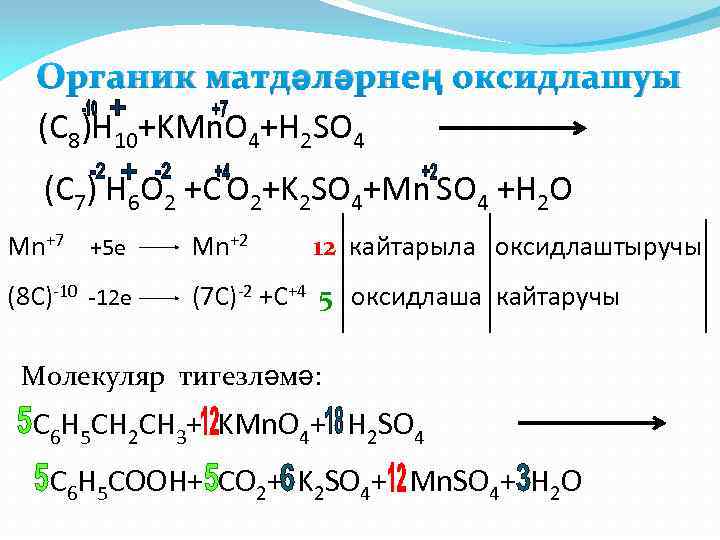 Органик матдәләрнең оксидлашуы (C 8)H 10+KMn. O 4+H 2 SO 4 (C 7) H 6 O 2 +C O 2+K 2 SO 4+Mn SO 4 +H 2 O Mn+7 +5 e Mn+2 12 кайтарыла оксидлаштыручы (8 C)-10 -12 e (7 C)-2 +C+4 5 оксидлаша кайтаручы Молекуляр тигезләмә: C 6 H 5 CH 2 CH 3+ KMn. O 4+ H 2 SO 4 C 6 H 5 COOH+ CO 2+ K 2 SO 4+ Mn. SO 4+ H 2 O
Органик матдәләрнең оксидлашуы (C 8)H 10+KMn. O 4+H 2 SO 4 (C 7) H 6 O 2 +C O 2+K 2 SO 4+Mn SO 4 +H 2 O Mn+7 +5 e Mn+2 12 кайтарыла оксидлаштыручы (8 C)-10 -12 e (7 C)-2 +C+4 5 оксидлаша кайтаручы Молекуляр тигезләмә: C 6 H 5 CH 2 CH 3+ KMn. O 4+ H 2 SO 4 C 6 H 5 COOH+ CO 2+ K 2 SO 4+ Mn. SO 4+ H 2 O
 C 2 H 5 OH +K 2 Cr 2 O 7 + H 2 SO 4 → ?
C 2 H 5 OH +K 2 Cr 2 O 7 + H 2 SO 4 → ?
 Өйгә эш Cr 2 O 3 + KNO 3 + KOH → ?
Өйгә эш Cr 2 O 3 + KNO 3 + KOH → ?


