Окончание предыдущей 11 лекции: Патология транспорта липидов кровью











































































Лекция 12 катаболизм липидов 2012.ppt
- Количество слайдов: 123
 Окончание предыдущей 11 лекции: Патология транспорта липидов кровью 2011 1
Окончание предыдущей 11 лекции: Патология транспорта липидов кровью 2011 1
 Патология поступления, переваривания, всасывания и транспорта липидов кровью • Гиперлипидемия (…) • Гиполипидемия (…) • Дислипидемия (…) • Виды
Патология поступления, переваривания, всасывания и транспорта липидов кровью • Гиперлипидемия (…) • Гиполипидемия (…) • Дислипидемия (…) • Виды
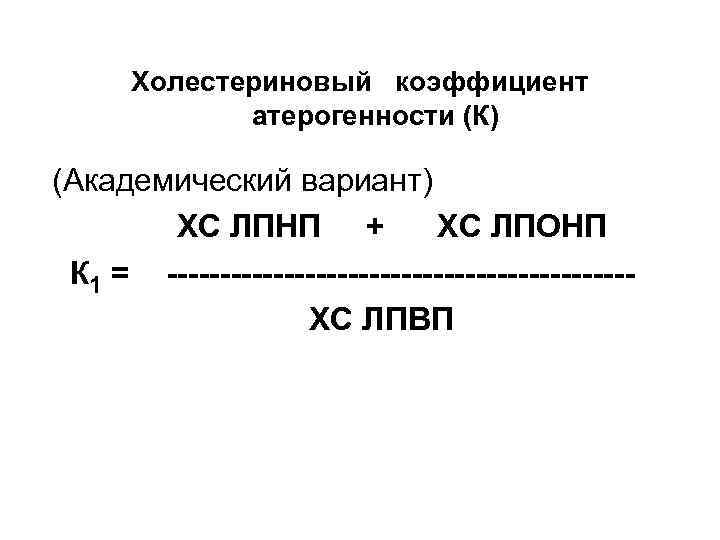
 Холестериновый коэффициент атерогенности (К) (Академический вариант) ХС ЛПНП + ХС ЛПОНП К 1 = ---------------------- ХС ЛПВП
Холестериновый коэффициент атерогенности (К) (Академический вариант) ХС ЛПНП + ХС ЛПОНП К 1 = ---------------------- ХС ЛПВП
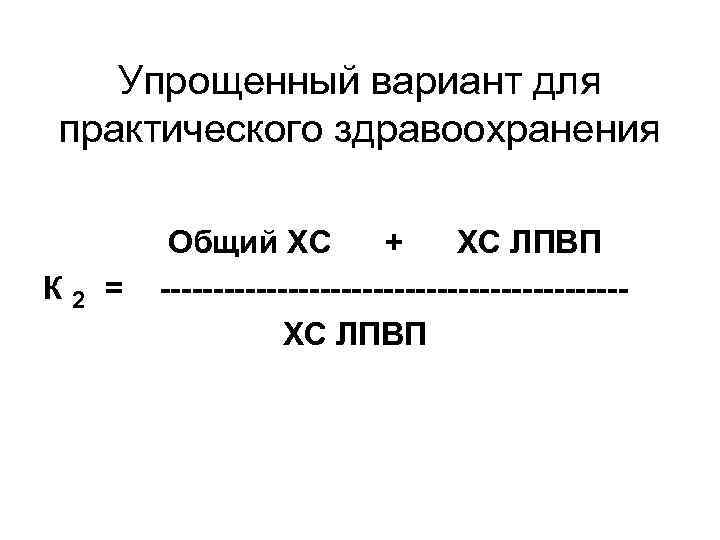
 Упрощенный вариант для практического здравоохранения Общий ХС + ХС ЛПВП К 2 = ---------------------- ХС ЛПВП
Упрощенный вариант для практического здравоохранения Общий ХС + ХС ЛПВП К 2 = ---------------------- ХС ЛПВП
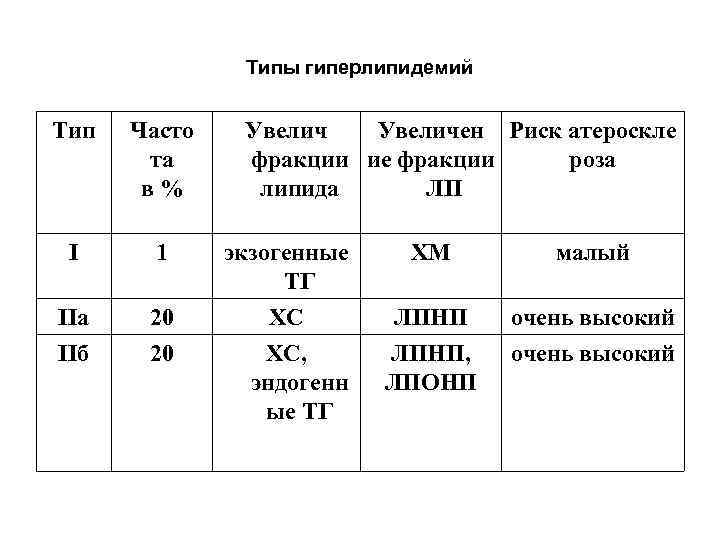
 Типы гиперлипидемий Тип Часто Увеличен Риск атероскле та фракции ие фракции роза в% липида ЛП I 1 экзогенные ХМ малый ТГ IIа 20 ХС ЛПНП очень высокий IIб 20 ХС, ЛПНП, очень высокий эндогенн ЛПОНП ые ТГ
Типы гиперлипидемий Тип Часто Увеличен Риск атероскле та фракции ие фракции роза в% липида ЛП I 1 экзогенные ХМ малый ТГ IIа 20 ХС ЛПНП очень высокий IIб 20 ХС, ЛПНП, очень высокий эндогенн ЛПОНП ые ТГ
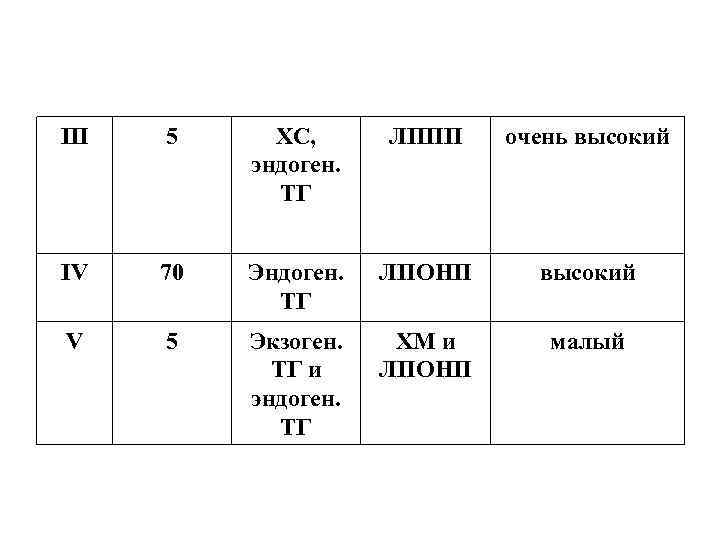
 III 5 ХС, ЛППП очень высокий эндоген. ТГ IV 70 Эндоген. ЛПОНП высокий ТГ V 5 Экзоген. ХМ и малый ТГ и ЛПОНП эндоген. ТГ
III 5 ХС, ЛППП очень высокий эндоген. ТГ IV 70 Эндоген. ЛПОНП высокий ТГ V 5 Экзоген. ХМ и малый ТГ и ЛПОНП эндоген. ТГ
 КАТАБОЛИЗМ ЛИПИДОВ ЖИРОВОЙ ТКАНИ Лектор зав. каф. биохимии доктор медицинских наук, профессор Мещанинов Виктор Николаевич Факультеты: лечебно-профилактический, педиатрический. 2 курс ЛЕКЦИЯ 12 ГБОУ ВПО УГМА РОСЗДРАВА КАФЕДРА БИОХИМИИ 2012
КАТАБОЛИЗМ ЛИПИДОВ ЖИРОВОЙ ТКАНИ Лектор зав. каф. биохимии доктор медицинских наук, профессор Мещанинов Виктор Николаевич Факультеты: лечебно-профилактический, педиатрический. 2 курс ЛЕКЦИЯ 12 ГБОУ ВПО УГМА РОСЗДРАВА КАФЕДРА БИОХИМИИ 2012
 ПЛАН ЛЕКЦИИ • Жировая ткань – белая и бурая: количество, локализация, особенности химического состава, метаболизма белкового, жирового, углеводного и энергетического обмена, функции. • Липолиз и липогенез: реакции, регуляция, значение. • β-окисление жирных кислот: насыщенных, ненасыщенных, с нечетным количеством атомов углерода (история вопроса, механизмы). Этапы реакции, регуляция, энергетический баланс.
ПЛАН ЛЕКЦИИ • Жировая ткань – белая и бурая: количество, локализация, особенности химического состава, метаболизма белкового, жирового, углеводного и энергетического обмена, функции. • Липолиз и липогенез: реакции, регуляция, значение. • β-окисление жирных кислот: насыщенных, ненасыщенных, с нечетным количеством атомов углерода (история вопроса, механизмы). Этапы реакции, регуляция, энергетический баланс.
 • Схема окисления ТГ до воды и углекислого газа. Энергетический баланс. Взаимосвязь окисления ТГ с обменом углеводов. • ПОЛ. Роль в физиологии и патологии клетки. Реакции образования диагностируемых продуктов ПОЛ. АОЗ: ферментативная и неферментативная (повторить). Синдром липидной пероксидации.
• Схема окисления ТГ до воды и углекислого газа. Энергетический баланс. Взаимосвязь окисления ТГ с обменом углеводов. • ПОЛ. Роль в физиологии и патологии клетки. Реакции образования диагностируемых продуктов ПОЛ. АОЗ: ферментативная и неферментативная (повторить). Синдром липидной пероксидации.
 Белая жировая ткань • Основные жировые отложения имеются под кожей (в подкожножировой клетчатке), и вокруг внутренних органов, преимущественно в области живота (висцеральный жир).
Белая жировая ткань • Основные жировые отложения имеются под кожей (в подкожножировой клетчатке), и вокруг внутренних органов, преимущественно в области живота (висцеральный жир).
 функции • Синтез липидов из углеводов • запасающая (95% ТГ в жировой ткани, 5% - во внутренних органах и костях); • теплоизоляционная; • механическая защита органов и тканей; • эндокринная (секреция: лептина, эстрогенов, ангиотензиногена, интерлейкина-6, ФНО-α);
функции • Синтез липидов из углеводов • запасающая (95% ТГ в жировой ткани, 5% - во внутренних органах и костях); • теплоизоляционная; • механическая защита органов и тканей; • эндокринная (секреция: лептина, эстрогенов, ангиотензиногена, интерлейкина-6, ФНО-α);
 • Антибактериальная защита (комплементарные факторы: адипсин, комплемент С 3, фактор В) • Регуляция воспаления (α 1 -кислый гликопротеин, гаптоглобин) • Накопление витаминов А, Д, Е • пассивное обезвреживание (депонирование) токсичных веществ • Участие в водном обмене • Обеспечивает поддержание гомеостаза
• Антибактериальная защита (комплементарные факторы: адипсин, комплемент С 3, фактор В) • Регуляция воспаления (α 1 -кислый гликопротеин, гаптоглобин) • Накопление витаминов А, Д, Е • пассивное обезвреживание (депонирование) токсичных веществ • Участие в водном обмене • Обеспечивает поддержание гомеостаза
 Химсостав жировой ткани 65 -85% - ТГ, 22% - вода, 5, 8% белок, 15 ммоль/кг калий. Из жирных кислот 42— 51% - олеиновая, 22— 31% пальмитиновая, 5— 14% пальмитоолеиновая, 3— 5 % миристиновая, 1— 5 % линолевая
Химсостав жировой ткани 65 -85% - ТГ, 22% - вода, 5, 8% белок, 15 ммоль/кг калий. Из жирных кислот 42— 51% - олеиновая, 22— 31% пальмитиновая, 5— 14% пальмитоолеиновая, 3— 5 % миристиновая, 1— 5 % линолевая
 ОСОБЕННОСТИ МЕТАБОЛИЗМА АДИПОЦИТА БЕЛОЙ ЖИРОВОЙ ТКАНИ • Энергетический обмен медленный, анаэробный, потребляет мало кислорода. Энергия АТФ тратится на транспорт жирных кислот через клеточные мембраны (с участием карнитина). • Белковый обмен низкий, белки синтезируются адипоцитами преимущественно для собственных нужд. На экспорт синтезируются лептин, белки острой фазы воспаления (α 1 -кислый гликопротеин, гаптоглобин), компоненты системы комплимента (адипсин, комплемент С 3, фактор В), интерлейкины.
ОСОБЕННОСТИ МЕТАБОЛИЗМА АДИПОЦИТА БЕЛОЙ ЖИРОВОЙ ТКАНИ • Энергетический обмен медленный, анаэробный, потребляет мало кислорода. Энергия АТФ тратится на транспорт жирных кислот через клеточные мембраны (с участием карнитина). • Белковый обмен низкий, белки синтезируются адипоцитами преимущественно для собственных нужд. На экспорт синтезируются лептин, белки острой фазы воспаления (α 1 -кислый гликопротеин, гаптоглобин), компоненты системы комплимента (адипсин, комплемент С 3, фактор В), интерлейкины.
 • Углеводный обмен. Невысокий, преобладает катаболизм. • Липидный обмен - интенсивно идут реакции липолиза и липогенеза.
• Углеводный обмен. Невысокий, преобладает катаболизм. • Липидный обмен - интенсивно идут реакции липолиза и липогенеза.
 Бурая жировая ткань • Мало у взрослого человека, много у новорожденного • Локализована около почек и щитовидной железы. • Смешанная жировая ткань: между лопатками, на грудной клетке и плечах.
Бурая жировая ткань • Мало у взрослого человека, много у новорожденного • Локализована около почек и щитовидной железы. • Смешанная жировая ткань: между лопатками, на грудной клетке и плечах.
 Функция бурой жировой ткани • термогенез • «взрывной» липолиз
Функция бурой жировой ткани • термогенез • «взрывной» липолиз
 ОСОБЕННОСТИ МЕТАБОЛИЗМА БУРОЙ ЖИРОВОЙ ТКАНИ • 1. потребляет много кислорода • 2. активно окисляет глюкозу и жирные кислоты • 3. энергетический обмен низкий • 4. АТФ образуется только в реакциях субстратного фосфорилирования (2 реакции гликолиза, 1 реакции ЦТК) • 5. разобщение в митохондриях белком термогенином (РБ-1) процессов окисления и фосфорилирования, низкая активность АТФ синтетазы
ОСОБЕННОСТИ МЕТАБОЛИЗМА БУРОЙ ЖИРОВОЙ ТКАНИ • 1. потребляет много кислорода • 2. активно окисляет глюкозу и жирные кислоты • 3. энергетический обмен низкий • 4. АТФ образуется только в реакциях субстратного фосфорилирования (2 реакции гликолиза, 1 реакции ЦТК) • 5. разобщение в митохондриях белком термогенином (РБ-1) процессов окисления и фосфорилирования, низкая активность АТФ синтетазы
 • 6. энергия рассеивается в виде тепла (несократительный термогенез). • 7. Термогенез активируется при переохлаждении, излишке липидов в крови, под действием лептина. • 8. Характерен феномен «взрывного липолиза»
• 6. энергия рассеивается в виде тепла (несократительный термогенез). • 7. Термогенез активируется при переохлаждении, излишке липидов в крови, под действием лептина. • 8. Характерен феномен «взрывного липолиза»
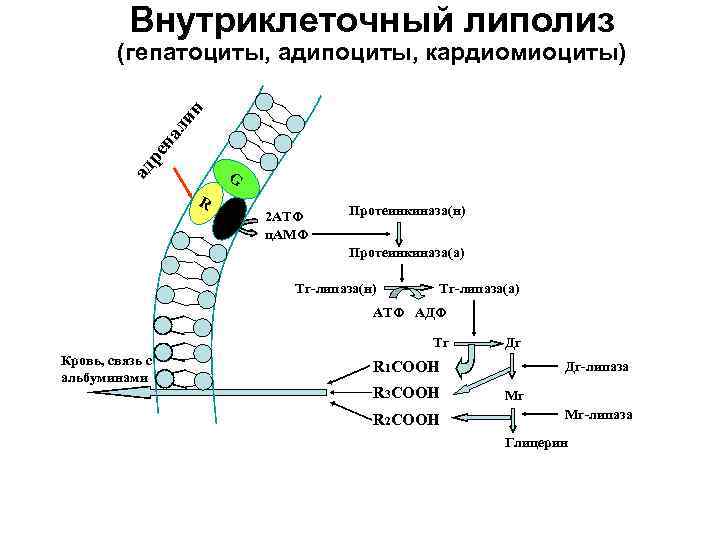
 Внутриклеточный липолиз (гепатоциты, адипоциты, кардиомиоциты) лин на ре ад G R AC 2 АТФ Протеинкиназа(н) ц. АМФ Протеинкиназа(а) Тг-липаза(н) Тг-липаза(а) АТФ АДФ Тг Дг Кровь, связь с R 1 СООН Дг-липаза альбуминами R 3 COOH Мг R 2 СООН Мг-липаза Глицерин
Внутриклеточный липолиз (гепатоциты, адипоциты, кардиомиоциты) лин на ре ад G R AC 2 АТФ Протеинкиназа(н) ц. АМФ Протеинкиназа(а) Тг-липаза(н) Тг-липаза(а) АТФ АДФ Тг Дг Кровь, связь с R 1 СООН Дг-липаза альбуминами R 3 COOH Мг R 2 СООН Мг-липаза Глицерин
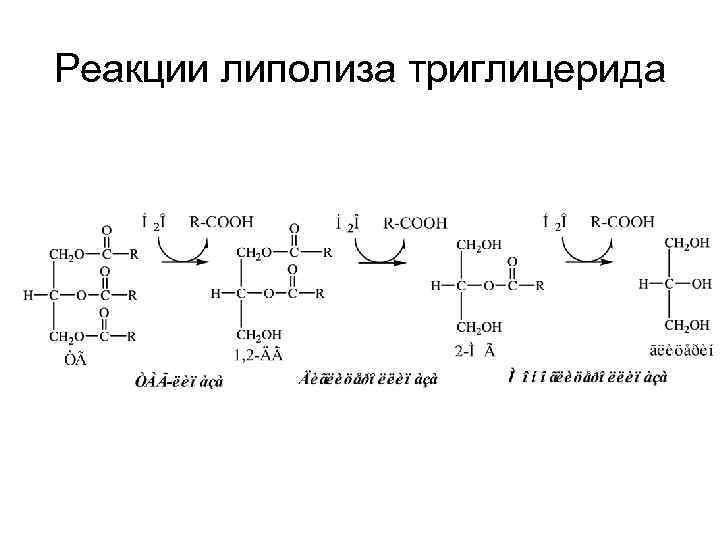
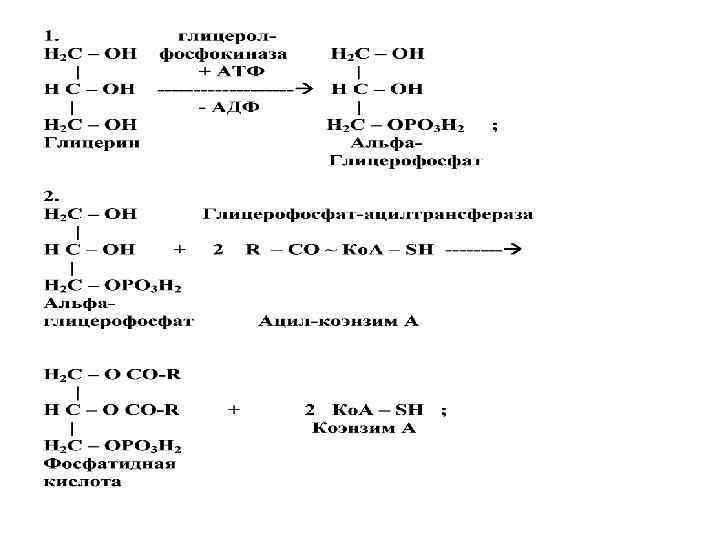
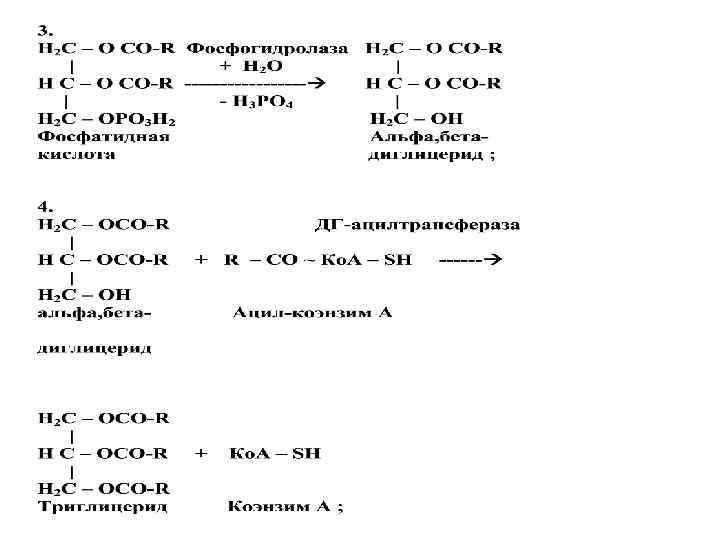
 Реакции липолиза триглицерида
Реакции липолиза триглицерида
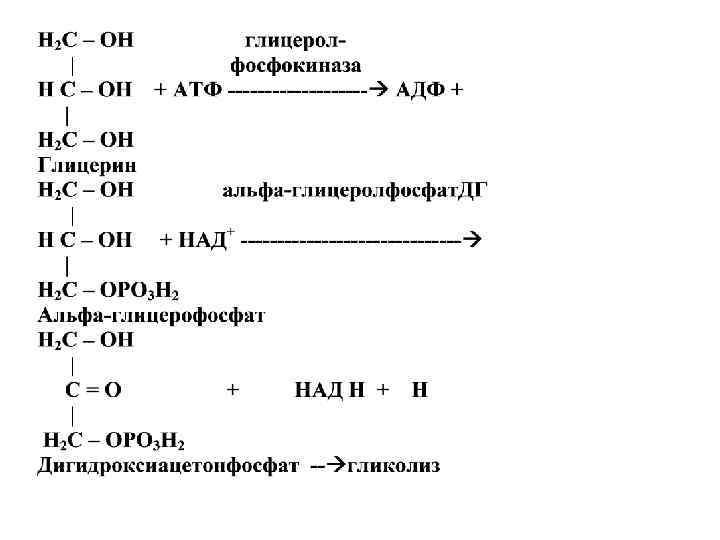
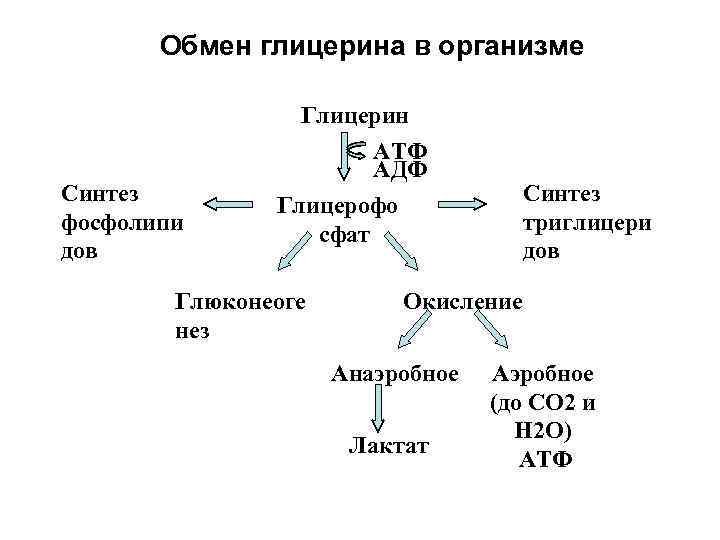
 Обмен глицерина в организме Глицерин АТФ АДФ Синтез Глицерофо фосфолипи триглицери сфат дов дов Глюконеоге Окисление нез Анаэробное Аэробное (до СО 2 и Н 2 О) Лактат АТФ
Обмен глицерина в организме Глицерин АТФ АДФ Синтез Глицерофо фосфолипи триглицери сфат дов дов Глюконеоге Окисление нез Анаэробное Аэробное (до СО 2 и Н 2 О) Лактат АТФ
 β-окисление ЖК • путь катаболизма ЖК с неразветвленной средней и короткой углеводородной цепью • протекает в матриксе митохондрий • от С конца ЖК последовательно отделяется по 2 атома С в виде Ацетил-Ко. А. • происходит в аэробных условиях • Является самым мощным источником энергии
β-окисление ЖК • путь катаболизма ЖК с неразветвленной средней и короткой углеводородной цепью • протекает в матриксе митохондрий • от С конца ЖК последовательно отделяется по 2 атома С в виде Ацетил-Ко. А. • происходит в аэробных условиях • Является самым мощным источником энергии
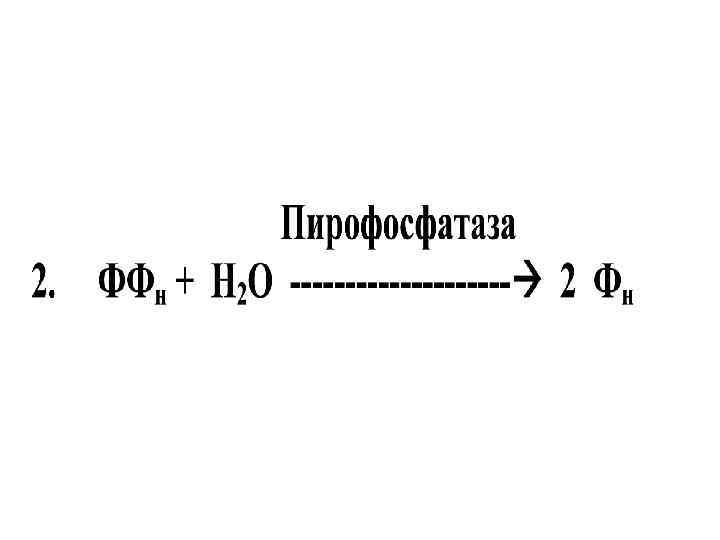
 Этапы b окисления • I Активирование жирных кислот (цитозоль) R-COOH + АТФ + Hs. Ko. A ЮR-СO~SKo. A+ АЦИЛ-Ко. А-СИНТАЗА АМФ + ФФн l II Транспорт в MХ СН 3 + + СН 3 -N-CH 2 -CH-CH 2 -COOH СН 3 ОН КАРНИТИН СН 3 О-СO~R + Ю АЦИЛКАРНИТИН + HSKo. A Ю R-СO~SKo. A КАРНИТИН-АЦИЛ Ко. А - ТРАНСФЕРАЗА В MХ, где распадается на R-СO~SKo. A и карнитин
Этапы b окисления • I Активирование жирных кислот (цитозоль) R-COOH + АТФ + Hs. Ko. A ЮR-СO~SKo. A+ АЦИЛ-Ко. А-СИНТАЗА АМФ + ФФн l II Транспорт в MХ СН 3 + + СН 3 -N-CH 2 -CH-CH 2 -COOH СН 3 ОН КАРНИТИН СН 3 О-СO~R + Ю АЦИЛКАРНИТИН + HSKo. A Ю R-СO~SKo. A КАРНИТИН-АЦИЛ Ко. А - ТРАНСФЕРАЗА В MХ, где распадается на R-СO~SKo. A и карнитин
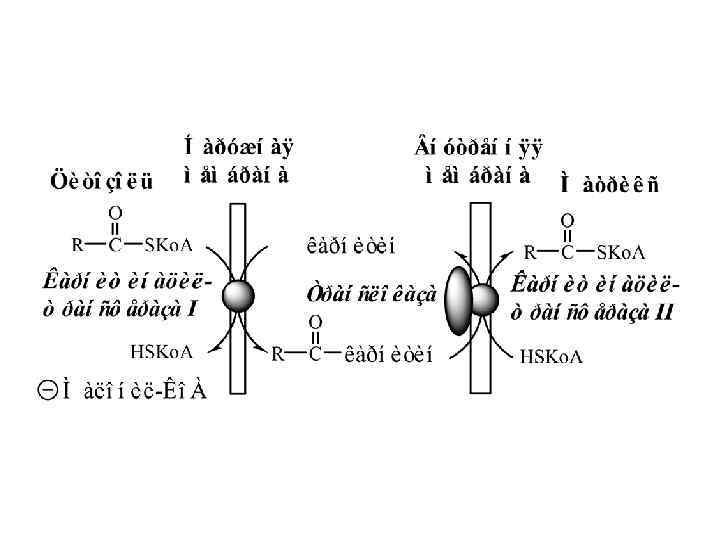
 Стадии транспорта ЖК в МХ
Стадии транспорта ЖК в МХ
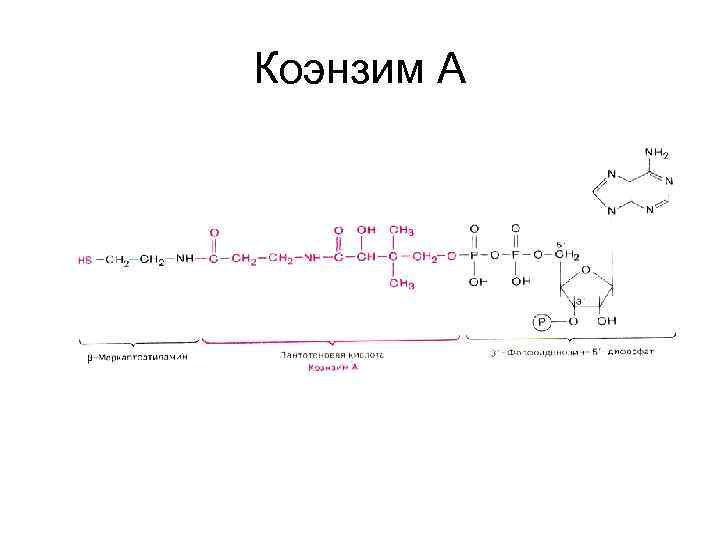
 Коэнзим А
Коэнзим А
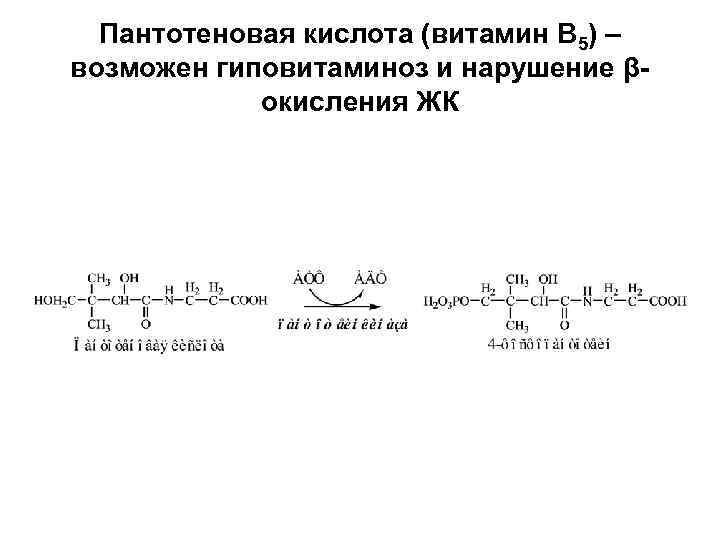
 Пантотеновая кислота (витамин В 5) – возможен гиповитаминоз и нарушение β- окисления ЖК
Пантотеновая кислота (витамин В 5) – возможен гиповитаминоз и нарушение β- окисления ЖК
 Стадии β-окисления ЖК в МХ
Стадии β-окисления ЖК в МХ
 Энергобаланс β-окисления ЖК
Энергобаланс β-окисления ЖК
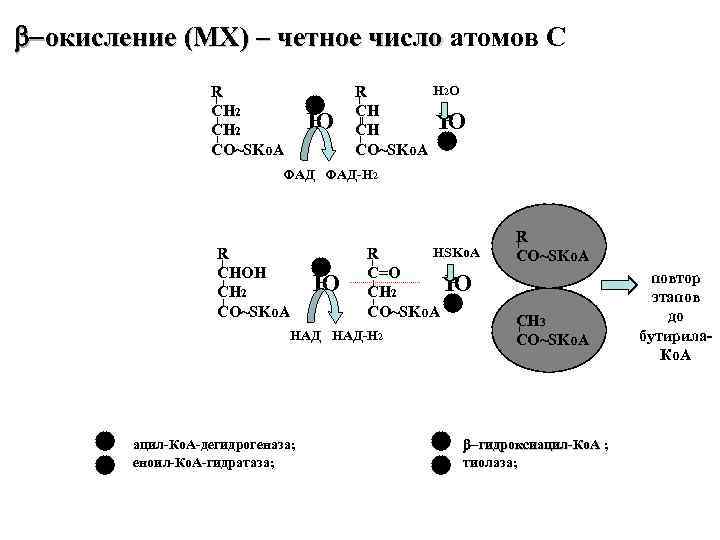
 b окисление (МХ) – четное число атомов С R Н 2 О CH 2 1 CH CH 2 Ю CH Ю CO~SKo. A 2 ФАД-Н 2 R HSKo. A CO~SKo. A CHOH 3 C=O повтор CH 2 Ю CH 2 Ю этапов CO~SKo. A 4 до СН 3 НАД-Н 2 CO~SKo. A бутирила- Ко. А 1 ацил-Ко. А-дегидрогеназа; 3 b гидроксиацил-Ко. А ; 2 еноил-Ко. А-гидратаза; 4 тиолаза;
b окисление (МХ) – четное число атомов С R Н 2 О CH 2 1 CH CH 2 Ю CH Ю CO~SKo. A 2 ФАД-Н 2 R HSKo. A CO~SKo. A CHOH 3 C=O повтор CH 2 Ю CH 2 Ю этапов CO~SKo. A 4 до СН 3 НАД-Н 2 CO~SKo. A бутирила- Ко. А 1 ацил-Ко. А-дегидрогеназа; 3 b гидроксиацил-Ко. А ; 2 еноил-Ко. А-гидратаза; 4 тиолаза;
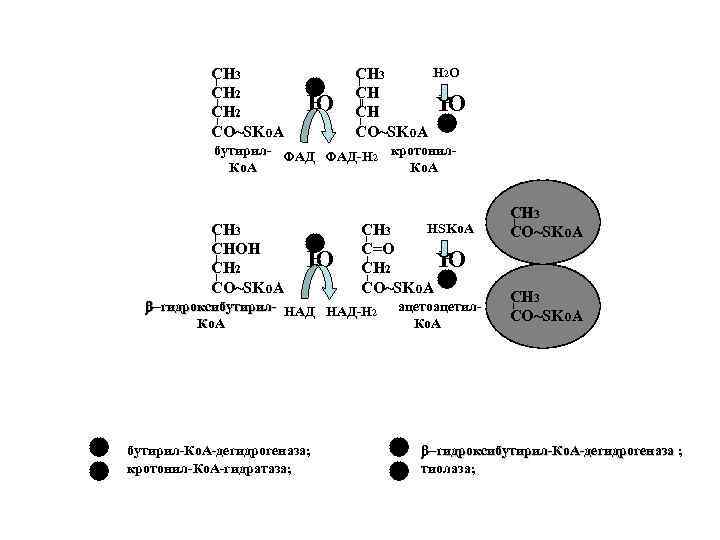
 СН 3 Н 2 О CH 2 1 CH 2 Ю CH Ю CO~SKo. A 2 бутирил- ФАД-Н 2 кротонил- Ко. А СН 3 HSKo. A CO~SKo. A CHOH 3 C=O CH 2 Ю CH 2 Ю CO~SKo. A 4 СН 3 b гидроксибутирил- НАД-Н 2 ацетоацетил- Ко. А CO~SKo. A 1 бутирил-Ко. А-дегидрогеназа; 3 b гидроксибутирил-Ко. А-дегидрогеназа ; 2 кротонил-Ко. А-гидратаза; 4 тиолаза;
СН 3 Н 2 О CH 2 1 CH 2 Ю CH Ю CO~SKo. A 2 бутирил- ФАД-Н 2 кротонил- Ко. А СН 3 HSKo. A CO~SKo. A CHOH 3 C=O CH 2 Ю CH 2 Ю CO~SKo. A 4 СН 3 b гидроксибутирил- НАД-Н 2 ацетоацетил- Ко. А CO~SKo. A 1 бутирил-Ко. А-дегидрогеназа; 3 b гидроксибутирил-Ко. А-дегидрогеназа ; 2 кротонил-Ко. А-гидратаза; 4 тиолаза;
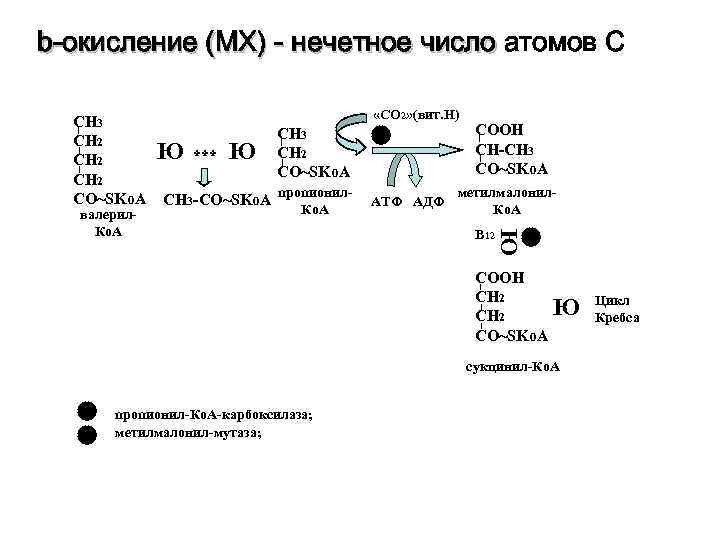
 b-окисление (МХ) - нечетное число атомов С «СО 2» (вит. Н) СН 3 1 СООН CH 2 Ю *** Ю СН 2 CH-СH 3 CO~SKo. A СН 2 метилмалонил- CO~SKo. A СН 3 -CO~SKo. A пропионил- АТФ АДФ валерил- Ко. А В 12 2 Ю СООН CН 2 Цикл CH 2 Ю Кребса CO~SKo. A сукцинил-Ко. А 1 пропионил-Ко. А-карбоксилаза; 2 метилмалонил-мутаза;
b-окисление (МХ) - нечетное число атомов С «СО 2» (вит. Н) СН 3 1 СООН CH 2 Ю *** Ю СН 2 CH-СH 3 CO~SKo. A СН 2 метилмалонил- CO~SKo. A СН 3 -CO~SKo. A пропионил- АТФ АДФ валерил- Ко. А В 12 2 Ю СООН CН 2 Цикл CH 2 Ю Кребса CO~SKo. A сукцинил-Ко. А 1 пропионил-Ко. А-карбоксилаза; 2 метилмалонил-мутаза;
 Регуляция β-окисления ЖК активируют НАД+, АДФ (энергодефицит), ЖК, кислород, глюкагон, адреналин, карнитин, ингибирование гликолиза (анаэробного и особенно - аэробного) ингибируют НАДH 2, АТФ, инсулин, недостаток карнитина, активация гликолиза (…)
Регуляция β-окисления ЖК активируют НАД+, АДФ (энергодефицит), ЖК, кислород, глюкагон, адреналин, карнитин, ингибирование гликолиза (анаэробного и особенно - аэробного) ингибируют НАДH 2, АТФ, инсулин, недостаток карнитина, активация гликолиза (…)
 Взаимопревращения кетоновых тел
Взаимопревращения кетоновых тел
 Нормальное содержание кетоновых тел у взрослых 35, 0 — 430, 0 мкмоль/л
Нормальное содержание кетоновых тел у взрослых 35, 0 — 430, 0 мкмоль/л
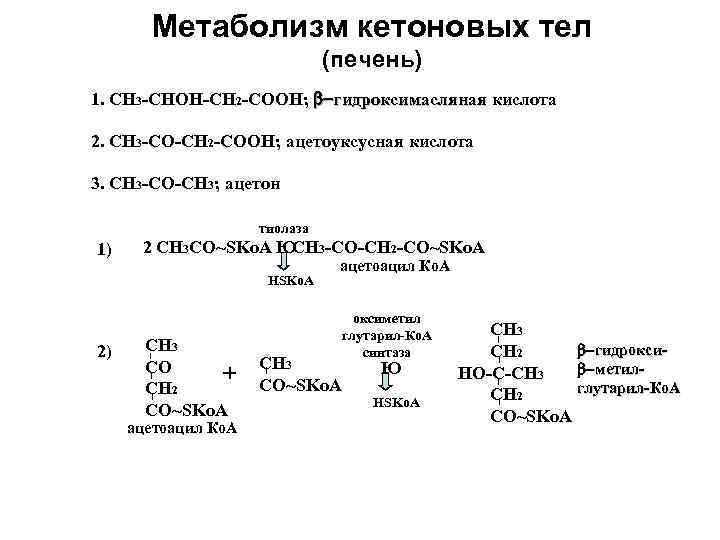
 Метаболизм кетоновых тел (печень) 1. СН 3 -СНОН-СН 2 -СООН; b гидроксимасляная кислота 2. СН 3 -СО-СН 2 -СООН; ацетоуксусная кислота 3. СН 3 -СО-СН 3; ацетон тиолаза 1) 2 СН 3 СО~SKo. A Ю 3 -СО-СН 2 -СО~SKo. A СН ацетоацил Ко. А HSKo. A оксиметил глутарил-Ко. А СН 3 2) СН 3 синтаза CH 2 b гидрокси- CО СН 3 Ю b метил- + CO~SKo. A НО-С-СН 3 CH 2 CH 2 глутарил-Ко. А HSKo. A CO~SKo. A CO~SKo. A ацетоацил Ко. А
Метаболизм кетоновых тел (печень) 1. СН 3 -СНОН-СН 2 -СООН; b гидроксимасляная кислота 2. СН 3 -СО-СН 2 -СООН; ацетоуксусная кислота 3. СН 3 -СО-СН 3; ацетон тиолаза 1) 2 СН 3 СО~SKo. A Ю 3 -СО-СН 2 -СО~SKo. A СН ацетоацил Ко. А HSKo. A оксиметил глутарил-Ко. А СН 3 2) СН 3 синтаза CH 2 b гидрокси- CО СН 3 Ю b метил- + CO~SKo. A НО-С-СН 3 CH 2 CH 2 глутарил-Ко. А HSKo. A CO~SKo. A CO~SKo. A ацетоацил Ко. А
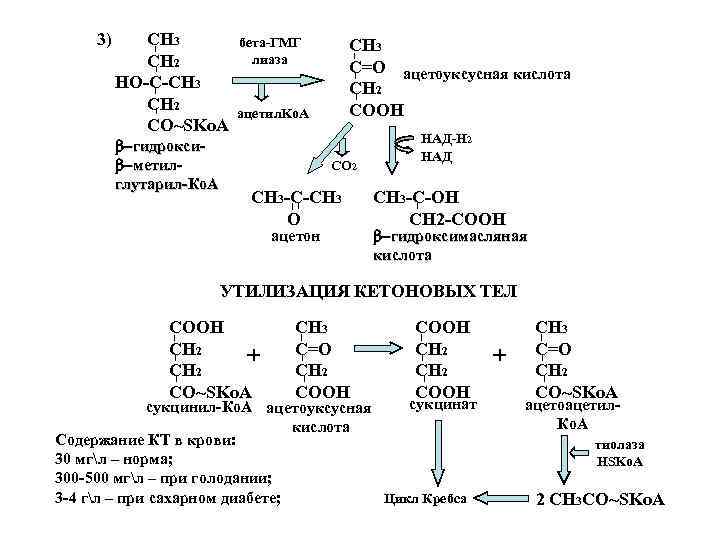
 3) СН 3 бета-ГМГ СН 3 CH 2 лиаза C=О ацетоуксусная кислота НО-С-СН 3 CH 2 ацетил. Ko. A COОН CO~SKo. A НАД-Н 2 b гидрокси- НАД b метил- СО 2 глутарил-Ко. А СН 3 -С-СН 3 СН 3 -С-ОН О СН 2 -СООН ацетон b гидроксимасляная кислота УТИЛИЗАЦИЯ КЕТОНОВЫХ ТЕЛ СООН СН 3 CH 2 + C=О CH 2 + C=О CH 2 CO~SKo. A COОН CO~SKo. A сукцинил-Ко. А ацетоуксусная сукцинат ацетоацетил- кислота Ко. А Содержание КТ в крови: тиолаза 30 мгл – норма; HSKo. A 300 -500 мгл – при голодании; 3 -4 гл – при сахарном диабете; Цикл Кребса 2 СН 3 СО~SKo. A
3) СН 3 бета-ГМГ СН 3 CH 2 лиаза C=О ацетоуксусная кислота НО-С-СН 3 CH 2 ацетил. Ko. A COОН CO~SKo. A НАД-Н 2 b гидрокси- НАД b метил- СО 2 глутарил-Ко. А СН 3 -С-СН 3 СН 3 -С-ОН О СН 2 -СООН ацетон b гидроксимасляная кислота УТИЛИЗАЦИЯ КЕТОНОВЫХ ТЕЛ СООН СН 3 CH 2 + C=О CH 2 + C=О CH 2 CO~SKo. A COОН CO~SKo. A сукцинил-Ко. А ацетоуксусная сукцинат ацетоацетил- кислота Ко. А Содержание КТ в крови: тиолаза 30 мгл – норма; HSKo. A 300 -500 мгл – при голодании; 3 -4 гл – при сахарном диабете; Цикл Кребса 2 СН 3 СО~SKo. A
 Нарушения окисления ЖК Снижение концентрации карнитина • 1. длительный гемодиализ • 2. нарушении синтеза карнитина Карнитинацилтрансфераза I ингибируется • 1. препаратами сульфонилмочевины (при лечении сахарного диабета) • 2. наследственные дефекты карнитинацилтрансферазы Генетический дефект дегидрогеназы ЖК
Нарушения окисления ЖК Снижение концентрации карнитина • 1. длительный гемодиализ • 2. нарушении синтеза карнитина Карнитинацилтрансфераза I ингибируется • 1. препаратами сульфонилмочевины (при лечении сахарного диабета) • 2. наследственные дефекты карнитинацилтрансферазы Генетический дефект дегидрогеназы ЖК
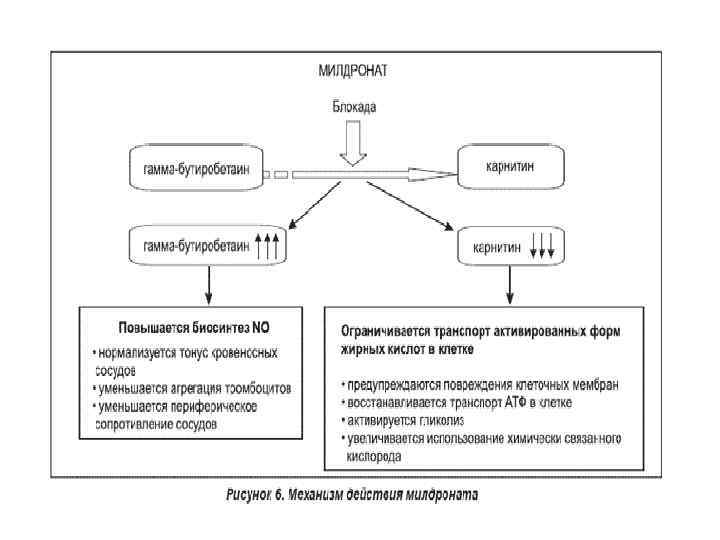
 Фармпрепарат - милдронат • подавляет гамма-бутиробетаингидроксиназу, снижает синтез карнитина и транспорт длинноцепочечных жирных кислот через оболочки клеток, препятствует накоплению в клетках активированных форм неокисленных жирных кислот - производных ацилкарнитина и ацилкоэнзима А. В условиях ишемии восстанавливает равновесие процессов доставки кислорода и его потребления в клетках; активирует гликолиз анаэробный. • фармакологические эффекты: повышение работоспособности, уменьшение симптомов психического и физического перенапряжения, активация тканевого и гуморального иммунитета, кардиопротекторное действие.
Фармпрепарат - милдронат • подавляет гамма-бутиробетаингидроксиназу, снижает синтез карнитина и транспорт длинноцепочечных жирных кислот через оболочки клеток, препятствует накоплению в клетках активированных форм неокисленных жирных кислот - производных ацилкарнитина и ацилкоэнзима А. В условиях ишемии восстанавливает равновесие процессов доставки кислорода и его потребления в клетках; активирует гликолиз анаэробный. • фармакологические эффекты: повышение работоспособности, уменьшение симптомов психического и физического перенапряжения, активация тканевого и гуморального иммунитета, кардиопротекторное действие.
 Перекисное окисление липидов – ОБЩАЯ ХАРАКТЕРИСТИКА • Синонимы (СРО липидов, ПОЛ, пероксидное окисление липидов, липопероксидация) • Определение понятия • ОТЛИЧИЯ ОТ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ • ЛОКАЛИЗАЦИЯ
Перекисное окисление липидов – ОБЩАЯ ХАРАКТЕРИСТИКА • Синонимы (СРО липидов, ПОЛ, пероксидное окисление липидов, липопероксидация) • Определение понятия • ОТЛИЧИЯ ОТ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ • ЛОКАЛИЗАЦИЯ
 Субстраты ПОЛ - полиненасыщенные жирные к –ты: • Линоленовая CH 3(CH 2 CH=CH)3(CH 2)7 COOH • Арахидоновая CH 3(CH 2)4(CH=CHCH 2)4(CH 2)2 COOH • и др.
Субстраты ПОЛ - полиненасыщенные жирные к –ты: • Линоленовая CH 3(CH 2 CH=CH)3(CH 2)7 COOH • Арахидоновая CH 3(CH 2)4(CH=CHCH 2)4(CH 2)2 COOH • и др.
 Митохондрии – источник АФК и пререкисных соединений
Митохондрии – источник АФК и пререкисных соединений
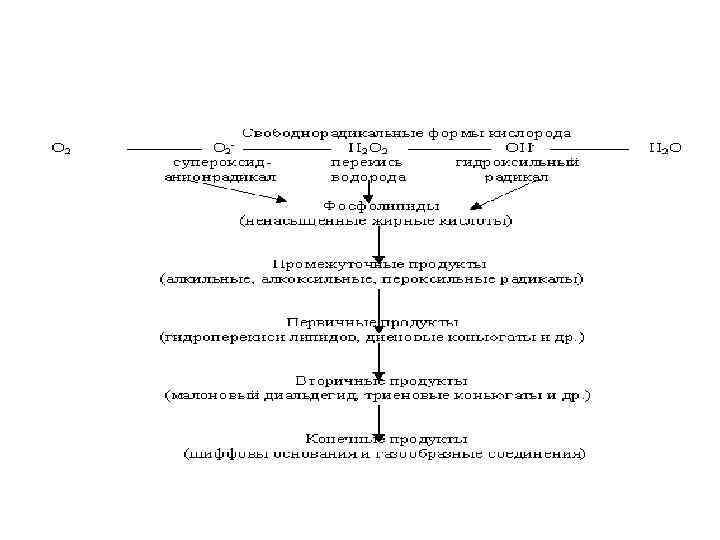
 АФК –активные формы кислорода • Супероксидные анион-радикалы О*2 - • Гидроксильные радикалы *ОН • Пероксид водорода Н 2 О 2 • Синглетные формы кислорода -О 2 • Молекулярный кислород О 2 • Пероксильный радикал ROO*
АФК –активные формы кислорода • Супероксидные анион-радикалы О*2 - • Гидроксильные радикалы *ОН • Пероксид водорода Н 2 О 2 • Синглетные формы кислорода -О 2 • Молекулярный кислород О 2 • Пероксильный радикал ROO*
 Электронная структура супероксид-анион-радикала
Электронная структура супероксид-анион-радикала
 Многообразие АФК • Молекулярный кислород О 2 • Оксид азота NO* • Пероксинитрит ОNOO- (0=N-0 -0 -) • Алкоксильный радикал RO* • Феноксил-радикал С 6 Н 5 О* • Гипохлорит-анион OСl - • Липидный пероксид LOOH
Многообразие АФК • Молекулярный кислород О 2 • Оксид азота NO* • Пероксинитрит ОNOO- (0=N-0 -0 -) • Алкоксильный радикал RO* • Феноксил-радикал С 6 Н 5 О* • Гипохлорит-анион OСl - • Липидный пероксид LOOH
 Прооксидантные ферменты фагоцитов НАДФН-оксидаза НАДФН + О 2 ----- Н+ + *О 2 – + НАДФ НАДН-оксидаза НАДН + Н+ + О 2 ------- НАД + + Н 2 О 2 миелопероксидаза I- + Н 2 О 2 + АН------- АI + ОН- + Н 2 O + О 2 Где I- иодид-анион, А – орг. в –ва (бактерий)
Прооксидантные ферменты фагоцитов НАДФН-оксидаза НАДФН + О 2 ----- Н+ + *О 2 – + НАДФ НАДН-оксидаза НАДН + Н+ + О 2 ------- НАД + + Н 2 О 2 миелопероксидаза I- + Н 2 О 2 + АН------- АI + ОН- + Н 2 O + О 2 Где I- иодид-анион, А – орг. в –ва (бактерий)
 Образование активных форм кислорода (АФК) ксантиндегидрогеназа + Ca 2+ + ONOO- ↓ ксантиноксидаза Гипоксантин, ксантин мочевая к-та + АФК
Образование активных форм кислорода (АФК) ксантиндегидрогеназа + Ca 2+ + ONOO- ↓ ксантиноксидаза Гипоксантин, ксантин мочевая к-та + АФК
 Изоферменты синтазы окисида азота (Nitric Oxide Synthase - NOS; КФ 1. 14. 13. 39. ) 1 тип (n. NOS) - нейрональная; 2 тип (i. NOS или mac. NOS)- в клетках различных типов 3 тип (e. NOS) - эндотелиальная. Классификация по по типу экспрессии • конститутивно присутствующие в клетках (c. NOS) • индуцибельные (i. NOS).
Изоферменты синтазы окисида азота (Nitric Oxide Synthase - NOS; КФ 1. 14. 13. 39. ) 1 тип (n. NOS) - нейрональная; 2 тип (i. NOS или mac. NOS)- в клетках различных типов 3 тип (e. NOS) - эндотелиальная. Классификация по по типу экспрессии • конститутивно присутствующие в клетках (c. NOS) • индуцибельные (i. NOS).
 Структура субъединицы димера NO-синтазы • редуктазный домен содержит флавины FAD (первичный акцептор электронов от NADPH) и FMN (переносит электроны от FAD на гем оксигеназного домена). • кальмодулинсвязывающий домен • оксигеназный домен содержит участки связывания гема, аргинина
Структура субъединицы димера NO-синтазы • редуктазный домен содержит флавины FAD (первичный акцептор электронов от NADPH) и FMN (переносит электроны от FAD на гем оксигеназного домена). • кальмодулинсвязывающий домен • оксигеназный домен содержит участки связывания гема, аргинина
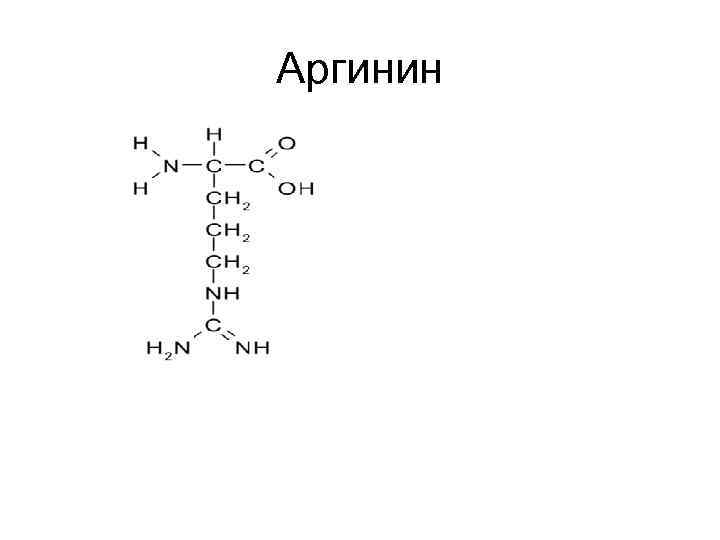
 Аргинин
Аргинин
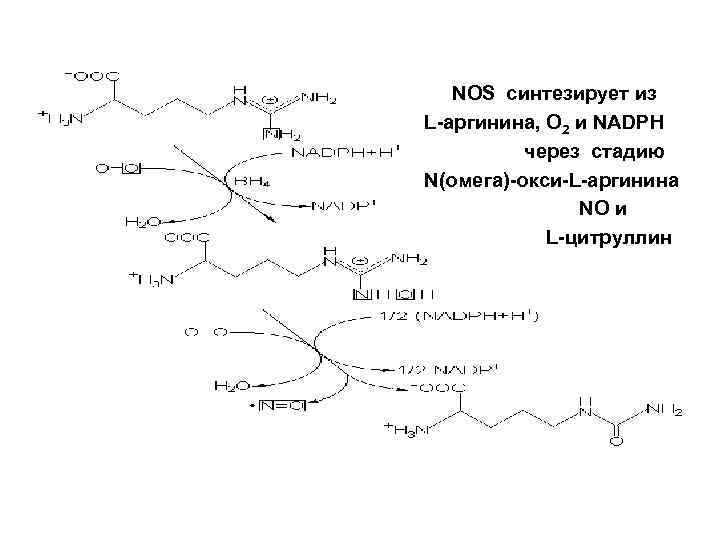
 NOS синтезирует из L-аргинина, О 2 и NADPH через стадию N(омега)-окси-L-аргинина NO и L-цитруллин
NOS синтезирует из L-аргинина, О 2 и NADPH через стадию N(омега)-окси-L-аргинина NO и L-цитруллин
 Роль АФК в норме и патологии
Роль АФК в норме и патологии
 Причины и последствия ↑ NO → ↑ ↑ ↑ иона нитрозония (NO+), нитроксила (NO-), пероксинитрита (ONOO-), нитритов и нитратов (NО 2 -, NО 3 -) →повреждение макромолекул → разрушение клеток → б. Альцгеймера, отторжение трансплантата, артрит, шок, эндотелиальная дисфункция, ишемия, аритмия
Причины и последствия ↑ NO → ↑ ↑ ↑ иона нитрозония (NO+), нитроксила (NO-), пероксинитрита (ONOO-), нитритов и нитратов (NО 2 -, NО 3 -) →повреждение макромолекул → разрушение клеток → б. Альцгеймера, отторжение трансплантата, артрит, шок, эндотелиальная дисфункция, ишемия, аритмия
 Генерация АФК при гипоксии ↓ О 2 ↑НАДН ↓ ↓ Fe 3+ ↑ Fe 2+ ↓ Н 2 О 2+↑Fe 2+ →↑ ОН– + Fe 3++ ↑ОН • (реакция Фентона)
Генерация АФК при гипоксии ↓ О 2 ↑НАДН ↓ ↓ Fe 3+ ↑ Fe 2+ ↓ Н 2 О 2+↑Fe 2+ →↑ ОН– + Fe 3++ ↑ОН • (реакция Фентона)
 Стадии и механизм ПОЛ Усл. обозначения ОН* - гидроксильный радикал R 1 H и R 2 H – разные жирные кислоты R 1*и R 2* - радикалы жирных кислот R 1 ООН – гидроперекись жирной к – ты R 1 ОО* - перекисный радикал жирн. к-ты
Стадии и механизм ПОЛ Усл. обозначения ОН* - гидроксильный радикал R 1 H и R 2 H – разные жирные кислоты R 1*и R 2* - радикалы жирных кислот R 1 ООН – гидроперекись жирной к – ты R 1 ОО* - перекисный радикал жирн. к-ты
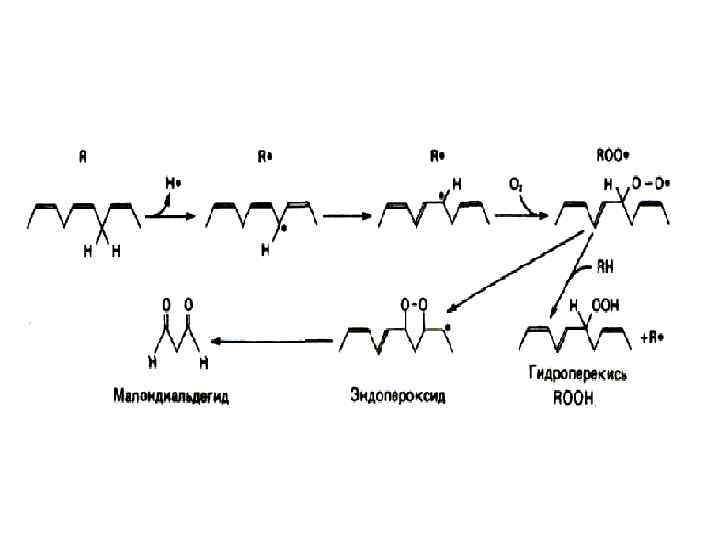
 Стадии и механизм ПОЛ 1. Инициация цепной реакции ОН* + R 1 H Н 2 О 2 + R 1* + О 2 R 1 ОО *
Стадии и механизм ПОЛ 1. Инициация цепной реакции ОН* + R 1 H Н 2 О 2 + R 1* + О 2 R 1 ОО *
 2. Развитие цепных реакций - роль Fe 2+ R 1* + О 2 R 1 ОО* + R 2 H R 1 ООН + R 2* R 1 ООН + Fe 2+ R 1 О* + НО- + Fe 3+
2. Развитие цепных реакций - роль Fe 2+ R 1* + О 2 R 1 ОО* + R 2 H R 1 ООН + R 2* R 1 ООН + Fe 2+ R 1 О* + НО- + Fe 3+
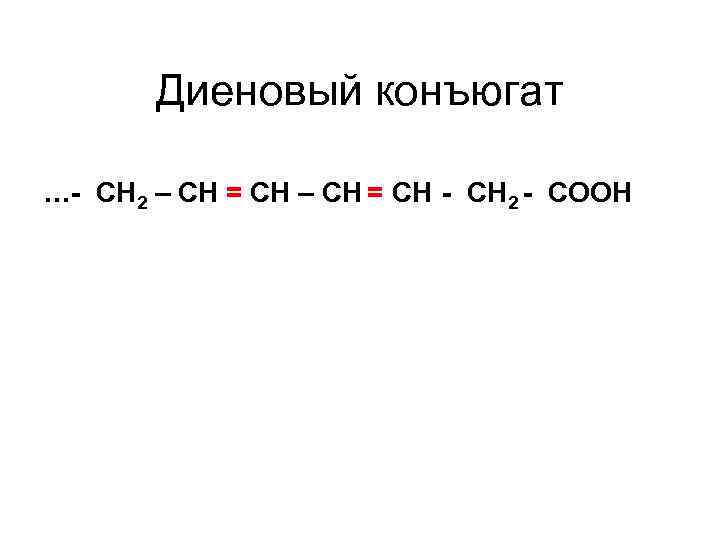
 Диеновый конъюгат …- СН 2 – СН = СН - СН 2 - СООН
Диеновый конъюгат …- СН 2 – СН = СН - СН 2 - СООН
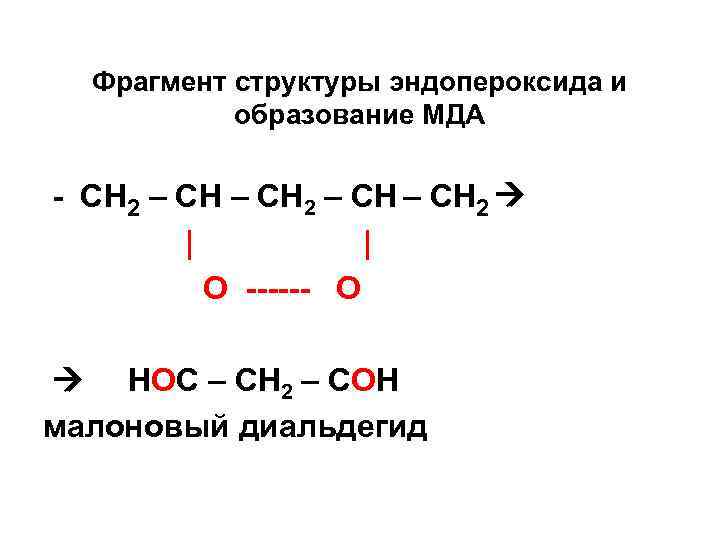
 Фрагмент структуры эндопероксида и образование МДА - СН 2 – СН 2 | О ------ О НОС – СН 2 – СОН малоновый диальдегид
Фрагмент структуры эндопероксида и образование МДА - СН 2 – СН 2 | О ------ О НОС – СН 2 – СОН малоновый диальдегид
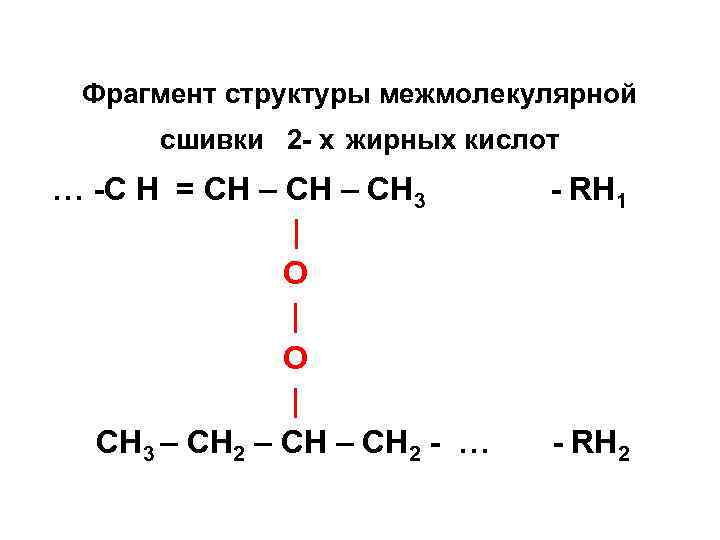
 Фрагмент структуры межмолекулярной сшивки 2 - х жирных кислот … -С Н = СН – СН 3 - RН 1 | О | O | СН 3 – СН 2 - … - RН 2
Фрагмент структуры межмолекулярной сшивки 2 - х жирных кислот … -С Н = СН – СН 3 - RН 1 | О | O | СН 3 – СН 2 - … - RН 2
 ФРАГМЕНТЫ СТРУКТУР МЕТАБОЛИТОВ ПОЛ
ФРАГМЕНТЫ СТРУКТУР МЕТАБОЛИТОВ ПОЛ
 2 а. Продолжение цепи ОН* + R 1 H Н 2 О 2 + R 1* + О 2 R 1 ОО* + R 2 H R 1 ООН + R*2
2 а. Продолжение цепи ОН* + R 1 H Н 2 О 2 + R 1* + О 2 R 1 ОО* + R 2 H R 1 ООН + R*2
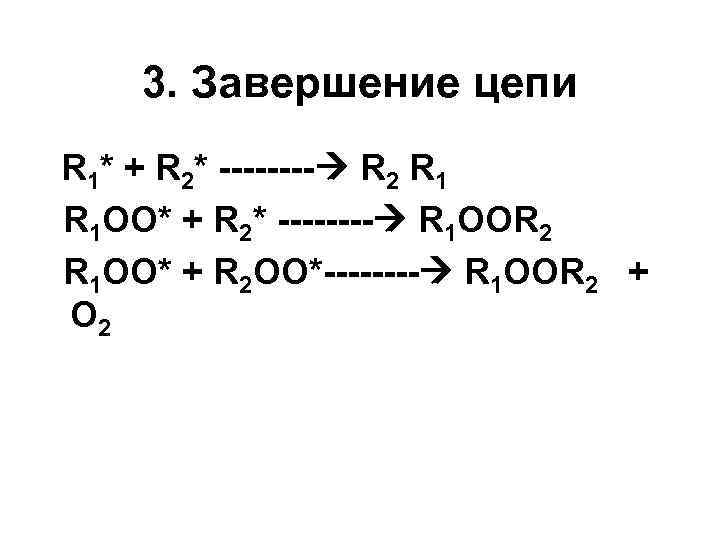
 3. Завершение цепи R 1* + R 2* ---- R 2 R 1 ОО* + R 2* ---- R 1 ООR 2 R 1 ОО* + R 2 ОО*---- R 1 ООR 2 + O 2
3. Завершение цепи R 1* + R 2* ---- R 2 R 1 ОО* + R 2* ---- R 1 ООR 2 R 1 ОО* + R 2 ОО*---- R 1 ООR 2 + O 2
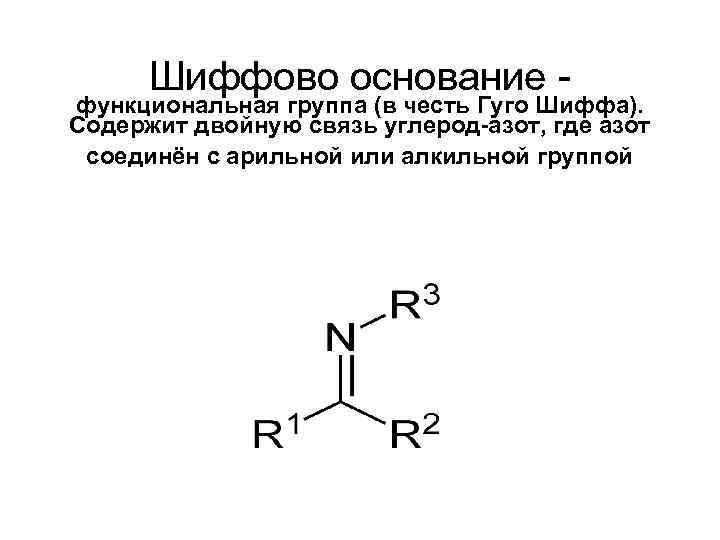
 Шиффово основание - функциональная группа (в честь Гуго Шиффа). Содержит двойную связь углерод-азот, где азот соединён с арильной или алкильной группой
Шиффово основание - функциональная группа (в честь Гуго Шиффа). Содержит двойную связь углерод-азот, где азот соединён с арильной или алкильной группой
 Регуляция ПОЛ • АОА – антиокислительная (=антиоксидантная) активность – способность хим. в –в тормозить процессы ПОЛ • АРА – антирадикальная активность - способность хим. в –в связывать свободные радикалы (в молекулы, → ↓ ПОЛ) • Восстановительная активность в-в в целом = АОА • Прооксидантная активность- способность хим. в –в активировать процессы ПОЛ = • Окислительная активность -
Регуляция ПОЛ • АОА – антиокислительная (=антиоксидантная) активность – способность хим. в –в тормозить процессы ПОЛ • АРА – антирадикальная активность - способность хим. в –в связывать свободные радикалы (в молекулы, → ↓ ПОЛ) • Восстановительная активность в-в в целом = АОА • Прооксидантная активность- способность хим. в –в активировать процессы ПОЛ = • Окислительная активность -
 Антиоксидантная защита (АОЗ) - классификация • 1. Неферментативная 2 а. Водорастворимые низкомолекулярные АО (витамин С - аскорбат) 2 б. Липидорастворимые низкомолекулярные АО (витамин Е - токоферол) • 2. Ферментативная
Антиоксидантная защита (АОЗ) - классификация • 1. Неферментативная 2 а. Водорастворимые низкомолекулярные АО (витамин С - аскорбат) 2 б. Липидорастворимые низкомолекулярные АО (витамин Е - токоферол) • 2. Ферментативная
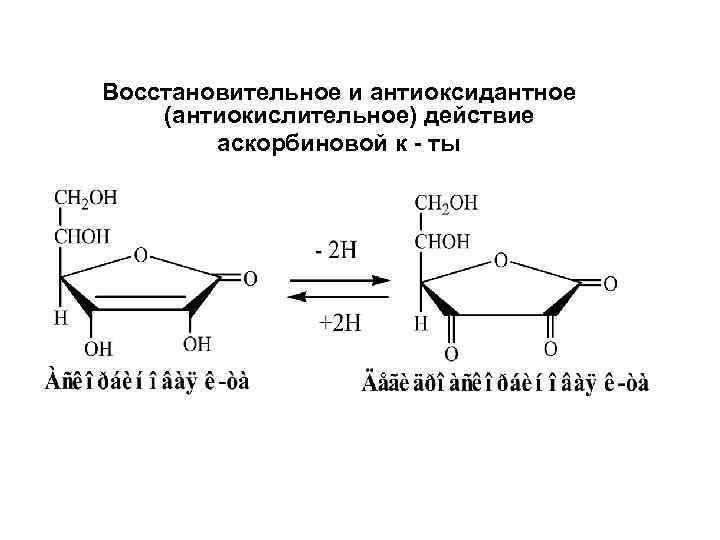
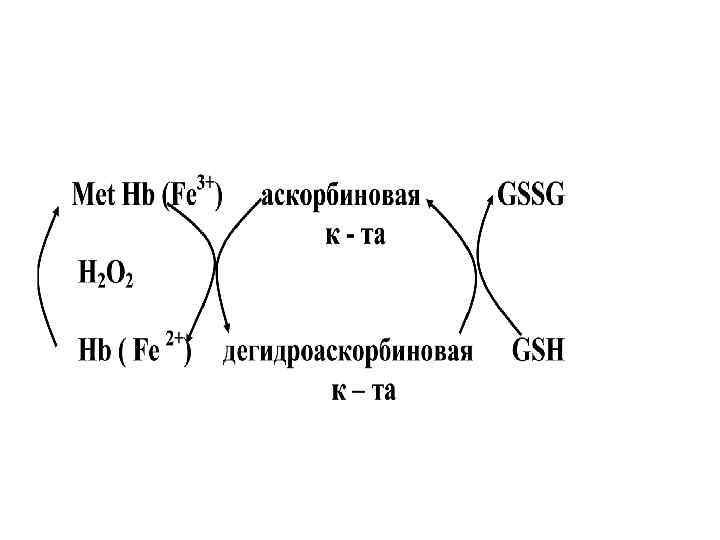
 Восстановительное и антиоксидантное (антиокислительное) действие аскорбиновой к - ты
Восстановительное и антиоксидантное (антиокислительное) действие аскорбиновой к - ты
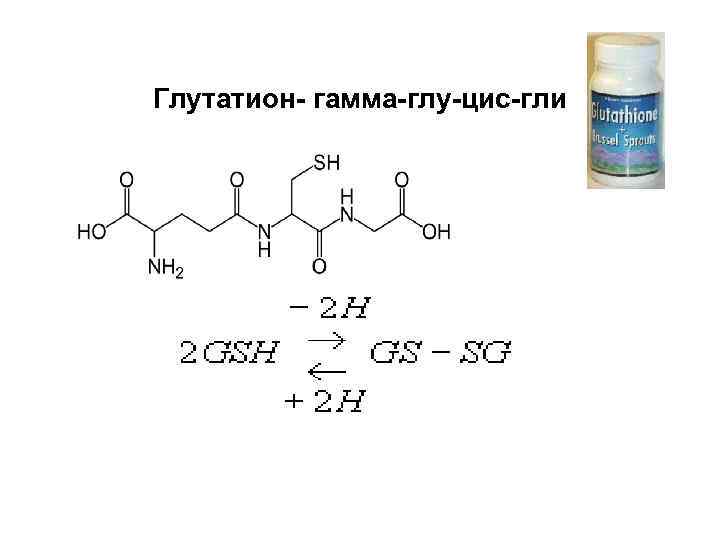
 Глутатион- гамма-глу-цис-гли
Глутатион- гамма-глу-цис-гли
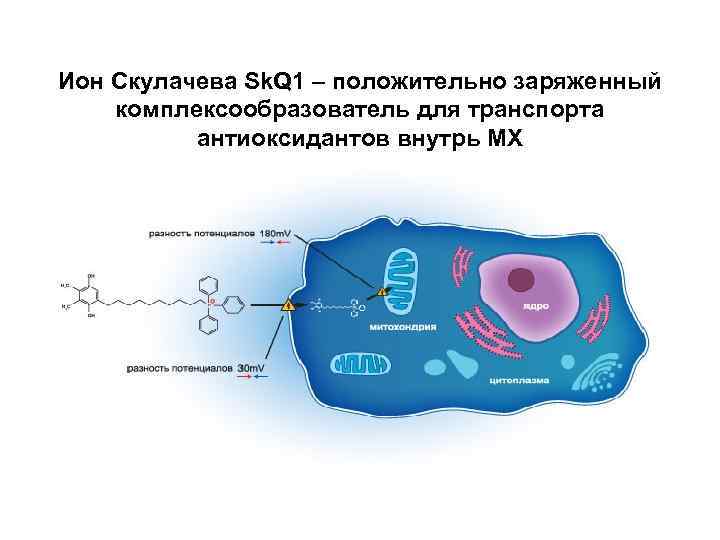
 Ион Скулачева Sk. Q 1 – положительно заряженный комплексообразователь для транспорта антиоксидантов внутрь МХ
Ион Скулачева Sk. Q 1 – положительно заряженный комплексообразователь для транспорта антиоксидантов внутрь МХ
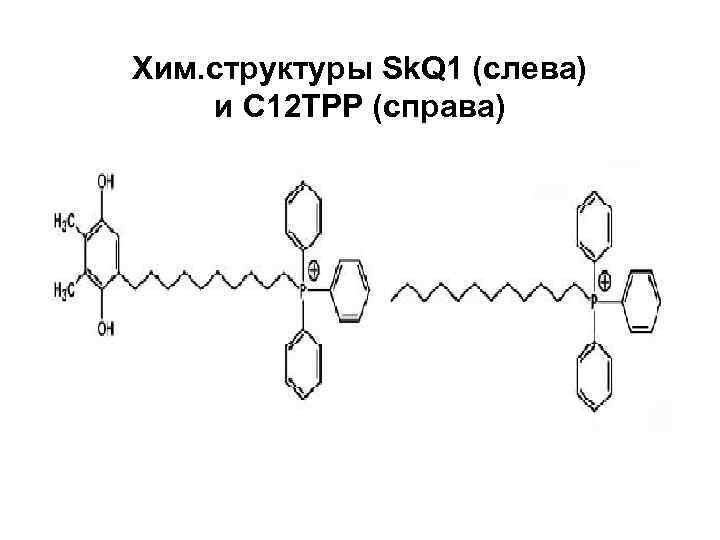
 Хим. структуры Sk. Q 1 (слева) и С 12 ТРР (справа)
Хим. структуры Sk. Q 1 (слева) и С 12 ТРР (справа)
 Препарат Sk. Q 1 - (ион Скулачева) - замедляет развитие признаков старения у мышей, в т. ч. продлевает циклическую эстральную функцию, замедляет развитие остеопороза, поседение • Препарат Sk. Q 1 ( «Ветомитин» ) предназначен для лечения глазных болезней – ретинопатий, врожденной дисплазии, дегенерации сетчатки у животных.
Препарат Sk. Q 1 - (ион Скулачева) - замедляет развитие признаков старения у мышей, в т. ч. продлевает циклическую эстральную функцию, замедляет развитие остеопороза, поседение • Препарат Sk. Q 1 ( «Ветомитин» ) предназначен для лечения глазных болезней – ретинопатий, врожденной дисплазии, дегенерации сетчатки у животных.
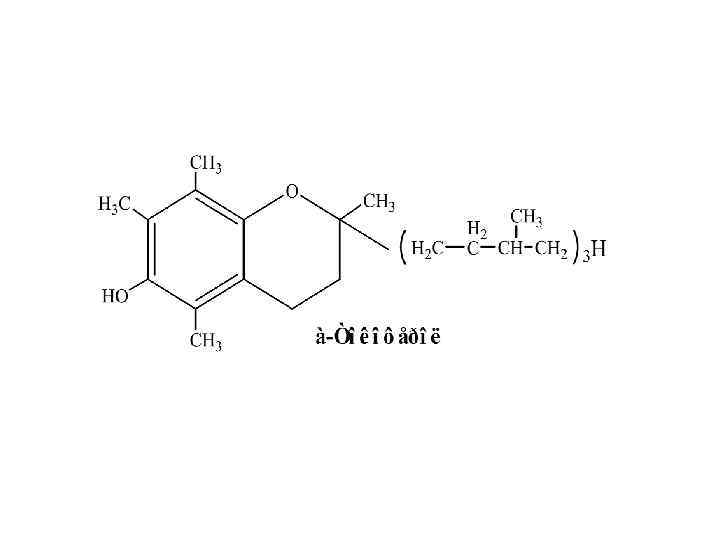
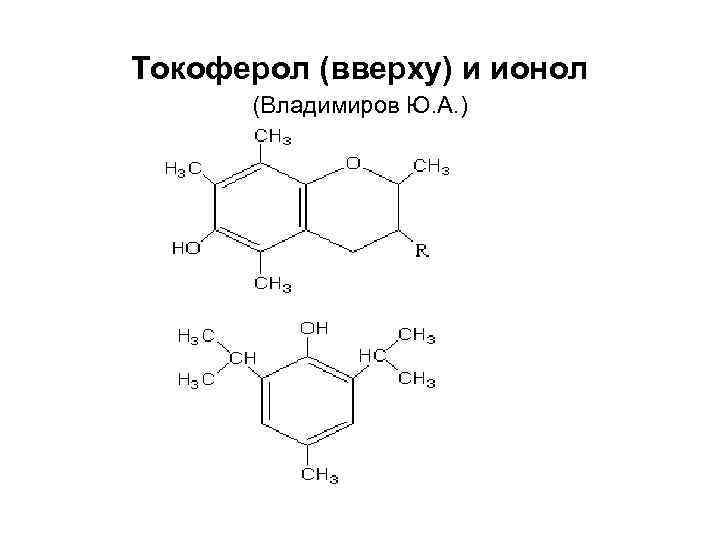
 Токоферол (вверху) и ионол (Владимиров Ю. А. )
Токоферол (вверху) и ионол (Владимиров Ю. А. )
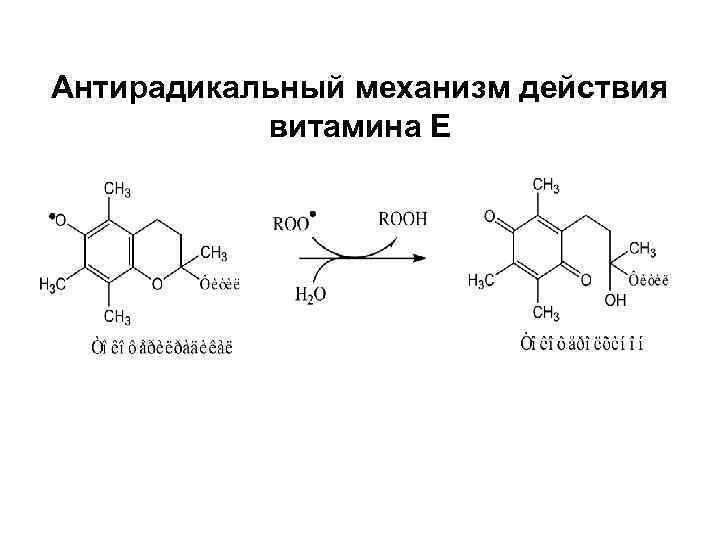
 Антирадикальный механизм действия витамина Е
Антирадикальный механизм действия витамина Е
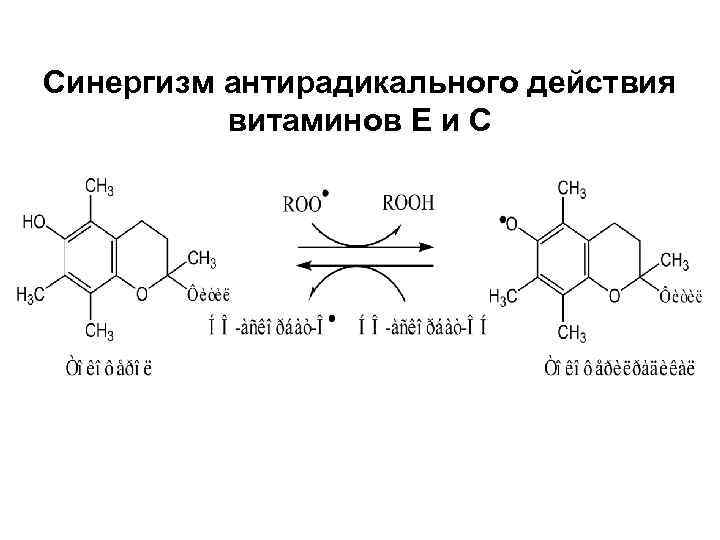
 Синергизм антирадикального действия витаминов Е и С
Синергизм антирадикального действия витаминов Е и С
 Роль холестерина инфаркт ↓ПОЛ ↑ХС↓ ↑ПОЛ опухоль
Роль холестерина инфаркт ↓ПОЛ ↑ХС↓ ↑ПОЛ опухоль
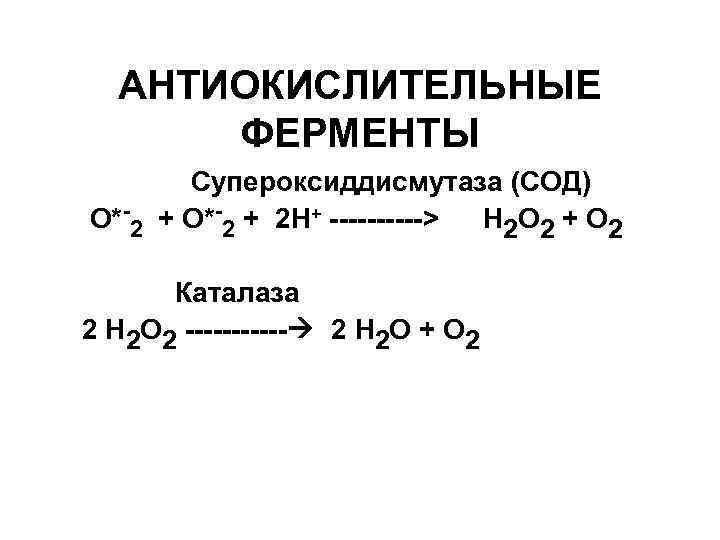
 АНТИОКИСЛИТЕЛЬНЫЕ ФЕРМЕНТЫ Супероксиддисмутаза (СОД) О*-2 + 2 Н+ -----> Н 2 О 2 + О 2 Каталаза 2 Н 2 О 2 ------ 2 Н 2 О + О 2
АНТИОКИСЛИТЕЛЬНЫЕ ФЕРМЕНТЫ Супероксиддисмутаза (СОД) О*-2 + 2 Н+ -----> Н 2 О 2 + О 2 Каталаза 2 Н 2 О 2 ------ 2 Н 2 О + О 2
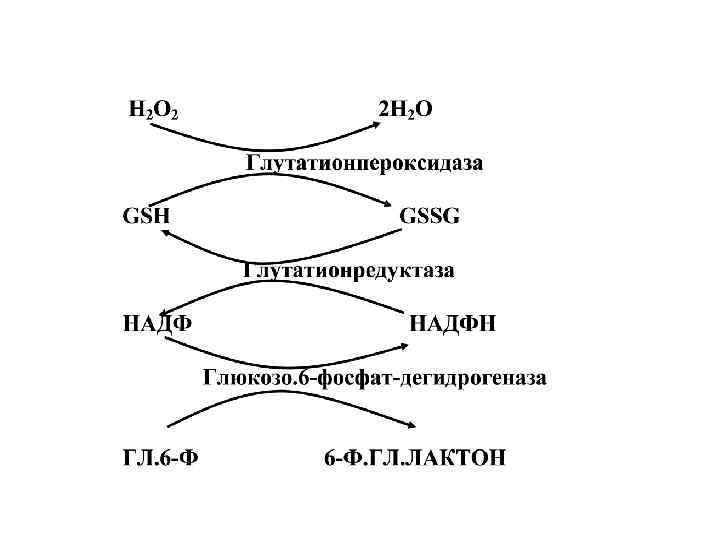
 Пероксидаза Н 2 О 2 + НО-S-ОН -----> 2 Н 2 О + О=S=О, S – субстрат окисления Глутатионпероксидаза (Se ) 2 GSH+ROOH -------> GSSG + ROH+ Н 2 О Глутатионредуктаза GSSG + НАДФН + Н+ ---- 2 GSH + НАДФ+ -------------------------------- Где, GSSG –глутатион окисленный GSH – глутатион восстановленный
Пероксидаза Н 2 О 2 + НО-S-ОН -----> 2 Н 2 О + О=S=О, S – субстрат окисления Глутатионпероксидаза (Se ) 2 GSH+ROOH -------> GSSG + ROH+ Н 2 О Глутатионредуктаза GSSG + НАДФН + Н+ ---- 2 GSH + НАДФ+ -------------------------------- Где, GSSG –глутатион окисленный GSH – глутатион восстановленный
 Фосфолипаза А 2 в мембране отщепляет от фосфолипидов окисленные жирные кислоты ROOH → разрушаются гидроперекиси липидов → предотвращается разветвление цепей окисления → ↓ПОЛ
Фосфолипаза А 2 в мембране отщепляет от фосфолипидов окисленные жирные кислоты ROOH → разрушаются гидроперекиси липидов → предотвращается разветвление цепей окисления → ↓ПОЛ
 Синдром липидной пероксидации • Синонимы: окислительный стресс, оксидативный стресс (липидная триада ? ) – клинико – патогенетический симптомокомплекс, являющийся неотъемлемой частью большинства патологий, развивающийся в связи с относительным преобладанием интенсивности ПОЛ над АОЗ и сопровождающийся выгоранием легкоокисляемых липидов, повышением проницаемости клеточных мембран, инактивацией ферментов, повреждением макромолекул, гемолизом, нарушением пролиферации ткани и ускоренным старением и нуждающийся в целенаправленной коррекции антиоксидантами (автор).
Синдром липидной пероксидации • Синонимы: окислительный стресс, оксидативный стресс (липидная триада ? ) – клинико – патогенетический симптомокомплекс, являющийся неотъемлемой частью большинства патологий, развивающийся в связи с относительным преобладанием интенсивности ПОЛ над АОЗ и сопровождающийся выгоранием легкоокисляемых липидов, повышением проницаемости клеточных мембран, инактивацией ферментов, повреждением макромолекул, гемолизом, нарушением пролиферации ткани и ускоренным старением и нуждающийся в целенаправленной коррекции антиоксидантами (автор).
 Синдром липидной пероксидации N ПОЛ ------- → НОРМА N АОА ↑ ПОЛ ------ → ПАТОЛОГИЯ N АОА ↑ N ПОЛ или ПОЛ -------------- → ПАТОЛОГИЯ ↓АОА
Синдром липидной пероксидации N ПОЛ ------- → НОРМА N АОА ↑ ПОЛ ------ → ПАТОЛОГИЯ N АОА ↑ N ПОЛ или ПОЛ -------------- → ПАТОЛОГИЯ ↓АОА
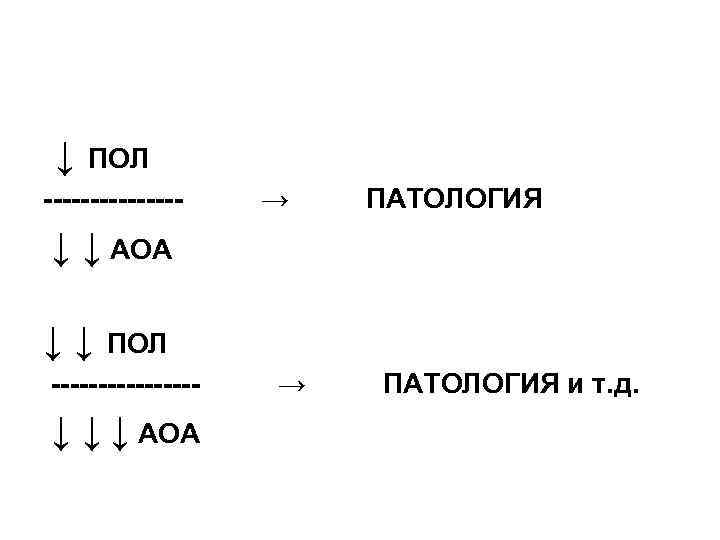
 ↓ ПОЛ -------- → ПАТОЛОГИЯ ↓ ↓ АОА ↓ ↓ ПОЛ -------- → ПАТОЛОГИЯ и т. д. ↓ ↓ ↓ АОА
↓ ПОЛ -------- → ПАТОЛОГИЯ ↓ ↓ АОА ↓ ↓ ПОЛ -------- → ПАТОЛОГИЯ и т. д. ↓ ↓ ↓ АОА
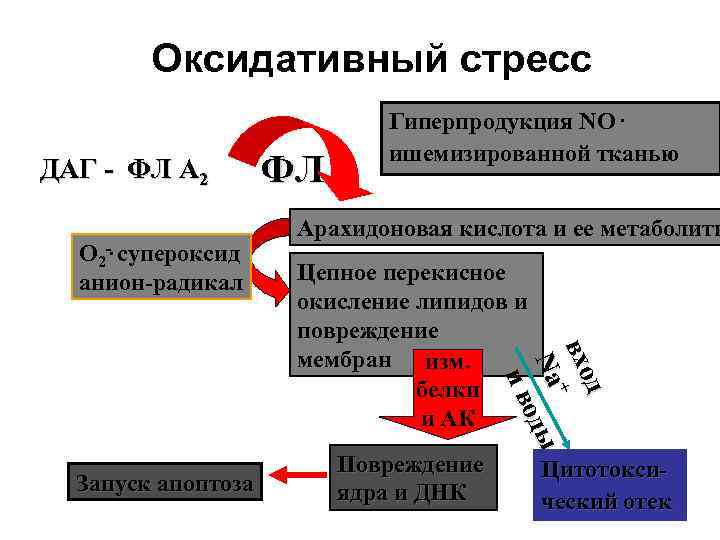
 Оксидативный стресс Гиперпродукция NO. ишемизированной тканью ДАГ - ФЛ A 2 ФЛ Арахидоновая кислота и ее метаболиты О 2 -. супероксид анион-радикал Цепное перекисное окисление липидов и повреждение вхо + мембран изм. Na оды ив белки дд и АК Повреждение Цитотокси- Запуск апоптоза ядра и ДНК ческий отек
Оксидативный стресс Гиперпродукция NO. ишемизированной тканью ДАГ - ФЛ A 2 ФЛ Арахидоновая кислота и ее метаболиты О 2 -. супероксид анион-радикал Цепное перекисное окисление липидов и повреждение вхо + мембран изм. Na оды ив белки дд и АК Повреждение Цитотокси- Запуск апоптоза ядра и ДНК ческий отек
 Практические рекомендации – алгоритм коррекции синдрома Скрининг ПОЛ -> развернутый анализ ПОЛ/АОА -> синдром липидной пероксидации -> назначение АО терапии -> повторное исследование ПОЛ/АОА
Практические рекомендации – алгоритм коррекции синдрома Скрининг ПОЛ -> развернутый анализ ПОЛ/АОА -> синдром липидной пероксидации -> назначение АО терапии -> повторное исследование ПОЛ/АОА
 КЛАССИФИКАЦИЯ АНТИОКСИДАНТОВ: 1. АНТИРАДИКАЛЬНЫЕ СРЕДСТВА ("СКЭВЕНДЖЕРЫ" - ОТ АНГЛ. "SCAVENGERS" - МУСОРЩИКИ): 1. 1. Эндогенные соединения: a-токоферол (витамин Е), кислота аскорбиновая (витамин С), ретинол (витамин А), b-каротин (провитамин А), убихинон (убинон). Механизм действия антирадикальных средств ("скэвенджеров") заключается в прямом взаимодействии со свободными радикалами с их нейтрализацией Наиболее изученное антирадикальное средство - a-токоферол (витамин Е). Витамин Е – природный антиоксидант, защищает различные вещества от окисления, участвует в биосинтезе белков, пролиферации клеток, тканевом дыхании и клеточном метаболизме.
КЛАССИФИКАЦИЯ АНТИОКСИДАНТОВ: 1. АНТИРАДИКАЛЬНЫЕ СРЕДСТВА ("СКЭВЕНДЖЕРЫ" - ОТ АНГЛ. "SCAVENGERS" - МУСОРЩИКИ): 1. 1. Эндогенные соединения: a-токоферол (витамин Е), кислота аскорбиновая (витамин С), ретинол (витамин А), b-каротин (провитамин А), убихинон (убинон). Механизм действия антирадикальных средств ("скэвенджеров") заключается в прямом взаимодействии со свободными радикалами с их нейтрализацией Наиболее изученное антирадикальное средство - a-токоферол (витамин Е). Витамин Е – природный антиоксидант, защищает различные вещества от окисления, участвует в биосинтезе белков, пролиферации клеток, тканевом дыхании и клеточном метаболизме.
 2. АНТИОКСИДАНТНЫЕ ФЕРМЕНТЫ И ИХ АКТИВАТОРЫ: СУПЕРОКСИДДИСМУТАЗА (ЭРИСОД, ОРГОТЕИН), НАТРИЯ СЕЛЕНИТ. 3. БЛОКАТОРЫ СВОБОДНЫХ РАДИКАЛОВ: АНТИГИПОКСАНТЫ. ПОКАЗАНИЯ К ПРИМЕНЕНИЮ АНТИОКСИДАНТОВ: ПРОЦЕССЫ СВОБОДНОРАДИКАЛЬНОГО ОКИСЛЕНИЯ ПРИ РАЗЛИЧНОЙ ПАТОЛОГИИ.
2. АНТИОКСИДАНТНЫЕ ФЕРМЕНТЫ И ИХ АКТИВАТОРЫ: СУПЕРОКСИДДИСМУТАЗА (ЭРИСОД, ОРГОТЕИН), НАТРИЯ СЕЛЕНИТ. 3. БЛОКАТОРЫ СВОБОДНЫХ РАДИКАЛОВ: АНТИГИПОКСАНТЫ. ПОКАЗАНИЯ К ПРИМЕНЕНИЮ АНТИОКСИДАНТОВ: ПРОЦЕССЫ СВОБОДНОРАДИКАЛЬНОГО ОКИСЛЕНИЯ ПРИ РАЗЛИЧНОЙ ПАТОЛОГИИ.
 Принципы построения диагностической панели для оценки показателей ПОЛ 1. Измерение ПОЛ должно производиться по нескольким показателям (диагностическая панель) 2. Параллельно необходимо исследовать показатели АОА 3. Интегральная оценка проводится путем суммирования и усреднения полученных данных по формуле
Принципы построения диагностической панели для оценки показателей ПОЛ 1. Измерение ПОЛ должно производиться по нескольким показателям (диагностическая панель) 2. Параллельно необходимо исследовать показатели АОА 3. Интегральная оценка проводится путем суммирования и усреднения полученных данных по формуле
 • 4. От момента забора биообразца до момента исследования – строго определенное время при стандартных условиях • 5. Исследование патологического процесса и его коррекции проводить в динамике – начало, середина, хвостовая реакция • 6. Единицы измерения показателей – на 1 л сыв. (плазмы) крови, г об. белка, г об. липида, г фосфолипида или ЖК, Т (1012) эритроцитов, г гемоглобина
• 4. От момента забора биообразца до момента исследования – строго определенное время при стандартных условиях • 5. Исследование патологического процесса и его коррекции проводить в динамике – начало, середина, хвостовая реакция • 6. Единицы измерения показателей – на 1 л сыв. (плазмы) крови, г об. белка, г об. липида, г фосфолипида или ЖК, Т (1012) эритроцитов, г гемоглобина
 • 7. Одновременное исследование ранних и поздних продуктов ПОЛ, водо и липидо- растворимых антиоксидантов, ферментативных и неферментативных АО. • 8. Синхронное изучение биообразцов в контрольной и исследуемой группе пациентов
• 7. Одновременное исследование ранних и поздних продуктов ПОЛ, водо и липидо- растворимых антиоксидантов, ферментативных и неферментативных АО. • 8. Синхронное изучение биообразцов в контрольной и исследуемой группе пациентов
 • 9. Соблюдение и учет всех общих принципов лаб диагностики (стабильность метаболического состояния, предупреждение ошибок пре -, аналитического и пост- аналитического этапа). • 10. Статистический анализ полученных данных непараметрическими и параметрическими методами
• 9. Соблюдение и учет всех общих принципов лаб диагностики (стабильность метаболического состояния, предупреждение ошибок пре -, аналитического и пост- аналитического этапа). • 10. Статистический анализ полученных данных непараметрическими и параметрическими методами
 Лабораторные показатели ПОЛ • МДА –малоновый диальдегид • ДК – диеновые конъюгаты • ГП – гидроперекиси • ХЛ – хемилюминесценция • а. спонтанная в. индуцированная • Шиффовы основания • Газы – этан, пентан
Лабораторные показатели ПОЛ • МДА –малоновый диальдегид • ДК – диеновые конъюгаты • ГП – гидроперекиси • ХЛ – хемилюминесценция • а. спонтанная в. индуцированная • Шиффовы основания • Газы – этан, пентан
 Люминометр - фотометр Lucy 3 (Anthos Labtec Instruments) США и анализатор АОА
Люминометр - фотометр Lucy 3 (Anthos Labtec Instruments) США и анализатор АОА
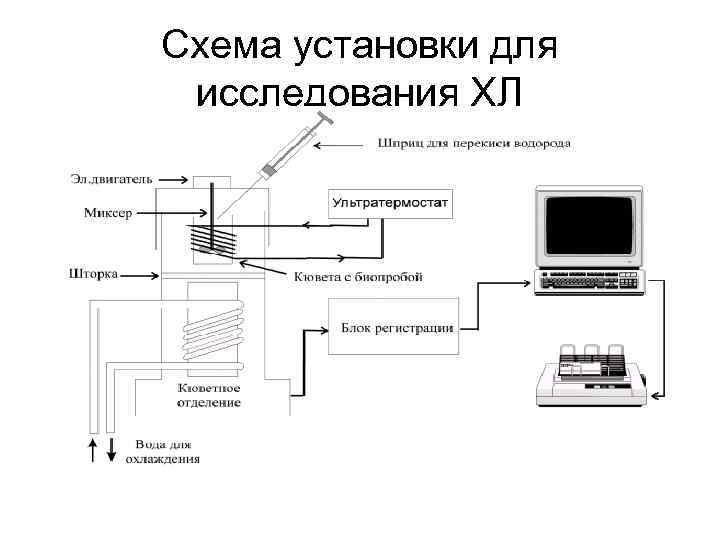
 Схема установки для исследования ХЛ
Схема установки для исследования ХЛ
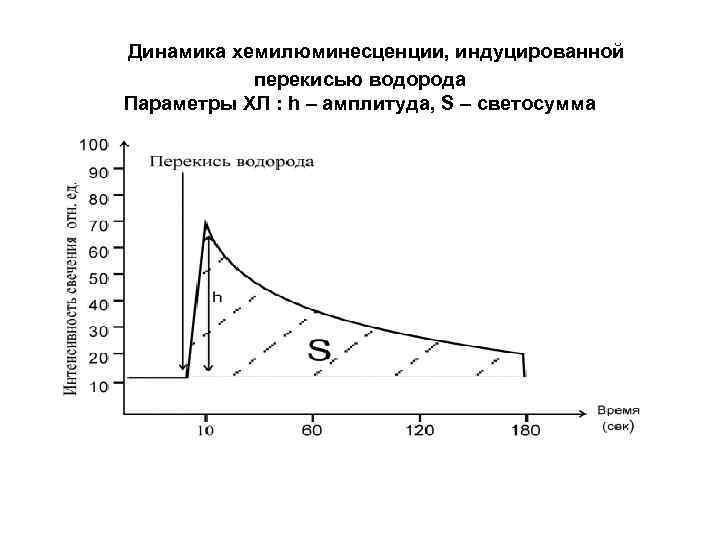
 Динамика хемилюминесценции, индуцированной перекисью водорода Параметры ХЛ : h – амплитуда, S – светосумма
Динамика хемилюминесценции, индуцированной перекисью водорода Параметры ХЛ : h – амплитуда, S – светосумма
 Лабораторные показатели АОА • Активность антиокислительных ферментов • Витамины С, Е, А • Мочевая кислота • Глутатион • Церулоплазмин • Трансферрин • Ферритин • Лактоферрин
Лабораторные показатели АОА • Активность антиокислительных ферментов • Витамины С, Е, А • Мочевая кислота • Глутатион • Церулоплазмин • Трансферрин • Ферритин • Лактоферрин
 Антиоксиданты крови и цитоплазмы • Церулоплазмин -окисляет Fe 2+ до Fe 3+ молекулярным кислородом • Апо-белок трансферрина - связывает Fe 3+ • Ферритин - окисляет Fe 2+ и депонирует Fe 3+ • Карнозин - связывает Fe 2+
Антиоксиданты крови и цитоплазмы • Церулоплазмин -окисляет Fe 2+ до Fe 3+ молекулярным кислородом • Апо-белок трансферрина - связывает Fe 3+ • Ферритин - окисляет Fe 2+ и депонирует Fe 3+ • Карнозин - связывает Fe 2+
 Оборудование Автоматический Спектрофотометр биохимический и сканирующий иммуноферментный UNICO-2802 анализатор Chem (UNICO, Япония) Well (Combi), (Awareness Technologi, США)
Оборудование Автоматический Спектрофотометр биохимический и сканирующий иммуноферментный UNICO-2802 анализатор Chem (UNICO, Япония) Well (Combi), (Awareness Technologi, США)
 Биофотонный сканер Pharmanex S 2 определяет уровень антиоксидантной защиты организма ? ? ?
Биофотонный сканер Pharmanex S 2 определяет уровень антиоксидантной защиты организма ? ? ?
 Интегральные показатели перекисного окисления липидов и антиокислительной активности (ПОЛ/АОА) 1. КАОЗ – коэффициент антиокислительной защиты (Нагорнев С. Н. с соавт. , 1996) 2. КПОЛ – коэффициент перекисного окисления липидов. 3. КАОА - коэффициент антиокислительной активности
Интегральные показатели перекисного окисления липидов и антиокислительной активности (ПОЛ/АОА) 1. КАОЗ – коэффициент антиокислительной защиты (Нагорнев С. Н. с соавт. , 1996) 2. КПОЛ – коэффициент перекисного окисления липидов. 3. КАОА - коэффициент антиокислительной активности
 • Нагорнев С. Н. Фармакологическая коррекция процесса липопероксидации при гипоксии и возможность повышения высотной устойчивости человека с помощью препаратов метаболического типа действия / С. Н. Нагорнев, С. И. Сытник, И. П. Боровницкий // Вестн. Рос. АМН. - 1996. - № 7. - С. 53 – 60. • А. П. ЯСТРЕБОВ, В. Н. МЕЩАНИНОВ. – Старение, перекисное окисление липидов и биовозраст. - Екатеринбург. - 2005. – 245 с.
• Нагорнев С. Н. Фармакологическая коррекция процесса липопероксидации при гипоксии и возможность повышения высотной устойчивости человека с помощью препаратов метаболического типа действия / С. Н. Нагорнев, С. И. Сытник, И. П. Боровницкий // Вестн. Рос. АМН. - 1996. - № 7. - С. 53 – 60. • А. П. ЯСТРЕБОВ, В. Н. МЕЩАНИНОВ. – Старение, перекисное окисление липидов и биовозраст. - Екатеринбург. - 2005. – 245 с.
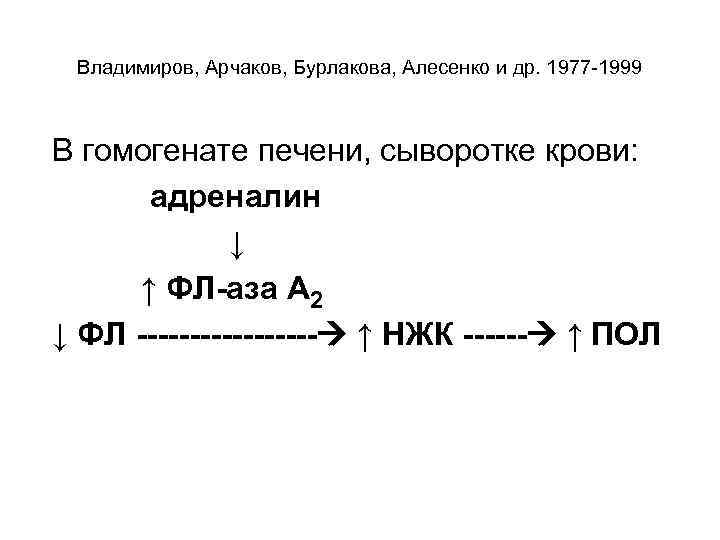
 Владимиров, Арчаков, Бурлакова, Алесенко и др. 1977 -1999 В гомогенате печени, сыворотке крови: адреналин ↓ ↑ ФЛ-аза А 2 ↓ ФЛ --------- ↑ НЖК ------ ↑ ПОЛ
Владимиров, Арчаков, Бурлакова, Алесенко и др. 1977 -1999 В гомогенате печени, сыворотке крови: адреналин ↓ ↑ ФЛ-аза А 2 ↓ ФЛ --------- ↑ НЖК ------ ↑ ПОЛ
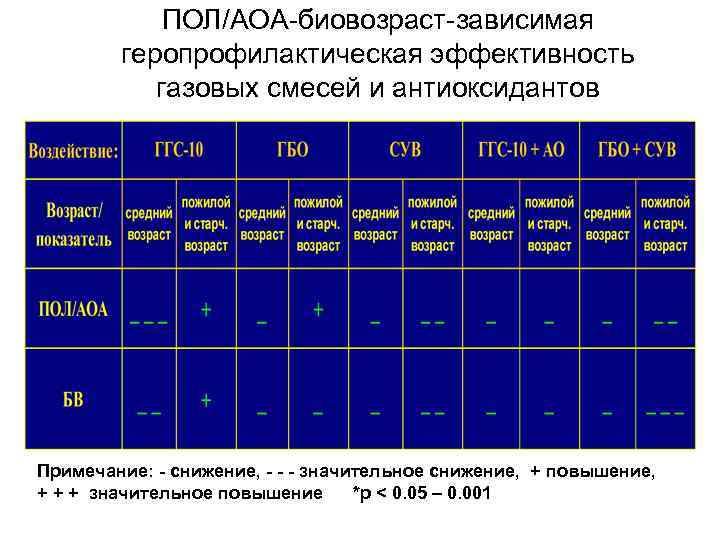
 ПОЛ/АОА-биовозраст-зависимая геропрофилактическая эффективность газовых смесей и антиоксидантов Примечание: - снижение, - - - значительное снижение, + повышение, + + + значительное повышение *р < 0. 05 – 0. 001
ПОЛ/АОА-биовозраст-зависимая геропрофилактическая эффективность газовых смесей и антиоксидантов Примечание: - снижение, - - - значительное снижение, + повышение, + + + значительное повышение *р < 0. 05 – 0. 001
 Механизм антиоксидантного и геропрофилактического действия озонотерапии у пациентов разного возраста • АФК→ зрелые → →↓ПОЛ→↑АОА→↓БВ • АФК→ пожилые →↑ПОЛ→↓АОА → ↑ гемолиз эритроцитов → = БВ Где БВ – биологический возраст
Механизм антиоксидантного и геропрофилактического действия озонотерапии у пациентов разного возраста • АФК→ зрелые → →↓ПОЛ→↑АОА→↓БВ • АФК→ пожилые →↑ПОЛ→↓АОА → ↑ гемолиз эритроцитов → = БВ Где БВ – биологический возраст
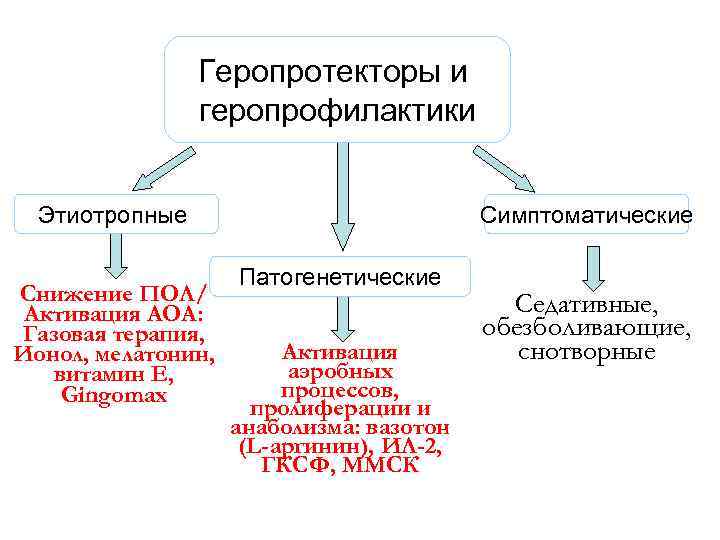
 Геропротекторы и геропрофилактики Этиотропные Симптоматические Патогенетические Снижение ПОЛ/ Седативные, Активация АОА: Газовая терапия, обезболивающие, Ионол, мелатонин, Активация снотворные витамин Е, аэробных Gingomax процессов, пролиферации и анаболизма: вазотон (L-аргинин), ИЛ-2, ГКСФ, ММСК
Геропротекторы и геропрофилактики Этиотропные Симптоматические Патогенетические Снижение ПОЛ/ Седативные, Активация АОА: Газовая терапия, обезболивающие, Ионол, мелатонин, Активация снотворные витамин Е, аэробных Gingomax процессов, пролиферации и анаболизма: вазотон (L-аргинин), ИЛ-2, ГКСФ, ММСК
 Спасибо за внимание!
Спасибо за внимание!




















