Окислительный стресс 19Feb10.ppt
- Количество слайдов: 32
 Окислительный стресс в мышечной ткани: изучение посттрансляционных модификаций белков методами протеомики Н. В. Кулева. Кафедра биохимии СПб. ГУ
Окислительный стресс в мышечной ткани: изучение посттрансляционных модификаций белков методами протеомики Н. В. Кулева. Кафедра биохимии СПб. ГУ
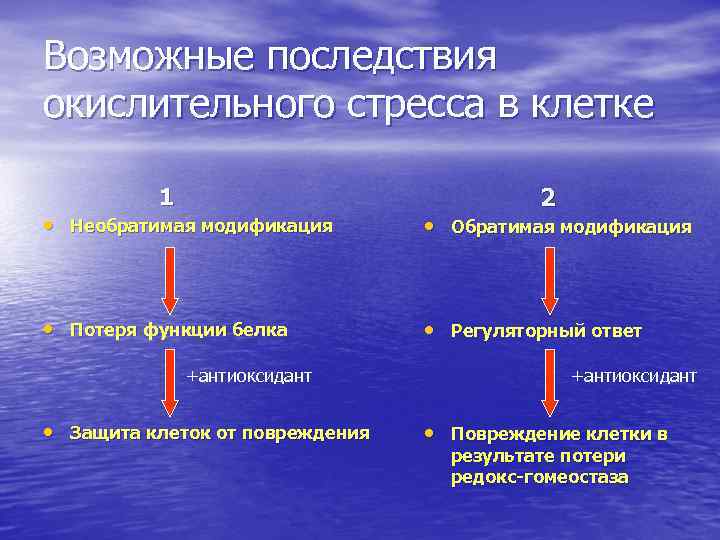 Возможные последствия окислительного стресса в клетке 1 • Необратимая модификация 2 • Обратимая модификация • Потеря функции белка • Регуляторный ответ +антиоксидант • Защита клеток от повреждения +антиоксидант • Повреждение клетки в результате потери редокс-гомеостаза
Возможные последствия окислительного стресса в клетке 1 • Необратимая модификация 2 • Обратимая модификация • Потеря функции белка • Регуляторный ответ +антиоксидант • Защита клеток от повреждения +антиоксидант • Повреждение клетки в результате потери редокс-гомеостаза
 Превращение оксидантного сигнала в регуляторный ответ Ключом к превращению регуляторного сигнала в регуляторный ответ являются окислительные модификации белков, которые приводят к изменению их функций и их взаимодействий с другими белками. Здесь присутствуют все элементы регуляторной системы: чувствительность, специфичность, обратимость.
Превращение оксидантного сигнала в регуляторный ответ Ключом к превращению регуляторного сигнала в регуляторный ответ являются окислительные модификации белков, которые приводят к изменению их функций и их взаимодействий с другими белками. Здесь присутствуют все элементы регуляторной системы: чувствительность, специфичность, обратимость.
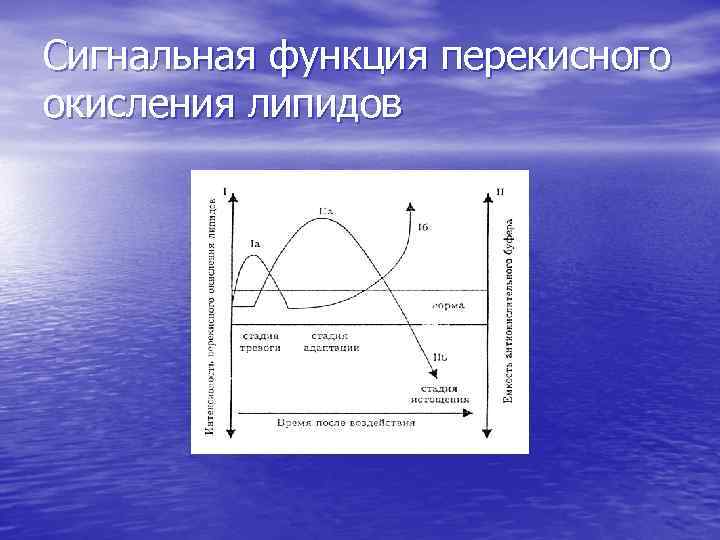 Сигнальная функция перекисного окисления липидов
Сигнальная функция перекисного окисления липидов
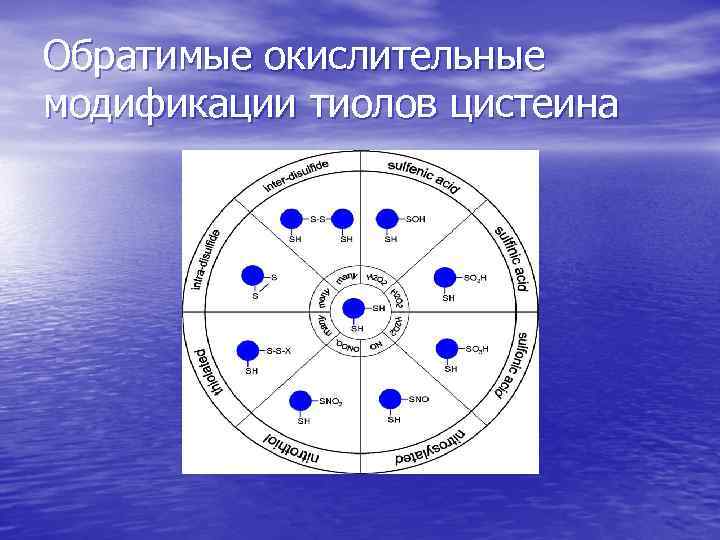 Обратимые окислительные модификации тиолов цистеина
Обратимые окислительные модификации тиолов цистеина
 Окисление тиолов цистеина Модификация Следствие 1. Глутатионилирование актина Торможение полимеризации, защита цитоскелета 2. Образование дисульфидов у регуляторной субъединицы ПК А Активация ПК А 3. Образование дисульфидов у регуляторной субъединицы ПК G 1α Активация белка, связанного с релаксацией сосудов 4. Цистеинилирование ПК С Регуляция активности
Окисление тиолов цистеина Модификация Следствие 1. Глутатионилирование актина Торможение полимеризации, защита цитоскелета 2. Образование дисульфидов у регуляторной субъединицы ПК А Активация ПК А 3. Образование дисульфидов у регуляторной субъединицы ПК G 1α Активация белка, связанного с релаксацией сосудов 4. Цистеинилирование ПК С Регуляция активности
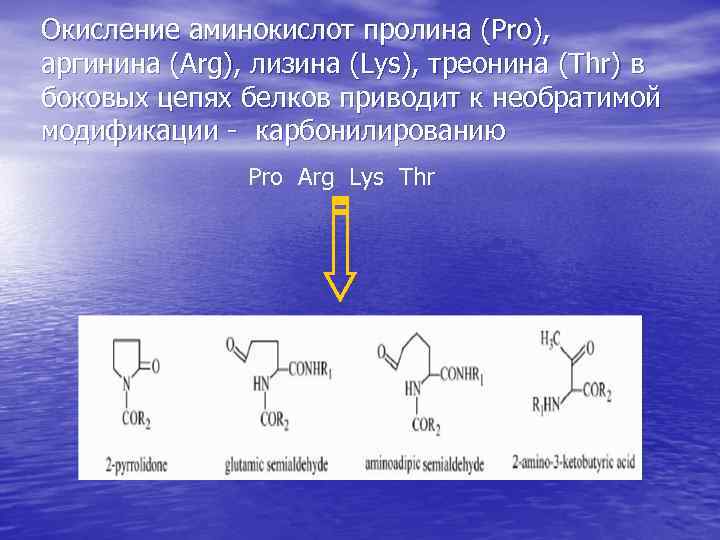 Окисление аминокислот пролина (Pro), аргинина (Arg), лизина (Lys), треонина (Thr) в боковых цепях белков приводит к необратимой модификации - карбонилированию Pro Arg Lys Thr
Окисление аминокислот пролина (Pro), аргинина (Arg), лизина (Lys), треонина (Thr) в боковых цепях белков приводит к необратимой модификации - карбонилированию Pro Arg Lys Thr
 Протеомика и окислительновосстановительная (редокс) сигнализация Биохимические методы для изучения редокссигнализации применимы только тогда, когда установлен редокс-чувствительный белок. Поэтому возникает необходимость глобально следить за всеми редокс-превращениями белков в клетке. Такой мониторинг в настоящее время возможен в связи с развитием протеомики.
Протеомика и окислительновосстановительная (редокс) сигнализация Биохимические методы для изучения редокссигнализации применимы только тогда, когда установлен редокс-чувствительный белок. Поэтому возникает необходимость глобально следить за всеми редокс-превращениями белков в клетке. Такой мониторинг в настоящее время возможен в связи с развитием протеомики.
 Термин «ПРОТЕОМ» , обозначающий белковый комплемент генома (в английской транскрипции PROTEOME: entire PROTEin complement expressed by the gen. OME), впервые прозвучал в докладах Международной конференции “ 2 D-Electrophoresis: from Peptide Maps to Genomes” в Италии в 1994 г. Теперь термины «протеом» и «протеомика» стали общепринятыми. Cтратегию протеомных исследований для какого-либо объекта можно представить в виде ряда последовательно реализуемых этапов, ключевые позиции среди которых занимают метод двухмерного электрофореза белков, идентификация их с помощью масс-спектрометрии и построение компьютерных банков данных. Роль современной протеомики может быть определена как интегральный анализ функционального состояния генома на уровне белковых продуктов генной экспрессии, включающий их посттрансляционные модификации.
Термин «ПРОТЕОМ» , обозначающий белковый комплемент генома (в английской транскрипции PROTEOME: entire PROTEin complement expressed by the gen. OME), впервые прозвучал в докладах Международной конференции “ 2 D-Electrophoresis: from Peptide Maps to Genomes” в Италии в 1994 г. Теперь термины «протеом» и «протеомика» стали общепринятыми. Cтратегию протеомных исследований для какого-либо объекта можно представить в виде ряда последовательно реализуемых этапов, ключевые позиции среди которых занимают метод двухмерного электрофореза белков, идентификация их с помощью масс-спектрометрии и построение компьютерных банков данных. Роль современной протеомики может быть определена как интегральный анализ функционального состояния генома на уровне белковых продуктов генной экспрессии, включающий их посттрансляционные модификации.
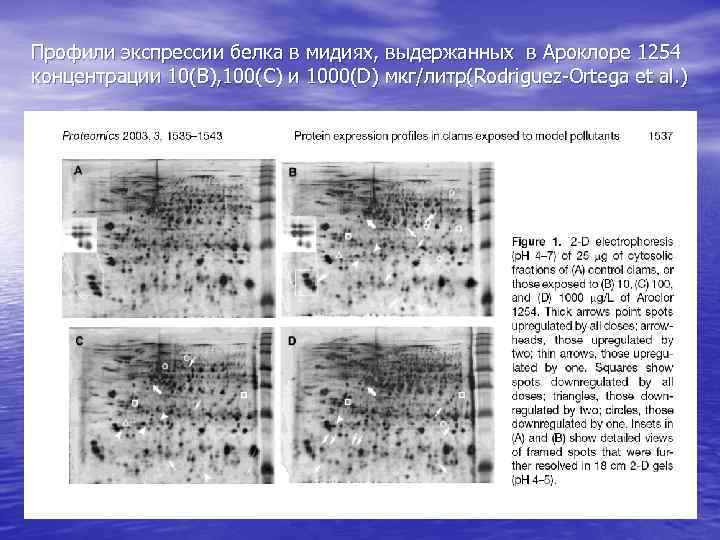 Профили экспрессии белка в мидиях, выдержанных в Ароклоре 1254 концентрации 10(В), 100(C) и 1000(D) мкг/литр(Rodriguez-Ortega et al. )
Профили экспрессии белка в мидиях, выдержанных в Ароклоре 1254 концентрации 10(В), 100(C) и 1000(D) мкг/литр(Rodriguez-Ortega et al. )
 Общая схема реализации протеомного подхода Операция 1. Сбор и приготовление образцов 2. Краткое описание методических приемов Различные приемы солюбилизации белков изучаемого объекта. Использование мочевины, тиомочевины, CHAPS, сульфобетаина, тритона Х-114 и др. детергентов, а также различных ингибиторов протеиназ Фракционирование белков посредством двухмерного электрофореза 3. 4. II стадия – изоэлектрофокусирование на полиакриламидном геле. Использование различных вариантов иммобилинов, создающих на полосках полиакриламидного геля иммобилизованный градиент р. Н (IPG). II стадия – электрофорез разделенных изоэлектрофокусированием белков во II направлении на полиакриламидном геле с додецилсульфатом натрия. Детекция белков на двухмерной электрофореграмме Окраска белковых пятен Кумасси R 250, серебрением, Кумасси другими красителями или авторадиография Сопоставление двумерных белковых карт при различных воздействиях на объект исследования Использование компьютерного анализа изображений. Выявление изменений в белковых картах при воздействии токсикантов Идентификация белков, экспрессия которых изменилась под действием токсикантов Масс-спектрометрия трипсиновых гидролизатов вырезанных из геля и экстрагированных белковых пятен; Использование компьютерных баз данных в Интернете (Swiss-Prot, NCBI и др. ); Микросеквинирование; Swiss- Prot, NCBI и др. ); Микросеквинирование; Иммуноблоттинг 5.
Общая схема реализации протеомного подхода Операция 1. Сбор и приготовление образцов 2. Краткое описание методических приемов Различные приемы солюбилизации белков изучаемого объекта. Использование мочевины, тиомочевины, CHAPS, сульфобетаина, тритона Х-114 и др. детергентов, а также различных ингибиторов протеиназ Фракционирование белков посредством двухмерного электрофореза 3. 4. II стадия – изоэлектрофокусирование на полиакриламидном геле. Использование различных вариантов иммобилинов, создающих на полосках полиакриламидного геля иммобилизованный градиент р. Н (IPG). II стадия – электрофорез разделенных изоэлектрофокусированием белков во II направлении на полиакриламидном геле с додецилсульфатом натрия. Детекция белков на двухмерной электрофореграмме Окраска белковых пятен Кумасси R 250, серебрением, Кумасси другими красителями или авторадиография Сопоставление двумерных белковых карт при различных воздействиях на объект исследования Использование компьютерного анализа изображений. Выявление изменений в белковых картах при воздействии токсикантов Идентификация белков, экспрессия которых изменилась под действием токсикантов Масс-спектрометрия трипсиновых гидролизатов вырезанных из геля и экстрагированных белковых пятен; Использование компьютерных баз данных в Интернете (Swiss-Prot, NCBI и др. ); Микросеквинирование; Swiss- Prot, NCBI и др. ); Микросеквинирование; Иммуноблоттинг 5.
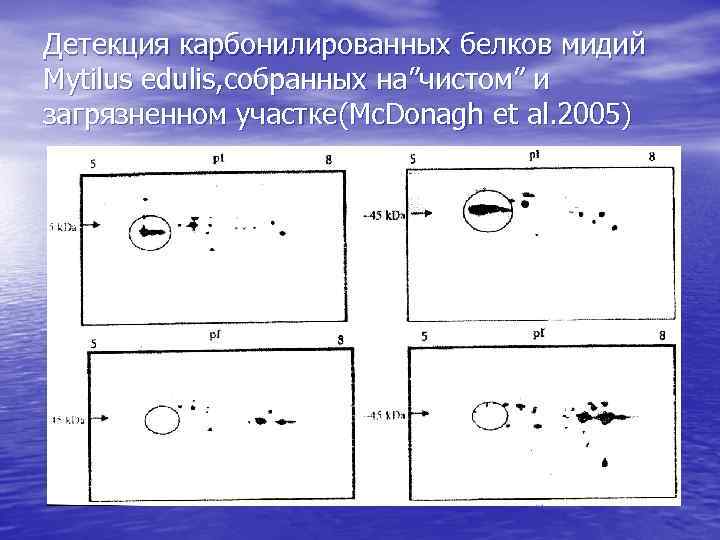 Детекция карбонилированных белков мидий Mytilus edulis, собранных на”чистом” и загрязненном участке(Mc. Donagh et al. 2005)
Детекция карбонилированных белков мидий Mytilus edulis, собранных на”чистом” и загрязненном участке(Mc. Donagh et al. 2005)
 Обнаружение карбонилированных белков методом иммуноблоттинга Коричневое окрашивание +Н 2 О 2 +диаминобензидин Вторичные антитела (с пероксидазой хрена) Кроличьи антитела к ДНФГ Динитрофенилгидразин (ДНФГ) СО- группы белка
Обнаружение карбонилированных белков методом иммуноблоттинга Коричневое окрашивание +Н 2 О 2 +диаминобензидин Вторичные антитела (с пероксидазой хрена) Кроличьи антитела к ДНФГ Динитрофенилгидразин (ДНФГ) СО- группы белка
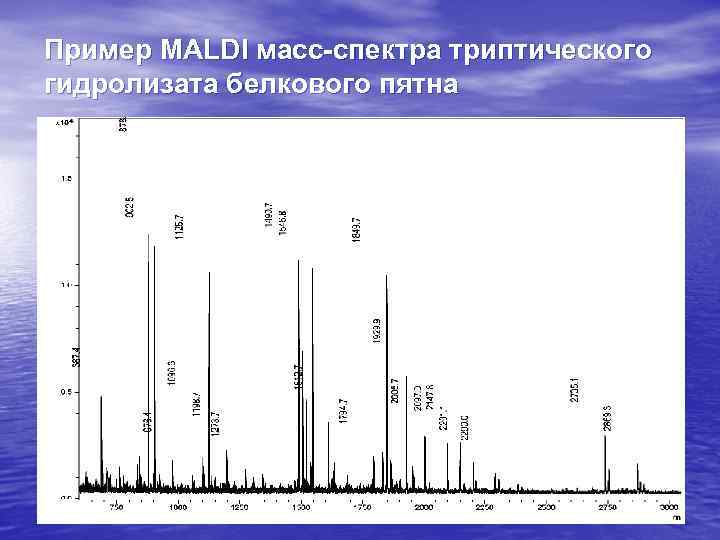 Пример MALDI масс-спектра триптического гидролизата белкового пятна
Пример MALDI масс-спектра триптического гидролизата белкового пятна
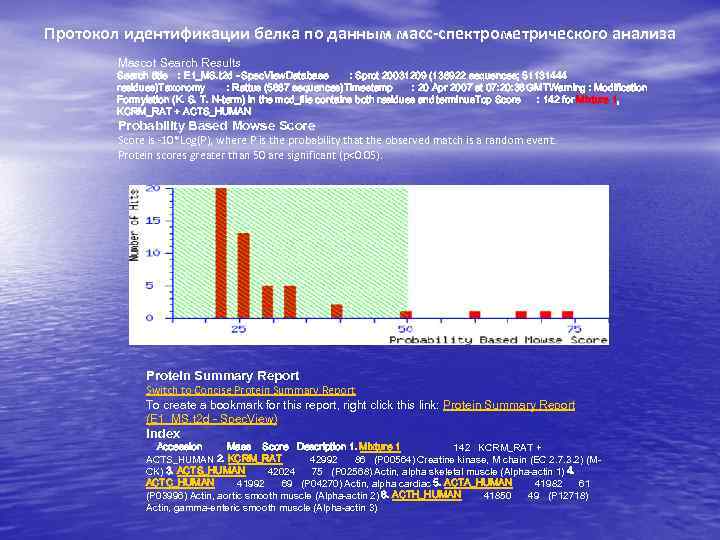 Протокол идентификации белка по данным масс-спектрометрического анализа Mascot Search Results Search title : E 1_MS. t 2 d - Spec. View. Database : Sprot 20031209 (138922 sequences; 51131444 residues)Taxonomy : Rattus (5687 sequences)Timestamp : 20 Apr 2007 at 07: 20: 36 GMTWarning : Modification Formylation (K. S. T. N-term) in the mod_file contains both residues and terminus. Top Score : 142 for Mixture 1, KCRM_RAT + ACTS_HUMAN Probability Based Mowse Score is -10*Log(P), where P is the probability that the observed match is a random event. Protein scores greater than 50 are significant (p<0. 05). Protein Summary Report Switch to Concise Protein Summary Report To create a bookmark for this report, right click this link: Protein Summary Report (E 1_MS. t 2 d - Spec. View) Index Accession Mass Score Description 1. Mixture 1 142 KCRM_RAT + ACTS_HUMAN 2. KCRM_RAT 42992 86 (P 00564) Creatine kinase, M chain (EC 2. 7. 3. 2) (MCK) 3. ACTS_HUMAN 42024 75 (P 02568) Actin, alpha skeletal muscle (Alpha-actin 1) 4. ACTC_HUMAN 41992 69 (P 04270) Actin, alpha cardiac 5. ACTA_HUMAN 41982 61 (P 03996) Actin, aortic smooth muscle (Alpha-actin 2) 6. ACTH_HUMAN 41850 49 (P 12718) Actin, gamma-enteric smooth muscle (Alpha-actin 3)
Протокол идентификации белка по данным масс-спектрометрического анализа Mascot Search Results Search title : E 1_MS. t 2 d - Spec. View. Database : Sprot 20031209 (138922 sequences; 51131444 residues)Taxonomy : Rattus (5687 sequences)Timestamp : 20 Apr 2007 at 07: 20: 36 GMTWarning : Modification Formylation (K. S. T. N-term) in the mod_file contains both residues and terminus. Top Score : 142 for Mixture 1, KCRM_RAT + ACTS_HUMAN Probability Based Mowse Score is -10*Log(P), where P is the probability that the observed match is a random event. Protein scores greater than 50 are significant (p<0. 05). Protein Summary Report Switch to Concise Protein Summary Report To create a bookmark for this report, right click this link: Protein Summary Report (E 1_MS. t 2 d - Spec. View) Index Accession Mass Score Description 1. Mixture 1 142 KCRM_RAT + ACTS_HUMAN 2. KCRM_RAT 42992 86 (P 00564) Creatine kinase, M chain (EC 2. 7. 3. 2) (MCK) 3. ACTS_HUMAN 42024 75 (P 02568) Actin, alpha skeletal muscle (Alpha-actin 1) 4. ACTC_HUMAN 41992 69 (P 04270) Actin, alpha cardiac 5. ACTA_HUMAN 41982 61 (P 03996) Actin, aortic smooth muscle (Alpha-actin 2) 6. ACTH_HUMAN 41850 49 (P 12718) Actin, gamma-enteric smooth muscle (Alpha-actin 3)
 Мониторинг стресса, сопровождающегося окислением цистеина, методом диагонального электрофореза
Мониторинг стресса, сопровождающегося окислением цистеина, методом диагонального электрофореза
 REVERSIBLE AND IRREVERSIBLE MODIFICATIONS OF SKELETAL MUSCLE PROTEINS IN A RAT MODEL OF ACUTE OXIDATIVE STRESS. Maria Fedorova 1, Nadezhda Kuleva 2 and Ralf Hoffmann 1, * (BBA-Molecular Basis of Disease-V. 179, i. 12, p. 11851193, 2009) 1 Institute of Bioanalytical Chemistry, Center for Biotechnology and Biomedicine, Faculty of Chemistry and Mineralogy, Leipzig University, Deutscher Platz 5, 04103 Leipzig, Germany 2 St. Petersburg State University, Department of Biochemistry, Faculty of Biology and Soil Science, Universitetskaya nab. 7/9, 199034 St. Petersburg, Russia
REVERSIBLE AND IRREVERSIBLE MODIFICATIONS OF SKELETAL MUSCLE PROTEINS IN A RAT MODEL OF ACUTE OXIDATIVE STRESS. Maria Fedorova 1, Nadezhda Kuleva 2 and Ralf Hoffmann 1, * (BBA-Molecular Basis of Disease-V. 179, i. 12, p. 11851193, 2009) 1 Institute of Bioanalytical Chemistry, Center for Biotechnology and Biomedicine, Faculty of Chemistry and Mineralogy, Leipzig University, Deutscher Platz 5, 04103 Leipzig, Germany 2 St. Petersburg State University, Department of Biochemistry, Faculty of Biology and Soil Science, Universitetskaya nab. 7/9, 199034 St. Petersburg, Russia
 Оксидативный стресс был вызван рентгеновским облучением крыс в дозе 5 Гр. Через 3, 9 и 24 часа после облучения крыс декапитировали, а мышцы задних конечностей измельчали и экстрагировали раствором высокой ионной силы. Затем белки осаждали ацетоном и растворяли в 2 м. М Трис-буфере р. Н 7. 5 с 0. 2 м. М хлоридом кальция. Нерастворившийся осадок удаляли центрифугированием. Концентрацию белка определяли методом Бредфорда. Актин осаждалили из мышечного экстракта посредством полимеризации при добавлении хлористого калия до 0. 1 М и хлористого магния до 2 м. М и центрифугирования в течение 2 час при 100 000 g пеллеты представляли собой фибриллярный (функциональный) актин.
Оксидативный стресс был вызван рентгеновским облучением крыс в дозе 5 Гр. Через 3, 9 и 24 часа после облучения крыс декапитировали, а мышцы задних конечностей измельчали и экстрагировали раствором высокой ионной силы. Затем белки осаждали ацетоном и растворяли в 2 м. М Трис-буфере р. Н 7. 5 с 0. 2 м. М хлоридом кальция. Нерастворившийся осадок удаляли центрифугированием. Концентрацию белка определяли методом Бредфорда. Актин осаждалили из мышечного экстракта посредством полимеризации при добавлении хлористого калия до 0. 1 М и хлористого магния до 2 м. М и центрифугирования в течение 2 час при 100 000 g пеллеты представляли собой фибриллярный (функциональный) актин.
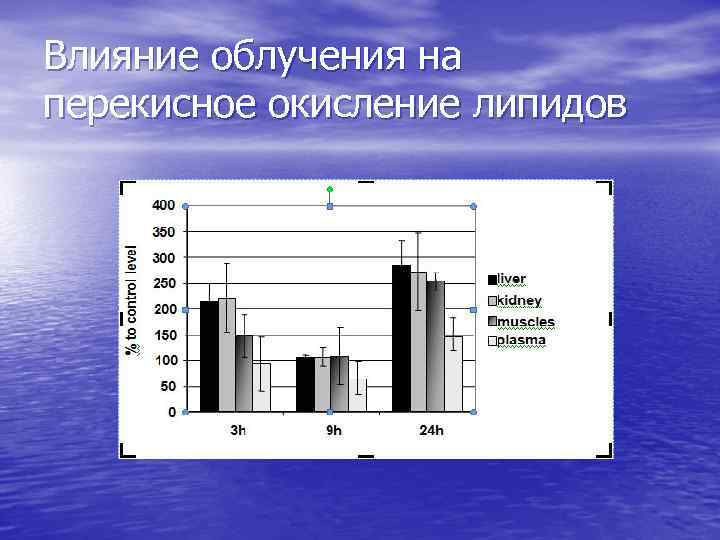 Влияние облучения на перекисное окисление липидов
Влияние облучения на перекисное окисление липидов
 Пострадиационное изменение И экспрессии мышечных белков з
Пострадиационное изменение И экспрессии мышечных белков з
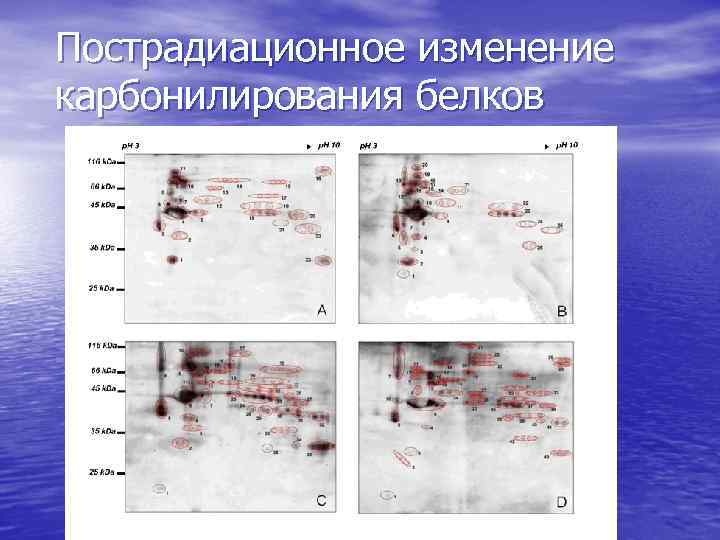 Пострадиационное изменение карбонилирования белков
Пострадиационное изменение карбонилирования белков
 Заключение по экспрессии и карбонилированию белков • 35 из 440 пятен изменяют свою • • интенсивность после облучения; Карбонилированию подвергаются 36 белков, из них 20 карбонилировано в контроле; По степени карбонилирования и количеству белка изменения различны, что показывает их зависимость от различных факторов: нейтрализации АФК, деградации и синтеза белка.
Заключение по экспрессии и карбонилированию белков • 35 из 440 пятен изменяют свою • • интенсивность после облучения; Карбонилированию подвергаются 36 белков, из них 20 карбонилировано в контроле; По степени карбонилирования и количеству белка изменения различны, что показывает их зависимость от различных факторов: нейтрализации АФК, деградации и синтеза белка.
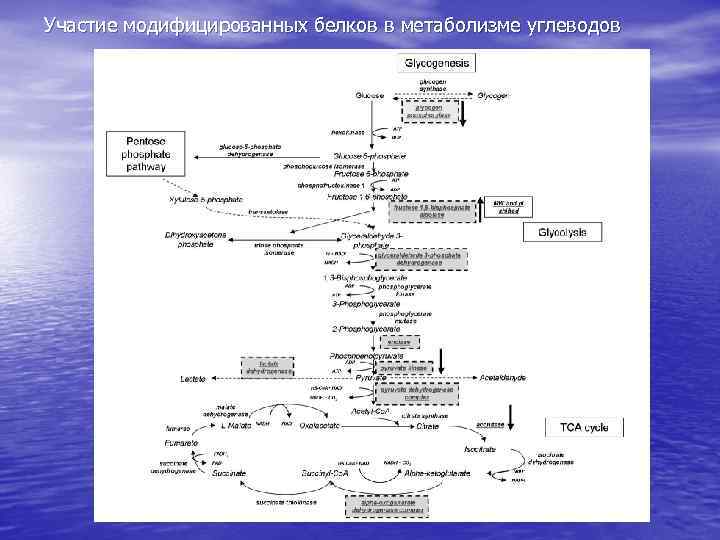 Участие модифицированных белков в метаболизме углеводов
Участие модифицированных белков в метаболизме углеводов
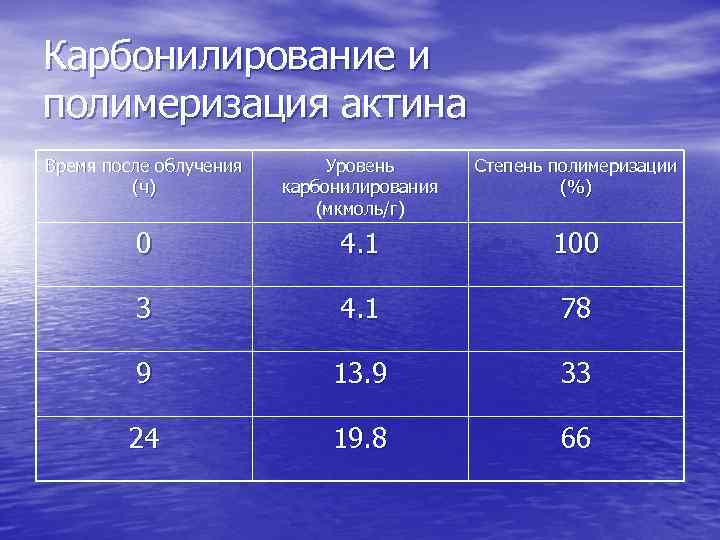 Карбонилирование и полимеризация актина Время после облучения (ч) Уровень карбонилирования (мкмоль/г) Степень полимеризации (%) 0 4. 1 100 3 4. 1 78 9 13. 9 33 24 19. 8 66
Карбонилирование и полимеризация актина Время после облучения (ч) Уровень карбонилирования (мкмоль/г) Степень полимеризации (%) 0 4. 1 100 3 4. 1 78 9 13. 9 33 24 19. 8 66
 Идентификация межбелковых дисульфидов после облучения
Идентификация межбелковых дисульфидов после облучения
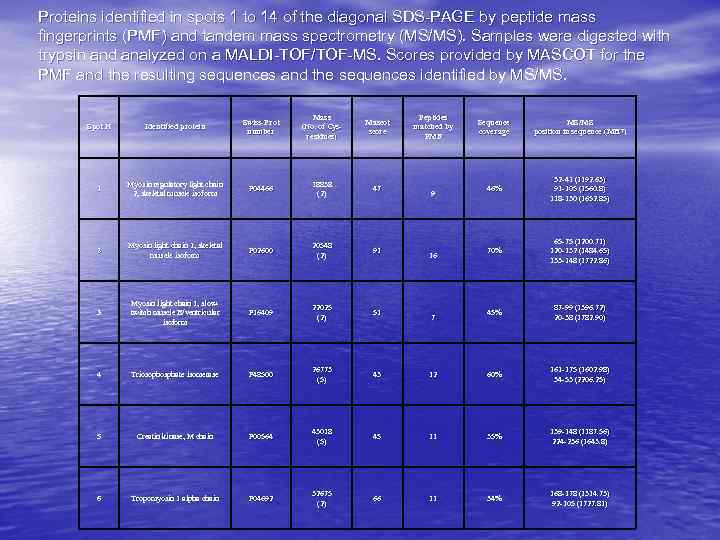 Proteins identified in spots 1 to 14 of the diagonal SDS-PAGE by peptide mass fingerprints (PMF) and tandem mass spectrometry (MS/MS). Samples were digested with trypsin and analyzed on a MALDI-TOF/TOF-MS. Scores provided by MASCOT for the PMF and the resulting sequences and the sequences identified by MS/MS. Spot N Identified protein Swiss-Prot number Mass (No. of Cysresidues) Mascot score 1 Myosin regulatory light chain 2, skeletal muscle isoform P 04466 18838 (2) 47 2 Myosin light chain 1, skeletal muscle isoform P 02600 20548 (2) 91 3 Myosin light chain 1, slowtwitch muscle B/ventricular isoform P 16409 22025 (2) 51 4 Triosophosphate isomerase P 48500 26773 (5) 43 5 Creatin kinase, M chain kinase, P 00564 43018 (5) 6 Tropomyosin 1 alpha chain P 04692 32675 (2) Peptides matched by PMF Sequence coverage MS/MS position in sequence (MH+) 46% 32 -41 (1192. 63) 91 -105 (1560. 8) 118 -130 (1652. 85) 70% 65 -75 (1200. 71) 120 -132 (1484. 65) 133 -148 (1722. 86) 45% 87 -99 (1396. 72) 20 -38 (1782. 90) 12 60% 161 -175 (1602. 98) 34 -53 (2206. 25) 45 11 35% 139 -148 (1187. 56) 224 -236 (1643. 8) 66 11 34% 168 -178 (1314. 73) 92 -105 (1727. 81) 9 16 7
Proteins identified in spots 1 to 14 of the diagonal SDS-PAGE by peptide mass fingerprints (PMF) and tandem mass spectrometry (MS/MS). Samples were digested with trypsin and analyzed on a MALDI-TOF/TOF-MS. Scores provided by MASCOT for the PMF and the resulting sequences and the sequences identified by MS/MS. Spot N Identified protein Swiss-Prot number Mass (No. of Cysresidues) Mascot score 1 Myosin regulatory light chain 2, skeletal muscle isoform P 04466 18838 (2) 47 2 Myosin light chain 1, skeletal muscle isoform P 02600 20548 (2) 91 3 Myosin light chain 1, slowtwitch muscle B/ventricular isoform P 16409 22025 (2) 51 4 Triosophosphate isomerase P 48500 26773 (5) 43 5 Creatin kinase, M chain kinase, P 00564 43018 (5) 6 Tropomyosin 1 alpha chain P 04692 32675 (2) Peptides matched by PMF Sequence coverage MS/MS position in sequence (MH+) 46% 32 -41 (1192. 63) 91 -105 (1560. 8) 118 -130 (1652. 85) 70% 65 -75 (1200. 71) 120 -132 (1484. 65) 133 -148 (1722. 86) 45% 87 -99 (1396. 72) 20 -38 (1782. 90) 12 60% 161 -175 (1602. 98) 34 -53 (2206. 25) 45 11 35% 139 -148 (1187. 56) 224 -236 (1643. 8) 66 11 34% 168 -178 (1314. 73) 92 -105 (1727. 81) 9 16 7
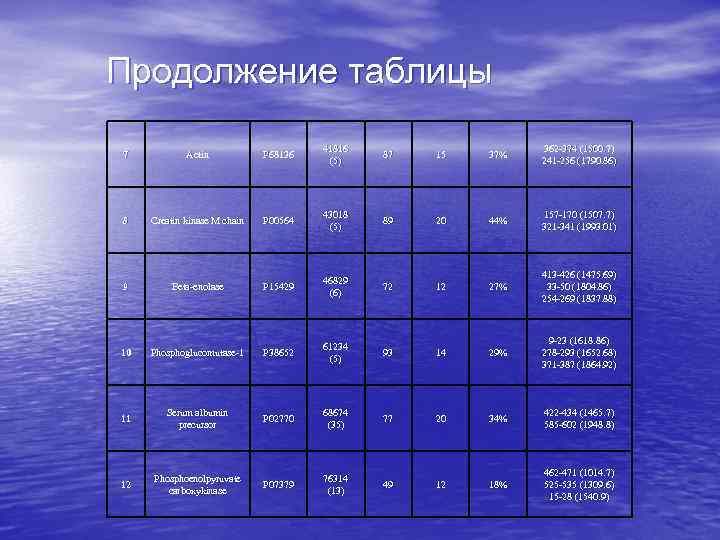 Продолжение таблицы 7 Actin P 68136 41816 (5) 87 15 37% 362 -374 (1500. 7) 241 -256 (1790. 86) 8 Creatin kinase M chain P 00564 43018 (5) 89 20 44% 157 -170 (1507. 7) 321 -341 (1993. 01) 9 Beta-enolase P 15429 46829 (6) 72 12 27% 413 -426 (1475. 69) 33 -50 (1804. 86) 254 -269 (1837. 88) 10 Phosphoglucomutase-1 P 38652 61234 (5) 93 14 29% 9 -23 (1618. 86) 278 -293 (1652. 68) 371 -387 (1864. 92) 11 Serum albumin precursor P 02770 68674 (35) 77 20 34% 422 -434 (1465. 7) 585 -602 (1948. 8) 12 Phosphoenolpyruvate carboxykinase P 07379 76314 (13) 49 12 18% 462 -471 (1014. 7) 525 -535 (1309. 6) 15 -28 (1540. 9)
Продолжение таблицы 7 Actin P 68136 41816 (5) 87 15 37% 362 -374 (1500. 7) 241 -256 (1790. 86) 8 Creatin kinase M chain P 00564 43018 (5) 89 20 44% 157 -170 (1507. 7) 321 -341 (1993. 01) 9 Beta-enolase P 15429 46829 (6) 72 12 27% 413 -426 (1475. 69) 33 -50 (1804. 86) 254 -269 (1837. 88) 10 Phosphoglucomutase-1 P 38652 61234 (5) 93 14 29% 9 -23 (1618. 86) 278 -293 (1652. 68) 371 -387 (1864. 92) 11 Serum albumin precursor P 02770 68674 (35) 77 20 34% 422 -434 (1465. 7) 585 -602 (1948. 8) 12 Phosphoenolpyruvate carboxykinase P 07379 76314 (13) 49 12 18% 462 -471 (1014. 7) 525 -535 (1309. 6) 15 -28 (1540. 9)
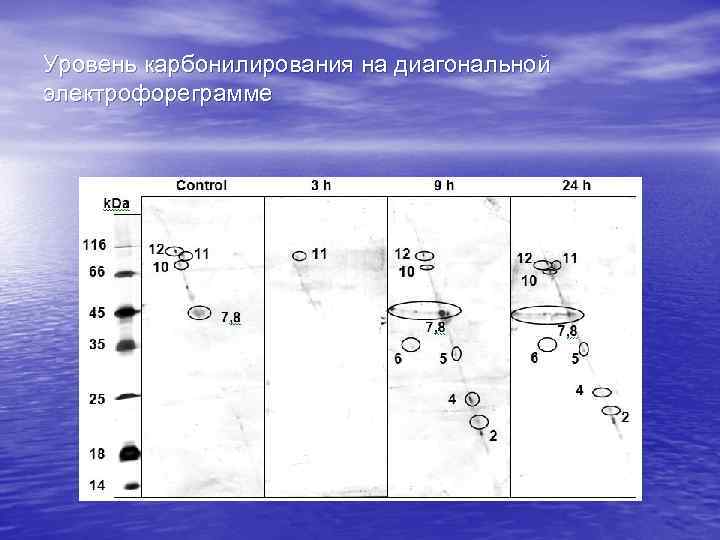 Уровень карбонилирования на диагональной электрофореграмме
Уровень карбонилирования на диагональной электрофореграмме
 Сопоставление данных по карбонилированию и дисульфидам • Наибольшее карбонилирование обнаружено в • пятнах на диагонали: пятна № 7 и 8 (актин и креатинкиназа); Образование S-S-связей (левая часть рисунка) уменьшает карбонилирование соответствующих белков, т. е. защищает их от необратимой модификации (регуляторная роль);
Сопоставление данных по карбонилированию и дисульфидам • Наибольшее карбонилирование обнаружено в • пятнах на диагонали: пятна № 7 и 8 (актин и креатинкиназа); Образование S-S-связей (левая часть рисунка) уменьшает карбонилирование соответствующих белков, т. е. защищает их от необратимой модификации (регуляторная роль);
 Identification of Cysteine, Methionine and Tryptophan Residues of Actin Oxidized In vivo during Oxidative Stress Maria Fedorova, Nadezda Kuleva, and Ralf Hoffmann J. Proteomics Res. , 2010(in press). Среди пяти цистеинов актина Cys-239 и Cys-259 были окислены до сульфеновой кислоты (Cys-SOH), сульфиновой кислоты (Cys-SO 2 H) и сульфоновой кислоты (Cys-SO 3 H), и их количество увеличивалось со временем после облучения. Содержание метионинсульфоксида также увеличивалось для 15 из 16 метиониновых остатков. Наибольшее содержание сульфоксида оказалось в Met-44, Met-47, Met-256. Имеют ли эти остатки регуляторное значение, пока не ясно.
Identification of Cysteine, Methionine and Tryptophan Residues of Actin Oxidized In vivo during Oxidative Stress Maria Fedorova, Nadezda Kuleva, and Ralf Hoffmann J. Proteomics Res. , 2010(in press). Среди пяти цистеинов актина Cys-239 и Cys-259 были окислены до сульфеновой кислоты (Cys-SOH), сульфиновой кислоты (Cys-SO 2 H) и сульфоновой кислоты (Cys-SO 3 H), и их количество увеличивалось со временем после облучения. Содержание метионинсульфоксида также увеличивалось для 15 из 16 метиониновых остатков. Наибольшее содержание сульфоксида оказалось в Met-44, Met-47, Met-256. Имеют ли эти остатки регуляторное значение, пока не ясно.
 Окисленные остатки в аминокислотной цепи актина
Окисленные остатки в аминокислотной цепи актина
 Institute of Bioanalytical Chemistry, Center for Biotechnology and Biomedicine, Faculty of Chemistry and Mineralogy, Leipzig University, Deutscher Platz 5, 04103 Leipzig, Germany
Institute of Bioanalytical Chemistry, Center for Biotechnology and Biomedicine, Faculty of Chemistry and Mineralogy, Leipzig University, Deutscher Platz 5, 04103 Leipzig, Germany


