c4072a82a1a7fbdd78d7a5ca4e4a1564.ppt
- Количество слайдов: 33
 Окислительный стресс Подготовила: студентка 5 курса медико-профилактического факультета Шишковец А. И.
Окислительный стресс Подготовила: студентка 5 курса медико-профилактического факультета Шишковец А. И.
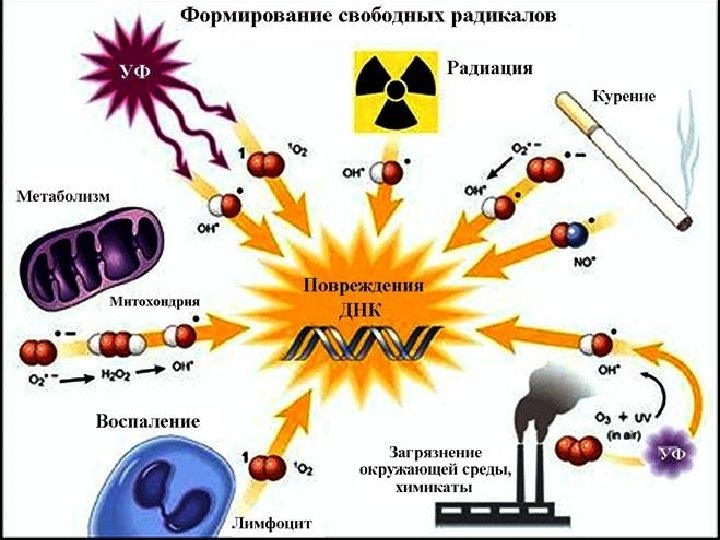
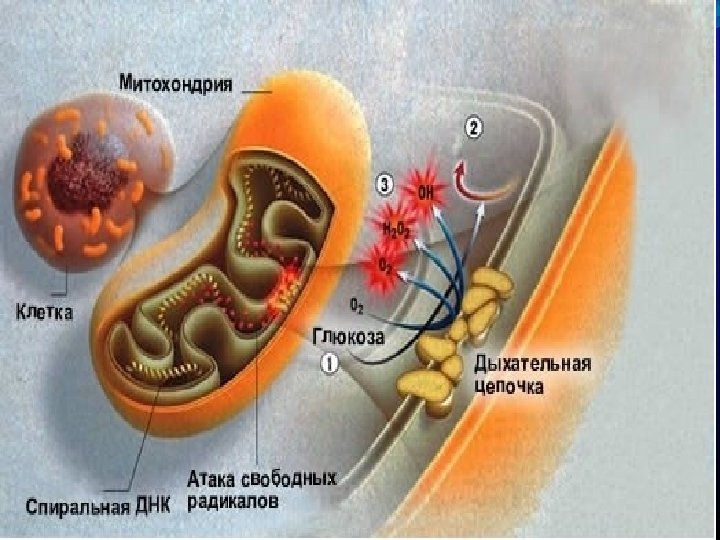
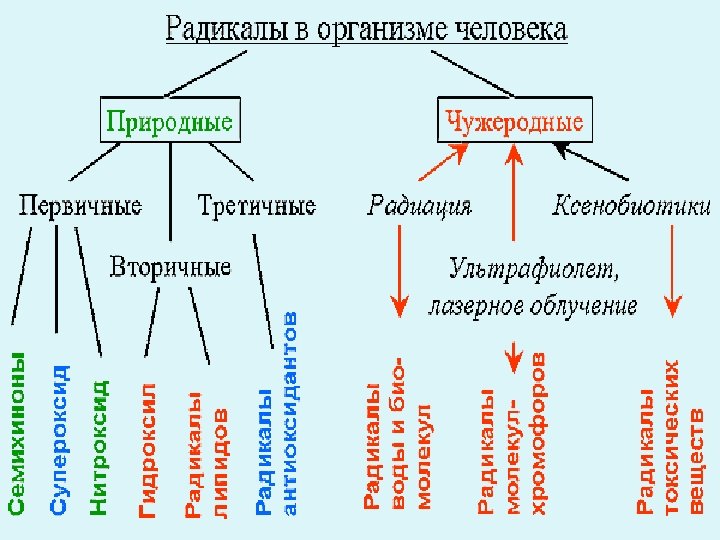
 ОКИСЛИТЕЛЬНЫЙ СТРЕСС состояние, характеризующееся избыточным образованием в клетках организма свободных радикалов и др. активных форм кислорода, превышающим возможности антиоксидантной защиты. введен в научную литературу в 1985 году Г. Зисом
ОКИСЛИТЕЛЬНЫЙ СТРЕСС состояние, характеризующееся избыточным образованием в клетках организма свободных радикалов и др. активных форм кислорода, превышающим возможности антиоксидантной защиты. введен в научную литературу в 1985 году Г. Зисом
 Характеризуется: 1. срывом системы АОЗ(антиоксидантной защиты) 2. интенсификацией процессов СРО (свободнорадикального окисления) 3. накоплением в органах и тканях токсичных продуктов окислительной деструкции биомолекул (белков, жиров, углеводов, нуклеиновых кислот).
Характеризуется: 1. срывом системы АОЗ(антиоксидантной защиты) 2. интенсификацией процессов СРО (свободнорадикального окисления) 3. накоплением в органах и тканях токсичных продуктов окислительной деструкции биомолекул (белков, жиров, углеводов, нуклеиновых кислот).

 Состояние стресс-системы стресс-реализующее звено СРО стресс-лимитирующее звено АОС
Состояние стресс-системы стресс-реализующее звено СРО стресс-лимитирующее звено АОС
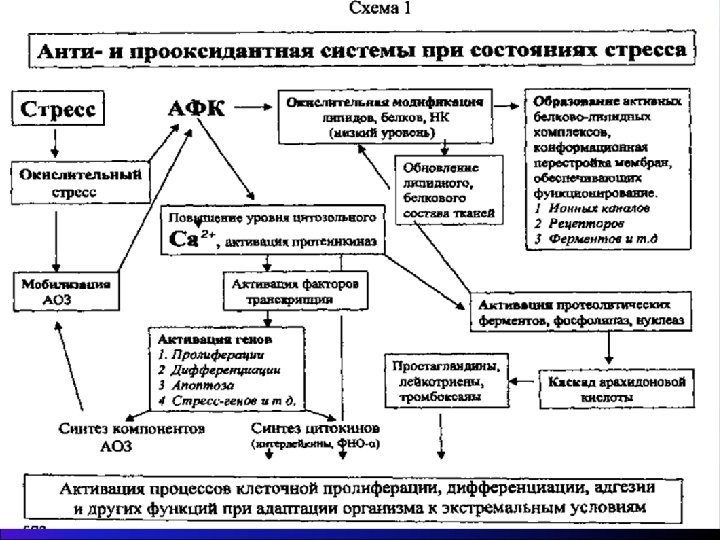

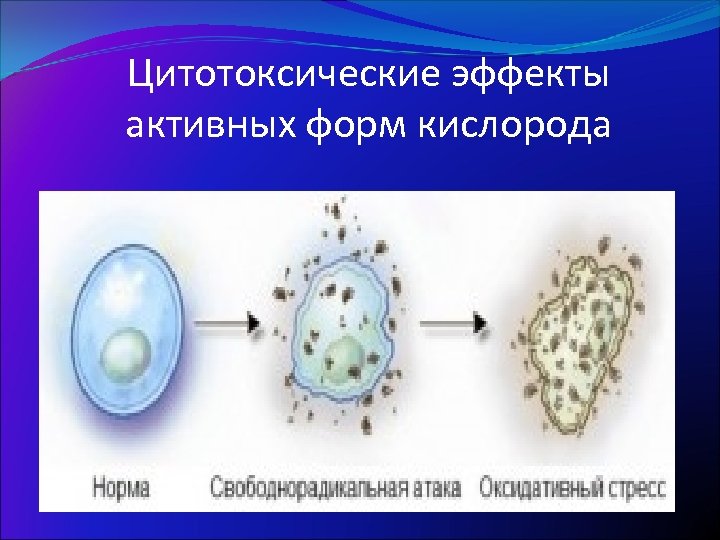 Цитотоксические эффекты активных форм кислорода
Цитотоксические эффекты активных форм кислорода
 Активные формы кислорода (АФК) -молекулы с высокой реакционной способностью: 1. супероксидный анион-радикал( • ОО-) 2. гидроксильный радикал (НО • ) 3. синглетный кислород (*О 2) 4. гидропероксильный радикал ( • ООН) 5. перекись водорода (Н 2 О 2)
Активные формы кислорода (АФК) -молекулы с высокой реакционной способностью: 1. супероксидный анион-радикал( • ОО-) 2. гидроксильный радикал (НО • ) 3. синглетный кислород (*О 2) 4. гидропероксильный радикал ( • ООН) 5. перекись водорода (Н 2 О 2)
 Ряд окислительной способности АФК O 2*- < HOO* < H 2 O 2 < HO*
Ряд окислительной способности АФК O 2*- < HOO* < H 2 O 2 < HO*
 Образования супероксидного анион-радикала ( • OO–) в клетке «утечка» электронов дыхательной цепи аутоокисление в процессе обезвреживания собственных и чужеродных токсических веществ
Образования супероксидного анион-радикала ( • OO–) в клетке «утечка» электронов дыхательной цепи аутоокисление в процессе обезвреживания собственных и чужеродных токсических веществ
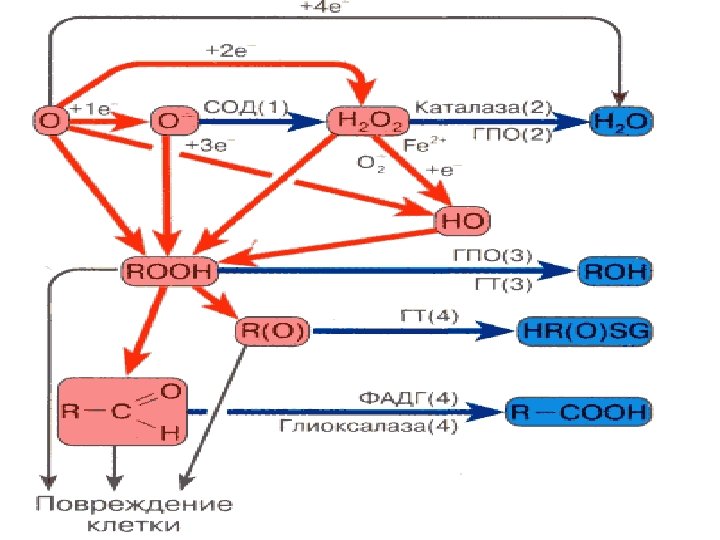
 Пероксида водорода H 2 О 2 стабильный продукт восстановления O 2 Образуется в клетке: как побочный продукт при окислительном катаболизме пуриновых нуклеотидов, ксантиноксидазой в реакции окислительного дезаминирования аминокислот
Пероксида водорода H 2 О 2 стабильный продукт восстановления O 2 Образуется в клетке: как побочный продукт при окислительном катаболизме пуриновых нуклеотидов, ксантиноксидазой в реакции окислительного дезаминирования аминокислот
 Гидроксильный радикал НО • 1. Высокий редокс-потенциал (Eо = +2, 32 B) 2. Скорость атаки (k = 10*– 1010 M– 1 c– 1) любого органического соединения (белки, нуклеиновые кислоты, липиды, углеводы). 3. Константа скорости его рекомбинации составляет 0, 55 • 1010 M– 1 c– 1. 4. Время жизни НО • в биологическом материале не более 10– 9 с 5. Радиус миграции – менее 0, 01 мкм (<100 Ао).
Гидроксильный радикал НО • 1. Высокий редокс-потенциал (Eо = +2, 32 B) 2. Скорость атаки (k = 10*– 1010 M– 1 c– 1) любого органического соединения (белки, нуклеиновые кислоты, липиды, углеводы). 3. Константа скорости его рекомбинации составляет 0, 55 • 1010 M– 1 c– 1. 4. Время жизни НО • в биологическом материале не более 10– 9 с 5. Радиус миграции – менее 0, 01 мкм (<100 Ао).
 Реакционная способность гидроксильного радикала превосходит даже атомарный кислород (почти в 300 раз)
Реакционная способность гидроксильного радикала превосходит даже атомарный кислород (почти в 300 раз)
 Реакция Фентона 2+ 3+ - 3+ 2+ + Fe + H 2 O 2 > Fe + HO* + HO Fe + H 2 O 2 > Fe + HOO* + H
Реакция Фентона 2+ 3+ - 3+ 2+ + Fe + H 2 O 2 > Fe + HO* + HO Fe + H 2 O 2 > Fe + HOO* + H
 АФК: повреждение ДНК
АФК: повреждение ДНК
 Молекула ДНК повреждается : гидроксид-радикалом супероксид-анионом радикаломи, образующимися при перекисном окислении липидов эндонуклеазами
Молекула ДНК повреждается : гидроксид-радикалом супероксид-анионом радикаломи, образующимися при перекисном окислении липидов эндонуклеазами
 Нарушения структуры хромосом
Нарушения структуры хромосом
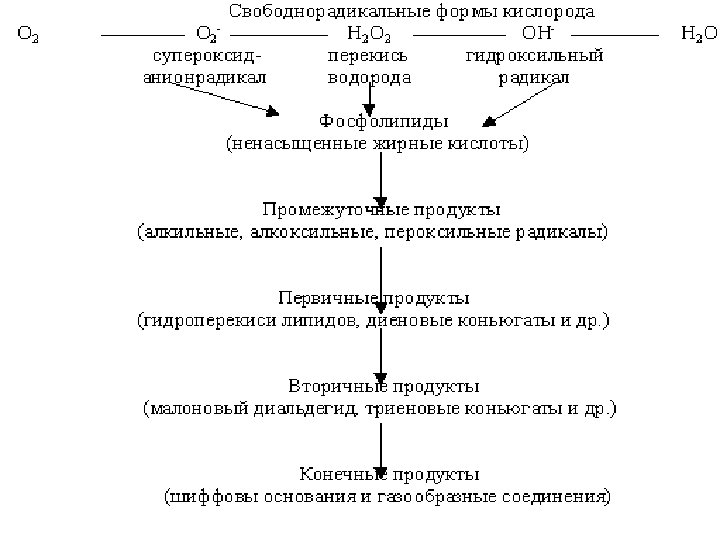
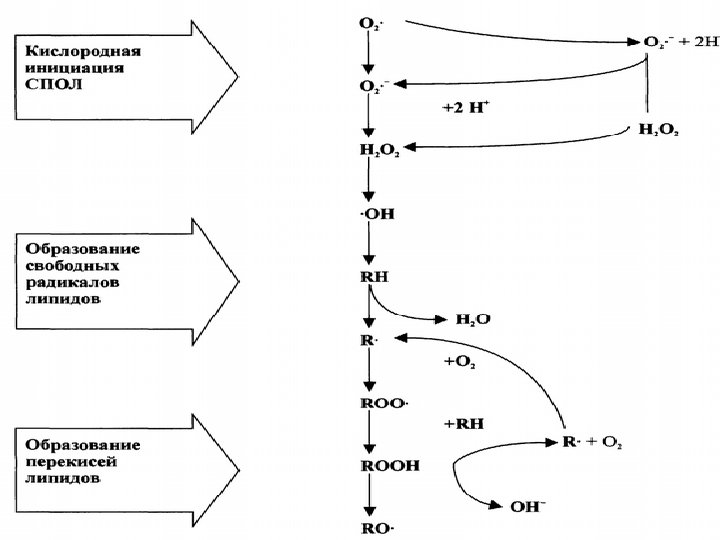
 Цепь превращений при ПОЛ: субстратом являются полиненасыщенные цепи жирных кислот ( ПНЖК ), 1) инициация процесса ПОЛ; 2) продолжение (рост) цепи ПОЛ; 3) разветвление цепи (амплификация процесса); 4) терминация процесса (обрыв цепей).
Цепь превращений при ПОЛ: субстратом являются полиненасыщенные цепи жирных кислот ( ПНЖК ), 1) инициация процесса ПОЛ; 2) продолжение (рост) цепи ПОЛ; 3) разветвление цепи (амплификация процесса); 4) терминация процесса (обрыв цепей).
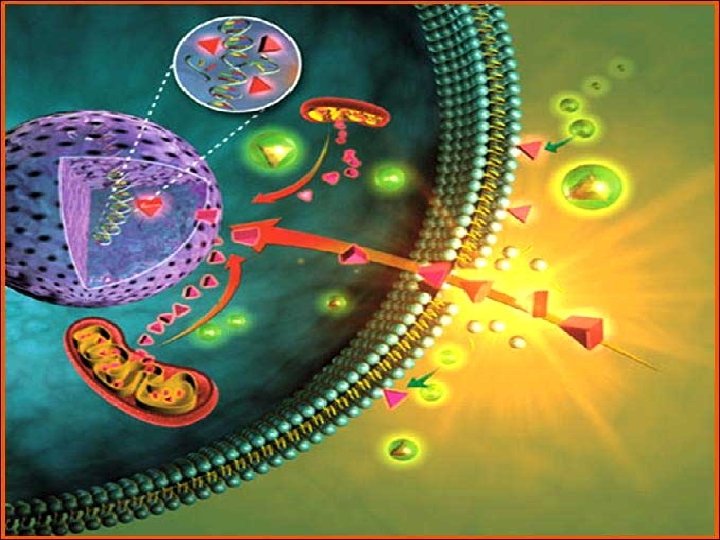
 Физиологические эффекты активных форм кислорода
Физиологические эффекты активных форм кислорода
 АОЗ обеспечивается за счет: 1. высокой степени упорядоченности и структурированности ферментативных систем в мембранах клеток 2. относительно низких значений р. О 2 в тканях 3. наличия биоантиоксидантов.
АОЗ обеспечивается за счет: 1. высокой степени упорядоченности и структурированности ферментативных систем в мембранах клеток 2. относительно низких значений р. О 2 в тканях 3. наличия биоантиоксидантов.
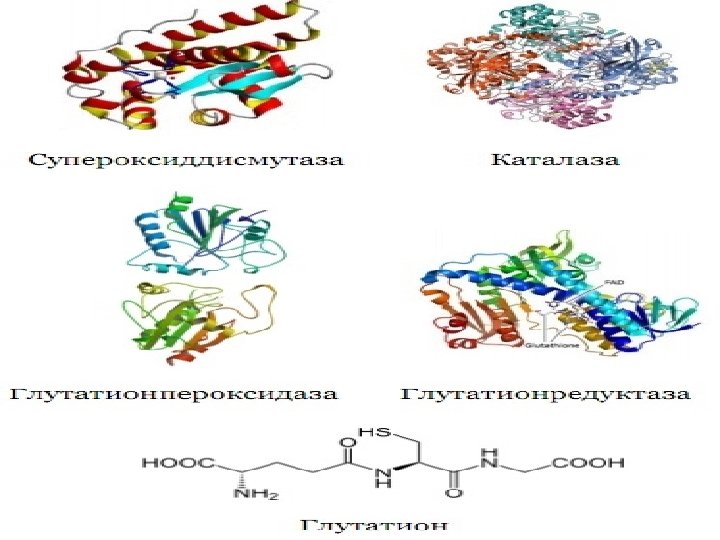
 Антиоксидантная защита: Супероксиддисмутаза (превращение супероксида в водородпероксид и кислород): 2 O 2*- + 2 H+ > H 2 O 2 + O 2 Каталаза (ускорение разложения избытка водородпероксида до кислорода и воды): 2 H 2 O 2 > 2 H 2 O + O 2 Глутатионпероксидаза (разрушение как пероксида водорода, так и гидропероксидов липидов): Н 2 О 2 + 2 GSH > 2 Н 2 О + GS-SG Окисленный кофермент глутатион восстанавливается глутатионредуктазой: GS-SG + НАДФ*Н + Н+ > 2 GSH + НАДФ+
Антиоксидантная защита: Супероксиддисмутаза (превращение супероксида в водородпероксид и кислород): 2 O 2*- + 2 H+ > H 2 O 2 + O 2 Каталаза (ускорение разложения избытка водородпероксида до кислорода и воды): 2 H 2 O 2 > 2 H 2 O + O 2 Глутатионпероксидаза (разрушение как пероксида водорода, так и гидропероксидов липидов): Н 2 О 2 + 2 GSH > 2 Н 2 О + GS-SG Окисленный кофермент глутатион восстанавливается глутатионредуктазой: GS-SG + НАДФ*Н + Н+ > 2 GSH + НАДФ+
 Локализация и антиоксидантные эффекты низкомолекулярных антиоксидантов в тканях человека Антиоксиданты Локализация Функция Витамин Е Биомембраны Тушение • ОН, LOO • , HOCl Убихинол Биомембраны Тушение • ОН, LOO • , HOCl Каротиноиды Биомембраны Тушение • ОН, LOO • , HOCl Витамин С Цитоплазма Тушение • ОН, • ОО– Карнозин Цитоплазма Тушение • ОН, • ОО–, нейтрализация гипохлорита N-ацетилцистеин Цитоплазма Неизбирательное тушение АФК Таурин Цитоплазма нейтрализация гипохлорита Глутатион Цитоплазма, митохондрии Тушение • ОН, • ОО– Мочевая кислота Кровь Предотвращение ПОЛ Билирубин Кровь Предотвращение ПОЛ
Локализация и антиоксидантные эффекты низкомолекулярных антиоксидантов в тканях человека Антиоксиданты Локализация Функция Витамин Е Биомембраны Тушение • ОН, LOO • , HOCl Убихинол Биомембраны Тушение • ОН, LOO • , HOCl Каротиноиды Биомембраны Тушение • ОН, LOO • , HOCl Витамин С Цитоплазма Тушение • ОН, • ОО– Карнозин Цитоплазма Тушение • ОН, • ОО–, нейтрализация гипохлорита N-ацетилцистеин Цитоплазма Неизбирательное тушение АФК Таурин Цитоплазма нейтрализация гипохлорита Глутатион Цитоплазма, митохондрии Тушение • ОН, • ОО– Мочевая кислота Кровь Предотвращение ПОЛ Билирубин Кровь Предотвращение ПОЛ
 Спасибо за внимание!
Спасибо за внимание!


