 Окислительновосстановительные реакции 8 класс
Окислительновосстановительные реакции 8 класс
 Расставьте степени окисления элементов в реакциях. Сравните, как ведут себя степени окисления в процессе реакции. +1 -1 +1 -2 +1 +1 -2 HCl + Na. OH = Na. Cl + H 2 O +1 -1 0 +2 -1 0 2 HCl + Zn = Zn. Cl 2 + H Окислительновосстановительная 2 реакция Реакции, в которых происходит изменение степеней окисления, называются окислительно-восстановительными
Расставьте степени окисления элементов в реакциях. Сравните, как ведут себя степени окисления в процессе реакции. +1 -1 +1 -2 +1 +1 -2 HCl + Na. OH = Na. Cl + H 2 O +1 -1 0 +2 -1 0 2 HCl + Zn = Zn. Cl 2 + H Окислительновосстановительная 2 реакция Реакции, в которых происходит изменение степеней окисления, называются окислительно-восстановительными
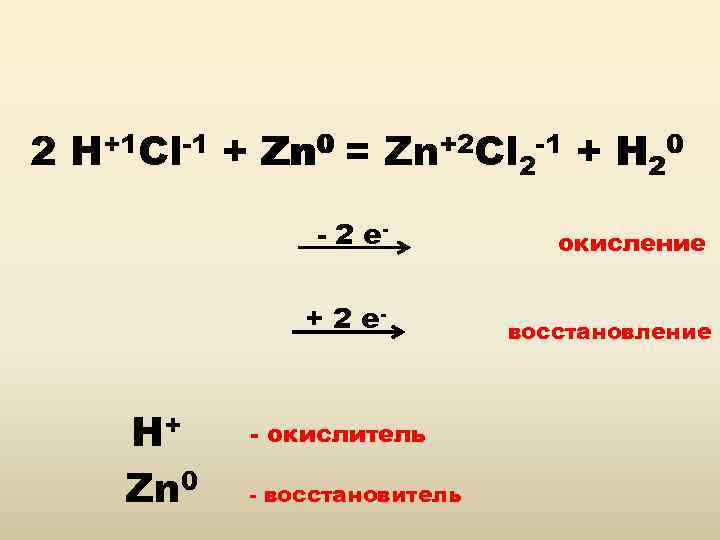 +1 2 H+ Cl-1 + Zn 0 = Zn+2 Cl 2 -1 + H 20 - 2 е+ 2 е- H+ Zn 0 окисление восстановление - окислитель - восстановитель
+1 2 H+ Cl-1 + Zn 0 = Zn+2 Cl 2 -1 + H 20 - 2 е+ 2 е- H+ Zn 0 окисление восстановление - окислитель - восстановитель
 Окисление – процесс отдачи электронов. Восстановление – процесс присоединения электронов. Окислитель – элемент, принимающий электроны. Восстановитель – элемент, отдающий электроны.
Окисление – процесс отдачи электронов. Восстановление – процесс присоединения электронов. Окислитель – элемент, принимающий электроны. Восстановитель – элемент, отдающий электроны.
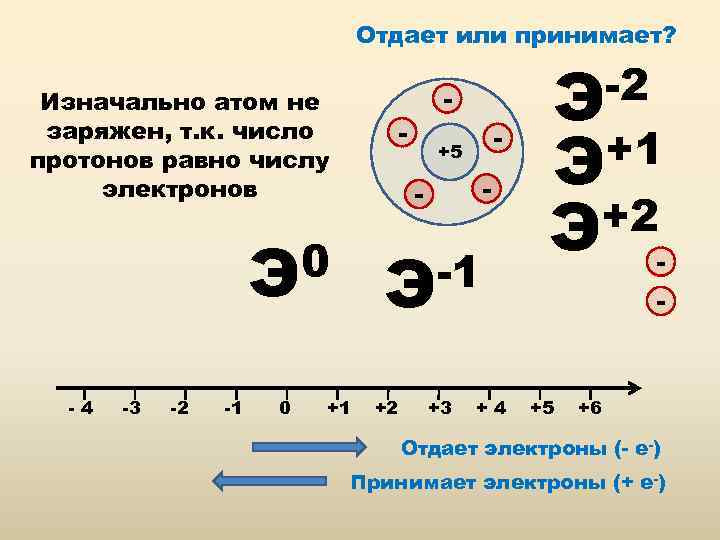 Отдает или принимает? Изначально атом не заряжен, т. к. число протонов равно числу электронов - -3 -2 -1 0 - +5 - - 0 Э -4 - -1 Э +1 +2 +3 +4 -2 Э +1 Э +2 Э - +5 +6 Отдает электроны (- е-) Принимает электроны (+ е-)
Отдает или принимает? Изначально атом не заряжен, т. к. число протонов равно числу электронов - -3 -2 -1 0 - +5 - - 0 Э -4 - -1 Э +1 +2 +3 +4 -2 Э +1 Э +2 Э - +5 +6 Отдает электроны (- е-) Принимает электроны (+ е-)
 Отдает или принимает? + 6 e- S+6 S 0 восстановление S+6 S-2 восстановление + 8 e- 2 e- S+4 S+6 окисление - 6 e- S-2 S+4 - 2 e- окисление Cu 0 Cu+2 + 8 e- окисление C+4 C- 4 восстановление C- 4 C+2 окисление - 6 e- - 4 e- C 0 C+4 окисление -3 -2 -1 0 +1 +2 +3 +4 отдает епринимает е-
Отдает или принимает? + 6 e- S+6 S 0 восстановление S+6 S-2 восстановление + 8 e- 2 e- S+4 S+6 окисление - 6 e- S-2 S+4 - 2 e- окисление Cu 0 Cu+2 + 8 e- окисление C+4 C- 4 восстановление C- 4 C+2 окисление - 6 e- - 4 e- C 0 C+4 окисление -3 -2 -1 0 +1 +2 +3 +4 отдает епринимает е-
 Какая польза от теории ОВР? Например, расстановка коэффициентов в сложных уравнениях – метод электронного баланса +1 -1 +1 +7 -2 +2 -1 +1 -1 0 +1 -2 16 HCl +2 KMn. O 4 =2 Mn. Cl 2 +2 KCl +5 Cl 2+ 8 H 2 O Mn+7 2 Cl-1 +5 e- 2 e- Mn+2 Cl 20 Mn+7 – окислитель Сl -1 – восстановитель 10 2 Восст-ие 5 окисление
Какая польза от теории ОВР? Например, расстановка коэффициентов в сложных уравнениях – метод электронного баланса +1 -1 +1 +7 -2 +2 -1 +1 -1 0 +1 -2 16 HCl +2 KMn. O 4 =2 Mn. Cl 2 +2 KCl +5 Cl 2+ 8 H 2 O Mn+7 2 Cl-1 +5 e- 2 e- Mn+2 Cl 20 Mn+7 – окислитель Сl -1 – восстановитель 10 2 Восст-ие 5 окисление
 Расставьте коэффициенты методом электронного баланса. Al + Mn. O 2 = Al 2 O 3 + Mn Fe 2 O 3 + Zn = Zn. O + Fe Mg + H 2 SO 4 = Mg. SO 4 + H 2 S + H 2 O Cu + HNO 3 = Cu(NO 3)2+ NO + H 2 O KI + Fe. Cl 3 = l 2 + KCl + Fe. Cl 2 Cr 2 O 3 + K 2 CO 3 + O 2 = K 2 Cr. O 4 + CO 2
Расставьте коэффициенты методом электронного баланса. Al + Mn. O 2 = Al 2 O 3 + Mn Fe 2 O 3 + Zn = Zn. O + Fe Mg + H 2 SO 4 = Mg. SO 4 + H 2 S + H 2 O Cu + HNO 3 = Cu(NO 3)2+ NO + H 2 O KI + Fe. Cl 3 = l 2 + KCl + Fe. Cl 2 Cr 2 O 3 + K 2 CO 3 + O 2 = K 2 Cr. O 4 + CO 2