Окислительно-восстановительные процессы_2.ppt
- Количество слайдов: 15
 Окислительновосстановительные процессы Часть № 2
Окислительновосстановительные процессы Часть № 2
 Окислительно-восстановительные потенциалы Количественной мерой окислительной способности окислителя (и одновременно восстановительной способности его восстановленной формы) является электродный потенциал Е, на котором одновременно и с равными скоростями протекают полуреакция его восстановления и обратная ей полуреакция окисления соответствующей восстановленной формы.
Окислительно-восстановительные потенциалы Количественной мерой окислительной способности окислителя (и одновременно восстановительной способности его восстановленной формы) является электродный потенциал Е, на котором одновременно и с равными скоростями протекают полуреакция его восстановления и обратная ей полуреакция окисления соответствующей восстановленной формы.
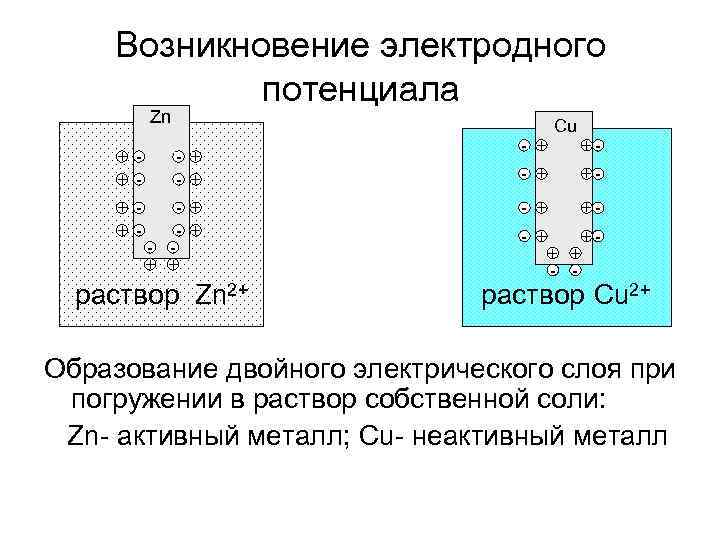 Возникновение электродного потенциала Zn Cu + - Zn- + + - + Cu - + + - - + +- - + - + + раствор Zn 2+ + + - - раствор Cu 2+ Образование двойного электрического слоя при погружении в раствор собственной соли: Zn- активный металл; Cu- неактивный металл
Возникновение электродного потенциала Zn Cu + - Zn- + + - + Cu - + + - - + +- - + - + + раствор Zn 2+ + + - - раствор Cu 2+ Образование двойного электрического слоя при погружении в раствор собственной соли: Zn- активный металл; Cu- неактивный металл
 Окислительно-восстановительный потенциал измеряется по отношению к стандартному водородному электроду и характеризует пару «окисленная форма – восстановленная форма» . Чем выше потенциал пары, тем сильнее выражена окислительная способность окислителя и, соответственно, слабее – восстановительная способность восстановителя.
Окислительно-восстановительный потенциал измеряется по отношению к стандартному водородному электроду и характеризует пару «окисленная форма – восстановленная форма» . Чем выше потенциал пары, тем сильнее выражена окислительная способность окислителя и, соответственно, слабее – восстановительная способность восстановителя.
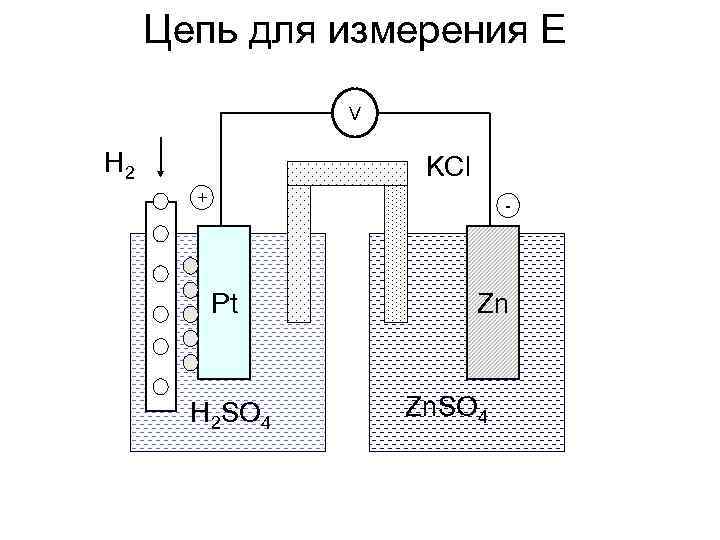 Цепь для измерения E V H 2 KCl + - Pt H 2 SO 4 Zn Zn. SO 4
Цепь для измерения E V H 2 KCl + - Pt H 2 SO 4 Zn Zn. SO 4
 Гальванический элемент Ячейка представляет собой пример гальванического элемента, в котором химическая энергия преобразуется в электрический ток. Состоит из двух полуэлементов, соединенных электрическим проводником. На аноде протекает окисление , на катоде – восстановление. Анод – цинковый электрод, катод – водородный.
Гальванический элемент Ячейка представляет собой пример гальванического элемента, в котором химическая энергия преобразуется в электрический ток. Состоит из двух полуэлементов, соединенных электрическим проводником. На аноде протекает окисление , на катоде – восстановление. Анод – цинковый электрод, катод – водородный.
 Электроны от анода по внешней цепи протекают к катоду. Схема элемента записывается: (-)Zn|Zn 2+||2 H+|H 2, Pt (+) Одна вертикальная линия изображает границу раздела фаз(металл-раствор), а две – границу между растворами. Причина возникновения и протекания тока – разность электродных потенциалов ( ): = к- а, , к> а,
Электроны от анода по внешней цепи протекают к катоду. Схема элемента записывается: (-)Zn|Zn 2+||2 H+|H 2, Pt (+) Одна вертикальная линия изображает границу раздела фаз(металл-раствор), а две – границу между растворами. Причина возникновения и протекания тока – разность электродных потенциалов ( ): = к- а, , к> а,
![Уравнение Нернста Е(Ox/Red) = Еo(Ox/Red) + RT/(n. F) ln [Ox]/[Red], отвечает условной записи полуреакции Уравнение Нернста Е(Ox/Red) = Еo(Ox/Red) + RT/(n. F) ln [Ox]/[Red], отвечает условной записи полуреакции](https://present5.com/presentation/3/49895079_62241568.pdf-img/49895079_62241568.pdf-8.jpg) Уравнение Нернста Е(Ox/Red) = Еo(Ox/Red) + RT/(n. F) ln [Ox]/[Red], отвечает условной записи полуреакции восстановления окислителя Ox + ne- = Red Каждая из концентраций под знаком логарифма в уравнении Нернста возводится в степень, соответствующую стехиометрическому коэффициенту данной частицы в уравнении полуреакции, n – число принимаемых окислителем электронов, R – универсальная газовая постоянная, T – температура, F – число Фарадея.
Уравнение Нернста Е(Ox/Red) = Еo(Ox/Red) + RT/(n. F) ln [Ox]/[Red], отвечает условной записи полуреакции восстановления окислителя Ox + ne- = Red Каждая из концентраций под знаком логарифма в уравнении Нернста возводится в степень, соответствующую стехиометрическому коэффициенту данной частицы в уравнении полуреакции, n – число принимаемых окислителем электронов, R – универсальная газовая постоянная, T – температура, F – число Фарадея.
 Квадратными скобками в уравнении Нернста обозначены равновесные (в условиях измерения) концентрации частиц. По мере протекания реакции вычисляемый по уравнению Нернста потенциал окислителя уменьшается, а отвечающий второй полуреакции потенциал восстановителя, напротив, увеличивается. Когда они выравниваются, реакция прекращается, и система приходит в состояние химического равновесия.
Квадратными скобками в уравнении Нернста обозначены равновесные (в условиях измерения) концентрации частиц. По мере протекания реакции вычисляемый по уравнению Нернста потенциал окислителя уменьшается, а отвечающий второй полуреакции потенциал восстановителя, напротив, увеличивается. Когда они выравниваются, реакция прекращается, и система приходит в состояние химического равновесия.
 Стандартные окислительновосстановительные потенциалы Первое слагаемое в правой части уравнения Нернста – это стандартный окислительно-восстановительный потенциал, т. е. потенциал, измеренный или чаще вычисленный при стандартных условиях. В стандартных условиях концентрации всех частиц в растворе по определению равны 1 моль/л, и второе слагаемое в правой части уравнения обращается в нуль.
Стандартные окислительновосстановительные потенциалы Первое слагаемое в правой части уравнения Нернста – это стандартный окислительно-восстановительный потенциал, т. е. потенциал, измеренный или чаще вычисленный при стандартных условиях. В стандартных условиях концентрации всех частиц в растворе по определению равны 1 моль/л, и второе слагаемое в правой части уравнения обращается в нуль.
 Критерий направления реакции в стандартных условиях Любая запись уравнения ОВР предполагает определенный выбор окислителя в левой части уравнения. Если в стандартных условиях этот окислитель сильнее, реакция пойдет в прямом направлении, если нет – в обратном. Потенциал окислителя - Ео. Ок потенциал восстановителя - Еовос.
Критерий направления реакции в стандартных условиях Любая запись уравнения ОВР предполагает определенный выбор окислителя в левой части уравнения. Если в стандартных условиях этот окислитель сильнее, реакция пойдет в прямом направлении, если нет – в обратном. Потенциал окислителя - Ео. Ок потенциал восстановителя - Еовос.
 Величина ΔЕо = Ео. Ок – Ео. Вос стандартная разность окислительновосстановительных потенциалов. Критерий направления реакции: Если ΔЕо > 0, реакция в стандартных условиях протекает в прямом направлении; если ΔЕо < 0, то в обратном.
Величина ΔЕо = Ео. Ок – Ео. Вос стандартная разность окислительновосстановительных потенциалов. Критерий направления реакции: Если ΔЕо > 0, реакция в стандартных условиях протекает в прямом направлении; если ΔЕо < 0, то в обратном.
 Стандартная энергия Гиббса реакции окисления-восстановления связана с разностью (Ео. Ок – Ео. Вос ) выражением ΔG 0298 = - n F (Ео. Ок – Ео. Вос ), где n - количество электронов (моль), передаваемое в соответствии с уравнением реакции от восстановителя к окислителю; F - постоянная Фарадея.
Стандартная энергия Гиббса реакции окисления-восстановления связана с разностью (Ео. Ок – Ео. Вос ) выражением ΔG 0298 = - n F (Ео. Ок – Ео. Вос ), где n - количество электронов (моль), передаваемое в соответствии с уравнением реакции от восстановителя к окислителю; F - постоянная Фарадея.
 Для самопроизвольно протекающих реакций окисления-восстановления выполняется критерий ΔG° 298 << 0 и, следовательно, (Ео. Ок – Ео. Вос ) >> 0. Такие реакции идут в прямом направлении; степень их протекания (Ео. Ок – Ео. Вос).
Для самопроизвольно протекающих реакций окисления-восстановления выполняется критерий ΔG° 298 << 0 и, следовательно, (Ео. Ок – Ео. Вос ) >> 0. Такие реакции идут в прямом направлении; степень их протекания (Ео. Ок – Ео. Вос).
 Реакции химически необратимы при ΔЕо > 0, 4. Если ΔЕо < – 0, 4 В, реакция всегда протекает до конца, но в обратном направлении. Причиной кинетических затруднений протекания реакций является кулоновское отталкивание катионов окислителя и восстановителя, мешающее им подойти друг к другу на расстояние, при котором возможен электронный переход.
Реакции химически необратимы при ΔЕо > 0, 4. Если ΔЕо < – 0, 4 В, реакция всегда протекает до конца, но в обратном направлении. Причиной кинетических затруднений протекания реакций является кулоновское отталкивание катионов окислителя и восстановителя, мешающее им подойти друг к другу на расстояние, при котором возможен электронный переход.


