Окислительно-восстановительное равновесие 2.ppt
- Количество слайдов: 23
 Окислительновосстановительное равновесие
Окислительновосстановительное равновесие
 Окислительно-восстановительное равновесие - это равновесие, основанное на окислительно восстановительных реакциях (процесах).
Окислительно-восстановительное равновесие - это равновесие, основанное на окислительно восстановительных реакциях (процесах).
 Окислительно-восстановительные реакции (редокс-реакции) n химические реакции, протекающие с изменением степени окисления реагирующих веществ, вследствие переноса электронов от одного реагирующего вещества (восстановителя) к другому веществу (окислителю).
Окислительно-восстановительные реакции (редокс-реакции) n химические реакции, протекающие с изменением степени окисления реагирующих веществ, вследствие переноса электронов от одного реагирующего вещества (восстановителя) к другому веществу (окислителю).
 Общая характеристика окислительно восстановительных реакций
Общая характеристика окислительно восстановительных реакций
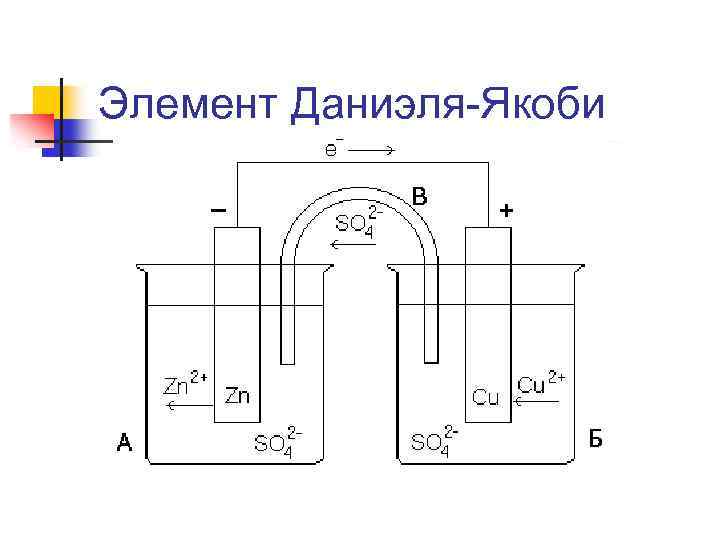 Элемент Даниэля-Якоби
Элемент Даниэля-Якоби
 n n Электродный потенциал (Е) характеризует индивидуальную окислительно восстановительную способность каждой сопряженной редокс пары и может быть измерен экспериментально. Зависимость равновесных редокс потенциалов от природы образующих редокс пару веществ, их концентрации, температуры и других факторов описывается уравнением Нернста:
n n Электродный потенциал (Е) характеризует индивидуальную окислительно восстановительную способность каждой сопряженной редокс пары и может быть измерен экспериментально. Зависимость равновесных редокс потенциалов от природы образующих редокс пару веществ, их концентрации, температуры и других факторов описывается уравнением Нернста:
 где EOx/Red равновесный окислительно восстановительный потенциал сопряженной редокс пары Ox/Red при заданной температуре Т и любом соотношении активностей окисленной и восстановленной форм; E 0 Ox/Red стандартный редокс потенциал сопряженной пары Ox/Red, В, при активностях a. Ox = a. Red = 1 моль/л; R – молярная газовая постоянная, равная 8, 314 Дж/моль; Т – абсолютная температура, К; F=96500 Кл/моль – число Фарадея; n – число электронов, участвующих в полуреакции Ox/Red.
где EOx/Red равновесный окислительно восстановительный потенциал сопряженной редокс пары Ox/Red при заданной температуре Т и любом соотношении активностей окисленной и восстановленной форм; E 0 Ox/Red стандартный редокс потенциал сопряженной пары Ox/Red, В, при активностях a. Ox = a. Red = 1 моль/л; R – молярная газовая постоянная, равная 8, 314 Дж/моль; Т – абсолютная температура, К; F=96500 Кл/моль – число Фарадея; n – число электронов, участвующих в полуреакции Ox/Red.

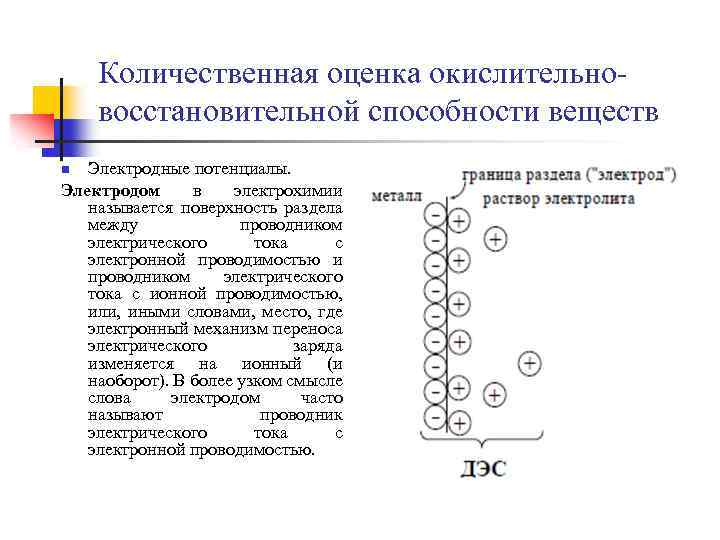 Количественная оценка окислительно восстановительной способности веществ Электродные потенциалы. Электродом в электрохимии называется поверхность раздела между проводником электрического тока с электронной проводимостью и проводником электрического тока с ионной проводимостью, или, иными словами, место, где электронный механизм переноса электрического заряда изменяется на ионный (и наоборот). В более узком смысле слова электродом часто называют проводник электрического тока с электронной проводимостью. n
Количественная оценка окислительно восстановительной способности веществ Электродные потенциалы. Электродом в электрохимии называется поверхность раздела между проводником электрического тока с электронной проводимостью и проводником электрического тока с ионной проводимостью, или, иными словами, место, где электронный механизм переноса электрического заряда изменяется на ионный (и наоборот). В более узком смысле слова электродом часто называют проводник электрического тока с электронной проводимостью. n
 Количественная оценка окислительно восстановительной способности веществ Стандартный электродный потенциал полуреакции (E 0, ϕ 0) это ЭДС гальванического элемента, состоящего из находящегося в стандартных условиях электрода, на котором протекает данная полуреакция, и стандартного водородного электрода. (А) Fe 3+ + e → Fe 2+ Восстановительный потенциал (Б) Fe 2+ e → Fe 3+ Окислительный потенциал Cr 2 O 72 + 14 H+ + 6 e → 2 Cr 3+ + 7 H 2 O E 0 = +1, 33 В Mn. O 4 + 8 H+ + 5 e → Mn 2+ + 4 H 2 O E 0 = +1, 51 В
Количественная оценка окислительно восстановительной способности веществ Стандартный электродный потенциал полуреакции (E 0, ϕ 0) это ЭДС гальванического элемента, состоящего из находящегося в стандартных условиях электрода, на котором протекает данная полуреакция, и стандартного водородного электрода. (А) Fe 3+ + e → Fe 2+ Восстановительный потенциал (Б) Fe 2+ e → Fe 3+ Окислительный потенциал Cr 2 O 72 + 14 H+ + 6 e → 2 Cr 3+ + 7 H 2 O E 0 = +1, 33 В Mn. O 4 + 8 H+ + 5 e → Mn 2+ + 4 H 2 O E 0 = +1, 51 В
 Стандартный водородный электрод n n n Условия измерений: температура 25 о. С, активность компонентов полуреакции равна 1 моль/л H 2(газ) = H 2 *(раствор) H*2 ↔ 2 H+ + 2 e
Стандартный водородный электрод n n n Условия измерений: температура 25 о. С, активность компонентов полуреакции равна 1 моль/л H 2(газ) = H 2 *(раствор) H*2 ↔ 2 H+ + 2 e
 Все системы в зависимости от величины стандартного редокс-потенциала можно условно разделить на три группы: 1. Если Eo 1 B, то Ox форма системы обладает сильными окислительными свойствами (система – окислитель). 2. Если Eo 0 B, то Red форма системы обладает сильными восстановительными свойствами (система – восстановитель). 3. Если 0 < Eo < 1 B, то система является редоксамфотерной, т. е. способной проявлять, как окислительные, так и восстановительные свойства, в зависимости от значения Eo системы, с которой она реагирует.
Все системы в зависимости от величины стандартного редокс-потенциала можно условно разделить на три группы: 1. Если Eo 1 B, то Ox форма системы обладает сильными окислительными свойствами (система – окислитель). 2. Если Eo 0 B, то Red форма системы обладает сильными восстановительными свойствами (система – восстановитель). 3. Если 0 < Eo < 1 B, то система является редоксамфотерной, т. е. способной проявлять, как окислительные, так и восстановительные свойства, в зависимости от значения Eo системы, с которой она реагирует.
 Количественная оценка окислительно восстановительной способности веществ Разность электродных потенциалов окислителя, участвующего в прямой реакции, и окисленной формы восстановителя, образующегося в процессе реакции, называется ЭДС реакции (ΔЕ). ЭДС = Е 0 Ox – Е 0 Red Если: 1. ЭДС > 0, то реакция протекает в прямом направлении. 2. ЭДС < 0, то реакция протекает в обратном направлении.
Количественная оценка окислительно восстановительной способности веществ Разность электродных потенциалов окислителя, участвующего в прямой реакции, и окисленной формы восстановителя, образующегося в процессе реакции, называется ЭДС реакции (ΔЕ). ЭДС = Е 0 Ox – Е 0 Red Если: 1. ЭДС > 0, то реакция протекает в прямом направлении. 2. ЭДС < 0, то реакция протекает в обратном направлении.
 Пример. Определить, может ли самопроизвольно протекать при стандартных условиях реакция окисления иодид-ионов ионами Fe 3+. 2 Fe 3+ + 2 I → 2 Fe 2+ + I 2 ΔE 0 = E 0 Fe 3+/Fe 2+ E 0 I 2/2 I− = 0, 771 0, 536 = 0, 235 В Данная реакция может самопроизвольно протекать в прямом направлении.
Пример. Определить, может ли самопроизвольно протекать при стандартных условиях реакция окисления иодид-ионов ионами Fe 3+. 2 Fe 3+ + 2 I → 2 Fe 2+ + I 2 ΔE 0 = E 0 Fe 3+/Fe 2+ E 0 I 2/2 I− = 0, 771 0, 536 = 0, 235 В Данная реакция может самопроизвольно протекать в прямом направлении.
 Влияние различных факторов на протекание окислительно восстановительных реакций 1. Температура. Влияние температуры на потенциал реакции видно из уравнения Нернста:
Влияние различных факторов на протекание окислительно восстановительных реакций 1. Температура. Влияние температуры на потенциал реакции видно из уравнения Нернста:
 Влияние различных факторов на протекание окислительно восстановительных реакций 2. Влияние р. Н: если в реакции принимают участие ионы водорода. Mn. O 4 + 8 H+ +5 e → Mn 2+ + 4 H 2 O
Влияние различных факторов на протекание окислительно восстановительных реакций 2. Влияние р. Н: если в реакции принимают участие ионы водорода. Mn. O 4 + 8 H+ +5 e → Mn 2+ + 4 H 2 O
 Влияние различных факторов на протекание окислительно восстановительных реакций 3. Образование малорастворимых соединений. Пример. Известно, что E 0 Ag+/Ag↓ = 0, 799 В, рассчитайте E 0 Ag. Cl ↓/Ag ↓
Влияние различных факторов на протекание окислительно восстановительных реакций 3. Образование малорастворимых соединений. Пример. Известно, что E 0 Ag+/Ag↓ = 0, 799 В, рассчитайте E 0 Ag. Cl ↓/Ag ↓
 Влияние различных факторов на протекание окислительно восстановительных реакций 4. Комплексообразование. Пример. Известно, что E 0 Fe 3+/Fe 2+= +0, 771 В. Рассчитайте величину Е 0[Fe(CN)6]3 /[Fe(CN)6]4
Влияние различных факторов на протекание окислительно восстановительных реакций 4. Комплексообразование. Пример. Известно, что E 0 Fe 3+/Fe 2+= +0, 771 В. Рассчитайте величину Е 0[Fe(CN)6]3 /[Fe(CN)6]4
 Влияние различных факторов на протекание окислительно восстановительных реакций n 5. Присутствие посторонних индифферентных ионов в растворе приводит, во первых, к повышению ионной силы раствора. Если коэффициенты активности окисленной и восстановленной формы при этом изменяются неодинаково, то изменяется и величина окислитель ного потенциала. Во вторых, посторонние ионы могут оказывать влияние на скорость реакции. Анионы влияют на реакцию между ка тионами, катионы на реакцию между анионами. Например, скорость реакции восстановления иона [Fe(CN)6]3 до [Fe(CN)6]4 максимальна, если в качестве катиона выступает ион K+. Иногда посторонние ионы могут являться катализаторами окислительно восстановительных ре акций. Например, ион. Ag+ является катализатором реакции окисления Mn 2+ до Mn. O 4 персульфат ионом.
Влияние различных факторов на протекание окислительно восстановительных реакций n 5. Присутствие посторонних индифферентных ионов в растворе приводит, во первых, к повышению ионной силы раствора. Если коэффициенты активности окисленной и восстановленной формы при этом изменяются неодинаково, то изменяется и величина окислитель ного потенциала. Во вторых, посторонние ионы могут оказывать влияние на скорость реакции. Анионы влияют на реакцию между ка тионами, катионы на реакцию между анионами. Например, скорость реакции восстановления иона [Fe(CN)6]3 до [Fe(CN)6]4 максимальна, если в качестве катиона выступает ион K+. Иногда посторонние ионы могут являться катализаторами окислительно восстановительных ре акций. Например, ион. Ag+ является катализатором реакции окисления Mn 2+ до Mn. O 4 персульфат ионом.
 Константа окислительно-восстановительного равновесия Рассмотрим реакцию: n 2 Ox 1 + n 1 Red 2 = n 2 Red 1 + n 1 Ox 2 состоящую их полуреакций: Ox 1 + n 1 e = Red 1 Ox 2 + n 2 e = Red 2
Константа окислительно-восстановительного равновесия Рассмотрим реакцию: n 2 Ox 1 + n 1 Red 2 = n 2 Red 1 + n 1 Ox 2 состоящую их полуреакций: Ox 1 + n 1 e = Red 1 Ox 2 + n 2 e = Red 2
 Термодинамическая константа равновесия этой реакции равна:
Термодинамическая константа равновесия этой реакции равна:
 В состоянии равновесия потенциалы составляющих реакцию полуреакций равны: В состоянии равновесия.
В состоянии равновесия потенциалы составляющих реакцию полуреакций равны: В состоянии равновесия.
 После преобразования получаем:
После преобразования получаем:


