Презентация5 Тк дых и ОФ.ppt
- Количество слайдов: 69
 ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ И ТРАНСПОРТНЫЕ СИСТЕМЫ МИТОХОНДРИЙ Итак, в результате окислительного декарбоксилирования ПВК и ЦТК образовались восстановительные эквиваленты - НАДН 2 и ФАДН 2. Образовались они при восстановлении (присоединении водорода) коферментов НАД+ и ФАД. Знак "+" включен в обозначение НАД+, чтобы показать, что эта молекула обычно несет положительный электрический заряд. НАД+ - это главный акцептор электронов при окислении топливных молекул. Реакциаонноспособная часть НАД+ - его никотинамидное кольцо
ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ И ТРАНСПОРТНЫЕ СИСТЕМЫ МИТОХОНДРИЙ Итак, в результате окислительного декарбоксилирования ПВК и ЦТК образовались восстановительные эквиваленты - НАДН 2 и ФАДН 2. Образовались они при восстановлении (присоединении водорода) коферментов НАД+ и ФАД. Знак "+" включен в обозначение НАД+, чтобы показать, что эта молекула обычно несет положительный электрический заряд. НАД+ - это главный акцептор электронов при окислении топливных молекул. Реакциаонноспособная часть НАД+ - его никотинамидное кольцо
 При окислении субстрата никотинамидное кольцо НАД+ присоединяет один протон и два электрона, при этом образуется НАД. Н 2 является главным промежуточным продуктом между ЦТК и ферментами во внутренней митохондриальной мембране, т. е. ферментами так называемой дыхательной цепи.
При окислении субстрата никотинамидное кольцо НАД+ присоединяет один протон и два электрона, при этом образуется НАД. Н 2 является главным промежуточным продуктом между ЦТК и ферментами во внутренней митохондриальной мембране, т. е. ферментами так называемой дыхательной цепи.
 Второй основной переносчик электронов - ФАД. Реакционноспособная часть ФАД - это его изоаллоксазиновое кольцо. Сами по себе НАДН 2 и ФАДН 2 еще не являются энергетическими молекулами. Для того, чтобы из них извлечь энергию, эти молекулы должны подвергнуться дальнейшему окислению в дыхательной цепи, которая расположена во внутренней мембране митохондрий.
Второй основной переносчик электронов - ФАД. Реакционноспособная часть ФАД - это его изоаллоксазиновое кольцо. Сами по себе НАДН 2 и ФАДН 2 еще не являются энергетическими молекулами. Для того, чтобы из них извлечь энергию, эти молекулы должны подвергнуться дальнейшему окислению в дыхательной цепи, которая расположена во внутренней мембране митохондрий.
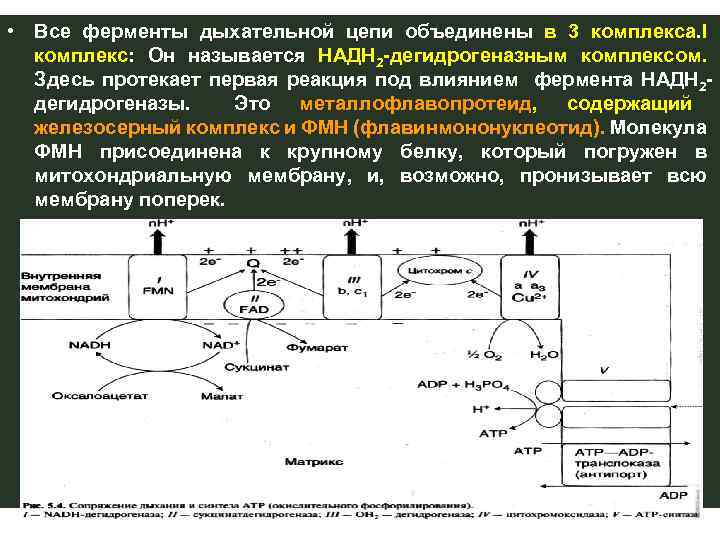 • Все ферменты дыхательной цепи объединены в 3 комплекса. I комплекс: Он называется НАДН 2 -дегидрогеназным комплексом. Здесь протекает первая реакция под влиянием фермента НАДН 2 - дегидрогеназы. Это металлофлавопротеид, содержащий железосерный комплекс и ФМН (флавинмононуклеотид). Молекула ФМН присоединена к крупному белку, который погружен в митохондриальную мембрану, и, возможно, пронизывает всю мембрану поперек.
• Все ферменты дыхательной цепи объединены в 3 комплекса. I комплекс: Он называется НАДН 2 -дегидрогеназным комплексом. Здесь протекает первая реакция под влиянием фермента НАДН 2 - дегидрогеназы. Это металлофлавопротеид, содержащий железосерный комплекс и ФМН (флавинмононуклеотид). Молекула ФМН присоединена к крупному белку, который погружен в митохондриальную мембрану, и, возможно, пронизывает всю мембрану поперек.
 При взаимодействии НАДН 2 с 1 -м комплексом НАДН 2 передает один протон и два электрона на ФМН. Кроме того, дополнительный протон ФМН забирает из внутренней среды. Так образуется восстановленная форма ФМН. Н 2: НАДН + Н+ + ФМН. Н 2 + НАД+ ФМН. Н 2 переносит два протона водорода с внутренней поверхности мембраны на внешнюю, т. е. сквозь мембрану в межмембранное пространство.
При взаимодействии НАДН 2 с 1 -м комплексом НАДН 2 передает один протон и два электрона на ФМН. Кроме того, дополнительный протон ФМН забирает из внутренней среды. Так образуется восстановленная форма ФМН. Н 2: НАДН + Н+ + ФМН. Н 2 + НАД+ ФМН. Н 2 переносит два протона водорода с внутренней поверхности мембраны на внешнюю, т. е. сквозь мембрану в межмембранное пространство.
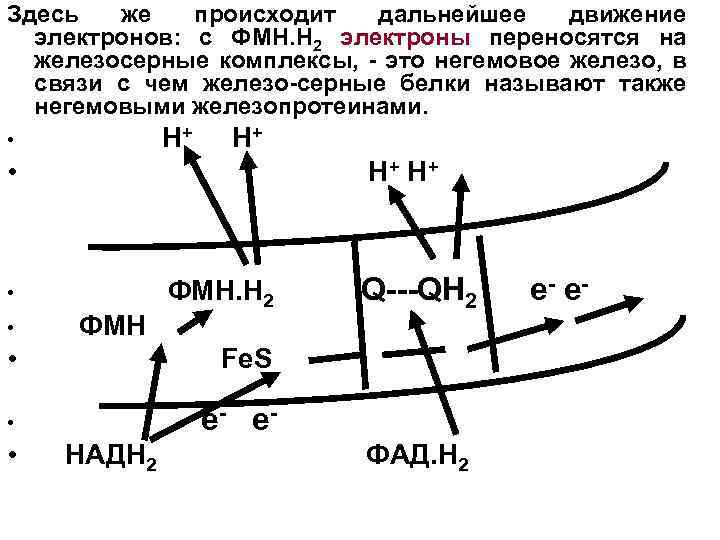 Здесь же происходит дальнейшее движение электронов: с ФМН. H 2 электроны переносятся на железосерные комплексы, - это негемовое железо, в связи с чем железо-серные белки называют также негемовыми железопротеинами. • H+ H+ • Н + Н+ • ФМН. H 2 Q---QH 2 е- е - • ФМН • Fe. S • e- e - • НАДН 2 ФАД. Н 2
Здесь же происходит дальнейшее движение электронов: с ФМН. H 2 электроны переносятся на железосерные комплексы, - это негемовое железо, в связи с чем железо-серные белки называют также негемовыми железопротеинами. • H+ H+ • Н + Н+ • ФМН. H 2 Q---QH 2 е- е - • ФМН • Fe. S • e- e - • НАДН 2 ФАД. Н 2
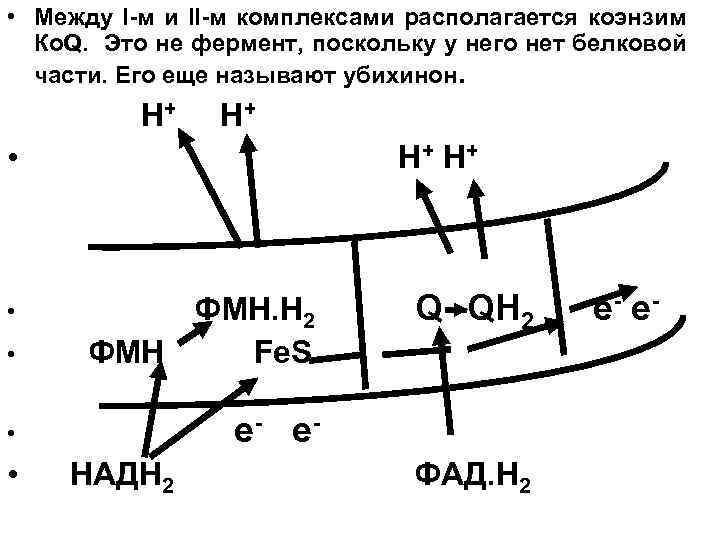 • Между I-м и II-м комплексами располагается коэнзим Ко. Q. Это не фермент, поскольку у него нет белковой части. Его еще называют убихинон. H+ • Н + Н+ • ФМН. H 2 Q--QH 2 е- е - • ФМН Fe. S • e- e - • НАДН 2 ФАД. Н 2
• Между I-м и II-м комплексами располагается коэнзим Ко. Q. Это не фермент, поскольку у него нет белковой части. Его еще называют убихинон. H+ • Н + Н+ • ФМН. H 2 Q--QH 2 е- е - • ФМН Fe. S • e- e - • НАДН 2 ФАД. Н 2
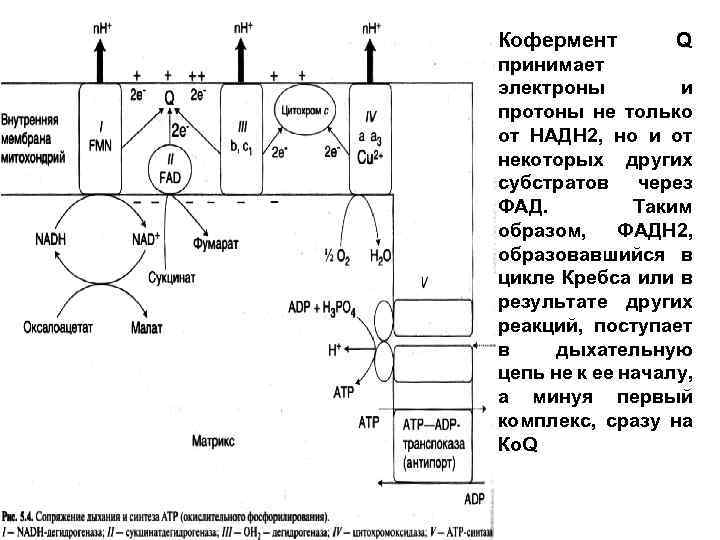 Кофермент Q принимает электроны и протоны не только от НАДН 2, но и от некоторых других субстратов через ФАД. Таким образом, ФАДН 2, образовавшийся в цикле Кребса или в результате других реакций, поступает в дыхательную цепь не к ее началу, а минуя первый комплекс, сразу на Ко. Q
Кофермент Q принимает электроны и протоны не только от НАДН 2, но и от некоторых других субстратов через ФАД. Таким образом, ФАДН 2, образовавшийся в цикле Кребса или в результате других реакций, поступает в дыхательную цепь не к ее началу, а минуя первый комплекс, сразу на Ко. Q
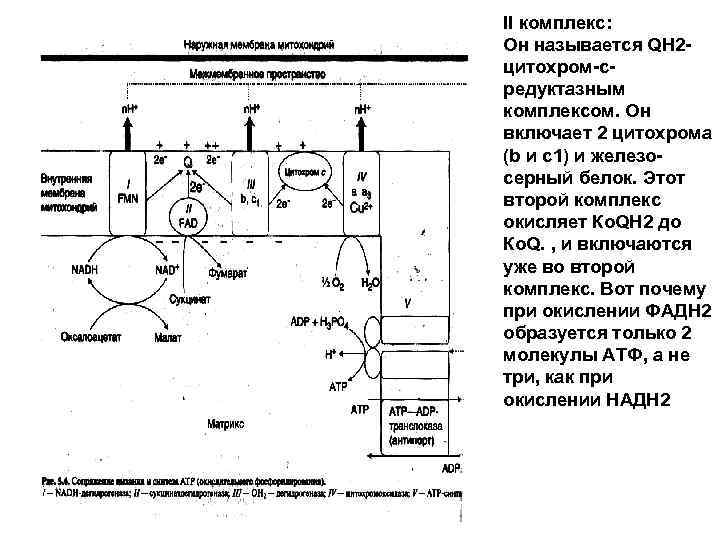 II комплекс: Он называется QH 2 - цитохром-с- редуктазным комплексом. Он включает 2 цитохрома (b и c 1) и железо- серный белок. Этот второй комплекс окисляет Ко. QH 2 до Ко. Q. , и включаются уже во второй комплекс. Вот почему при окислении ФАДН 2 образуется только 2 молекулы АТФ, а не три, как при окислении НАДН 2
II комплекс: Он называется QH 2 - цитохром-с- редуктазным комплексом. Он включает 2 цитохрома (b и c 1) и железо- серный белок. Этот второй комплекс окисляет Ко. QH 2 до Ко. Q. , и включаются уже во второй комплекс. Вот почему при окислении ФАДН 2 образуется только 2 молекулы АТФ, а не три, как при окислении НАДН 2
 Молекула QH 2, восстановленной формы убихинона, переносит свои электроны на цитохром b. Далее - перенос электронов на железосерный комплекс, затем на цитохром с1 и далее - на цитохром с. Цитохромы - это переносящий электроны белки, которые содержат в качестве простетической группы гем. В ходе переноса электронов атом железа находится то в восстановленной форме (+2), то в окисленной форме (+3).
Молекула QH 2, восстановленной формы убихинона, переносит свои электроны на цитохром b. Далее - перенос электронов на железосерный комплекс, затем на цитохром с1 и далее - на цитохром с. Цитохромы - это переносящий электроны белки, которые содержат в качестве простетической группы гем. В ходе переноса электронов атом железа находится то в восстановленной форме (+2), то в окисленной форме (+3).
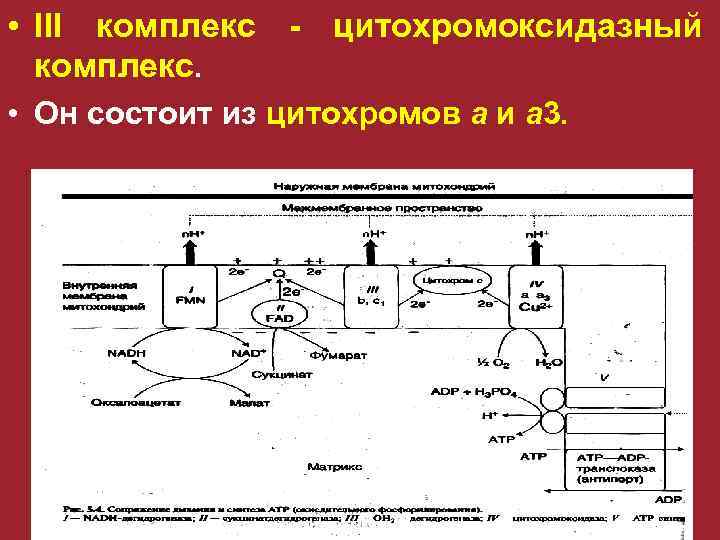 • III комплекс - цитохромоксидазный комплекс. • Он состоит из цитохромов а и а 3.
• III комплекс - цитохромоксидазный комплекс. • Он состоит из цитохромов а и а 3.
 III комплекс принимает от цитохрома с четыре электрона (по одному) и передает их на одну молекулу связанного О 2. • Каждые два электрона сначала попадают к цитохрому а. Затем они переходят к цитохрому а 3. а затем электроны переходят на атом кислорода, который связан с атомом меди и с гемом цитохрома а 3. • Водород, необходимый для образования воды, захватываются из внутренней среды Мх, так образуются две молекулы воды. • На этой стадии образуется еще одна - третья молекула АТФ.
III комплекс принимает от цитохрома с четыре электрона (по одному) и передает их на одну молекулу связанного О 2. • Каждые два электрона сначала попадают к цитохрому а. Затем они переходят к цитохрому а 3. а затем электроны переходят на атом кислорода, который связан с атомом меди и с гемом цитохрома а 3. • Водород, необходимый для образования воды, захватываются из внутренней среды Мх, так образуются две молекулы воды. • На этой стадии образуется еще одна - третья молекула АТФ.
 • В каждом из 3 пунктов: • 1 -й пункт - это НАДН-дегидрогеназный комплекс; • 2 -й пункт - QН 2 -цитохром -с-редуктазный комплекс; • 3 -й пункт - цитохром-с-оксидазный комплекс • при переносе пары электронов от НАДН 2 одновременно на наружную поверхность внутренней мембраны Мх, т. е. в межмембранное пространство выносится по паре протонов.
• В каждом из 3 пунктов: • 1 -й пункт - это НАДН-дегидрогеназный комплекс; • 2 -й пункт - QН 2 -цитохром -с-редуктазный комплекс; • 3 -й пункт - цитохром-с-оксидазный комплекс • при переносе пары электронов от НАДН 2 одновременно на наружную поверхность внутренней мембраны Мх, т. е. в межмембранное пространство выносится по паре протонов.

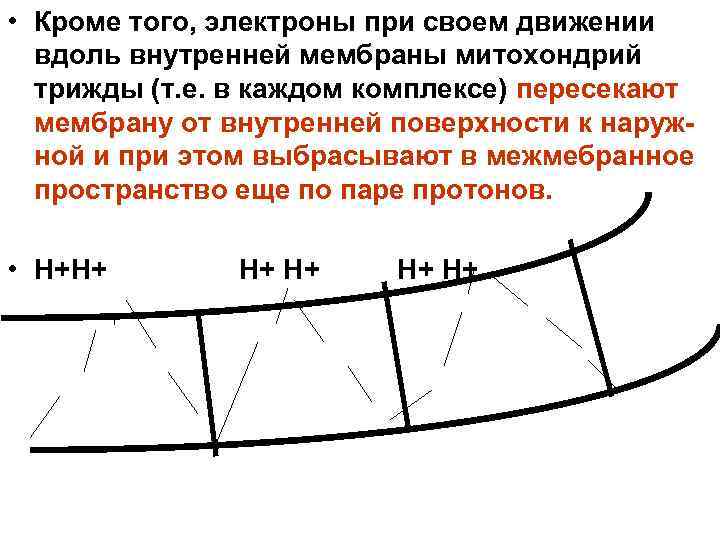 • Кроме того, электроны при своем движении вдоль внутренней мембраны митохондрий трижды (т. е. в каждом комплексе) пересекают мембрану от внутренней поверхности к наруж- ной и при этом выбрасывают в межмебранное пространство еще по паре протонов. • Н+Н+ Н+ Н+
• Кроме того, электроны при своем движении вдоль внутренней мембраны митохондрий трижды (т. е. в каждом комплексе) пересекают мембрану от внутренней поверхности к наруж- ной и при этом выбрасывают в межмебранное пространство еще по паре протонов. • Н+Н+ Н+ Н+
 Поток электронов в Мх представляет собой не что иное, как электрический ток. Благодаря этому потоку протонов создается большая разница в концентрации Н+ между наружной поверхностью внутренней мембраны и матриксом, т. е. создается протонный градиент. Это и является условием для образования АТФ.
Поток электронов в Мх представляет собой не что иное, как электрический ток. Благодаря этому потоку протонов создается большая разница в концентрации Н+ между наружной поверхностью внутренней мембраны и матриксом, т. е. создается протонный градиент. Это и является условием для образования АТФ.
 ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ И ТРАНСПОРТНЫЕ СИСТЕМЫ МИТОХОНДРИЙ Итак, в результате окислительного декарбоксилирования ПВК и ЦТК образовались восстановительные эквиваленты - НАДН 2 и ФАДН 2. Образовались они при восстановлении (присоединении водорода) коферментов НАД+ и ФАД. Знак "+" включен в обозначение НАД+, чтобы показать, что эта молекула обычно несет положительный электрический заряд. НАД+ - это главный акцептор электронов при окислении топливных молекул. Реакциаонноспособная часть НАД+ - его никотинамидное кольцо
ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ И ТРАНСПОРТНЫЕ СИСТЕМЫ МИТОХОНДРИЙ Итак, в результате окислительного декарбоксилирования ПВК и ЦТК образовались восстановительные эквиваленты - НАДН 2 и ФАДН 2. Образовались они при восстановлении (присоединении водорода) коферментов НАД+ и ФАД. Знак "+" включен в обозначение НАД+, чтобы показать, что эта молекула обычно несет положительный электрический заряд. НАД+ - это главный акцептор электронов при окислении топливных молекул. Реакциаонноспособная часть НАД+ - его никотинамидное кольцо
 При окислении субстрата никотинамидное кольцо НАД+ присоединяет один протон и два электрона, при этом образуется НАД. Н 2 является главным промежуточным продуктом между ЦТК и ферментами во внутренней митохондриальной мембране, т. е. ферментами так называемой дыхательной цепи.
При окислении субстрата никотинамидное кольцо НАД+ присоединяет один протон и два электрона, при этом образуется НАД. Н 2 является главным промежуточным продуктом между ЦТК и ферментами во внутренней митохондриальной мембране, т. е. ферментами так называемой дыхательной цепи.
 Второй основной переносчик электронов - ФАД. Реакционноспособная часть ФАД - это его изоаллоксазиновое кольцо. Сами по себе НАДН 2 и ФАДН 2 еще не являются энергетическими молекулами. Для того, чтобы из них извлечь энергию, эти молекулы должны подвергнуться дальнейшему окислению в дыхательной цепи, которая расположена в митохондриях.
Второй основной переносчик электронов - ФАД. Реакционноспособная часть ФАД - это его изоаллоксазиновое кольцо. Сами по себе НАДН 2 и ФАДН 2 еще не являются энергетическими молекулами. Для того, чтобы из них извлечь энергию, эти молекулы должны подвергнуться дальнейшему окислению в дыхательной цепи, которая расположена в митохондриях.

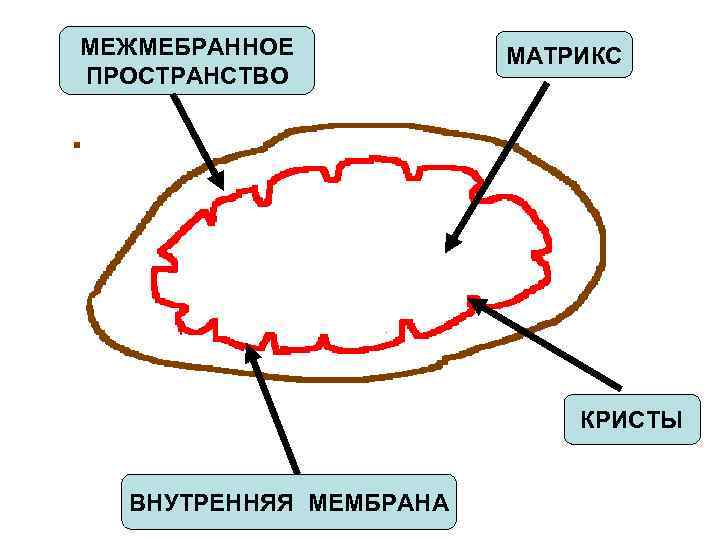 МЕЖМЕБРАННОЕ МАТРИКС ПРОСТРАНСТВО КРИСТЫ ВНУТРЕННЯЯ МЕМБРАНА
МЕЖМЕБРАННОЕ МАТРИКС ПРОСТРАНСТВО КРИСТЫ ВНУТРЕННЯЯ МЕМБРАНА
 • В матриксе содержатся ферменты окислительного декарбоксилирования ПВК и ферменты ЦТК. • Ферменты же дыхательной цепи встроены во внутреннюю митохондриальную мембрану и важны для всего процесса терминального окисления и, в особенности, для окислительного фосфорилирования.
• В матриксе содержатся ферменты окислительного декарбоксилирования ПВК и ферменты ЦТК. • Ферменты же дыхательной цепи встроены во внутреннюю митохондриальную мембрану и важны для всего процесса терминального окисления и, в особенности, для окислительного фосфорилирования.
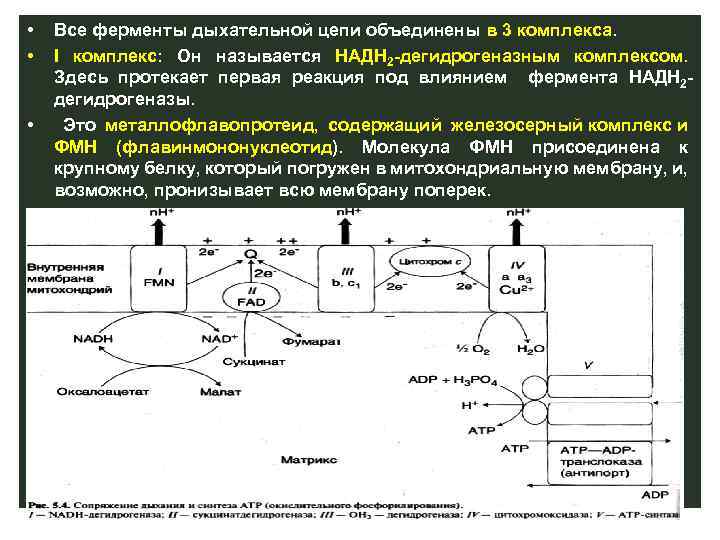 • Все ферменты дыхательной цепи объединены в 3 комплекса. • I комплекс: Он называется НАДН 2 -дегидрогеназным комплексом. Здесь протекает первая реакция под влиянием фермента НАДН 2 - дегидрогеназы. • Это металлофлавопротеид, содержащий железосерный комплекс и ФМН (флавинмононуклеотид). Молекула ФМН присоединена к крупному белку, который погружен в митохондриальную мембрану, и, возможно, пронизывает всю мембрану поперек.
• Все ферменты дыхательной цепи объединены в 3 комплекса. • I комплекс: Он называется НАДН 2 -дегидрогеназным комплексом. Здесь протекает первая реакция под влиянием фермента НАДН 2 - дегидрогеназы. • Это металлофлавопротеид, содержащий железосерный комплекс и ФМН (флавинмононуклеотид). Молекула ФМН присоединена к крупному белку, который погружен в митохондриальную мембрану, и, возможно, пронизывает всю мембрану поперек.
 При взаимодействии НАДН 2 с 1 -м комплексом НАДН 2 передает один протон и два электрона на ФМН. Кроме того, дополнительный протон ФМН забирает из внутренней среды. Так образуется восстановленная форма ФМН. Н 2: НАДН + Н+ + ФМН. Н 2 + НАД+ ФМН. Н 2 переносит два атома водорода с внутренней поверхности мембраны на внешнюю. Там водород ионизируется, и образовавшиеся протоны высвобождаются наружу, так что первые два протона переходят сквозь мембрану в межмембранное пространство.
При взаимодействии НАДН 2 с 1 -м комплексом НАДН 2 передает один протон и два электрона на ФМН. Кроме того, дополнительный протон ФМН забирает из внутренней среды. Так образуется восстановленная форма ФМН. Н 2: НАДН + Н+ + ФМН. Н 2 + НАД+ ФМН. Н 2 переносит два атома водорода с внутренней поверхности мембраны на внешнюю. Там водород ионизируется, и образовавшиеся протоны высвобождаются наружу, так что первые два протона переходят сквозь мембрану в межмембранное пространство.
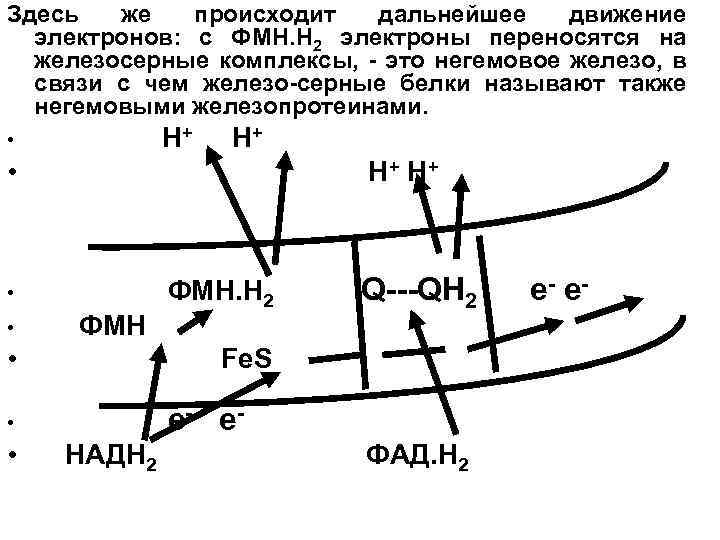 Здесь же происходит дальнейшее движение электронов: с ФМН. H 2 электроны переносятся на железосерные комплексы, - это негемовое железо, в связи с чем железо-серные белки называют также негемовыми железопротеинами. • H+ • Н + Н+ • ФМН. H 2 Q---QH 2 е- е - • ФМН • Fe. S • e- e - • НАДН 2 ФАД. Н 2
Здесь же происходит дальнейшее движение электронов: с ФМН. H 2 электроны переносятся на железосерные комплексы, - это негемовое железо, в связи с чем железо-серные белки называют также негемовыми железопротеинами. • H+ • Н + Н+ • ФМН. H 2 Q---QH 2 е- е - • ФМН • Fe. S • e- e - • НАДН 2 ФАД. Н 2
 • Между I-м и II-м комплексами располагается Ко. Q. Это не фермент, поскольку у него нет белковой части. Его еще называют убихинон.
• Между I-м и II-м комплексами располагается Ко. Q. Это не фермент, поскольку у него нет белковой части. Его еще называют убихинон.
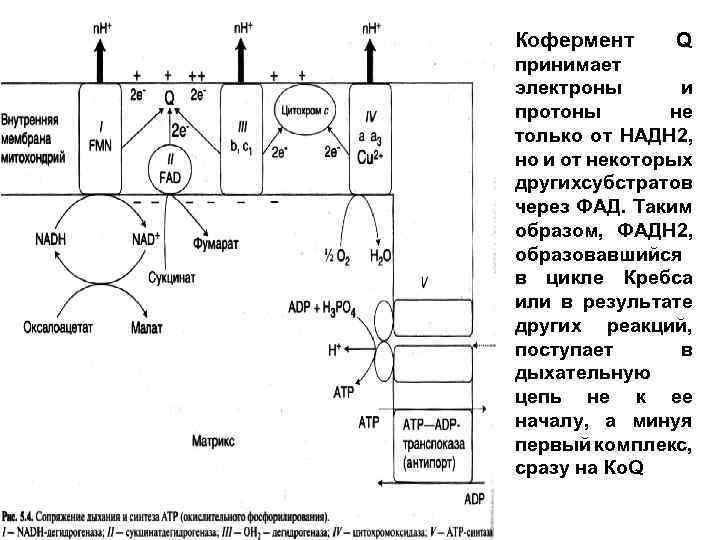 Кофермент Q принимает электроны и протоны не только от НАДН 2, но и от некоторых другихсубстратов через ФАД. Таким образом, ФАДН 2, образовавшийся в цикле Кребса или в результате других реакций, поступает в дыхательную цепь не к ее началу, а минуя первый комплекс, сразу на Ко. Q
Кофермент Q принимает электроны и протоны не только от НАДН 2, но и от некоторых другихсубстратов через ФАД. Таким образом, ФАДН 2, образовавшийся в цикле Кребса или в результате других реакций, поступает в дыхательную цепь не к ее началу, а минуя первый комплекс, сразу на Ко. Q
 II комплекс: Он называется QH 2 -цитохром-с- редуктазным комплексом. Он включает 2 цитохрома (b и c 1) и железо-серный белок. Этот второй комплекс окисляет Ко. QH 2 до Ко. Q. , и включаются уже во второй комплекс. Вот почему при окислении ФАДН 2 образуется только 2 молекулы АТФ, а не три, как при окислении НАДН 2
II комплекс: Он называется QH 2 -цитохром-с- редуктазным комплексом. Он включает 2 цитохрома (b и c 1) и железо-серный белок. Этот второй комплекс окисляет Ко. QH 2 до Ко. Q. , и включаются уже во второй комплекс. Вот почему при окислении ФАДН 2 образуется только 2 молекулы АТФ, а не три, как при окислении НАДН 2
 Молекула QH 2, восстановленной формы убихинона, переносит свои электроны на цитохром b. Далее - перенос электронов на железосерный комплекс, затем на цитохром с1 и далее - на цитохром с. Цитохромы - это переносящий электроны белки, которые содержат в качестве простетической группы гем. В ходе переноса электронов атом железа находится то в восстановленной форме (+2), то в окисленной форме (+3).
Молекула QH 2, восстановленной формы убихинона, переносит свои электроны на цитохром b. Далее - перенос электронов на железосерный комплекс, затем на цитохром с1 и далее - на цитохром с. Цитохромы - это переносящий электроны белки, которые содержат в качестве простетической группы гем. В ходе переноса электронов атом железа находится то в восстановленной форме (+2), то в окисленной форме (+3).
 В процессе работы второго комплекса также происходит выброс Н+ на наружную поверхность внутренней мембраны МХ, а следовательно, есть возможность образования энергетического потенциала. Т. е. здесь образуется вторая молекула АТФ. Цитохром с переносит электроны на следующий III комплекс
В процессе работы второго комплекса также происходит выброс Н+ на наружную поверхность внутренней мембраны МХ, а следовательно, есть возможность образования энергетического потенциала. Т. е. здесь образуется вторая молекула АТФ. Цитохром с переносит электроны на следующий III комплекс
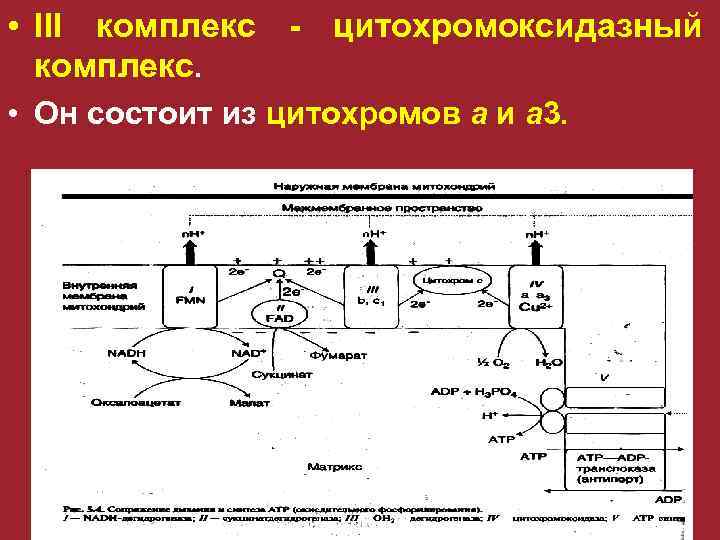 • III комплекс - цитохромоксидазный комплекс. • Он состоит из цитохромов а и а 3.
• III комплекс - цитохромоксидазный комплекс. • Он состоит из цитохромов а и а 3.
 III комплекс принимает от цитохрома с четыре электрона (по одному) и передает их на одну молекулу связанного О 2. • Каждые два электрона сначала попадают к цитохрому а. Затем они переходят к цитохрому а 3. а затем электроны переходят на атом кислорода, который связан с атомом меди и с гемом цитохрома а 3. • Водород, необходимый для образования воды, захватываются из внутренней среды Мх, так образуются две молекулы воды. • На этой стадии образуется еще одна - третья молекула АТФ.
III комплекс принимает от цитохрома с четыре электрона (по одному) и передает их на одну молекулу связанного О 2. • Каждые два электрона сначала попадают к цитохрому а. Затем они переходят к цитохрому а 3. а затем электроны переходят на атом кислорода, который связан с атомом меди и с гемом цитохрома а 3. • Водород, необходимый для образования воды, захватываются из внутренней среды Мх, так образуются две молекулы воды. • На этой стадии образуется еще одна - третья молекула АТФ.
 • В каждом из 3 пунктов: • 1 -й пункт - это НАДН-дегидрогеназный комплекс; • 2 -й пункт - QН 2 -цитохром -с-редуктазный комплекс; • 3 -й пункт - цитохром-с-оксидазный комплекс • при переносе пары электронов от НАДН 2 одновременно на наружную поверхность внутренней мембраны Мх, т. е. в межмембранное пространство выносится по паре протонов.
• В каждом из 3 пунктов: • 1 -й пункт - это НАДН-дегидрогеназный комплекс; • 2 -й пункт - QН 2 -цитохром -с-редуктазный комплекс; • 3 -й пункт - цитохром-с-оксидазный комплекс • при переносе пары электронов от НАДН 2 одновременно на наружную поверхность внутренней мембраны Мх, т. е. в межмембранное пространство выносится по паре протонов.

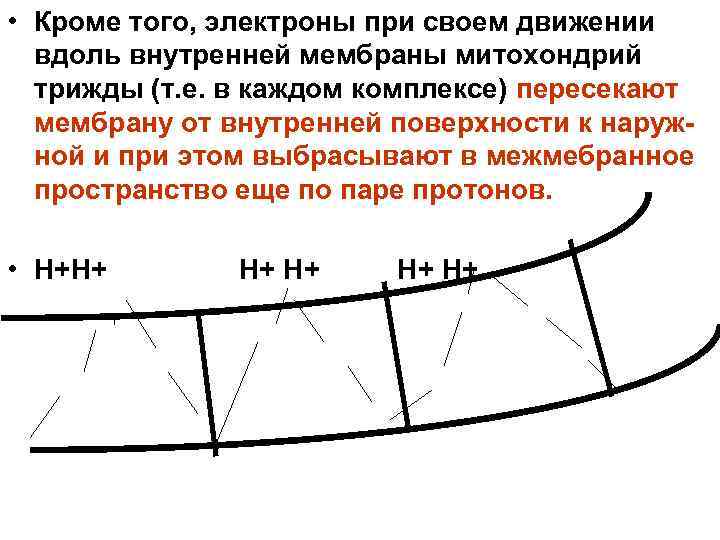 • Кроме того, электроны при своем движении вдоль внутренней мембраны митохондрий трижды (т. е. в каждом комплексе) пересекают мембрану от внутренней поверхности к наруж- ной и при этом выбрасывают в межмебранное пространство еще по паре протонов. • Н+Н+ Н+ Н+
• Кроме того, электроны при своем движении вдоль внутренней мембраны митохондрий трижды (т. е. в каждом комплексе) пересекают мембрану от внутренней поверхности к наруж- ной и при этом выбрасывают в межмебранное пространство еще по паре протонов. • Н+Н+ Н+ Н+
 Поток электронов в Мх представляет собой не что иное, как электрический ток. Разница потенциалов между НАДН 2 и О 2 составляет около 1, 2 мэ. В, а суммарный ток в Мх человека в состоянии покоя составляет около 100 А, так что общая мощность равна 120 Вт. Благодаря этому потоку протонов создается большая разница в концентрации Н+ между наружной поверхностью внутренней мембраны и матриксом, т. е. создается протонный градиент. Это и является условием для образования АТФ.
Поток электронов в Мх представляет собой не что иное, как электрический ток. Разница потенциалов между НАДН 2 и О 2 составляет около 1, 2 мэ. В, а суммарный ток в Мх человека в состоянии покоя составляет около 100 А, так что общая мощность равна 120 Вт. Благодаря этому потоку протонов создается большая разница в концентрации Н+ между наружной поверхностью внутренней мембраны и матриксом, т. е. создается протонный градиент. Это и является условием для образования АТФ.
 МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ • Свободная энергия, высвобождающаяся при окислении питательных веществ, прежде чем быть использованной клетками, должна быть преобразована в специальную форму. Таким специальным носителем свободной энергии, своего рода энергетической валютой, является аденозинтрифосфат (АТФ). Это нуклеотид, состоящий из остатков аденина, рибозы и трех молекул фосфорной кислоты: А-R-P-P-P.
МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ • Свободная энергия, высвобождающаяся при окислении питательных веществ, прежде чем быть использованной клетками, должна быть преобразована в специальную форму. Таким специальным носителем свободной энергии, своего рода энергетической валютой, является аденозинтрифосфат (АТФ). Это нуклеотид, состоящий из остатков аденина, рибозы и трех молекул фосфорной кислоты: А-R-P-P-P.
 • АТФ - молекула богатая энергией, поскольку ее трифосфатный компонент содержит 2 фосфангидридные связи. При гидролизе АТФ до АДФ и ортофосфата (Рi) или до АМФ и пирофосфата (РРi) высвобождается большое количество свободной энергии. При условиях, существующих в клетке, эта величина (дельта G) составляет около 12 ккал/моль. АТФ, АДФ и АМФ могут превращаться друг в друга. Благодаря этому АТФ является переносчиком активированных фосфатных групп.
• АТФ - молекула богатая энергией, поскольку ее трифосфатный компонент содержит 2 фосфангидридные связи. При гидролизе АТФ до АДФ и ортофосфата (Рi) или до АМФ и пирофосфата (РРi) высвобождается большое количество свободной энергии. При условиях, существующих в клетке, эта величина (дельта G) составляет около 12 ккал/моль. АТФ, АДФ и АМФ могут превращаться друг в друга. Благодаря этому АТФ является переносчиком активированных фосфатных групп.
 • В некоторых случаях такими переносчиками могут быть нуклеотиды - аналоги АТФ, а именно: гуанозинтрифосфат (ГТФ), уридинтрифосфат (УТФ) и цитидинтрифосфат (ЦТФ). Тогда биосинтетические реакции запускаются ими. • АТФ - не является формой запасания свободной энергии в организме. Это главный непосредственно используемый донор свободной энергии в биологических системах.
• В некоторых случаях такими переносчиками могут быть нуклеотиды - аналоги АТФ, а именно: гуанозинтрифосфат (ГТФ), уридинтрифосфат (УТФ) и цитидинтрифосфат (ЦТФ). Тогда биосинтетические реакции запускаются ими. • АТФ - не является формой запасания свободной энергии в организме. Это главный непосредственно используемый донор свободной энергии в биологических системах.
 В обычной клетке молекула АТФ расходуется в течение 1 мин после ее образования. Оборот АТФ очень высок. Например, человек в покое расходует около 40 кг АТФ за 24 ч. Во время интенсивных упражнений скорость использования АТФ может достигать 0, 5 кг/мин.
В обычной клетке молекула АТФ расходуется в течение 1 мин после ее образования. Оборот АТФ очень высок. Например, человек в покое расходует около 40 кг АТФ за 24 ч. Во время интенсивных упражнений скорость использования АТФ может достигать 0, 5 кг/мин.
 Целый ряд других соединений в биологических системах имеют высокий потенциал переноса фосфатной группы: креатинфосфат, фосфоэнолпировиноградная кислота (ФЭПК), ацетилфосфат, 1, 3 -дифосфоглицериновая кислота (ДГК).
Целый ряд других соединений в биологических системах имеют высокий потенциал переноса фосфатной группы: креатинфосфат, фосфоэнолпировиноградная кислота (ФЭПК), ацетилфосфат, 1, 3 -дифосфоглицериновая кислота (ДГК).
 АТФ образуется из АДФ путем присоединения к нему фосфатной группы, т. е. путем фосфорилирования АДФ. Эти реакции называются реакциями окислительного фосфорилирования на уровне дыхательной цепи.
АТФ образуется из АДФ путем присоединения к нему фосфатной группы, т. е. путем фосфорилирования АДФ. Эти реакции называются реакциями окислительного фосфорилирования на уровне дыхательной цепи.
 В процессе терминального окисления (тканевое дыхание + окислительное фосфорилирование) происходит преобразование химической энергии, освобождаемой при окислении топливных молекул сначала в электрохимическую энергию, а затем снова в химическую энергию в форме высокоэнергетических фосфатов. Т. е. процессы окисления в дыхательной цепи должны быть тесно связаны, сопряжены с процессом окислительного фосфорилирования.
В процессе терминального окисления (тканевое дыхание + окислительное фосфорилирование) происходит преобразование химической энергии, освобождаемой при окислении топливных молекул сначала в электрохимическую энергию, а затем снова в химическую энергию в форме высокоэнергетических фосфатов. Т. е. процессы окисления в дыхательной цепи должны быть тесно связаны, сопряжены с процессом окислительного фосфорилирования.
 Сопряжение между окислением НАДН 2 и фосфорилированием АДФ происходит с помощью механизма, который постулировал Питер Митчелл в 1961 г. Это хемиосмотический механизм. Митчелл предположил, что сопряжение переноса электронов и синтеза АТФ обеспечивается протонным градиентом, т. е. разницей в концентрации протонов между внутренней и внешней стороной внутренней митохондриальной мембраны.
Сопряжение между окислением НАДН 2 и фосфорилированием АДФ происходит с помощью механизма, который постулировал Питер Митчелл в 1961 г. Это хемиосмотический механизм. Митчелл предположил, что сопряжение переноса электронов и синтеза АТФ обеспечивается протонным градиентом, т. е. разницей в концентрации протонов между внутренней и внешней стороной внутренней митохондриальной мембраны.
 • Согласно этой модели перенос электронов по дыхательной цепи приводит к выбросу протонов из матрикса в межмембранное пространство, где таким образом возрастает концентрация ионов Н+. • Протонный градиент, образованный окислительным транспортом электронов, представляет собой резервуар свободной энергии. Теперь, если обеспечить поток протонов обратно сквозь мембрану, можно получить энергию.
• Согласно этой модели перенос электронов по дыхательной цепи приводит к выбросу протонов из матрикса в межмембранное пространство, где таким образом возрастает концентрация ионов Н+. • Протонный градиент, образованный окислительным транспортом электронов, представляет собой резервуар свободной энергии. Теперь, если обеспечить поток протонов обратно сквозь мембрану, можно получить энергию.
 Энергия накапливается в протонном градиенте за счет двух компонентов: 1 -й компонент - это разница в концентрации протонов на противоположных сторонах мембраны. Концентрационный градиент протонов обозначается как дельта р. Н (δ р. Н). Энергия концентрационного градиента не зависит от абсолютной величины р. Н. Она обусловлена разницей р. Н по
Энергия накапливается в протонном градиенте за счет двух компонентов: 1 -й компонент - это разница в концентрации протонов на противоположных сторонах мембраны. Концентрационный градиент протонов обозначается как дельта р. Н (δ р. Н). Энергия концентрационного градиента не зависит от абсолютной величины р. Н. Она обусловлена разницей р. Н по
 2) Но протон является заряженной частицей. Поэтому второй компонент энергии протонного градиента - это градиент электрического заряда протонов. Движение зарядов через мембрану создает разницу в электрическом потенциале. В результате возникает электростатическое поле, которое действует на все заряженные частицы. Этот компонент обозначается как мембранный потенциал - дельта пси (δ ) и
2) Но протон является заряженной частицей. Поэтому второй компонент энергии протонного градиента - это градиент электрического заряда протонов. Движение зарядов через мембрану создает разницу в электрическом потенциале. В результате возникает электростатическое поле, которое действует на все заряженные частицы. Этот компонент обозначается как мембранный потенциал - дельта пси (δ ) и
 Общая энергия протонного градиента, т. е. разность электрохимического потенциала протонов - это сумма концентрационного (или осмотического) и электрического компонентов: Н = р. Н + = 230 -240 мэ. В. • Таким образом, основной смысл хемиосмотического механизма состоит в том, что первичным запасающим энергию актом является перенос протонов через внутреннюю митохондриальную
Общая энергия протонного градиента, т. е. разность электрохимического потенциала протонов - это сумма концентрационного (или осмотического) и электрического компонентов: Н = р. Н + = 230 -240 мэ. В. • Таким образом, основной смысл хемиосмотического механизма состоит в том, что первичным запасающим энергию актом является перенос протонов через внутреннюю митохондриальную
 • Сопряжение тканевого дыхания и окислительного фосфорилирования определяется уникальными свойствами внутренней митохондриальной мембраны. Она плотнее, чем наружная Мх-мембрана. За счет этого она выдерживает высокое электрическое напряжение, имеет высокое электрическое сопротивление. • Мембрана находится под огромным напряжением (400 000 мэ. В/см). Такое напряжение может выдерживать только неповрежденная мембрана.
• Сопряжение тканевого дыхания и окислительного фосфорилирования определяется уникальными свойствами внутренней митохондриальной мембраны. Она плотнее, чем наружная Мх-мембрана. За счет этого она выдерживает высокое электрическое напряжение, имеет высокое электрическое сопротивление. • Мембрана находится под огромным напряжением (400 000 мэ. В/см). Такое напряжение может выдерживать только неповрежденная мембрана.
 • При повреждении мембраны (недостаток кислорода - гипоксия или, наоборот, подача большого количества О 2, активация перекисного окисления липидов, набухание митохондрий) ведет к пробою мембраны. В этом случае протоны не могут накапливаться в межмембранном пространстве, и Мх не выполняет своей главной функции - производства энергии и снабжения этой энергией всей клетки.
• При повреждении мембраны (недостаток кислорода - гипоксия или, наоборот, подача большого количества О 2, активация перекисного окисления липидов, набухание митохондрий) ведет к пробою мембраны. В этом случае протоны не могут накапливаться в межмембранном пространстве, и Мх не выполняет своей главной функции - производства энергии и снабжения этой энергией всей клетки.
 Пути расходования энергии Н: • 1) Использование на механическую работу (движение сперматозоидов, вращение жгутиков). • 2) Использование на осмотическую работу (перенос частиц через мембраны, например, перенос в матрикс митохондрий ионов Са 2+, или вынос ионов Н+ в полость желудка при образовании соляной кислоты). • .
Пути расходования энергии Н: • 1) Использование на механическую работу (движение сперматозоидов, вращение жгутиков). • 2) Использование на осмотическую работу (перенос частиц через мембраны, например, перенос в матрикс митохондрий ионов Са 2+, или вынос ионов Н+ в полость желудка при образовании соляной кислоты). • .
 • 3) Использование на теплообразование. • 4) Использование для образования АТФ. Для внутриклеточных процессов энергия может использоваться только в виде АТФ. Только в 3 -х точках дыхательной цепи создается достаточный уровень дельта-мю. Н+, а следовательно только в этих трех точках может образоваться АТФ
• 3) Использование на теплообразование. • 4) Использование для образования АТФ. Для внутриклеточных процессов энергия может использоваться только в виде АТФ. Только в 3 -х точках дыхательной цепи создается достаточный уровень дельта-мю. Н+, а следовательно только в этих трех точках может образоваться АТФ
 • Синтез АТФ осуществляется с помощью митохондриальной АТФ-азы (АТФ- синтетаза). Митохондриальная АТФ-аза состоит из нескольких частей: 1 -я часть называется сопрягающий фактор 1 или F 1. Физиологическая роль этого компонента состоит в том, чтобы катализировать синтез АТФ. • F 1 - это белок с массой в 360 к. Да, он содержит 5 видов полипептидных цепей. Но это только часть АТФ-синтезирующего механизма
• Синтез АТФ осуществляется с помощью митохондриальной АТФ-азы (АТФ- синтетаза). Митохондриальная АТФ-аза состоит из нескольких частей: 1 -я часть называется сопрягающий фактор 1 или F 1. Физиологическая роль этого компонента состоит в том, чтобы катализировать синтез АТФ. • F 1 - это белок с массой в 360 к. Да, он содержит 5 видов полипептидных цепей. Но это только часть АТФ-синтезирующего механизма
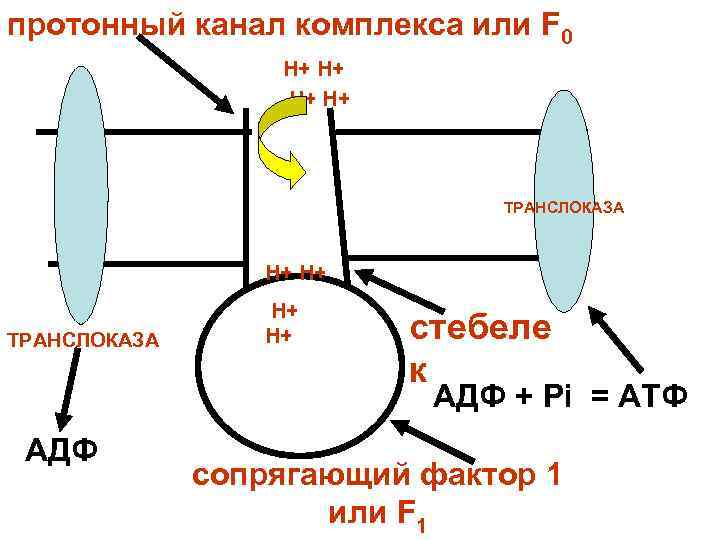 протонный канал комплекса или F 0 Н+ Н+ ТРАНСЛОКАЗА Н+ Н+ ТРАНСЛОКАЗА Н+ стебеле к АДФ + Рi = АТФ АДФ сопрягающий фактор 1 или F 1
протонный канал комплекса или F 0 Н+ Н+ ТРАНСЛОКАЗА Н+ Н+ ТРАНСЛОКАЗА Н+ стебеле к АДФ + Рi = АТФ АДФ сопрягающий фактор 1 или F 1
 Согласно гипотезе П. Митчелла ток протонов непосредственно действует на реакцию синтеза АТФ. При этом фосфатная группа связывается с ферментом в активном участке F 1 - компонента комплекса, но ближе к концу протонного канала через Fо. По этому каналу под действием мембранного потенциала и градиента р. Н переходят два протона.
Согласно гипотезе П. Митчелла ток протонов непосредственно действует на реакцию синтеза АТФ. При этом фосфатная группа связывается с ферментом в активном участке F 1 - компонента комплекса, но ближе к концу протонного канала через Fо. По этому каналу под действием мембранного потенциала и градиента р. Н переходят два протона.
 Эти два протона воздействуют на один из кислородов фосфата и соединяются с ним, образуя молекулу воды. Фосфатная группа при этом становится реактивной. В этом состоянии она легко связывается непосредственно с АДФ, образуя АТФ.
Эти два протона воздействуют на один из кислородов фосфата и соединяются с ним, образуя молекулу воды. Фосфатная группа при этом становится реактивной. В этом состоянии она легко связывается непосредственно с АДФ, образуя АТФ.
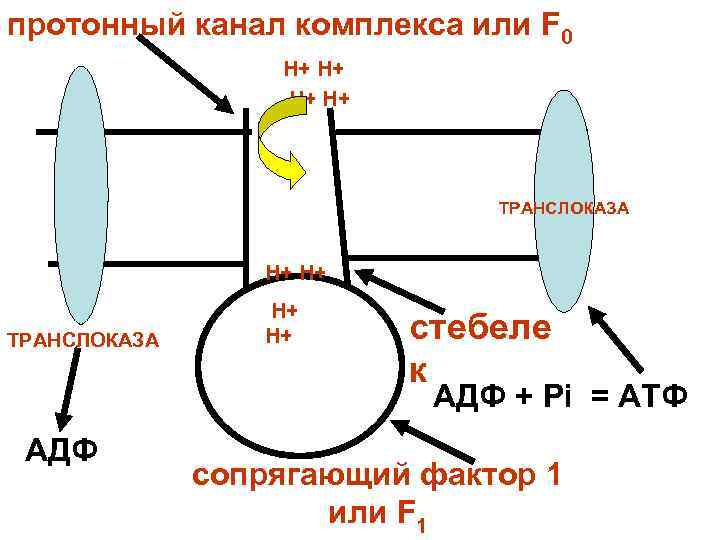 протонный канал комплекса или F 0 Н+ Н+ ТРАНСЛОКАЗА Н+ Н+ ТРАНСЛОКАЗА Н+ стебеле к АДФ + Рi = АТФ АДФ сопрягающий фактор 1 или F 1
протонный канал комплекса или F 0 Н+ Н+ ТРАНСЛОКАЗА Н+ Н+ ТРАНСЛОКАЗА Н+ стебеле к АДФ + Рi = АТФ АДФ сопрягающий фактор 1 или F 1
 • Как расходуется АТФ? • 1) на осмотическую работу; • 2) на механическую работу; • 2) на химическую работу: • а)АТФ - аллостерический регулятор; • б)пластический материал для синтеза нуклеиновых кислот, коферментов; • в)из АТФ образуется ц. АМФ; • г)Это источник фосфатных групп для образования фосфорных эфиров. • д)Источник энергии для процессов синтеза
• Как расходуется АТФ? • 1) на осмотическую работу; • 2) на механическую работу; • 2) на химическую работу: • а)АТФ - аллостерический регулятор; • б)пластический материал для синтеза нуклеиновых кислот, коферментов; • в)из АТФ образуется ц. АМФ; • г)Это источник фосфатных групп для образования фосфорных эфиров. • д)Источник энергии для процессов синтеза
 ДЫХАТЕЛЬНЫЙ КОНТРОЛЬ. • Скорость дыхания Мх, а следовательно, скорость образования энергии - регулируемый процесс. Она может контролироваться концентрацией АДФ. • Это обусловлено тем, что окисление и фосфорилирование жестко сопряжены, т. е. функционирование дыхательной цепи не может осуществляться, если оно не сопровождается фосфорилированием АДФ.
ДЫХАТЕЛЬНЫЙ КОНТРОЛЬ. • Скорость дыхания Мх, а следовательно, скорость образования энергии - регулируемый процесс. Она может контролироваться концентрацией АДФ. • Это обусловлено тем, что окисление и фосфорилирование жестко сопряжены, т. е. функционирование дыхательной цепи не может осуществляться, если оно не сопровождается фосфорилированием АДФ.
 • ИНГИБИТОРЫ ДЫХАТЕЛЬНОЙ ЦЕПИ И ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ • Ингибиторы можно разделить на 3 группы: 1) Ингибиторы собственно дыхательной цепи; 2)Ингибиторы окислительного фосфорилирования; 3)Разобщители окислительного фосфорилирования.
• ИНГИБИТОРЫ ДЫХАТЕЛЬНОЙ ЦЕПИ И ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ • Ингибиторы можно разделить на 3 группы: 1) Ингибиторы собственно дыхательной цепи; 2)Ингибиторы окислительного фосфорилирования; 3)Разобщители окислительного фосфорилирования.
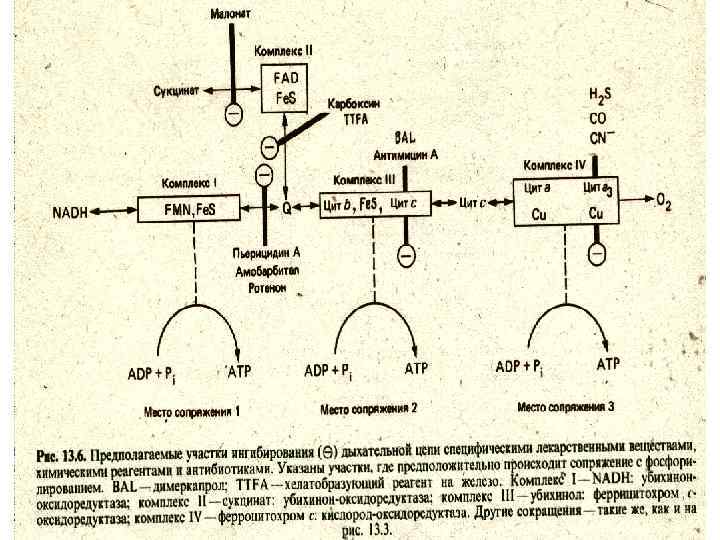
 • 1) Ингибиторы, блокирующие дыхательную цепь, могут действовать в 3 местах, соответствующих трем комплексам дыхательной цепи: • В первом комплексе дыхательная цепь ингибируется барбитуратами (например, амобарбиталом), а также ротеноном (высокотоксичное в-во, добываемое из растений, которое использовалось американскими индейцами в качестве яда при ловле рыб). Эти ингибиторы препятствуют НАД-зависимому окислению субстратов.
• 1) Ингибиторы, блокирующие дыхательную цепь, могут действовать в 3 местах, соответствующих трем комплексам дыхательной цепи: • В первом комплексе дыхательная цепь ингибируется барбитуратами (например, амобарбиталом), а также ротеноном (высокотоксичное в-во, добываемое из растений, которое использовалось американскими индейцами в качестве яда при ловле рыб). Эти ингибиторы препятствуют НАД-зависимому окислению субстратов.
 • Второй участок, где может блокироваться дыхательная цепь - это участок между цитохромом b и цитохромом с, т. е. во втором комплексе. Таким ингибитором является антибиотик антимицин А. • Третий участок - это цитохромоксидаза. Он ингибируется классическими ядами - сернистым водородом, окисью углерода и цианидом.
• Второй участок, где может блокироваться дыхательная цепь - это участок между цитохромом b и цитохромом с, т. е. во втором комплексе. Таким ингибитором является антибиотик антимицин А. • Третий участок - это цитохромоксидаза. Он ингибируется классическими ядами - сернистым водородом, окисью углерода и цианидом.
 • 2) К ингибиторам, подавляющим стадию фосфорилирования относится антибиотик олигомицин. Он полностью блокирует окисление и фосфорилирование в интактных митохондриях за счет того, что не пропускает протоны через канал F 0. • Атрактилозид также ингибирует окислительное фосфорилирование. Он ингибирует фермент - транслоказу, который производит поступление АДФ в митохондрию и выход АТФ из митохондрий.
• 2) К ингибиторам, подавляющим стадию фосфорилирования относится антибиотик олигомицин. Он полностью блокирует окисление и фосфорилирование в интактных митохондриях за счет того, что не пропускает протоны через канал F 0. • Атрактилозид также ингибирует окислительное фосфорилирование. Он ингибирует фермент - транслоказу, который производит поступление АДФ в митохондрию и выход АТФ из митохондрий.
 Разобщители отличаются тем, что они нарушают систему сопряжения процессов окисления в дыхательной цепи и фосфорилирования. • В этих условиях процесс дыхания происходит неконтролируемым образом. • Т. е. концентрации АДФ и Рi в этом случае не являются лимитирующими. • Различают разные типы разобщения
Разобщители отличаются тем, что они нарушают систему сопряжения процессов окисления в дыхательной цепи и фосфорилирования. • В этих условиях процесс дыхания происходит неконтролируемым образом. • Т. е. концентрации АДФ и Рi в этом случае не являются лимитирующими. • Различают разные типы разобщения
 1) Либо разобщители увеличивают проницаемость митохондриальной мембраны, и тогда не может набраться достаточно водородных ионов для создания достаточной дельта-мю. Н+. К этому типу разобщителей относятся некоторые кислые продукты метаболизма или продукты ПОЛ. 2) Либо разобщители сами проникают через митохондриальную мембрану и нейтрализуют заряд протонов, тем самым опять-таки снижая дельта-мю. Н+. К ним относятся многие антибиотики.
1) Либо разобщители увеличивают проницаемость митохондриальной мембраны, и тогда не может набраться достаточно водородных ионов для создания достаточной дельта-мю. Н+. К этому типу разобщителей относятся некоторые кислые продукты метаболизма или продукты ПОЛ. 2) Либо разобщители сами проникают через митохондриальную мембрану и нейтрализуют заряд протонов, тем самым опять-таки снижая дельта-мю. Н+. К ним относятся многие антибиотики.
 Разобщители, как правило легко растворимы в липидном слое мембран, этим и объясняется их действие как разобщителей. • Среди разобщителей надо назвать некоторые лекарственные вещества: строфантин, папаверин, салицилаты. • Разобщителями могут быть и собственные соединения организма, его естественные метаболиты, например, жирные кислоты. Это имеет большое значение для организма на
Разобщители, как правило легко растворимы в липидном слое мембран, этим и объясняется их действие как разобщителей. • Среди разобщителей надо назвать некоторые лекарственные вещества: строфантин, папаверин, салицилаты. • Разобщителями могут быть и собственные соединения организма, его естественные метаболиты, например, жирные кислоты. Это имеет большое значение для организма на
 • Снижение температуры возбуждает терморецепторы, это ведет к повышению выделения норадреналина. Затем увеличивается липолиз, повышается содержание ВЖК, увеличивается концентрация ацетил-Ко. А. Это ведет к повышению активности цикла Кребса, повышению содержания НАДН и ФАДН 2. Увеличивается активность тканевого дыхания, возрастает электрохимический
• Снижение температуры возбуждает терморецепторы, это ведет к повышению выделения норадреналина. Затем увеличивается липолиз, повышается содержание ВЖК, увеличивается концентрация ацетил-Ко. А. Это ведет к повышению активности цикла Кребса, повышению содержания НАДН и ФАДН 2. Увеличивается активность тканевого дыхания, возрастает электрохимический
 • Т. к. ВЖК снижают дельта-мю. Н+, ее становится недостаточно для создания АТФ, но эта дельта-мю. Н+ будет расходоваться на согревание. При этом на холоде человек дрожит. Рефлекторно возникает возбуждение терморецепторов, снижается содержание АТФ, увеличивается - АДФ. Они регулируют активность ферментов ЦТК. Увеличивается концентрация НАДН, повышается разность электрохимического потенциала - человек согревается.
• Т. к. ВЖК снижают дельта-мю. Н+, ее становится недостаточно для создания АТФ, но эта дельта-мю. Н+ будет расходоваться на согревание. При этом на холоде человек дрожит. Рефлекторно возникает возбуждение терморецепторов, снижается содержание АТФ, увеличивается - АДФ. Они регулируют активность ферментов ЦТК. Увеличивается концентрация НАДН, повышается разность электрохимического потенциала - человек согревается.


