Окислительно-восстановительные реакции Реакции, в







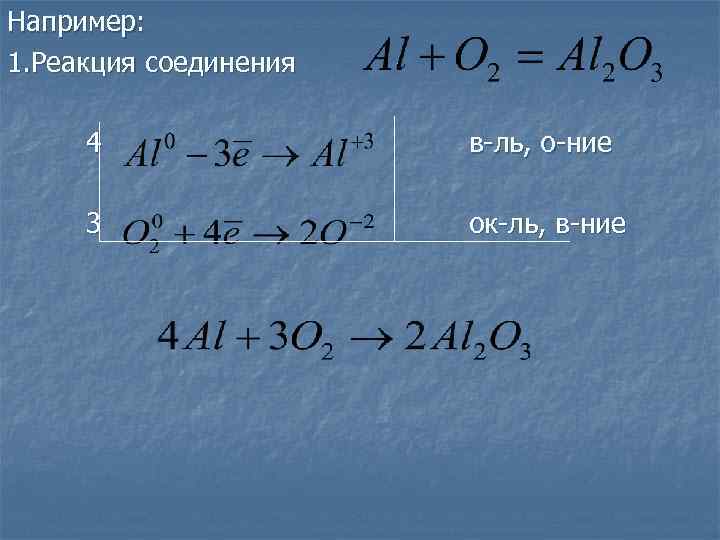





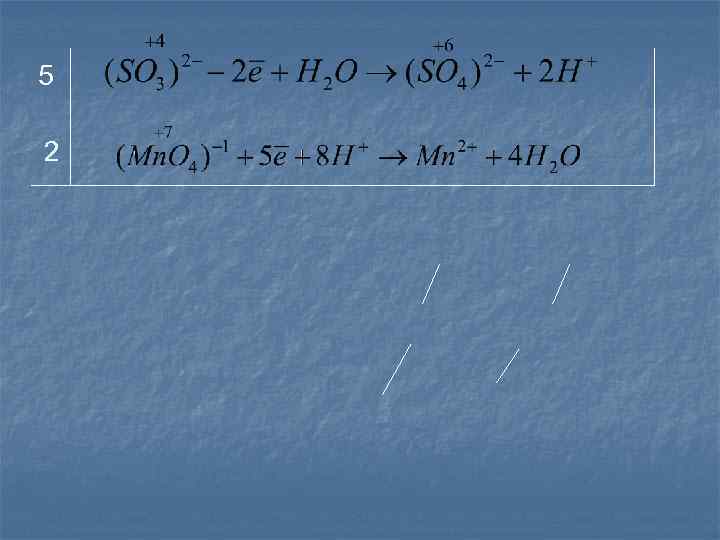


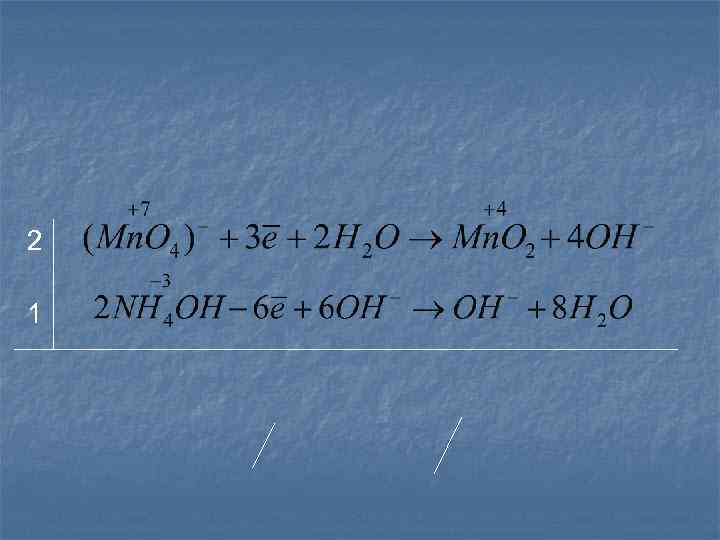
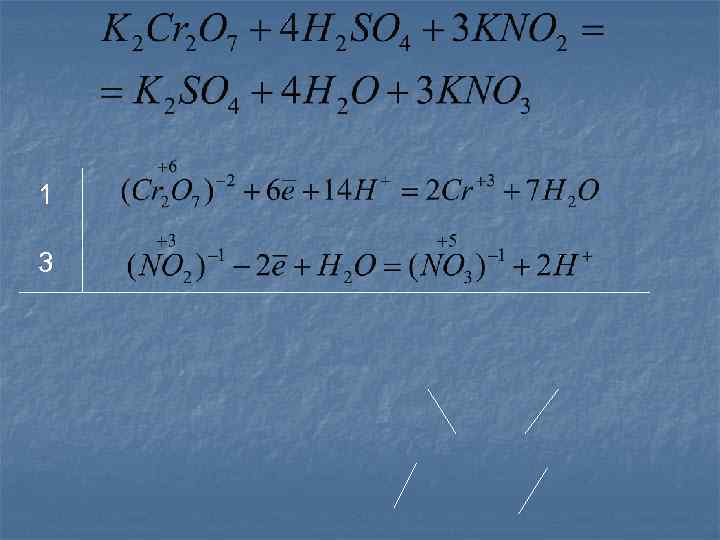









Окислительно-восстановительные реакции.ppt
- Количество слайдов: 26
 Окислительно-восстановительные реакции Реакции, в которых происходит изменение степени окисления веществ, относятся к ОВР. Валентность не учитывает электроотрицательность и не имеет знака (+или-), она характеризует лишь число связей.
Окислительно-восстановительные реакции Реакции, в которых происходит изменение степени окисления веществ, относятся к ОВР. Валентность не учитывает электроотрицательность и не имеет знака (+или-), она характеризует лишь число связей.
 Степень окисления атома в молекуле – это электрический заряд данного атома, вызванный смещением валентных электронов к более электроотрицательному атому. Степень окисления атома обозначается числом со знаком + или -. Минимальная степень окисления определяется числом электронов, которые принимаются элементом до полного заполнения подуровня электронами. n=2
Степень окисления атома в молекуле – это электрический заряд данного атома, вызванный смещением валентных электронов к более электроотрицательному атому. Степень окисления атома обозначается числом со знаком + или -. Минимальная степень окисления определяется числом электронов, которые принимаются элементом до полного заполнения подуровня электронами. n=2
 Максимальная степень окисления – это количество электронов, которое может отдать элемент с последнего уровня. Правила определения степени окисления: 1. Степень окисления молекул простых веществ всегда равна нулю. 2. Степень окисления щелочных металлов равна +1. 3. Степень окисления водорода в соединениях равна +1, за исключением гидридов металлов(Na. H, Ca. H 2 и т. д. ), в которых степень окисления водорода равна -1.
Максимальная степень окисления – это количество электронов, которое может отдать элемент с последнего уровня. Правила определения степени окисления: 1. Степень окисления молекул простых веществ всегда равна нулю. 2. Степень окисления щелочных металлов равна +1. 3. Степень окисления водорода в соединениях равна +1, за исключением гидридов металлов(Na. H, Ca. H 2 и т. д. ), в которых степень окисления водорода равна -1.
 4. Степень окисления кислорода в соединениях -2, за исключением соединений(H 2 O 2, Na 2 O 2), где степень окисления водорода равна -1. 5. Молекула нейтральна, поэтому сумма степеней окисления элементов, входящих в молекулу, равна нулю. Например: ст. окисления хрома в соединении бихромат калия равна +6. калий +1 Кислород -2 (+1*2)+(2 х)+(-2*7)=0 2 х=+12; х=+6
4. Степень окисления кислорода в соединениях -2, за исключением соединений(H 2 O 2, Na 2 O 2), где степень окисления водорода равна -1. 5. Молекула нейтральна, поэтому сумма степеней окисления элементов, входящих в молекулу, равна нулю. Например: ст. окисления хрома в соединении бихромат калия равна +6. калий +1 Кислород -2 (+1*2)+(2 х)+(-2*7)=0 2 х=+12; х=+6
 В окислительно-восстановительных реакциях протекают два процесса: 1. Окисление 2. Восстановление 3. Сущность окисления состоит в отдаче окисляющихся веществом валентных электронов окислителю, который принимая электроны восстанавливается. 4. Сущность восстановления состоит в присоединении восстановляющимся веществом восстановителя. 5. Процесс отдачи веществом электронов – окисление. 6. Процесс присоединения веществом электронов – восстановление. 7. Вещества отдающие электроны –
В окислительно-восстановительных реакциях протекают два процесса: 1. Окисление 2. Восстановление 3. Сущность окисления состоит в отдаче окисляющихся веществом валентных электронов окислителю, который принимая электроны восстанавливается. 4. Сущность восстановления состоит в присоединении восстановляющимся веществом восстановителя. 5. Процесс отдачи веществом электронов – окисление. 6. Процесс присоединения веществом электронов – восстановление. 7. Вещества отдающие электроны –
 Составление уравнений ОВР 1. Метод электронного баланса. n При составлении уравнений ОВР необходимо определить окислитель и восстановитель. n Определить число электронов отдаваемых восстановителем и принимаемых окислителем. n Коэффициенты в уравнениях подбираются с таким расчетом, чтобы число электронов отданных восстановителем равнялось числу принятых окислителем.
Составление уравнений ОВР 1. Метод электронного баланса. n При составлении уравнений ОВР необходимо определить окислитель и восстановитель. n Определить число электронов отдаваемых восстановителем и принимаемых окислителем. n Коэффициенты в уравнениях подбираются с таким расчетом, чтобы число электронов отданных восстановителем равнялось числу принятых окислителем.
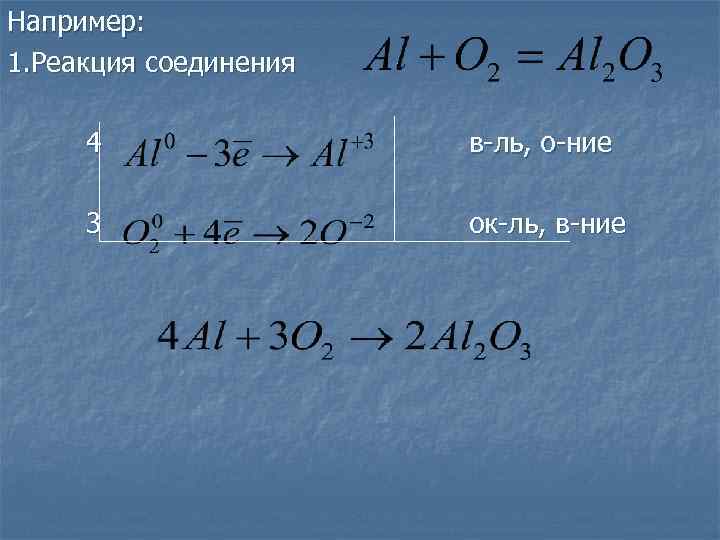 Например: 1. Реакция соединения 4 в-ль, о-ние 3 ок-ль, в-ние
Например: 1. Реакция соединения 4 в-ль, о-ние 3 ок-ль, в-ние
 2. Реакция замещения. 12 вос-ль, ок-ние 12 ок-ль, вост-ние
2. Реакция замещения. 12 вос-ль, ок-ние 12 ок-ль, вост-ние
 2. Метод электронно-ионного баланса На скорость и направление ОВР влияют: 1. природа реагирующих веществ 2. характер среды 3. концентрации реагентов 4. температура 5. катализатор Влияние среды на ОВ процессы настолько велико, что в некоторых случаях оно изменяет и направление процесса.
2. Метод электронно-ионного баланса На скорость и направление ОВР влияют: 1. природа реагирующих веществ 2. характер среды 3. концентрации реагентов 4. температура 5. катализатор Влияние среды на ОВ процессы настолько велико, что в некоторых случаях оно изменяет и направление процесса.
 При составлении уравнений ОВР, протекающих в различных средах, необходимо учитывать: 1. Если образующиеся вещества содержат больше кислорода, чем исходные соединения, то недостающее количество кислорода пополняется в кислых и нейтральных средах за счет молекул воды, а в щелочных средах за счет ионов 2. Если образующиеся соединения содержат меньше кислорода, чем исходные соединения, то освобождающийся кислород в кислой среде связывается ионами водорода с образованием молекул воды, а в нейтральной и щелочной средах – с образованием гидроксид ионов.
При составлении уравнений ОВР, протекающих в различных средах, необходимо учитывать: 1. Если образующиеся вещества содержат больше кислорода, чем исходные соединения, то недостающее количество кислорода пополняется в кислых и нейтральных средах за счет молекул воды, а в щелочных средах за счет ионов 2. Если образующиеся соединения содержат меньше кислорода, чем исходные соединения, то освобождающийся кислород в кислой среде связывается ионами водорода с образованием молекул воды, а в нейтральной и щелочной средах – с образованием гидроксид ионов.
 Например: Марганец в ионе
Например: Марганец в ионе
 Пример: В кислой среде.
Пример: В кислой среде.
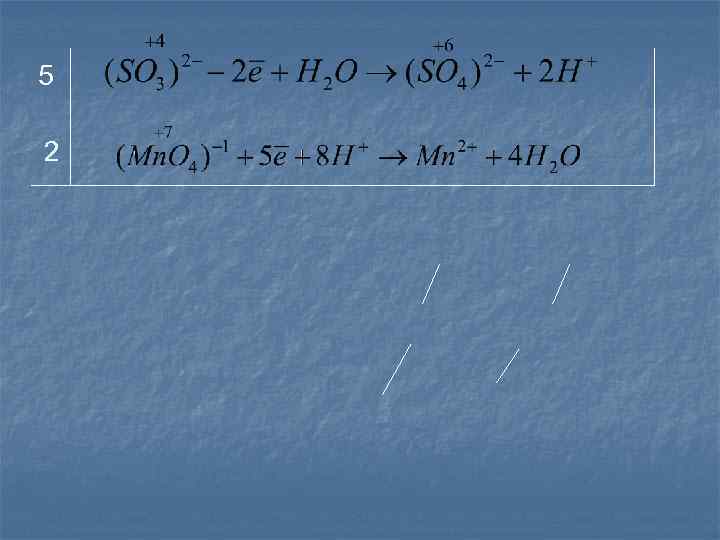 5 2
5 2
 В нейтральной среде 3 2
В нейтральной среде 3 2
 В щелочной среде 2 ок-ль, вост-ние 1 в-ль, о-ние
В щелочной среде 2 ок-ль, вост-ние 1 в-ль, о-ние
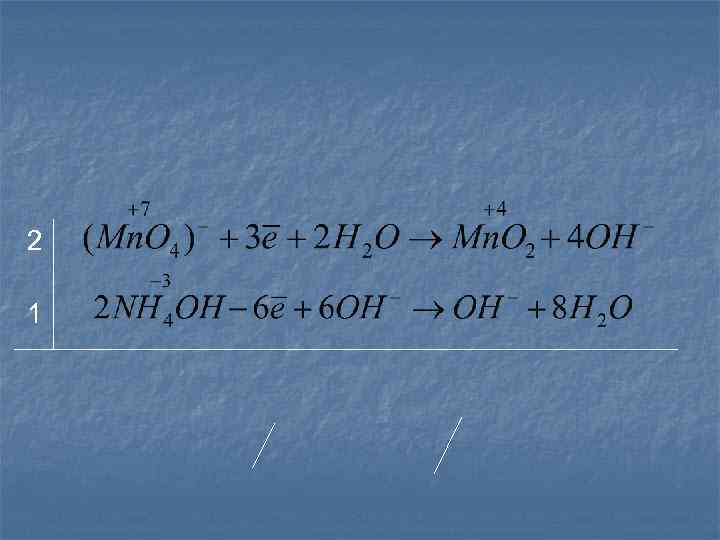 2 1
2 1
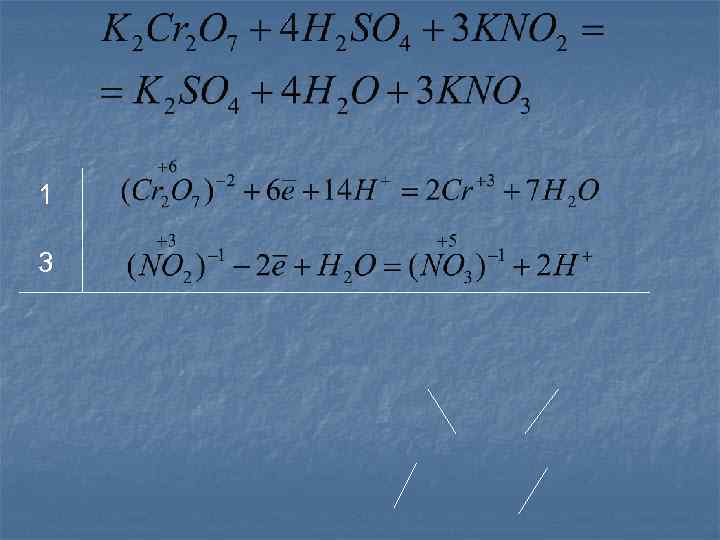 1 3
1 3
 Направление ОВР Мерой окислительно-восстановительной стойкости веществ служат их электродные или окислительно- восстановительные потенциалы. Чем больше алгебраическая величина стандартного электродного потенциала атома или иона, тем больше его окислительные свойства. Чем меньше, тем больше его восстановительные свойства. Например: -сильный окислитель -сильный восстановитель
Направление ОВР Мерой окислительно-восстановительной стойкости веществ служат их электродные или окислительно- восстановительные потенциалы. Чем больше алгебраическая величина стандартного электродного потенциала атома или иона, тем больше его окислительные свойства. Чем меньше, тем больше его восстановительные свойства. Например: -сильный окислитель -сильный восстановитель
 Если активность окисленной и восстановленной формы данного вещества не равны единице, тогда их потенциалы рассчитываются по уравнению Нернста. Х и Y – коэффициенты при окислителе и восстановителе.
Если активность окисленной и восстановленной формы данного вещества не равны единице, тогда их потенциалы рассчитываются по уравнению Нернста. Х и Y – коэффициенты при окислителе и восстановителе.
 Будет ли протекать реакция? Если конц. в. в 1 моль/л находим в таблице
Будет ли протекать реакция? Если конц. в. в 1 моль/л находим в таблице
 1 1 Pb. O 2 – окислитель KI – восстановитель Реакция возможна, т. к. E` значительно > 0
1 1 Pb. O 2 – окислитель KI – восстановитель Реакция возможна, т. к. E` значительно > 0
 Классификация ОВР 1. Реакции межатомного или межмолекулярного окисления-восстановления. 2 4 1 2 В таких реакциях обмен электронами происходит между различными атомами, молекулами или ионами
Классификация ОВР 1. Реакции межатомного или межмолекулярного окисления-восстановления. 2 4 1 2 В таких реакциях обмен электронами происходит между различными атомами, молекулами или ионами
 2. Реакция диспропорционирования (самоокисления и самовосстановления) 1 в-ль 2 ок-ль В этом случае ионы одного и того же вещества реагируют друг с другом как восстановитель и окислитель, т. к. содержащиеся в них элементы находятся в промежуточной степени окисления.
2. Реакция диспропорционирования (самоокисления и самовосстановления) 1 в-ль 2 ок-ль В этом случае ионы одного и того же вещества реагируют друг с другом как восстановитель и окислитель, т. к. содержащиеся в них элементы находятся в промежуточной степени окисления.
 3. Реакции внутримолекулярного окисления- восстановления. В этих реакциях окислитель и восстановитель находятся в одной и той же молекуле. Хлор является окислителем, а кислород восстановителем.
3. Реакции внутримолекулярного окисления- восстановления. В этих реакциях окислитель и восстановитель находятся в одной и той же молекуле. Хлор является окислителем, а кислород восстановителем.
 Важнейшие окислители 1. Нейтральные атомы неметаллов. 2. Положительно заряженные ионы металлов находятся в высшей степени окисления. 3. Сложные ионы и молекулы, содержащие атомы в высшей степени окисления. 4. Сложные ионы и молекулы, содержащие атомы в высшей степени окисления. 5. Сложные ионы и молекулы, содержащие атомы неметаллов в промежуточной степени окисления.
Важнейшие окислители 1. Нейтральные атомы неметаллов. 2. Положительно заряженные ионы металлов находятся в высшей степени окисления. 3. Сложные ионы и молекулы, содержащие атомы в высшей степени окисления. 4. Сложные ионы и молекулы, содержащие атомы в высшей степени окисления. 5. Сложные ионы и молекулы, содержащие атомы неметаллов в промежуточной степени окисления.
 Важнейшие восстановители 1. Нейтральные атомы металлов. 2. отрицательно заряженные ионы неметаллов. 3. Положительно заряженные металлов в низшей степени окисления. 4. Сложные ионы и молекулы, содержащие атомы неметаллов в промежуточной степени окисления.
Важнейшие восстановители 1. Нейтральные атомы металлов. 2. отрицательно заряженные ионы неметаллов. 3. Положительно заряженные металлов в низшей степени окисления. 4. Сложные ионы и молекулы, содержащие атомы неметаллов в промежуточной степени окисления.

