ОВР в гидросфере.ppt
- Количество слайдов: 32
 Окислительно-восстановительные процессы в гидросфере • Окислительно-восстановительные процессы играют исключительно важную роль в описани процессов, протекающих в природных водоёмах • Предистория и качество природных вод в значительной степени зависят от: от • вида окислительно-восстановительных реакций • их кинетических характеристик • величины окислительно-восстановительного потенциала • 2 основные особенности ОВР в природных водоёмах: 1) Большинство наиболее важных ОВР катализируются микроорганизмами - окисление органического вещества молекулярным кислородом - восстановление Fe(III) Fe(II) 2) Присутствие в водных водоёмах таких сильных окислителей как - свободные радикалы - озон - пероксид водорода
Окислительно-восстановительные процессы в гидросфере • Окислительно-восстановительные процессы играют исключительно важную роль в описани процессов, протекающих в природных водоёмах • Предистория и качество природных вод в значительной степени зависят от: от • вида окислительно-восстановительных реакций • их кинетических характеристик • величины окислительно-восстановительного потенциала • 2 основные особенности ОВР в природных водоёмах: 1) Большинство наиболее важных ОВР катализируются микроорганизмами - окисление органического вещества молекулярным кислородом - восстановление Fe(III) Fe(II) 2) Присутствие в водных водоёмах таких сильных окислителей как - свободные радикалы - озон - пероксид водорода
 Окислительно-восстановительные процессы в гидросфере к Окисленные формы + nē восстановленные формы (ок. ф. ) (восст. ф. ) К = аi(восст. ф. ) / аi(ок. ф. ) * (аē)n ci(восст. ф. ) / сi(ок. ф. ) * (аē)n aē - активность ē - способноть системы поставлять ē для ОВР ē H+ растворы этих веществ в воде лишь удобная абстракция a. H+ [ H+ ] ~> шахтные воды – кислые ж. к. [ H+ ] велико высокое значение aē - восстановительная вода : сероводородные воды; «мёртвая» вода из народных сказок : хлорированная окислительная вода или озонированная вода ; «живая» вода низкое значение aē p. H = - lg [ H+ ] = - lg a. H+ ↓ по аналогии ↓ pē = - lg aē
Окислительно-восстановительные процессы в гидросфере к Окисленные формы + nē восстановленные формы (ок. ф. ) (восст. ф. ) К = аi(восст. ф. ) / аi(ок. ф. ) * (аē)n ci(восст. ф. ) / сi(ок. ф. ) * (аē)n aē - активность ē - способноть системы поставлять ē для ОВР ē H+ растворы этих веществ в воде лишь удобная абстракция a. H+ [ H+ ] ~> шахтные воды – кислые ж. к. [ H+ ] велико высокое значение aē - восстановительная вода : сероводородные воды; «мёртвая» вода из народных сказок : хлорированная окислительная вода или озонированная вода ; «живая» вода низкое значение aē p. H = - lg [ H+ ] = - lg a. H+ ↓ по аналогии ↓ pē = - lg aē
 Окислительно-восстановительные процессы в гидросфере K = аi(восст. ф. ) / аi(ок. ф. ) * (аē)n = аi(восст. ф. ) / K * аi(ок. ф. ) n lg aē = lg аi(восст. ф) – lg K – lg аi(ок. ф. ) - lg aē = 1/n (- аi(восст. ф) ) + lg K + lg аi(ок. ф. ) pē=1/n (lg K +lg аi(восст. ф) / lg аi(восст. ф) )
Окислительно-восстановительные процессы в гидросфере K = аi(восст. ф. ) / аi(ок. ф. ) * (аē)n = аi(восст. ф. ) / K * аi(ок. ф. ) n lg aē = lg аi(восст. ф) – lg K – lg аi(ок. ф. ) - lg aē = 1/n (- аi(восст. ф) ) + lg K + lg аi(ок. ф. ) pē=1/n (lg K +lg аi(восст. ф) / lg аi(восст. ф) )
 Окислительно-восстановительные процессы в гидросфере Для реакции 2 H+(вода) + 2ē↔ Н 2 (газ) ∆G° = 0 • Эта реакция характеризует стандартный водородный электрод (h) • Потенциалы других рекций измеряються по отношению к водородному элекроду (Eh) • В стандартных условиях для ОВР ΔGºреакции = - n. FEhº ΔGº - значение энергии Гиббса в стандартных условиях n – число ē, участвующих в процессе F – число Фарадея (!) Ehº - относительно-восстановительный потенциал , измеренный в стационарных условиях относительно стандартного водородного елекрода Уравнение Вант-Гоффа или = -RT ln Kº ΔGº = -2, 3 RT lg Kº= n. FEºh / 2, 3 RT Pē = 1/n (n F Ehº/ 2, 3 RT + lg аi (окис. ф) / ai(воcст. ф)
Окислительно-восстановительные процессы в гидросфере Для реакции 2 H+(вода) + 2ē↔ Н 2 (газ) ∆G° = 0 • Эта реакция характеризует стандартный водородный электрод (h) • Потенциалы других рекций измеряються по отношению к водородному элекроду (Eh) • В стандартных условиях для ОВР ΔGºреакции = - n. FEhº ΔGº - значение энергии Гиббса в стандартных условиях n – число ē, участвующих в процессе F – число Фарадея (!) Ehº - относительно-восстановительный потенциал , измеренный в стационарных условиях относительно стандартного водородного елекрода Уравнение Вант-Гоффа или = -RT ln Kº ΔGº = -2, 3 RT lg Kº= n. FEºh / 2, 3 RT Pē = 1/n (n F Ehº/ 2, 3 RT + lg аi (окис. ф) / ai(воcст. ф)
 Окислительно-восстановительные процессы в гидросфере После преобразований с учётом известного уравнения Нернста Eh = Eh° + (2, 3/F)lg [ ai(окисл. ф. ) / аi(восст. ф. ) ] получим: pē = FEh/(2, 3 RT) pē = 104*Eh/1, 98 T (pē)° = 16, 9 Eh° • В реальных условиях в природной воде условия далеки от равновесия • Можно говорить о (pē)° или Eh° для отдельной ред-окс пары • Стандартные значения (pē)° и Eh° табулированны
Окислительно-восстановительные процессы в гидросфере После преобразований с учётом известного уравнения Нернста Eh = Eh° + (2, 3/F)lg [ ai(окисл. ф. ) / аi(восст. ф. ) ] получим: pē = FEh/(2, 3 RT) pē = 104*Eh/1, 98 T (pē)° = 16, 9 Eh° • В реальных условиях в природной воде условия далеки от равновесия • Можно говорить о (pē)° или Eh° для отдельной ред-окс пары • Стандартные значения (pē)° и Eh° табулированны
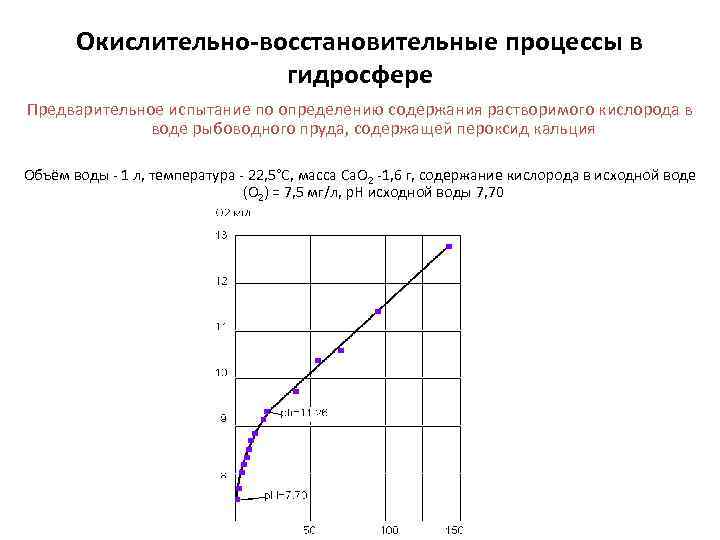 Окислительно-восстановительные процессы в гидросфере Предварительное испытание по определению содержания растворимого кислорода в воде рыбоводного пруда, содержащей пероксид кальция Объём воды - 1 л, температура - 22, 5°С, масса Са. О 2 -1, 6 г, содержание кислорода в исходной воде (О 2) = 7, 5 мг/л, р. Н исходной воды 7, 70
Окислительно-восстановительные процессы в гидросфере Предварительное испытание по определению содержания растворимого кислорода в воде рыбоводного пруда, содержащей пероксид кальция Объём воды - 1 л, температура - 22, 5°С, масса Са. О 2 -1, 6 г, содержание кислорода в исходной воде (О 2) = 7, 5 мг/л, р. Н исходной воды 7, 70
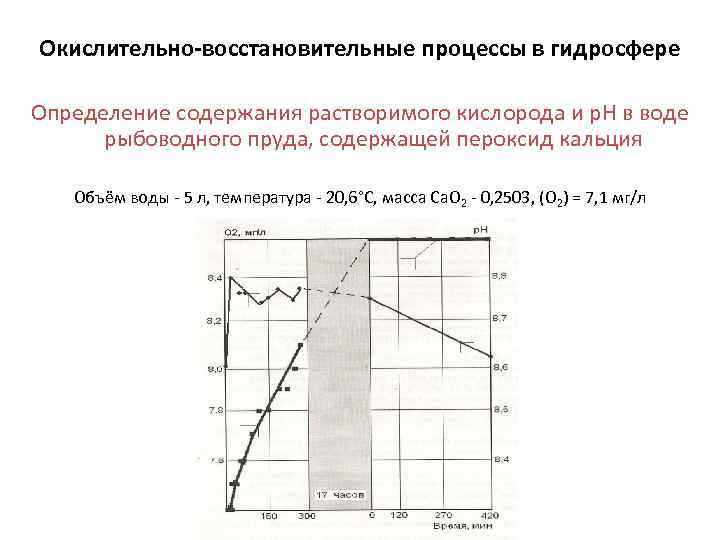 Окислительно-восстановительные процессы в гидросфере Определение содержания растворимого кислорода и р. Н в воде рыбоводного пруда, содержащей пероксид кальция Объём воды - 5 л, температура - 20, 6°С, масса Са. О 2 - 0, 2503, (О 2) = 7, 1 мг/л
Окислительно-восстановительные процессы в гидросфере Определение содержания растворимого кислорода и р. Н в воде рыбоводного пруда, содержащей пероксид кальция Объём воды - 5 л, температура - 20, 6°С, масса Са. О 2 - 0, 2503, (О 2) = 7, 1 мг/л
 Окислительно-восстановительные процессы в гидросфере Величины р. Н, О 2 и Еh связаны между собой соотношением: 20, 8 + 1/4 lg(PO 2) - p. H = Eh • 104/(1, 98 T) Eh является одним из основных параметров контроля качества воды
Окислительно-восстановительные процессы в гидросфере Величины р. Н, О 2 и Еh связаны между собой соотношением: 20, 8 + 1/4 lg(PO 2) - p. H = Eh • 104/(1, 98 T) Eh является одним из основных параметров контроля качества воды
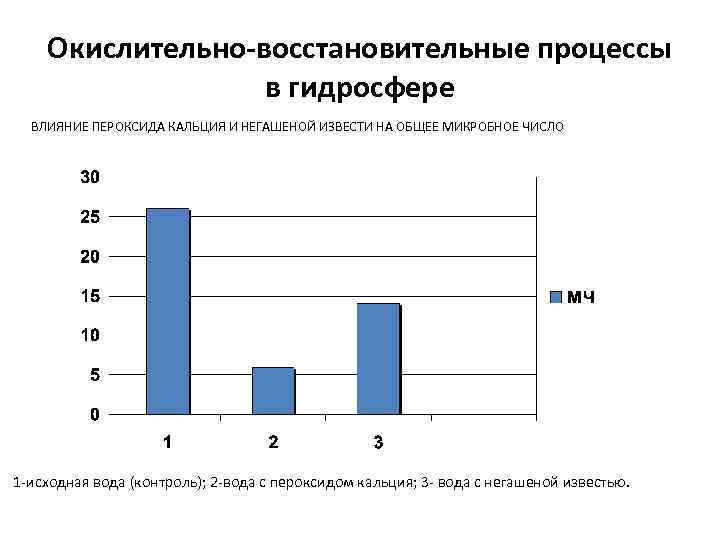 Окислительно-восстановительные процессы в гидросфере ВЛИЯНИЕ ПЕРОКСИДА КАЛЬЦИЯ И НЕГАШЕНОЙ ИЗВЕСТИ НА ОБЩЕЕ МИКРОБНОЕ ЧИСЛО 1 -исходная вода (контроль); 2 -вода с пероксидом кальция; 3 - вода с негашеной известью.
Окислительно-восстановительные процессы в гидросфере ВЛИЯНИЕ ПЕРОКСИДА КАЛЬЦИЯ И НЕГАШЕНОЙ ИЗВЕСТИ НА ОБЩЕЕ МИКРОБНОЕ ЧИСЛО 1 -исходная вода (контроль); 2 -вода с пероксидом кальция; 3 - вода с негашеной известью.
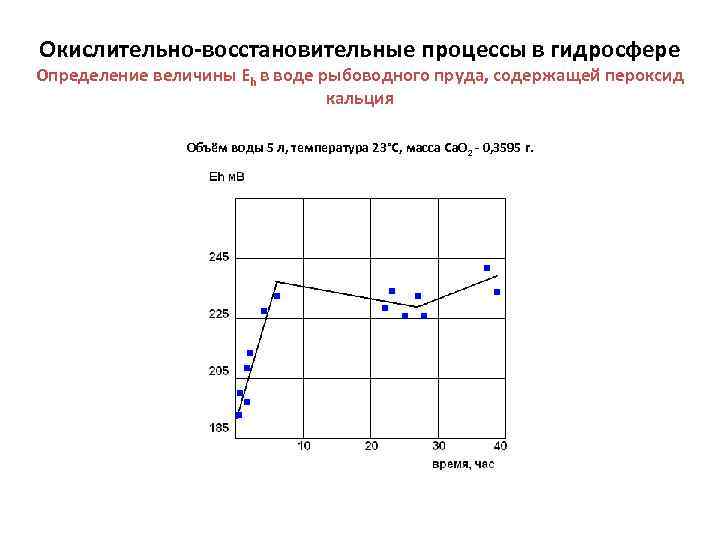 Окислительно-восстановительные процессы в гидросфере Определение величины Еh в воде рыбоводного пруда, содержащей пероксид кальция Объём воды 5 л, температура 23°С, масса Са. О 2 - 0, 3595 г.
Окислительно-восстановительные процессы в гидросфере Определение величины Еh в воде рыбоводного пруда, содержащей пероксид кальция Объём воды 5 л, температура 23°С, масса Са. О 2 - 0, 3595 г.
 Окислительно-восстановительные процессы в гидросфере Взаимосвязь между окислительно-восстановительными и кислотно-основными характеристиками природных вод Существует жёсткая взаимосвязь между окислительновосстановительными и кислотно-основным равновесием, например Fe(II) Fe(III) [Fe(H 2 O)]2+ Fe(OH)3 + 3 H 2 O + 3 H+ + ē (Пример для “шахтных” вод - эта вода - кислая) • Кислотно-основной характеристикой водоёма является p. H • Вода может окисляться 2 Н 2 O + 4 H+ + 4ē а может восстанавливаться 2 H 2 O + 2ē H 2 + 2 OH • Эти две реакции определяют изменение в воде, а р. Н оказывает влияние на характеристики обеих реакций •
Окислительно-восстановительные процессы в гидросфере Взаимосвязь между окислительно-восстановительными и кислотно-основными характеристиками природных вод Существует жёсткая взаимосвязь между окислительновосстановительными и кислотно-основным равновесием, например Fe(II) Fe(III) [Fe(H 2 O)]2+ Fe(OH)3 + 3 H 2 O + 3 H+ + ē (Пример для “шахтных” вод - эта вода - кислая) • Кислотно-основной характеристикой водоёма является p. H • Вода может окисляться 2 Н 2 O + 4 H+ + 4ē а может восстанавливаться 2 H 2 O + 2ē H 2 + 2 OH • Эти две реакции определяют изменение в воде, а р. Н оказывает влияние на характеристики обеих реакций •
 Окислительно-восстановительные процессы в гидросфере Взаимосвязь между окислительно-восстановительными и кислотно-основными характеристиками природных вод • Процесс окисления воды 2 Н 2 О О 2 + 4 Н+ + 4ē перепишем в воде к 1/4 О 2 + Н+ + ē 1/2 Н 2 О • K = a 1/2 H 2 O / ( р1/4 О 2 а. Н+аē) Определим граничные условия как: а. Н 2 О = 1 и р. О 2 = 1, тогда K = 1/a. Н+аē аē = 1/Ka. Н+ pē = lg. K - p. H • Величину lg. K легко определить из ∆GH 2 O, т. к. ∆GO 2, ∆GH+ и ∆Gē = 0 (по термодинамическим конвенциям) lg. K = - 1/2 ∆GH 2 O/(2, 3 RT) = 20, 8
Окислительно-восстановительные процессы в гидросфере Взаимосвязь между окислительно-восстановительными и кислотно-основными характеристиками природных вод • Процесс окисления воды 2 Н 2 О О 2 + 4 Н+ + 4ē перепишем в воде к 1/4 О 2 + Н+ + ē 1/2 Н 2 О • K = a 1/2 H 2 O / ( р1/4 О 2 а. Н+аē) Определим граничные условия как: а. Н 2 О = 1 и р. О 2 = 1, тогда K = 1/a. Н+аē аē = 1/Ka. Н+ pē = lg. K - p. H • Величину lg. K легко определить из ∆GH 2 O, т. к. ∆GO 2, ∆GH+ и ∆Gē = 0 (по термодинамическим конвенциям) lg. K = - 1/2 ∆GH 2 O/(2, 3 RT) = 20, 8
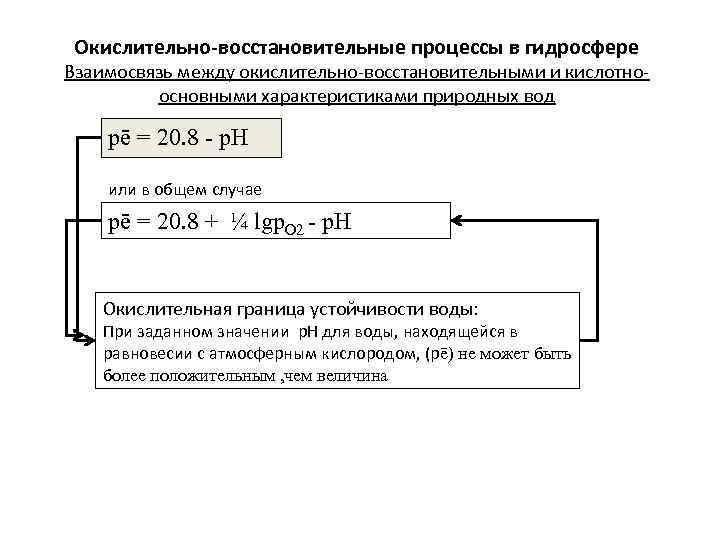 Окислительно-восстановительные процессы в гидросфере Взаимосвязь между окислительно-восстановительными и кислотноосновными характеристиками природных вод pē = 20. 8 - p. H или в общем случае pē = 20. 8 + ¼ lgp. O 2 - p. H Окислительная граница устойчивости воды: При заданном значении p. H для воды, находящейся в равновесии с атмосферным кислородом, (pē) не может быть более положительным , чем величина
Окислительно-восстановительные процессы в гидросфере Взаимосвязь между окислительно-восстановительными и кислотноосновными характеристиками природных вод pē = 20. 8 - p. H или в общем случае pē = 20. 8 + ¼ lgp. O 2 - p. H Окислительная граница устойчивости воды: При заданном значении p. H для воды, находящейся в равновесии с атмосферным кислородом, (pē) не может быть более положительным , чем величина
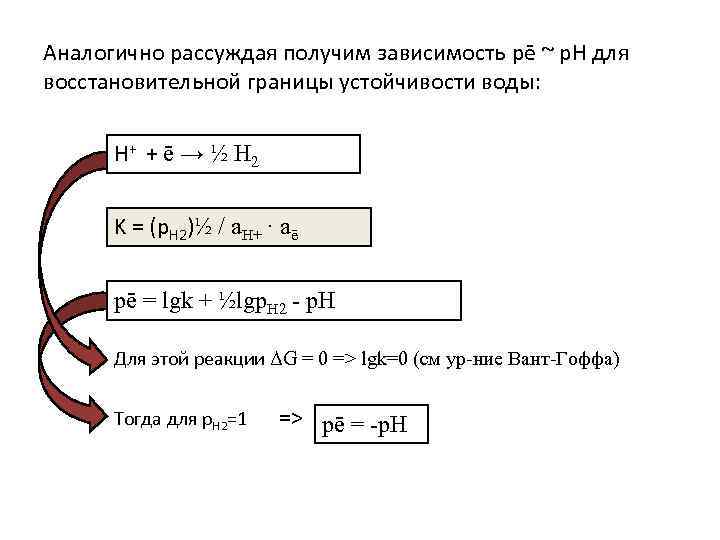 Аналогично рассуждая получим зависимость pē ~ p. H для восстановительной границы устойчивости воды: H+ + ē → ½ H 2 K = (p. H 2)½ / a. H+ · aē pē = lgk + ½lgp. H 2 - p. H Для этой реакции ΔG = 0 => lgk=0 (см ур-ние Вант-Гоффа) Тогда для p. H 2=1 => pē = -p. H
Аналогично рассуждая получим зависимость pē ~ p. H для восстановительной границы устойчивости воды: H+ + ē → ½ H 2 K = (p. H 2)½ / a. H+ · aē pē = lgk + ½lgp. H 2 - p. H Для этой реакции ΔG = 0 => lgk=0 (см ур-ние Вант-Гоффа) Тогда для p. H 2=1 => pē = -p. H
 Окислительно-восстановительные процессы в гидросфере Взаимосвязь между окислительно-восстановительными и кислотно-основными характеристиками природных вод В реальных условиях, при контакте воды с воздухом, p. H 2 и p. O 2 < 1 атм, поэтому значение pē в зависимости от p. H изменяется в некотором интервале: Диаграмма pē~p. H является удобным способом изображения областей устойчивости окисленных и восстановленных форм определенных окислительно-восстановительных систем.
Окислительно-восстановительные процессы в гидросфере Взаимосвязь между окислительно-восстановительными и кислотно-основными характеристиками природных вод В реальных условиях, при контакте воды с воздухом, p. H 2 и p. O 2 < 1 атм, поэтому значение pē в зависимости от p. H изменяется в некотором интервале: Диаграмма pē~p. H является удобным способом изображения областей устойчивости окисленных и восстановленных форм определенных окислительно-восстановительных систем.
 Окислительно-восстановительные процессы в гидросфере Редоксбуферность природных вод • Редокс-буферность (или редокс-емкость) – аналог кислотно-основной буферности. Система является «забуференной» относительно редокс-процессов, если в ней присутствуют соединения, способные окисляться или восстанавливаться, что препятствует значительным изменениям pē при добавлении небольших количеств окислителей или восстановителей Для природных вод, контактирующих с воздухом, содержащим кислород, важное значение имеет промежуточное образование пероксида водорода в процессе восстановления кислорода: O 2 + 2 H+ + 2ē ↔ H 2 O 2 + 2 H+ + 2ē ↔ 2 H 2 O часто: лимитирующая стадия Если контакт природных вод с воздухом, содержащим кислород, будет нарушен, достаточно быстро может резко измениться редокс-состояние воды. Пример: В замкнутом объеме (без контакта с воздухом) может быть окислено лишь Пример 7, 9 мг/л органических веществ. При этом весь кислород будет израсходован.
Окислительно-восстановительные процессы в гидросфере Редоксбуферность природных вод • Редокс-буферность (или редокс-емкость) – аналог кислотно-основной буферности. Система является «забуференной» относительно редокс-процессов, если в ней присутствуют соединения, способные окисляться или восстанавливаться, что препятствует значительным изменениям pē при добавлении небольших количеств окислителей или восстановителей Для природных вод, контактирующих с воздухом, содержащим кислород, важное значение имеет промежуточное образование пероксида водорода в процессе восстановления кислорода: O 2 + 2 H+ + 2ē ↔ H 2 O 2 + 2 H+ + 2ē ↔ 2 H 2 O часто: лимитирующая стадия Если контакт природных вод с воздухом, содержащим кислород, будет нарушен, достаточно быстро может резко измениться редокс-состояние воды. Пример: В замкнутом объеме (без контакта с воздухом) может быть окислено лишь Пример 7, 9 мг/л органических веществ. При этом весь кислород будет израсходован.
 Реакции, оказывающие наибольшее влияние на редокс-буферность природных вод 1. Денитрификация - превращение нитрата (компонент питания) в биологически инертный молекулярный азот. -бактерии используют для окисления органики, окислитель – NO 3 в H+ среде. pē = - 4. 5 2. 5 Cорг + 2 NO 3 + 2 H+ → N 2 + 2. 5 CO 2 + H 2 O Т. к. [NO 3 -] в природных водах низкая, эти ионы не оказывают влияния на редоксбуферность природных вод. 2. Восстановление сульфатов ( «сульфат-редукция» ) - бактерии используют для окисления органики кислород сульфат-ионе 2 Cорг + SO 42 - = 2 H 2 O→ H 2 S = 2 HCO 3 -
Реакции, оказывающие наибольшее влияние на редокс-буферность природных вод 1. Денитрификация - превращение нитрата (компонент питания) в биологически инертный молекулярный азот. -бактерии используют для окисления органики, окислитель – NO 3 в H+ среде. pē = - 4. 5 2. 5 Cорг + 2 NO 3 + 2 H+ → N 2 + 2. 5 CO 2 + H 2 O Т. к. [NO 3 -] в природных водах низкая, эти ионы не оказывают влияния на редоксбуферность природных вод. 2. Восстановление сульфатов ( «сульфат-редукция» ) - бактерии используют для окисления органики кислород сульфат-ионе 2 Cорг + SO 42 - = 2 H 2 O→ H 2 S = 2 HCO 3 -
 • при p. H >7 образуются HS- → Me. S↓ • H 2 S – высокотоксичен и оказывает существенное влияние на флору и фауну. • Микроэлементы Cu, Zn, Mo, Pb, Hg → переходят в Me. S, для которых очень малое ПР~10 -50(!) • SO 2 - - главный ион, присутствующий в природных водоемах 4 Восстановление сульфатов оказывает существенное влияние на состояние экосистем водоемов. Поскольку SO 42 - является главным анионом природных вод – они способны стабилизировать редокс-буферность 3. Ферментация Cорг(А) → Cорг (B) + CO 2 (сложное) (простое) Cорг + 2 H 2 O → CH 4 + CO 2 Процессы ферментации протекают при значениях pē < -4. 5 вплоть до границы устойчивости воды
• при p. H >7 образуются HS- → Me. S↓ • H 2 S – высокотоксичен и оказывает существенное влияние на флору и фауну. • Микроэлементы Cu, Zn, Mo, Pb, Hg → переходят в Me. S, для которых очень малое ПР~10 -50(!) • SO 2 - - главный ион, присутствующий в природных водоемах 4 Восстановление сульфатов оказывает существенное влияние на состояние экосистем водоемов. Поскольку SO 42 - является главным анионом природных вод – они способны стабилизировать редокс-буферность 3. Ферментация Cорг(А) → Cорг (B) + CO 2 (сложное) (простое) Cорг + 2 H 2 O → CH 4 + CO 2 Процессы ферментации протекают при значениях pē < -4. 5 вплоть до границы устойчивости воды
![Изменение pē пресной воды ([O 2]=10 мг/л; [SO 42 -]=96 мг/л) в зависимости от Изменение pē пресной воды ([O 2]=10 мг/л; [SO 42 -]=96 мг/л) в зависимости от](https://present5.com/presentation/3/139580403_70025306.pdf-img/139580403_70025306.pdf-19.jpg) Изменение pē пресной воды ([O 2]=10 мг/л; [SO 42 -]=96 мг/л) в зависимости от концентрации разложившегося органического вещества (в пересчете на углерод) при p. H=7
Изменение pē пресной воды ([O 2]=10 мг/л; [SO 42 -]=96 мг/л) в зависимости от концентрации разложившегося органического вещества (в пересчете на углерод) при p. H=7
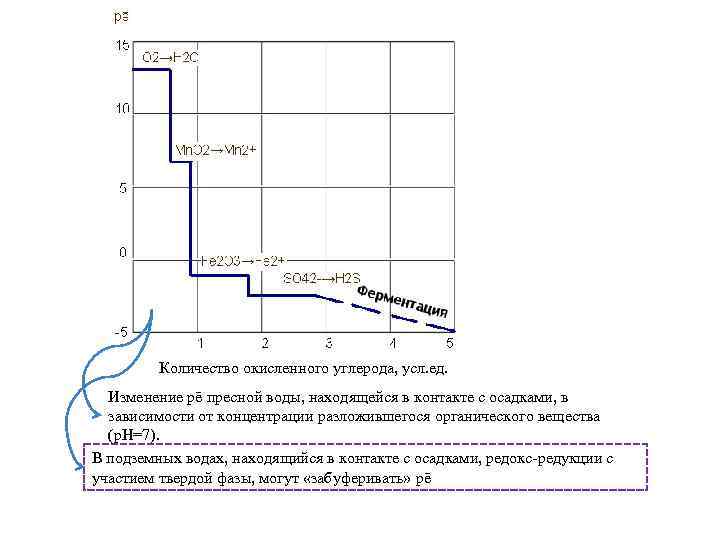 Количество окисленного углерода, усл. ед. Изменение pē пресной воды, находящейся в контакте с осадками, в зависимости от концентрации разложившегося органического вещества (p. H=7). В подземных водах, находящийся в контакте с осадками, редокс-редукции с участием твердой фазы, могут «забуферивать» pē
Количество окисленного углерода, усл. ед. Изменение pē пресной воды, находящейся в контакте с осадками, в зависимости от концентрации разложившегося органического вещества (p. H=7). В подземных водах, находящийся в контакте с осадками, редокс-редукции с участием твердой фазы, могут «забуферивать» pē
 Окислительно-восстановительные процессы в гидросфере Особенности окислительно-восстановительных процессов в озерах Редокс-условия в озерах определяются балансом между окислением органического вещества и поступлением кислорода за счет циркуляции или вертикального воды Специфическая зависимость плотности воды от температуры, приводит к возникновению ярко выраженной слоистой структуры озер, расположенных в районах с умеренно континентальным климатом
Окислительно-восстановительные процессы в гидросфере Особенности окислительно-восстановительных процессов в озерах Редокс-условия в озерах определяются балансом между окислением органического вещества и поступлением кислорода за счет циркуляции или вертикального воды Специфическая зависимость плотности воды от температуры, приводит к возникновению ярко выраженной слоистой структуры озер, расположенных в районах с умеренно континентальным климатом
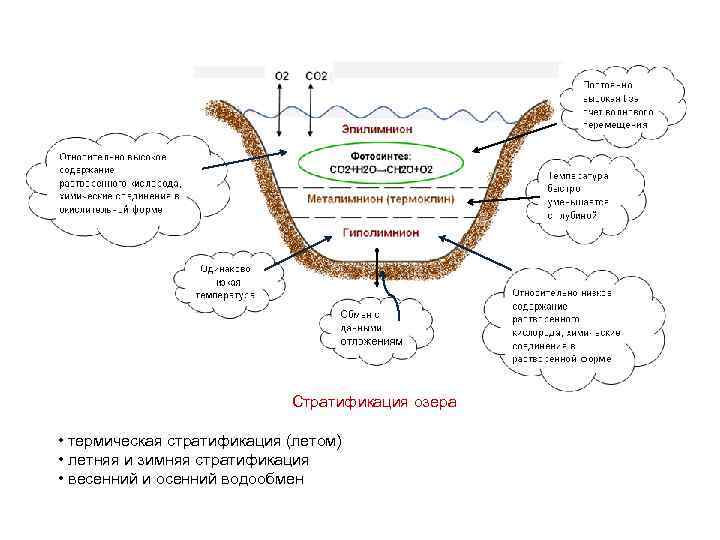 Стратификация озера • термическая стратификация (летом) • летняя и зимняя стратификация • весенний и осенний водообмен
Стратификация озера • термическая стратификация (летом) • летняя и зимняя стратификация • весенний и осенний водообмен
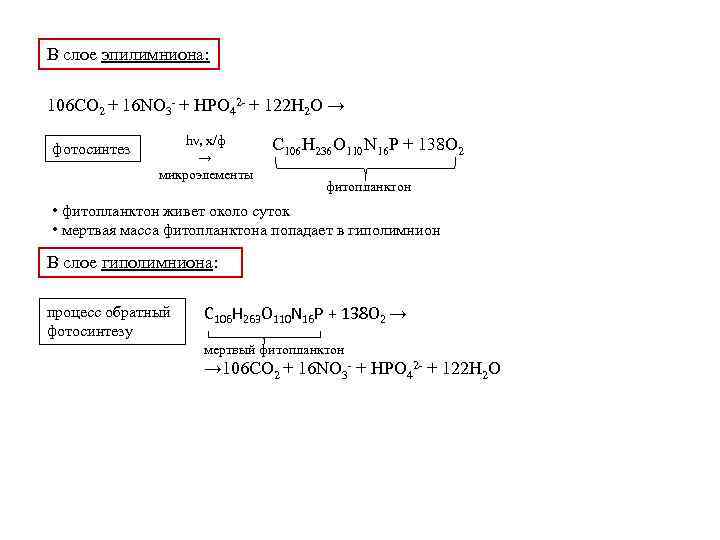 В слое эпилимниона: 106 CO 2 + 16 NO 3 - + HPO 42 - + 122 H 2 O → фотосинтез hν, х/ф → микроэлементы C 106 H 236 O 110 N 16 P + 138 O 2 фитопланктон • фитопланктон живет около суток • мертвая масса фитопланктона попадает в гиполимнион В слое гиполимниона: процесс обратный фотосинтезу C 106 H 263 O 110 N 16 P + 138 O 2 → мертвый фитопланктон → 106 CO 2 + 16 NO 3 - + HPO 42 - + 122 H 2 O
В слое эпилимниона: 106 CO 2 + 16 NO 3 - + HPO 42 - + 122 H 2 O → фотосинтез hν, х/ф → микроэлементы C 106 H 236 O 110 N 16 P + 138 O 2 фитопланктон • фитопланктон живет около суток • мертвая масса фитопланктона попадает в гиполимнион В слое гиполимниона: процесс обратный фотосинтезу C 106 H 263 O 110 N 16 P + 138 O 2 → мертвый фитопланктон → 106 CO 2 + 16 NO 3 - + HPO 42 - + 122 H 2 O
 • при наличии стратификации – содержание кислорода в воде гиполимниона устойчиво снижается из-за разложения органического вещества, выпадающего из эпилимниона. • олиготрофное озеро -продуктивность фотосинтеза мала -вода содержит кислород на всех глубинах • эвтрофное озеро -рост биопродуктивности связанный с интенсивным поступлением питательных веществ - весь кислород в гиполимнионе может быть израсходован, pē резко снижается, начинается сульфат-редукция – условия токсичные для живых организмов - вся рыба – в эпилимнионе - перемешивание воды – замор рыбы - олиготрофное озеро →эвтрофное озеро, в результате антропогенной деятельности. Процесс необратим!
• при наличии стратификации – содержание кислорода в воде гиполимниона устойчиво снижается из-за разложения органического вещества, выпадающего из эпилимниона. • олиготрофное озеро -продуктивность фотосинтеза мала -вода содержит кислород на всех глубинах • эвтрофное озеро -рост биопродуктивности связанный с интенсивным поступлением питательных веществ - весь кислород в гиполимнионе может быть израсходован, pē резко снижается, начинается сульфат-редукция – условия токсичные для живых организмов - вся рыба – в эпилимнионе - перемешивание воды – замор рыбы - олиготрофное озеро →эвтрофное озеро, в результате антропогенной деятельности. Процесс необратим!
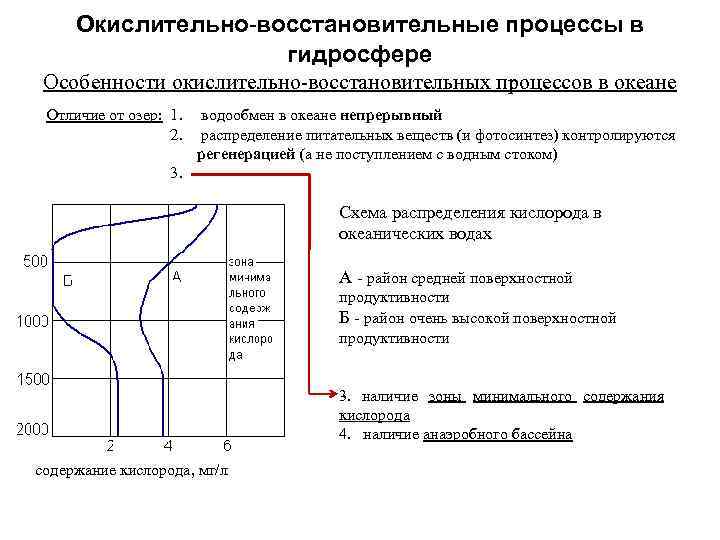 Окислительно-восстановительные процессы в гидросфере Особенности окислительно-восстановительных процессов в океане Отличие от озер: 1. 2. водообмен в океане непрерывный распределение питательных веществ (и фотосинтез) контролируются регенерацией (а не поступлением с водным стоком) 3. Схема распределения кислорода в океанических водах А - район средней поверхностной продуктивности Б - район очень высокой поверхностной продуктивности 3. наличие зоны минимального содержания кислорода 4. наличие анаэробного бассейна содержание кислорода, мг/л
Окислительно-восстановительные процессы в гидросфере Особенности окислительно-восстановительных процессов в океане Отличие от озер: 1. 2. водообмен в океане непрерывный распределение питательных веществ (и фотосинтез) контролируются регенерацией (а не поступлением с водным стоком) 3. Схема распределения кислорода в океанических водах А - район средней поверхностной продуктивности Б - район очень высокой поверхностной продуктивности 3. наличие зоны минимального содержания кислорода 4. наличие анаэробного бассейна содержание кислорода, мг/л
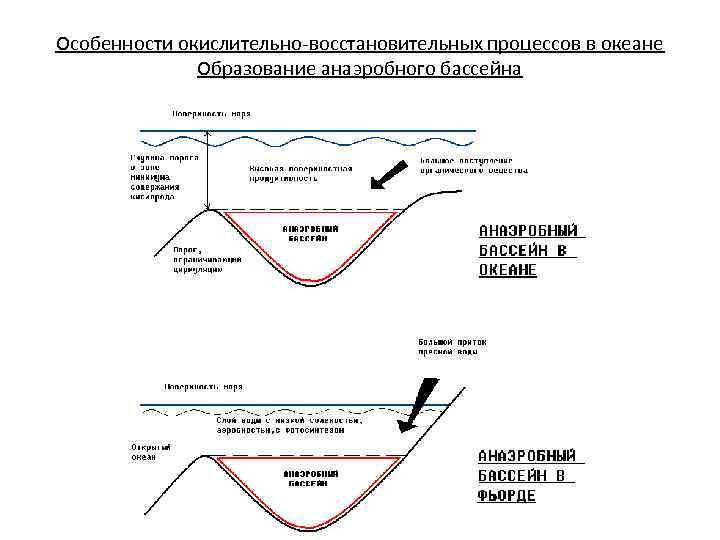 Особенности окислительно-восстановительных процессов в океане Образование анаэробного бассейна
Особенности окислительно-восстановительных процессов в океане Образование анаэробного бассейна
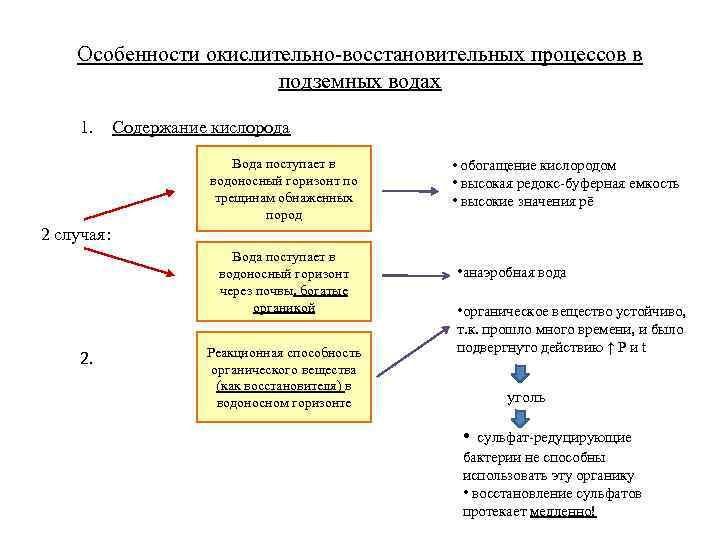 Особенности окислительно-восстановительных процессов в подземных водах 1. Содержание кислорода Вода поступает в водоносный горизонт по трещинам обнаженных пород • обогащение кислородом • высокая редокс-буферная емкость • высокие значения pē 2 случая: Вода поступает в водоносный горизонт через почвы, богатые органикой 2. Реакционная способность органического вещества (как восстановителя) в водоносном горизонте • анаэробная вода • органическое вещество устойчиво, т. к. прошло много времени, и было подвергнуто действию ↑ P и t уголь • сульфат-редуцирующие бактерии не способны использовать эту органику • восстановление сульфатов протекает медленно!
Особенности окислительно-восстановительных процессов в подземных водах 1. Содержание кислорода Вода поступает в водоносный горизонт по трещинам обнаженных пород • обогащение кислородом • высокая редокс-буферная емкость • высокие значения pē 2 случая: Вода поступает в водоносный горизонт через почвы, богатые органикой 2. Реакционная способность органического вещества (как восстановителя) в водоносном горизонте • анаэробная вода • органическое вещество устойчиво, т. к. прошло много времени, и было подвергнуто действию ↑ P и t уголь • сульфат-редуцирующие бактерии не способны использовать эту органику • восстановление сульфатов протекает медленно!
 3. Редокс-уровни подземных вод часто соответствуют величинам pē, задаваемым редокс-парами Mn 2+/Mn. O 2 Fe 2+/Fe(OH)3 Fe 2+/Fe 2 O 3 4. Скорость циркуляции подземных вод мала: pē зависит от времени пребывания воды в водоносном горизонте: чем ↑ время пребывания, тем ↓ pē
3. Редокс-уровни подземных вод часто соответствуют величинам pē, задаваемым редокс-парами Mn 2+/Mn. O 2 Fe 2+/Fe(OH)3 Fe 2+/Fe 2 O 3 4. Скорость циркуляции подземных вод мала: pē зависит от времени пребывания воды в водоносном горизонте: чем ↑ время пребывания, тем ↓ pē
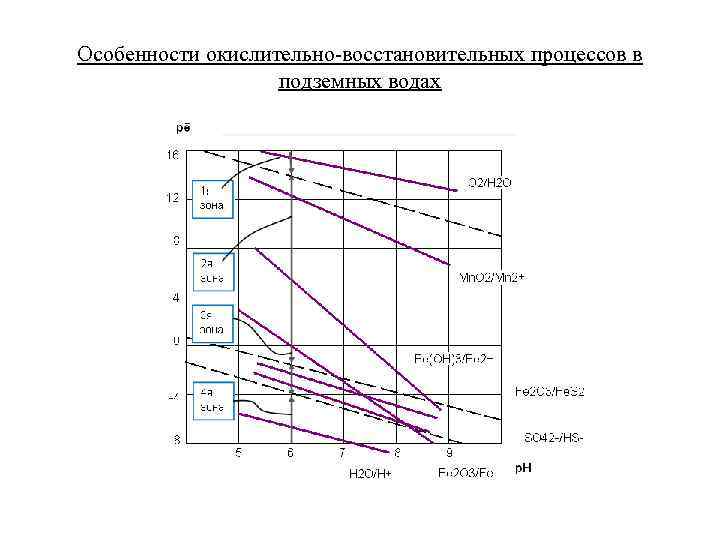 Особенности окислительно-восстановительных процессов в подземных водах
Особенности окислительно-восстановительных процессов в подземных водах
 Окислительно-восстановительные процессы в гидросфере • Большинство подземных вод относятся к зоне 2. Вода не содержит свободного кислорода, но в ней и не наблюдается сульфат-редукция. Вода может быть использована для бытового водоснабжения. Иногда [Fen+] и [Mnn+] ≥ 1 ppm, что создает проблемы. • Зона 3 Воды, забуференные сульфат-редукцией - долгое время пребывания воды в водоносном горизонте + присутствие большого количества органического вещества. Высшие концентрации сульфидов делают эти воды непригодными для бытового водоснабжения. • Зона 4 Располагаются ниже границы сульфат/сульфид→ характерны для современных илов.
Окислительно-восстановительные процессы в гидросфере • Большинство подземных вод относятся к зоне 2. Вода не содержит свободного кислорода, но в ней и не наблюдается сульфат-редукция. Вода может быть использована для бытового водоснабжения. Иногда [Fen+] и [Mnn+] ≥ 1 ppm, что создает проблемы. • Зона 3 Воды, забуференные сульфат-редукцией - долгое время пребывания воды в водоносном горизонте + присутствие большого количества органического вещества. Высшие концентрации сульфидов делают эти воды непригодными для бытового водоснабжения. • Зона 4 Располагаются ниже границы сульфат/сульфид→ характерны для современных илов.
 Окислительно-восстановительные процессы в гидросфере Окислительно-восстановительные условия и миграция элементов • некоторые рудные месторождения (например месторождения U) являются следствием редокс-реакции в подземных водах. • интенсивность миграции элементов характеризуют коэффициентом водной миграции Kx = mx 100/anx mx – содержание элемента x в воде, мг/л nx – содержание элемента x в породах, % a – минерализация воды, мг/л • чем ↑ величина Kx, тем больше миграционная способность данных элементов. Kx > 20 Очень подвижные мигранты Kx=20 подвижные мигранты kx< 0. 1 слабоподвижные мигранты Zn Fe, Ti, Al • кислотно-основные и окислительно-восстановительные характеристики среды влияют на миграцию элементов • живые организмы способны в значительной мере трансформировать процессы миграции
Окислительно-восстановительные процессы в гидросфере Окислительно-восстановительные условия и миграция элементов • некоторые рудные месторождения (например месторождения U) являются следствием редокс-реакции в подземных водах. • интенсивность миграции элементов характеризуют коэффициентом водной миграции Kx = mx 100/anx mx – содержание элемента x в воде, мг/л nx – содержание элемента x в породах, % a – минерализация воды, мг/л • чем ↑ величина Kx, тем больше миграционная способность данных элементов. Kx > 20 Очень подвижные мигранты Kx=20 подвижные мигранты kx< 0. 1 слабоподвижные мигранты Zn Fe, Ti, Al • кислотно-основные и окислительно-восстановительные характеристики среды влияют на миграцию элементов • живые организмы способны в значительной мере трансформировать процессы миграции
 Окислительно-восстановительные процессы в гидросфере Окислительно-восстановительные условия и миграция элементов • Геохимический барьер – зона, где происходит резкое уменьшение интенсивности миграции, что приводит к концентрированию химических элементов • Барьеры возникают при резких изменениях величины ph или p. H/ Ek
Окислительно-восстановительные процессы в гидросфере Окислительно-восстановительные условия и миграция элементов • Геохимический барьер – зона, где происходит резкое уменьшение интенсивности миграции, что приводит к концентрированию химических элементов • Барьеры возникают при резких изменениях величины ph или p. H/ Ek


