Окисление разбавленной HNO 3 Азотная


Окисление разбавленной HNO 3 Азотная кислота используется в основном для реакций деструктивного окисления циклических соединений или соединений с ненасыщенными связями, которое идет в ее присутствии с лучшими выходами, чем например, при использовании молекулярного кислорода. В промышленности типичным процессом окисления с использованием HNO 3 является окисление циклогексанола 60% HNO 3. с образованием адипиновой и валериановой кислот. Азотная кислота никогда не используется для окисления парафинов

Циклогексанол и свежую 60% HNO 3 (в двукратном количестве по отношению к стехиометрическому и с добавкой медь ванадиевого катализатора) подают на всасывающую линию насоса 1, где они разбавляются большим объемом циркулирующего оксидата, и затем в трубчатый реактор 2, охлаждаемый водой, где при 60 80 о С и 0. 3 0. 5 МПа происходит основная часть превращений. Оксидат первой стадии выходит с верха реактора 2 и освобождается в сепараторе 3 от образовавшихся оксидов азота, после чего большую его часть подают на рециркуляцию, а меньшую направляют в реактор 4 второй ступени окисления. Оксидат второй ступени отделяют от оксидов азота в сепараторе 5 и затем дополнительно отдувают их воздухом в скруббере 6. Отдувочный газ вместе с оксидами азота после сепараторов 3 и 5 поступает в скруббер 7, орошаемый слабой азотной кислотой, которая «укрепляется» до необходимой для окисления концентрации (60%). Оксидат из скруббера 6 направляют в вакуум ректификационную колонну 8, где отгоняется валериановая кислота. Кубовую жидкость колонны 8 охлаждают в кристаллизаторе 9, выпавшие кристаллы адипиновой кислоты отделяют от маточного раствора на центрифуге 10.

Из всей гаммы окислительных процессов, протекающих под действием HNO 3, остановимся на окислении метилбензолов в ароматические кислоты Окисление азотной кислотой менее экзотермическая реакция, чем окисление молекулярным кислородом, т. к. при окислении образуются окислы азота, а процесс их образования является эндотермическим, что и снижает общий тепловой эффект реакции. Окисление азотной кислотой является радикально цепным процессом. Азотная кислота, (реже окислы азота) являются вторым по масштабам при менения окислительным агентом. Однако, ее действие нередко сопровождается побочной реакцией нитрования, которая усиливается при увеличении концентрации азотной кислоты. Поэтому для окисления используется обычно 40 60% HNO 3

Механизм окисления В основу современных представлений о механизме окисления HNO 3 положен тезис, выдвинутый еще в начале столетия Титовым, что азотная кислота в молекулярной форме окислителем не является. При высокой температуре HNO 3 разлагается с образованием радикалов Радикалы НО. И NO 3. зафиксированы при разложении HNO 3 в газовой фазе. При высокой температуре образование радикалов NO 2. может происходить и при взаимодействии HNO 3 с окислами азота.

Наиболее активны радикалы OH. И NO 3. , однако, вероятность их образования мала, хотя в начальный период, когда концентрация NO 2. еще мала, они могут служить источниками бензильных радикалов. 1. Инициирование цепи начинается с зарождения бензильного радикала Эта стадия определяет скорость реакции. Роль NO 2. подтверждена многочисленными опытами по влиянию диффузии и концентрации NO 2. на скорость реакции окисления. 2. Рекомбинация радикалов является продолжением цепи При температурах меньше 100 о. С их можно выделить из реакционной массы.

3. Продукты рекомбинации могут взаимодействовать с окислительной средой При 0 о. С динитросоединения являются основными продуктами, т. е. когда К 1 К 2. При 70 100 о. С К 1=К 2. Ароматические альдегиды и спирты гораздо менее устойчивы к радикальной атаке, чем исходные соединения и гораздо быстрее окисляются до Ar. COOH.

Промежуточно образующийся ацильный радикал может взаимодействовать с исходным соединением осуществляя передачу цепи Аналогично метилбензолам в реакцию с ацильным и перацильным радикалам могут вступать и промежуточные продукты нитросоединения, спирты, альдегиды Однако, вероятность этих реакций мала

Согласно этому механизму для успешного окисления метилбензолов необходимы условия, способствующих образованию радикалов, в первую очередь NO 2, который определяет начало цепи. Такими условиями являются: -Температура окисления. Высокие температуры будут способствовать образованию радикалов и увеличению их концентрации. При низких температурах скорость окисления мала и метилбензолы успевают пронитроваться. Оптимальные температуры – 140 240 (160 170)о. С, выше 250 о. С – большой вклад окислительных процессов. Давление. При высоких температурах HNO 3 будет находиться в газовой фазе, а окисление должно протекать в гомогенной, жидкой фазе, поэтому необходимо применять давление. Необходимое давление определяется температурой кипения используемой водной азотной кислоты -Концентрация HNO 3 и модуль ее по отношению к МБ. Обычно используется 10 60% (иногда 80%). Ниже 10% скорость окисления мала, необходим очень большой модуль, требуемый для создания необходимого окислительного потенциала Больше 60% сильный вклад побочных процессов, обусловленных нитрованием ароматики. Модуль (отношение HNO 3 к МБ) = 2 -4. При модуле 2 в продуктах реакции остается метилбензол, в газовую фазу переходит значительное количество HNO 3 (при 200 о. С около 15%), что вызывает неопределенные условия эксперимента.

Т. к. окисление протекает под давлением с выделением большого количества газа коэффициент заполнения автоклава =0. 2 -0. 8 Верхний предел обусловлен тем, что в остающееся газовое пространство выделяется большое количество газов, которые создают дополнительное давление, иногда превышающее максимально допустимое для данной аппаратуры. Например, использование 40% HNO 3 при температуре 180 о. C и =0. 9 , М= 4 давление доходит до 200 атм. Поэтому для каждого нитротолуола ( а в общем случае замещенного) есть оптимальный коэффициент заполнения, который можно рассчитать исходя из молекулярной массы, объема аппарата (автоклава), плотности окисляемого соединения и концентрации используемой кислоты. Реакционные газы: NO 2, CO 2, N 2 и небольшое количество NO.
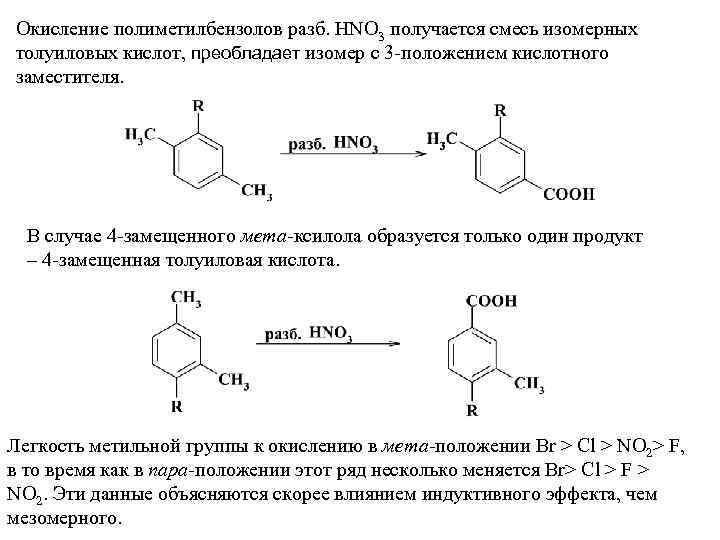
Окисление полиметилбензолов разб. HNO 3 получается смесь изомерных толуиловых кислот, преобладает изомер с 3 положением кислотного заместителя. В случае 4 замещенного мета ксилола образуется только один продукт – 4 замещенная толуиловая кислота. Легкость метильной группы к окислению в мета положении Br > Cl > NO 2> F, в то время как в пара-положении этот ряд несколько меняется Br> Cl > F > NO 2. Эти данные объясняются скорее влиянием индуктивного эффекта, чем мезомерного.

Получение нитробензойных кислот. Способам получения нитробензойных кислот уделяется большое внимание уже достаточно долгое время. При этом усилия, направленные на окисление различных изомерных нитротолуолов неравноценны. Мета нитробензойную кислоту можно получать прямым электрофильным нитрованием бензойной кислоты серно азотными или олеум азотными смесями, хотя они характеризуются значительным расходом кислот и большим количеством отработанных кислот. Выход мета-НБК составляет 80%, однако в полученных продуктах нитрования содержится до 10 12% изомеров, что вызывает необходимость сложной очистки ее. Нитрующие смеси: HNO 3, М 3 2. HNO 3 + H 2 SO 4 В промышленности мета нитробензойную кислоту получают нитрованием бензойной кислоты под действием KNO 3 в конц. H 2 SO 4 при 20— 240 C. При этом образуется 20% орто нитробензойной кислоты, 1, 5% пара нитробензойной кислоты, которые отделяют от основного продукта фракционной кристаллизацией натриевых солей этих кислот.

В лаборатории мета НБК получают нитрованием метилового эфира бензойной кислоты с последующим гидролизом. Принципиально другим способом получения мета НБК является окисление мета-НТ кислородом воздуха в среде уксусной кислоты в присутствии катализаторов (Co, Ni, Br 2) при температуре 100 2000 C и давлении 0. 3 3. 9 МПа (Японский патент). Выход составляет 20%. Основной недостаток: низкий выход целевого продукта сложность выделения мета НБК из уксусной кислоты, насыщенной тяжелыми металлами и бромом большая опасность процесс, т. к. окисление проходит в пределах взрывоопасных концентраций уксусной кислоты в воздушной среде. огромный расход УК (600 м 3 на 1 м 3 мета НТ) трудности регенерации отработанной УК

Многие недостатки исключаются при окислении мета НТ разбавленной азотной кислотой. Используется 30% HNO 3 , Т 180 200 о. С, давление 25 30 атм. Т. к. имеется возможность протекания побочной реакции дальнейшего нитрования, то селективность достигается подбором времени контакта для выбранных температур, давления модуля и концентрации HNO 3. Выход в пересчете на мета НТ составляет 85%. В условиях большого избытка HNO 3 равновесие реакции смешено вправо, в результате чего в продуктах реакции преобладает двуокись азота Целевой продукт мета-нитробензойная кислота при значительном време ни выдержки частично подвергается распаду с образованием мета-ДНБ и ТНБ

Оптимум : температура 180 220 о. С (200 о. С); давление 15 35 атм. (20 атм) концентрация HNO 3 – 25 35 % (30%); модуль 1, 5 2, 0 (2. 0) время контакта – 5 120 мин. (20 30 мин) Получение осуществляется в системе последовательно соединенных аппаратов вытеснения, состоит из основного аппарата – окислителя, буферного аппарата и аппарата выгрузки продуктов реакции. Перед входом в реактор – окислитель исходные компоненты подогреваются в теплообменнике до 160 200 о. С. Конструкция реактора окислителя – колонный аппарат, секционированный вертикальными коаксиальными трубами, приближает гидродинамический режим движения жидкости к режиму идеального вытеснения. Жидкость последовательно проходит все секции реактора, при этом ее уровень остается постоянным и задается срезом давильной трубы, по которой реакционная масса выходит из реактора. Верхние открытые концы трубы, выступающие над уровнем жидкости, играет роль сепаратора и предотвращает переброс жидкой фазы из одной секции в другую.

Вывод продуктов реакции осуществляется с помощью дросселирующих клапанов. После дросселирования реакционная масса собирается в кристаллизаторе низкого давления. Газообразные продукты реакции непрерывно с помощью вакуума поступают на абсорбцию. Очистка мета-НБК: от органики промывание толуолом, этанолом от неорганики – перекристаллизация из 45 50% HNO 3. Утилизация ОК: 20% HNO 3, содержит 0. 15% мета НБК, 0. 1 0. 4% ДНБК. Удаление нитротел – с помощью микропористых активированных углей. Пропускают через колонну с АУ под давлением сжатого воздуха, десорбция нитротел ацетоном. Процесс экологически безопасен при условии надежной работы систем абсорбции и адсорбции. Расход компонентов на 1 т : HNO 3 1. 035 т.
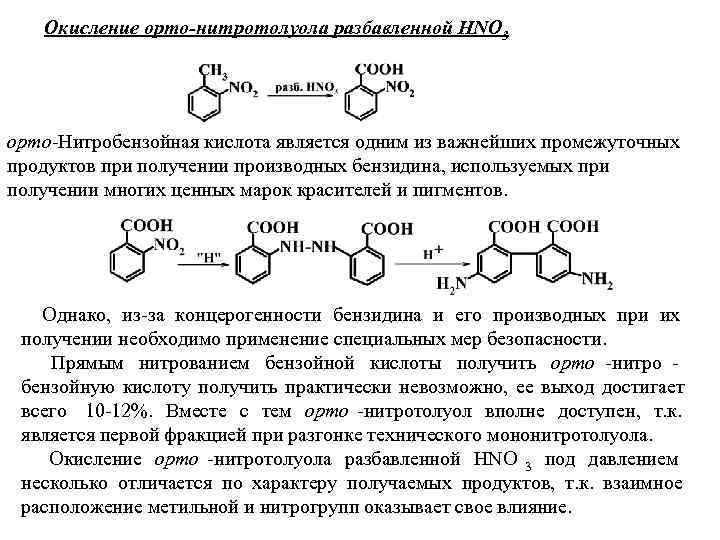
Окисление орто-нитротолуола разбавленной HNO 3 орто-Нитробензойная кислота является одним из важнейших промежуточных продуктов при получении производных бензидина, используемых при получении многих ценных марок красителей и пигментов. Однако, из за концерогенности бензидина и его производных при их получении необходимо применение специальных мер безопасности. Прямым нитрованием бензойной кислоты получить орто нитро бензойную кислоту получить практически невозможно, ее выход достигает всего 10 12%. Вместе с тем орто нитротолуол вполне доступен, т. к. является первой фракцией при разгонке технического мононитротолуола. Окисление орто нитротолуола разбавленной HNO 3 под давлением несколько отличается по характеру получаемых продуктов, т. к. взаимное расположение метильной и нитрогрупп оказывает свое влияние.

О параметрах процесса: -температура окисления 210 2200 С -концентрация HNO 3 – 35 45%, что несколько выше, чем при окислении мета-нитротолуола -модуль по кислоте – 4 4, 5, что также несколько выше, чем при окислении мета нитротолуола давление 60 70 атм. α 0. 6. Такой большой модуль, большой расход HNO 3 объясняется большим ее расходом на побочные окислительные процессы, вкладом образования пикриновой кислоты и ее деструкцией, деструктивных процессов вообще, и необходимостью поддержания необходимого окислительного потенциала Увеличение модуля сверх 5 нецелесообразно, вследствие трудности выделения орто нитробензойной кислоты из реакционной массы, увеличения уноса орто НБК с отработанной кислотой за счет растворимости
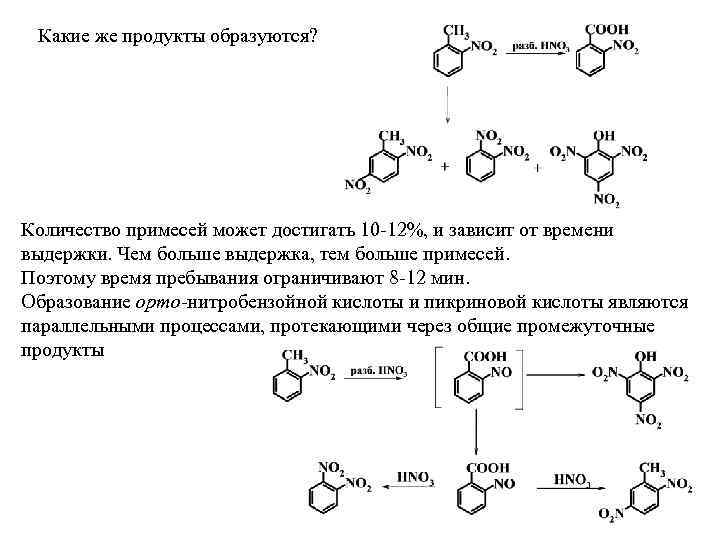
Какие же продукты образуются? Количество примесей может достигать 10 12%, и зависит от времени выдержки. Чем больше выдержка, тем больше примесей. Поэтому время пребывания ограничивают 8 12 мин. Образование орто нитробензойной кислоты и пикриновой кислоты являются параллельными процессами, протекающими через общие промежуточные продукты

Увеличение количества окислов в реакционном объеме сдвигает направление реакции окисления в сторону образования пикриновой кислоты. Реакция протекает по схеме Разложение пикриновой кислоты идет по реакции динитробензола по реакции динитробензойной кислоты по реакции орто нитробензойной кислоты

Т. о. реакционные газы состоят из N 2, CO 2, NO 2 и небольшого количества NO. Выход орто нитробензойной кислоты – 65%. Выделение орто нитробензойной кислоты – медленная кристаллизация ее из реакционной массы с последующей промывкой водой на фильтре. При содержании примесей до 0, 5 % для удовлетворительной чистоты продукта достаточно 2 х промывок при соотношении продукт: вода = 1: 1. Режим кристаллизации: скорость охлаждения 100 в мин, что позволяет получать крупные кристаллы (≈100 μ) с минимальным количеством примесей. Если оценить процесс высокотемпературного окисления разбавленной HNO 3 в целом, необходимо отметить, что он сочетает в себе непрерывные и периодические стадии: окисление НТ до НБК – осуществляется непрерывно и дистанционно, все остальные стадии периодические. Это обеспечивает удобство в эксплуатации и мобильность в решении задач на отдельных стадиях Окисление разбавленной HNO 3 применяется при получении ДНБК, тринитробензойной кислоты (далее до ТНБ), фталевой, хлорнитробензойной , полихлорбензойных, пиридин 2. 5 дикарбоновой, никотиновой кислот. Окисление ксилолов, мезитилена, цимола. лигнина дает до 10% НС.
Презентация 9-окисление разб. HNO3.ppt
- Количество слайдов: 20

