Окисление органических соединений.ppt
- Количество слайдов: 46
 ОКИСЛЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
ОКИСЛЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
 МЫ РАССМОТРИМ Окисление различных классов органических соединений Примеры заданий
МЫ РАССМОТРИМ Окисление различных классов органических соединений Примеры заданий
 ОПРЕДЕЛЕНИЯ
ОПРЕДЕЛЕНИЯ
 ОПРЕДЕЛЕНИЯ
ОПРЕДЕЛЕНИЯ
 ОПРЕДЕЛЕНИЯ
ОПРЕДЕЛЕНИЯ
 КЛАССЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Алканы и циклоалканы Алкены Алкины Ароматические соединения Спирты и простые эфиры Альдегиды и кетоны Карбоновые кислоты
КЛАССЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Алканы и циклоалканы Алкены Алкины Ароматические соединения Спирты и простые эфиры Альдегиды и кетоны Карбоновые кислоты
 ТИПЫ РЕАКЦИЙ ОКИСЛЕНИЯ Полное окисление (горение) Каталитическое окисление кислородом Препаративное окисление KMn. O 4 K 2 Cr 2 O 7 H 2 O 2 Mn. O 2 и другие
ТИПЫ РЕАКЦИЙ ОКИСЛЕНИЯ Полное окисление (горение) Каталитическое окисление кислородом Препаративное окисление KMn. O 4 K 2 Cr 2 O 7 H 2 O 2 Mn. O 2 и другие
 АЛКАНЫ И ЦИКЛОАЛКАНЫ При внесении в открытое пламя алканы горят. При этом в избытке кислорода происходит их полное окисление до СО 2, где углерод имеет высшую степень окисления +4, и воды. Уравнение реакции горения алканов в общем виде:
АЛКАНЫ И ЦИКЛОАЛКАНЫ При внесении в открытое пламя алканы горят. При этом в избытке кислорода происходит их полное окисление до СО 2, где углерод имеет высшую степень окисления +4, и воды. Уравнение реакции горения алканов в общем виде:
 АЛКАНЫ И ЦИКЛОАЛКАНЫ При горении высших алканов (n >>1) кислорода, содержащегося в воздухе, может оказаться недостаточно для их полного окисления. Тогда образуются продукты частичного окисления: угарный газ СО (степень окисления углерода +2), сажа (мелкодисперсный углерод, нулевая степень окисления).
АЛКАНЫ И ЦИКЛОАЛКАНЫ При горении высших алканов (n >>1) кислорода, содержащегося в воздухе, может оказаться недостаточно для их полного окисления. Тогда образуются продукты частичного окисления: угарный газ СО (степень окисления углерода +2), сажа (мелкодисперсный углерод, нулевая степень окисления).
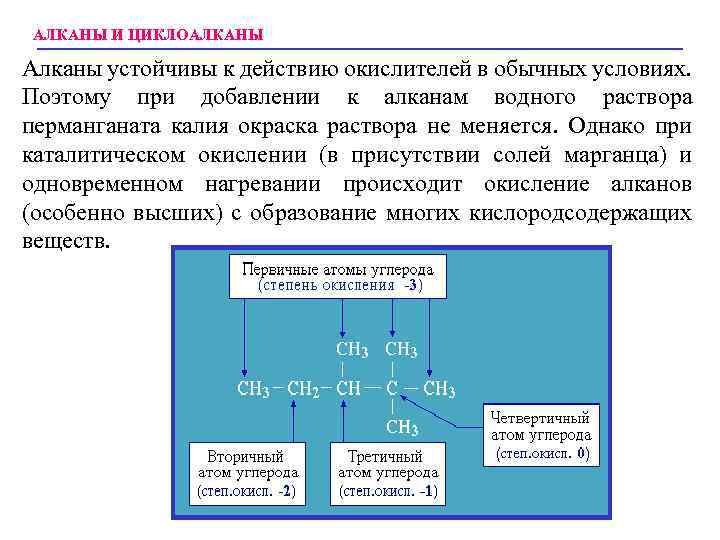 АЛКАНЫ И ЦИКЛОАЛКАНЫ Алканы устойчивы к действию окислителей в обычных условиях. Поэтому при добавлении к алканам водного раствора перманганата калия окраска раствора не меняется. Однако при каталитическом окислении (в присутствии солей марганца) и одновременном нагревании происходит окисление алканов (особенно высших) с образование многих кислородсодержащих веществ.
АЛКАНЫ И ЦИКЛОАЛКАНЫ Алканы устойчивы к действию окислителей в обычных условиях. Поэтому при добавлении к алканам водного раствора перманганата калия окраска раствора не меняется. Однако при каталитическом окислении (в присутствии солей марганца) и одновременном нагревании происходит окисление алканов (особенно высших) с образование многих кислородсодержащих веществ.
 АЛКАНЫ И ЦИКЛОАЛКАНЫ Частичное окисление алканов при относительно невысокой температуре и с применением катализаторов сопровождается разрывом только части связей С–С и С–Н и используется для получения ценных продуктов: карбоновых кислот, кетонов, альдегидов, спиртов. Например, при повышенной Т на медном катализаторе метан окисляется до метанола: 2 СН 4+О 2 2 СН 3 ОН А при неполном окислении бутана (разрыв связи С 2–С 3) получают уксусную кислоту: Высшие алканы (n>25) под действием кислорода воздуха в жидкой фазе в присутствии солей марганца превращаются в смесь карбоновых кислот со средней длиной цепи С 12–С 18, которые используются для получения моющих средств и поверхностно-активных веществ.
АЛКАНЫ И ЦИКЛОАЛКАНЫ Частичное окисление алканов при относительно невысокой температуре и с применением катализаторов сопровождается разрывом только части связей С–С и С–Н и используется для получения ценных продуктов: карбоновых кислот, кетонов, альдегидов, спиртов. Например, при повышенной Т на медном катализаторе метан окисляется до метанола: 2 СН 4+О 2 2 СН 3 ОН А при неполном окислении бутана (разрыв связи С 2–С 3) получают уксусную кислоту: Высшие алканы (n>25) под действием кислорода воздуха в жидкой фазе в присутствии солей марганца превращаются в смесь карбоновых кислот со средней длиной цепи С 12–С 18, которые используются для получения моющих средств и поверхностно-активных веществ.
 АЛКАНЫ И ЦИКЛОАЛКАНЫ Основным способом переработки метана является его конверсия окисление водяным паром, кислородом или оксидом углерода (IV) в присутствии катализатора и при высокой температуре: СН 4 + H 2 O CO + 3 H 2 CH 4 + 1/2 O 2 CO + 2 H 2 CH 4 + CO 2 2 CO + 2 H 2 В результате этих реакций образуется синтез-газ (водяной газ) — ценное сырье для получения многих органических соединений (углеводородов, метилового и других спиртов и т. д. ).
АЛКАНЫ И ЦИКЛОАЛКАНЫ Основным способом переработки метана является его конверсия окисление водяным паром, кислородом или оксидом углерода (IV) в присутствии катализатора и при высокой температуре: СН 4 + H 2 O CO + 3 H 2 CH 4 + 1/2 O 2 CO + 2 H 2 CH 4 + CO 2 2 CO + 2 H 2 В результате этих реакций образуется синтез-газ (водяной газ) — ценное сырье для получения многих органических соединений (углеводородов, метилового и других спиртов и т. д. ).
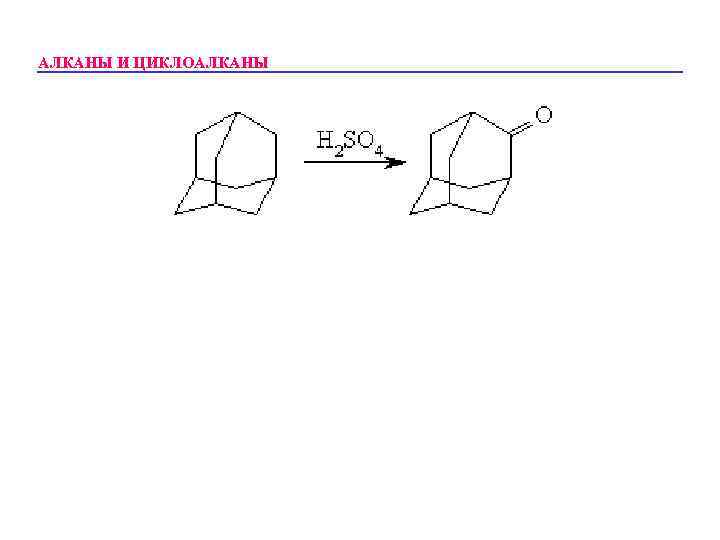 АЛКАНЫ И ЦИКЛОАЛКАНЫ
АЛКАНЫ И ЦИКЛОАЛКАНЫ
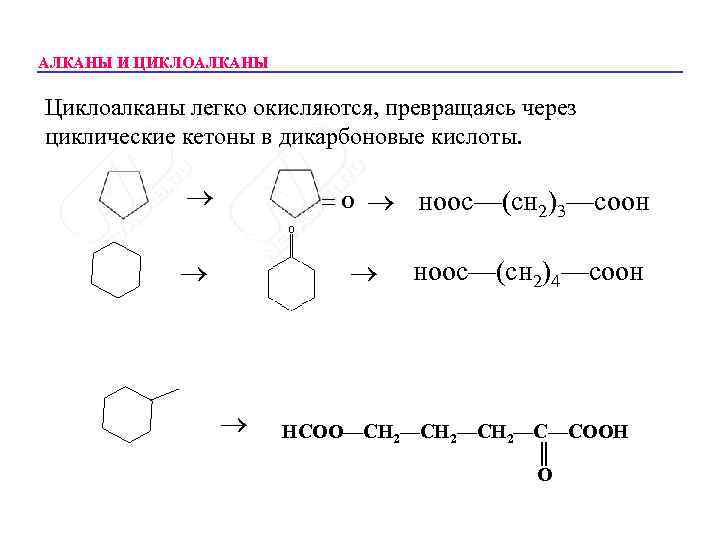 АЛКАНЫ И ЦИКЛОАЛКАНЫ Циклоалканы легко окисляются, превращаясь через циклические кетоны в дикарбоновые кислоты. О ноос—(сн 2)3—соон ноос—(сн 2)4—соон НСОО—СН 2—СН 2—С—СООН ║ О
АЛКАНЫ И ЦИКЛОАЛКАНЫ Циклоалканы легко окисляются, превращаясь через циклические кетоны в дикарбоновые кислоты. О ноос—(сн 2)3—соон ноос—(сн 2)4—соон НСОО—СН 2—СН 2—С—СООН ║ О
 АЛКЕНЫ • Алкены легко дают продукты окисления в мягких условиях– диолы, альдегиды, кетоны, кислоты. ● Каталитическое окисление приводит к эпоксидам. • Под действием в/р KMn. O 4 дают диолы. • Под действием KMn. O 4/H 2 SO 4 дают кетоны или кислоты.
АЛКЕНЫ • Алкены легко дают продукты окисления в мягких условиях– диолы, альдегиды, кетоны, кислоты. ● Каталитическое окисление приводит к эпоксидам. • Под действием в/р KMn. O 4 дают диолы. • Под действием KMn. O 4/H 2 SO 4 дают кетоны или кислоты.
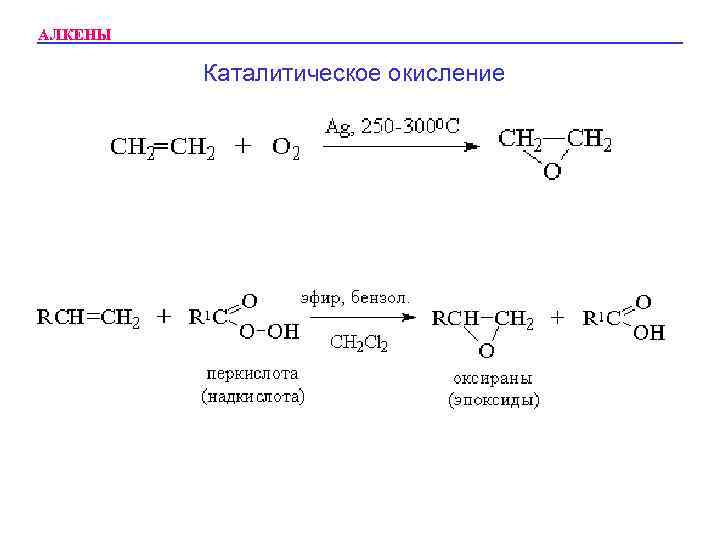 АЛКЕНЫ Каталитическое окисление
АЛКЕНЫ Каталитическое окисление
 АЛКЕНЫ Реакция Вагнера +7 -2 -1 +4 СН 2 + KMn. O 4 + H 2 O CH 2(OH)—CH 2(OH) + Mn. O 2 + KOH -2 e C 2 -2 C 2 -1 3 + 3 e Mn+7 Mn+4 2 3 СН 2 + 2 KMn. O 4 + 4 H 2 O 3 CH 2(OH)—CH 2(OH) + 2 Mn. O 2 + 2 KOH
АЛКЕНЫ Реакция Вагнера +7 -2 -1 +4 СН 2 + KMn. O 4 + H 2 O CH 2(OH)—CH 2(OH) + Mn. O 2 + KOH -2 e C 2 -2 C 2 -1 3 + 3 e Mn+7 Mn+4 2 3 СН 2 + 2 KMn. O 4 + 4 H 2 O 3 CH 2(OH)—CH 2(OH) + 2 Mn. O 2 + 2 KOH
 АЛКЕНЫ При окислении алкенов щелочным водным раствором перманганата калия при нагревании или раствором KMn. O 4 в водной серной кислоте, а также при окислении алкенов дихроматом калия и серной кислотой первоначально образующийся гликоль подвергается окислительной деструкции. Конечным результатом является расщепление углеродного скелета по месту двойной связи и образование в качестве конечных продуктов кетонов и (или) карбоновых кислот в зависимости от заместителей при двойной связи. Если оба атома углерода при двойной связи содержат только по одной алкильной группе, конечным продуктом исчерпывающего окисления будет смесь карбоновых кислот, тетразамещенный при двойной связи алкен окисляется до двух кетонов. Однозамещанные алкены с концевой двойной связью расщепляются до карбоновой кислоты и углекислого газа.
АЛКЕНЫ При окислении алкенов щелочным водным раствором перманганата калия при нагревании или раствором KMn. O 4 в водной серной кислоте, а также при окислении алкенов дихроматом калия и серной кислотой первоначально образующийся гликоль подвергается окислительной деструкции. Конечным результатом является расщепление углеродного скелета по месту двойной связи и образование в качестве конечных продуктов кетонов и (или) карбоновых кислот в зависимости от заместителей при двойной связи. Если оба атома углерода при двойной связи содержат только по одной алкильной группе, конечным продуктом исчерпывающего окисления будет смесь карбоновых кислот, тетразамещенный при двойной связи алкен окисляется до двух кетонов. Однозамещанные алкены с концевой двойной связью расщепляются до карбоновой кислоты и углекислого газа.
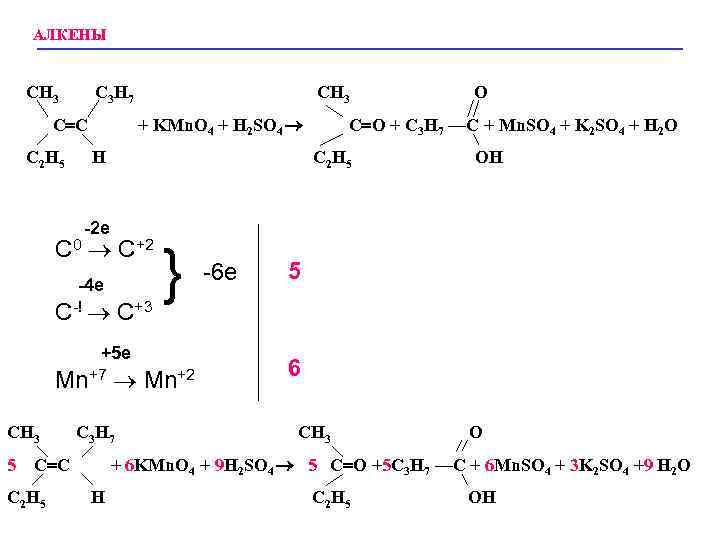 АЛКЕНЫ CH 3 C 3 H 7 + KMn. O 4 + H 2 SO 4 C C C 2 H 5 CH 3 H C 0 C+2 -4 e C-! C+3 } +5 e Mn+7 Mn+2 CH 3 C 3 H 7 -6 e OH 5 6 CH 3 O + 6 KMn. O 4 + 9 H 2 SO 4 5 C O +5 C 3 H 7 —C + 6 Mn. SO 4 + 3 K 2 SO 4 +9 H 2 O 5 C C C 2 H 5 C O + C 3 H 7 —C + Mn. SO 4 + K 2 SO 4 + H 2 O C 2 H 5 -2 e O H C 2 H 5 OH
АЛКЕНЫ CH 3 C 3 H 7 + KMn. O 4 + H 2 SO 4 C C C 2 H 5 CH 3 H C 0 C+2 -4 e C-! C+3 } +5 e Mn+7 Mn+2 CH 3 C 3 H 7 -6 e OH 5 6 CH 3 O + 6 KMn. O 4 + 9 H 2 SO 4 5 C O +5 C 3 H 7 —C + 6 Mn. SO 4 + 3 K 2 SO 4 +9 H 2 O 5 C C C 2 H 5 C O + C 3 H 7 —C + Mn. SO 4 + K 2 SO 4 + H 2 O C 2 H 5 -2 e O H C 2 H 5 OH
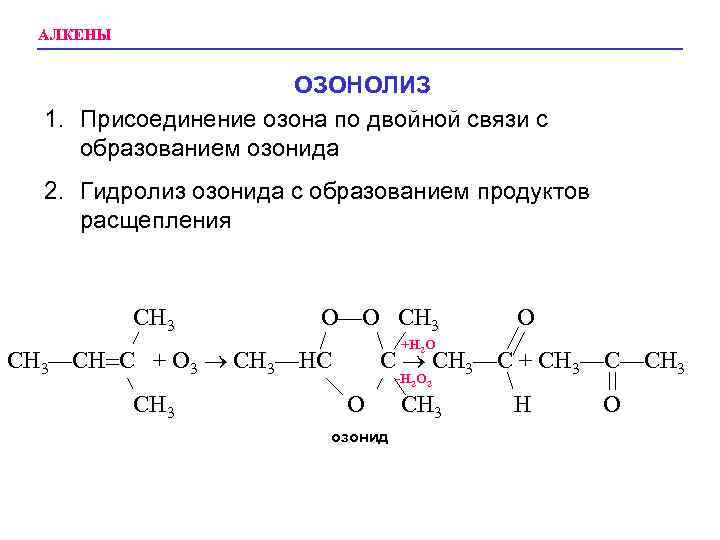 АЛКЕНЫ ОЗОНОЛИЗ 1. Присоединение озона по двойной связи с образованием озонида 2. Гидролиз озонида с образованием продуктов расщепления CH 3 O—O CH 3 +H 2 O CH 3—CH C + O 3 CH 3—HC CH 3 O C CH 3—C + CH 3—C—CH 3 -H 2 O 2 O озонид CH 3 H O
АЛКЕНЫ ОЗОНОЛИЗ 1. Присоединение озона по двойной связи с образованием озонида 2. Гидролиз озонида с образованием продуктов расщепления CH 3 O—O CH 3 +H 2 O CH 3—CH C + O 3 CH 3—HC CH 3 O C CH 3—C + CH 3—C—CH 3 -H 2 O 2 O озонид CH 3 H O
 АЛКИНЫ • Алкины еще легче вступают в реакции окисления. Мгновенно обесцвечивают р-р KMn. O 4. • Ацетилен под действием в/р KMn. O 4 превращается в оксолат калия, другие алкины дают дикетоны. • Под действием KMn. O 4/H 2 SO 4 и озона дают кислоты.
АЛКИНЫ • Алкины еще легче вступают в реакции окисления. Мгновенно обесцвечивают р-р KMn. O 4. • Ацетилен под действием в/р KMn. O 4 превращается в оксолат калия, другие алкины дают дикетоны. • Под действием KMn. O 4/H 2 SO 4 и озона дают кислоты.
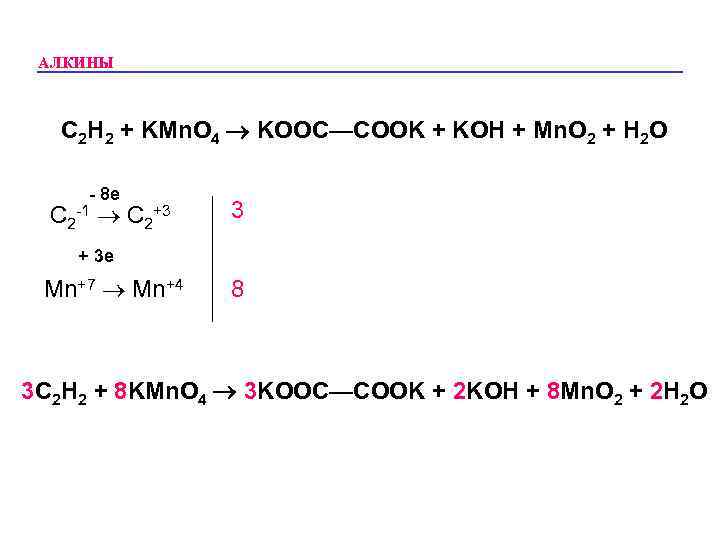 АЛКИНЫ C 2 H 2 + KMn. O 4 KOOC—COOK + KOH + Mn. O 2 + H 2 O - 8 e C 2+3 -1 3 + 3 e Mn+7 Mn+4 8 3 C 2 H 2 + 8 KMn. O 4 3 KOOC—COOK + 2 KOH + 8 Mn. O 2 + 2 H 2 O
АЛКИНЫ C 2 H 2 + KMn. O 4 KOOC—COOK + KOH + Mn. O 2 + H 2 O - 8 e C 2+3 -1 3 + 3 e Mn+7 Mn+4 8 3 C 2 H 2 + 8 KMn. O 4 3 KOOC—COOK + 2 KOH + 8 Mn. O 2 + 2 H 2 O
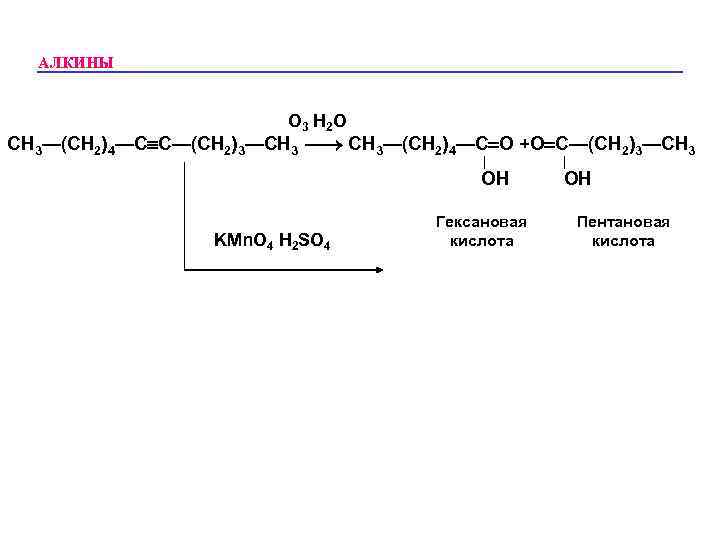 АЛКИНЫ O 3 H 2 O CH 3—(CH 2)4—C C—(CH 2)3—CH 3 — CH 3—(CH 2)4—C O +O C—(CH 2)3—CH 3 OH KMn. O 4 H 2 SO 4 Гексановая кислота OH Пентановая кислота
АЛКИНЫ O 3 H 2 O CH 3—(CH 2)4—C C—(CH 2)3—CH 3 — CH 3—(CH 2)4—C O +O C—(CH 2)3—CH 3 OH KMn. O 4 H 2 SO 4 Гексановая кислота OH Пентановая кислота
 ВАЖНОЕ ЗАМЕЧАНИЕ В задачах на экзаменах – KMn. O 4 и K 2 Cr 2 O 7 (K 2 Cr. O 4). В кислой среде: KMn. O 4 K+, Mn 2+, H 2 O K 2 Cr 2 O 7 K+, Cr 3+, H 2 O В нейтральной среде: KMn. O 4 K+, Mn. O 2, H 2 O K 2 Cr 2 O 7 (K 2 Cr. O 4) K 2 CO 3, Cr(OH)3, H 2 O В щелочной среде: KMn. O 4 K+, K 2 Mn. O 4, H 2 O K 2 Cr 2 O 7 (K 2 Cr. O 4) K[Cr(OH)4], H 2 O
ВАЖНОЕ ЗАМЕЧАНИЕ В задачах на экзаменах – KMn. O 4 и K 2 Cr 2 O 7 (K 2 Cr. O 4). В кислой среде: KMn. O 4 K+, Mn 2+, H 2 O K 2 Cr 2 O 7 K+, Cr 3+, H 2 O В нейтральной среде: KMn. O 4 K+, Mn. O 2, H 2 O K 2 Cr 2 O 7 (K 2 Cr. O 4) K 2 CO 3, Cr(OH)3, H 2 O В щелочной среде: KMn. O 4 K+, K 2 Mn. O 4, H 2 O K 2 Cr 2 O 7 (K 2 Cr. O 4) K[Cr(OH)4], H 2 O
 ЗАДАЧА Районная олимпиада по химии 1997
ЗАДАЧА Районная олимпиада по химии 1997
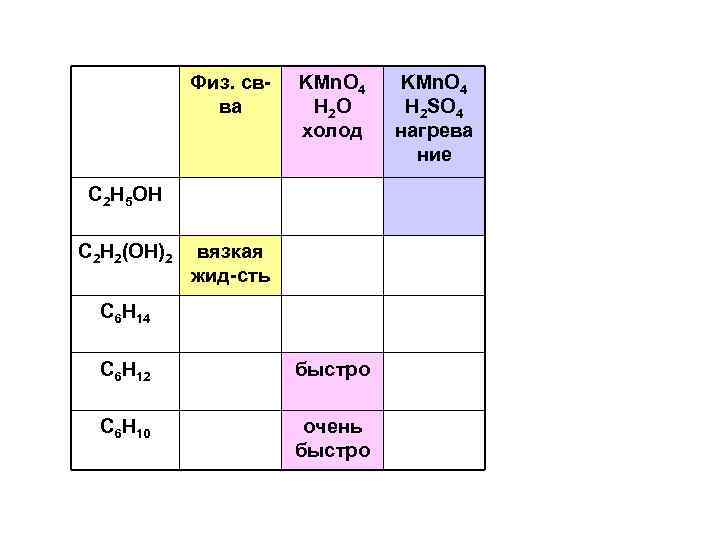 Физ. свва KMn. O 4 H 2 O холод C 2 H 5 OH C 2 H 2(OH)2 вязкая жид-сть C 6 H 14 C 6 H 12 быстро C 6 H 10 очень быстро KMn. O 4 H 2 SO 4 нагрева ние
Физ. свва KMn. O 4 H 2 O холод C 2 H 5 OH C 2 H 2(OH)2 вязкая жид-сть C 6 H 14 C 6 H 12 быстро C 6 H 10 очень быстро KMn. O 4 H 2 SO 4 нагрева ние
 АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ • Бензол устойчив к действию окислителей, однако каталитическое окисление кислородом в присутствии V 2 O 5 приводит к малеиновому ангидриду. • Гомологи в мягких условиях окисляются до бензойных кислот. • Поликонденсированные ароматические углеводороды при окислении теряют один цикл, модифицируясь в дикарбоновые кислоты или дикетоны.
АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ • Бензол устойчив к действию окислителей, однако каталитическое окисление кислородом в присутствии V 2 O 5 приводит к малеиновому ангидриду. • Гомологи в мягких условиях окисляются до бензойных кислот. • Поликонденсированные ароматические углеводороды при окислении теряют один цикл, модифицируясь в дикарбоновые кислоты или дикетоны.
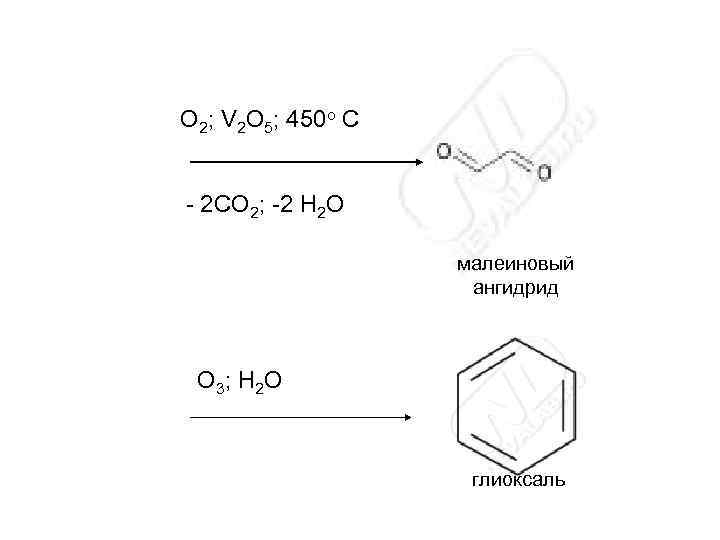 O 2; V 2 O 5; 450 o C - 2 CO 2; -2 H 2 O малеиновый ангидрид O 3; H 2 O глиоксаль
O 2; V 2 O 5; 450 o C - 2 CO 2; -2 H 2 O малеиновый ангидрид O 3; H 2 O глиоксаль
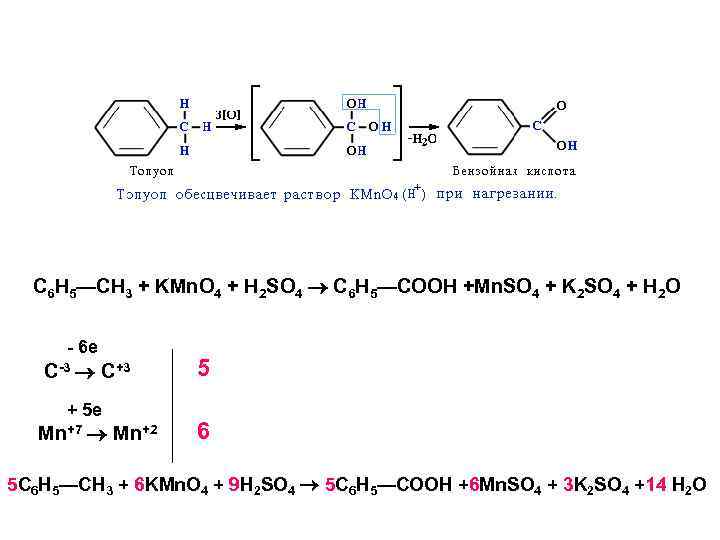 C 6 H 5—CH 3 + KMn. O 4 + H 2 SO 4 C 6 H 5—COOH +Mn. SO 4 + K 2 SO 4 + H 2 O - 6 e C-3 C+3 + 5 e Mn+7 Mn+2 5 6 5 C 6 H 5—CH 3 + 6 KMn. O 4 + 9 H 2 SO 4 5 C 6 H 5—COOH +6 Mn. SO 4 + 3 K 2 SO 4 +14 H 2 O
C 6 H 5—CH 3 + KMn. O 4 + H 2 SO 4 C 6 H 5—COOH +Mn. SO 4 + K 2 SO 4 + H 2 O - 6 e C-3 C+3 + 5 e Mn+7 Mn+2 5 6 5 C 6 H 5—CH 3 + 6 KMn. O 4 + 9 H 2 SO 4 5 C 6 H 5—COOH +6 Mn. SO 4 + 3 K 2 SO 4 +14 H 2 O
 МЕТОД ЭЛЕКТРОННО-ИОННОГО БАЛАНСА ! Задача из варианта вступительного экзамена на биологический факультет МГУ
МЕТОД ЭЛЕКТРОННО-ИОННОГО БАЛАНСА ! Задача из варианта вступительного экзамена на биологический факультет МГУ
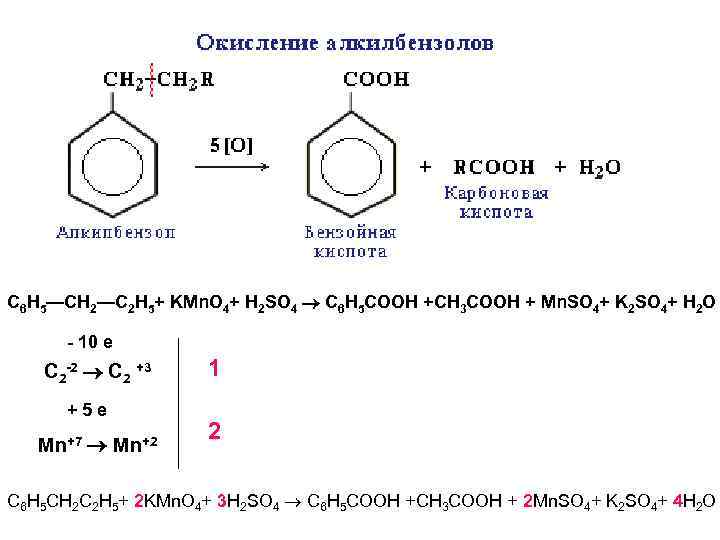 C 6 H 5—CH 2—C 2 H 5+ KMn. O 4+ H 2 SO 4 C 6 H 5 COOH +CH 3 COOH + Mn. SO 4+ K 2 SO 4+ H 2 O - 10 e C 2 -2 C 2 +3 +5 e Mn+7 Mn+2 1 2 C 6 H 5 CH 2 C 2 H 5+ 2 KMn. O 4+ 3 H 2 SO 4 C 6 H 5 COOH +CH 3 COOH + 2 Mn. SO 4+ K 2 SO 4+ 4 H 2 O
C 6 H 5—CH 2—C 2 H 5+ KMn. O 4+ H 2 SO 4 C 6 H 5 COOH +CH 3 COOH + Mn. SO 4+ K 2 SO 4+ H 2 O - 10 e C 2 -2 C 2 +3 +5 e Mn+7 Mn+2 1 2 C 6 H 5 CH 2 C 2 H 5+ 2 KMn. O 4+ 3 H 2 SO 4 C 6 H 5 COOH +CH 3 COOH + 2 Mn. SO 4+ K 2 SO 4+ 4 H 2 O
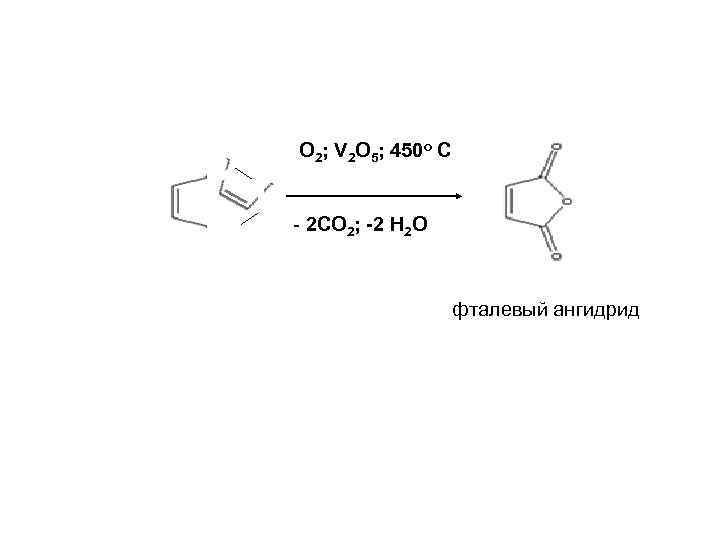 O 2; V 2 O 5; 450 o C - 2 CO 2; -2 H 2 O фталевый ангидрид
O 2; V 2 O 5; 450 o C - 2 CO 2; -2 H 2 O фталевый ангидрид
 ЗАДАЧА Задача из варианта вступительного экзамена на химический факультет МГУ
ЗАДАЧА Задача из варианта вступительного экзамена на химический факультет МГУ
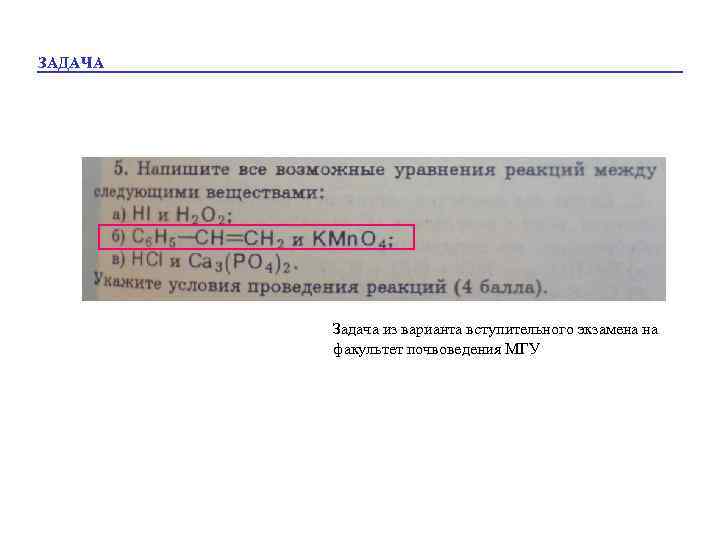 ЗАДАЧА Задача из варианта вступительного экзамена на факультет почвоведения МГУ
ЗАДАЧА Задача из варианта вступительного экзамена на факультет почвоведения МГУ
 ЗАДАЧА Задача из варианта вступительного экзамена на химический факультет МГУ
ЗАДАЧА Задача из варианта вступительного экзамена на химический факультет МГУ
 ЗАДАЧА Задача из варианта вступительного экзамена на биологический факультет МГУ
ЗАДАЧА Задача из варианта вступительного экзамена на биологический факультет МГУ
 ЗАДАЧА * ** Задача из варианта вступительного экзамена на химический факультет МГУ
ЗАДАЧА * ** Задача из варианта вступительного экзамена на химический факультет МГУ
 СПИРТЫ И ПРОСТЫЕ ЭФИРЫ • Конечными продуктами окисления первичных спиртов являются карбоновые кислоты. • Вторичные спирты при окислении дают кетоны. • Третичные спирты устойчивы к окислению, но в жестких условиях подвергаются деструкции. • Простые эфиры при окислении дают гидроперекиси.
СПИРТЫ И ПРОСТЫЕ ЭФИРЫ • Конечными продуктами окисления первичных спиртов являются карбоновые кислоты. • Вторичные спирты при окислении дают кетоны. • Третичные спирты устойчивы к окислению, но в жестких условиях подвергаются деструкции. • Простые эфиры при окислении дают гидроперекиси.
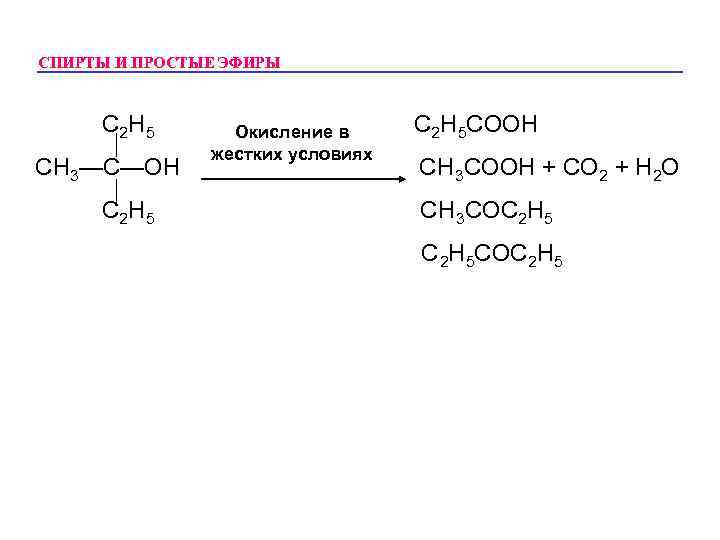 СПИРТЫ И ПРОСТЫЕ ЭФИРЫ С 2 H 5 CH 3—C—OH C 2 H 5 Окисление в жестких условиях C 2 H 5 COOH CH 3 COOH + CO 2 + H 2 O CH 3 COC 2 H 5 COC 2 H 5
СПИРТЫ И ПРОСТЫЕ ЭФИРЫ С 2 H 5 CH 3—C—OH C 2 H 5 Окисление в жестких условиях C 2 H 5 COOH CH 3 COOH + CO 2 + H 2 O CH 3 COC 2 H 5 COC 2 H 5
![ПРОСТЫЕ ЭФИРЫ [O] CH 3—CH 2—O—CH 2—CH 3—CH 2—O—CH—CH 3 O—OH гидроперекиси ПРОСТЫЕ ЭФИРЫ [O] CH 3—CH 2—O—CH 2—CH 3—CH 2—O—CH—CH 3 O—OH гидроперекиси](https://present5.com/presentation/3/34379216_100920524.pdf-img/34379216_100920524.pdf-40.jpg) ПРОСТЫЕ ЭФИРЫ [O] CH 3—CH 2—O—CH 2—CH 3—CH 2—O—CH—CH 3 O—OH гидроперекиси
ПРОСТЫЕ ЭФИРЫ [O] CH 3—CH 2—O—CH 2—CH 3—CH 2—O—CH—CH 3 O—OH гидроперекиси
 АЛЬДЕГИДЫ И КЕТОНЫ • Продуктами окисления всех альдегидов, кроме формальдегида, являются карбоновые кислоты. • Кетоны окисляются труднее, превращаясь в конечном итоге в CO 2. CH 2 O + KMn. O 4 K 2 CO 3+ KHCO 3 +Mn. O 2 + H 2 O - 4 e C 0 C+4 3 + 3 e Mn+7 Mn+4 4 3 CH 2 O + 4 KMn. O 4 K 2 CO 3+ 2 KHCO 3 +4 Mn. O 2 +2 H 2 O
АЛЬДЕГИДЫ И КЕТОНЫ • Продуктами окисления всех альдегидов, кроме формальдегида, являются карбоновые кислоты. • Кетоны окисляются труднее, превращаясь в конечном итоге в CO 2. CH 2 O + KMn. O 4 K 2 CO 3+ KHCO 3 +Mn. O 2 + H 2 O - 4 e C 0 C+4 3 + 3 e Mn+7 Mn+4 4 3 CH 2 O + 4 KMn. O 4 K 2 CO 3+ 2 KHCO 3 +4 Mn. O 2 +2 H 2 O
![АЛЬДЕГИДЫ И КЕТОНЫ CH 3 CHO + [Ag(NH 3)2]OH CH 3 COONH 4 + АЛЬДЕГИДЫ И КЕТОНЫ CH 3 CHO + [Ag(NH 3)2]OH CH 3 COONH 4 +](https://present5.com/presentation/3/34379216_100920524.pdf-img/34379216_100920524.pdf-42.jpg) АЛЬДЕГИДЫ И КЕТОНЫ CH 3 CHO + [Ag(NH 3)2]OH CH 3 COONH 4 + Ag + NH 3·H 2 O+NH 3 - 2 e C+1 C+3 + 1 e Ag+1 Ag 0 1 2 CH 3 CHO + 2[Ag(NH 3)2]OH CH 3 COONH 4+2 Ag+NH 3·H 2 O+2 NH 3
АЛЬДЕГИДЫ И КЕТОНЫ CH 3 CHO + [Ag(NH 3)2]OH CH 3 COONH 4 + Ag + NH 3·H 2 O+NH 3 - 2 e C+1 C+3 + 1 e Ag+1 Ag 0 1 2 CH 3 CHO + 2[Ag(NH 3)2]OH CH 3 COONH 4+2 Ag+NH 3·H 2 O+2 NH 3
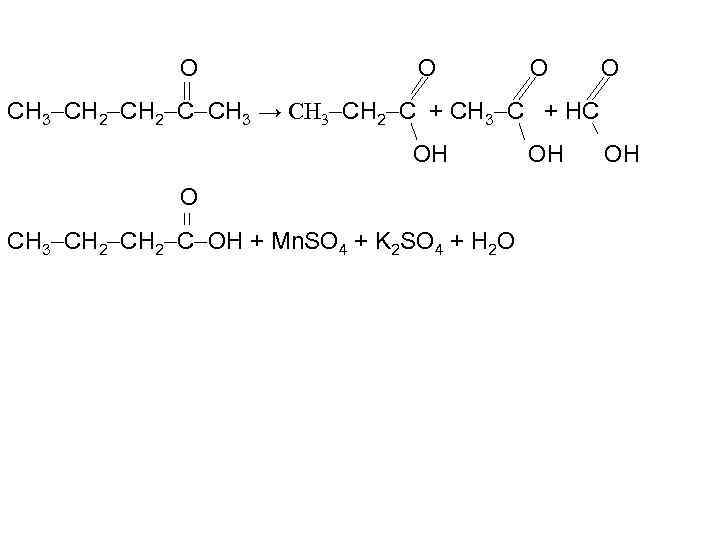 O O CH 3 CH 2 C CH 3 → CH 3 CH 2 C + CH 3 C + HC OH O CH 3 CH 2 C OH + Mn. SO 4 + K 2 SO 4 + H 2 O OH OH
O O CH 3 CH 2 C CH 3 → CH 3 CH 2 C + CH 3 C + HC OH O CH 3 CH 2 C OH + Mn. SO 4 + K 2 SO 4 + H 2 O OH OH
 КАРБОНОВЫЕ КИСЛОТЫ • Из всех карбоновых кислот только муравьиная окисляется в мягких условиях перманганатом калия. • Под действием H 2 O 2 карбоновые кислоты превращаются в β-оксикислоты.
КАРБОНОВЫЕ КИСЛОТЫ • Из всех карбоновых кислот только муравьиная окисляется в мягких условиях перманганатом калия. • Под действием H 2 O 2 карбоновые кислоты превращаются в β-оксикислоты.
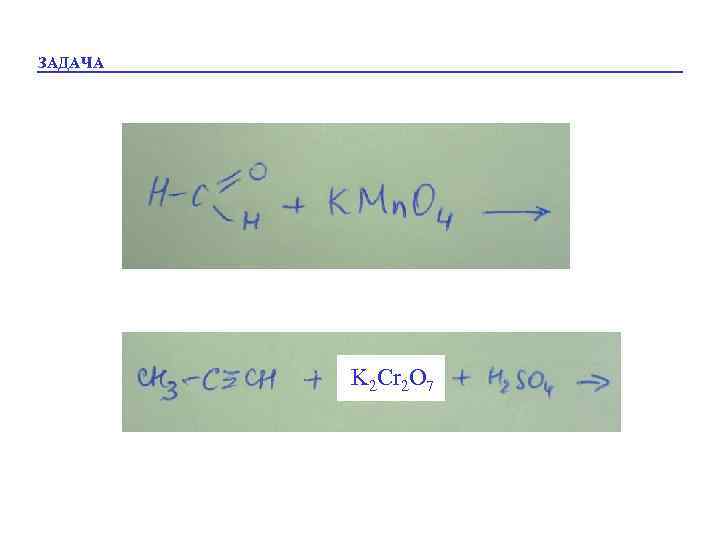 ЗАДАЧА K 2 Cr 2 O 7
ЗАДАЧА K 2 Cr 2 O 7
 МЫ РАССМОТРЕЛИ Окисление различных классов органических соединений Примеры заданий
МЫ РАССМОТРЕЛИ Окисление различных классов органических соединений Примеры заданий


