6.Окисление.ppt
- Количество слайдов: 53

Окисление Лекция 6

Продукты Спирты ¡ Карбонильные соединения (альдегиды и кетоны) ¡ Карбоновые кислоты ¡ Масштаб используемых количеств окисляемых субстратов – граммы (дорогие хиральные продукты)

Окисление спиртов

Химические способы окисления спиртов Окислители – KMn. O 4, K 2 Cr 2 O 7+H 2 SO 4, Cu. O, O 2+катализатор. Легкость окисления спиртов уменьшается в ряду: первичные ≥ вторичные >> третичные. Первичные спирты при окислении образуют альдегиды, которые затем легко окисляются до карбоновых кислот.

При окислении вторичных спиртов образуются кетоны:

Третичные спирты более устойчивы к действию окислителей. Они окисляются только в жестких условиях (кислая среда, повышенная температура), что приводит к разрушению углеродного скелета молекулы и образованию смеси продуктов (карбоновых кислот и кетонов с меньшей молекулярной массой).

Алкогольдегидрогеназа (Алкоголь: НАД-оксидоредуктаза 1. 1) ¡ ¡ ¡ фермент класса дегидрогеназ, катализирующий окисление спиртов и ацеталей до альдегидов и кетонов в присутствии никотинамидадениндинуклеотида (НАД). Алкогольдегидрогеназы (алкоголь. НАД+оксидоредуктазы) являются димерами, состоящими из субъединиц с молекулярным весом около 40000 и содержащими ион цинка Zn 2+. ингибируется хелатами и солями Ag+, Hg 2+ и Cu 2+.

Structure of horse liver alcohol dehydrogenase complexed with substrates (Ramaswamy et al. , 1994)

Основная проблема процесса Регенерация кофермента (НАД+) Решается добавлением каталитических количеств рибофлавинфосфата, которыфй окисляет НАДН до НАД+ , восстановленая форма флавина окисляется кислородом воздуха

Окисление диола, сопряженное с регенерацией НАД+ в реакции получения L- альфа- аминоадипиновой кислоты из альфа – оксоадипиновой кислоты

Разделение рацематов лучше всего идет в случае циклицеских спиртов

Энантиоселективность процесса окисления зависит даже от малых структурных различий

Хорошие показатели энантиоселективности при окислении и у рацематов бициклицеских спиртов

Окисление прохиральных диолов

Интересные с препаративной точки зрения реакции

Получение феромона (+) - грандизола с использованием предшественика, полученного биокаталитическим способом

Получение из диолов соответствующих карбоновых кислот (фермент алкогольдегидрогеназа)
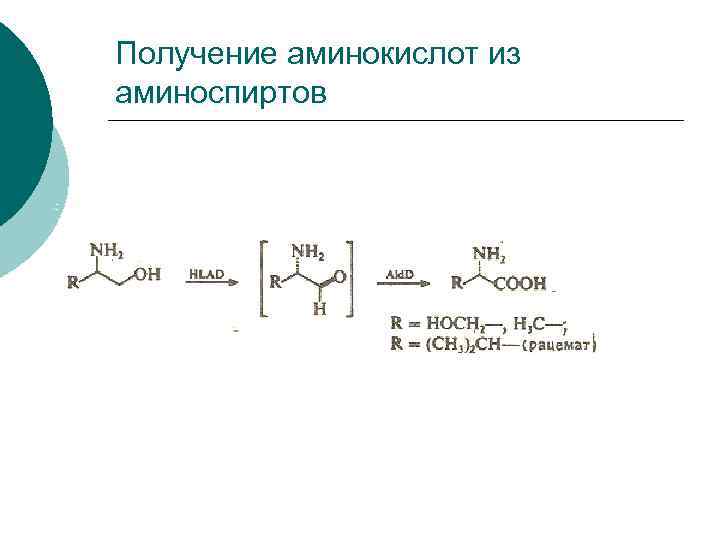
Получение аминокислот из аминоспиртов

Получение L-ксилозы из ксилита галактозооксидаза

Химическое окисление метионина

Окисление аминопроизводных в карбонильные соединения

Разделение рацематов аминокислот При использовании оксидазы L- аминокислот в реакцию не вступает D-аминокислота и наоборот

Проблема При регенерации ФАД кислородом воздуха необходимо внесение в систему катализатора разложения перекиси водорода, в противном случае альфа-оксикислота окисляется с отщеплением СО 2 и сокращением цепи на один атом

Данное явление используется в химии цефаспоринов и катализируется живыми клетками бактерий

Диаминоксидаза из почек свиньи или молодых ростках гороха окисляет одну группу СН 2 -Н 2 в диамине до альдегидной. Продукты реакции могут быть использованы в синтезе алкалоидов
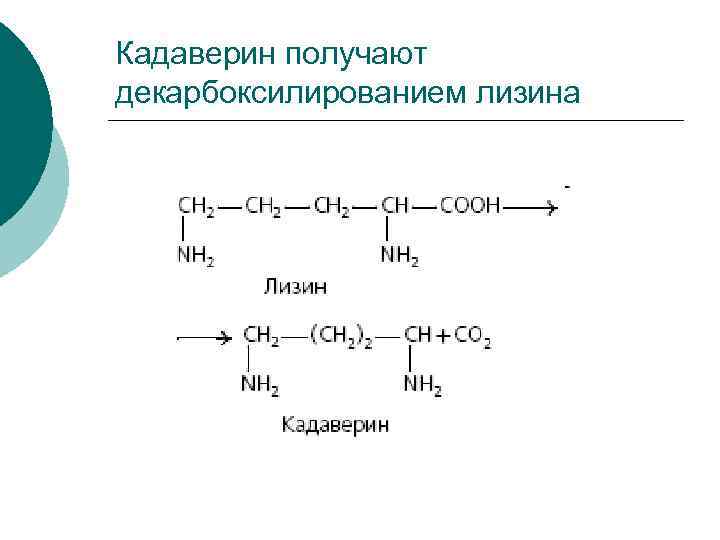
Кадаверин получают декарбоксилированием лизина

Гидроксилирование

Ферменты пероксидазы позволяют проводитьокисление в мягких условиях. Важным аспектом является региоспецифичность ферментативных реакций.
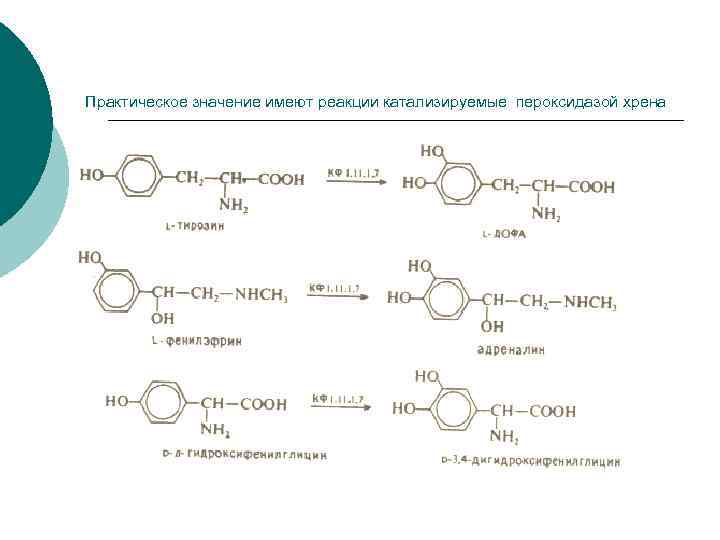
Практическое значение имеют реакции катализируемые пероксидазой хрена

L-ДОФА или Леводопа (Levodopa) ИЮПАК 3 -гидрокси-L-тирозин показания к применению – болезнь Паркинсона CAS 59 -92 -7

Микробиологическое окисление терпенов с получением диолов

Энантиоселективное гидроксилирование бициклогептанового скелета

Окисление боковой цепи в ароматическом углеводороде

Микробиологическое гидроксилирование стероидов (промышленно значимый процесс)

В холевой кислоте можно региоспецифично окислять первую, вторую или третью СНОН группы

Гидроксилирование в экологической биотехнологии

Окисление азотсодержащих гетероциклических соединений

Азотсодержащие гетероциклы можно окислять с помощью ксантиноксидазы (ксантиноксидоредуктазы) КФ 1. 17. 3. 2 (содержится в коровьем молоке) Окисление петридинов-4 замещенных в положение 7 Получение биокатализатора: Фермент можно иммобилизовать на желатине или высушив лиофильно белок коровьего молока

Аналогичные реакции катализируются альдегидоксидазой из печени кролика (кф 1. 2. 1. 5)

Дегидрирование связи СН-СН

Классическая реакция - дегидрирование гидрокортизона с образованием преднизола. Катализатор – высушенные или иммобилизованные клетки Arthrobacter simplex либо реакция ведется в двухфазной системе растворителей
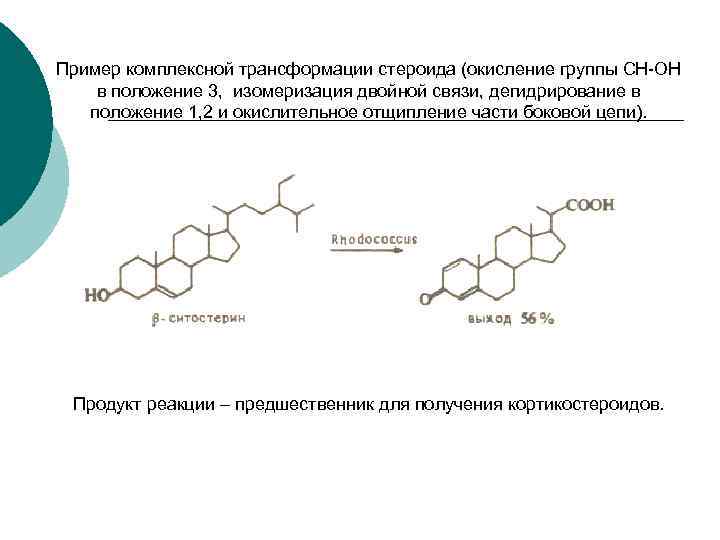
Пример комплексной трансформации стероида (окисление группы СН-ОН в положение 3, изомеризация двойной связи, дегидрирование в положение 1, 2 и окислительное отщипление части боковой цепи). Продукт реакции – предшественник для получения кортикостероидов.

Кортикостероиды (антистрессовое, противошоковое, иммунорегулирующее, противовоспалительное и противоаллергическое действие) ¡ подкласс стероидных гормонов, производимых исключительно корой надпочечников, но не половыми железами, и не обладающих ни эстрогенной, ни андрогенной, ни гестагенной активностью, но обладающих в той или иной степени либо глюкокортикоидной, либо минералокортикоидной активностью.

Окисление азотсодержащих гетероциклических сединений

Некоторые монооксигеназы катализируют и окисление гетероатомов, например хлорпероксидаза катализирует окисление аминогруппы до нитрозо- и даже нитрогруппы

Получение оптически активных сульфоксидов

Микробиологическое окисление сульфидов до сульфоксидов
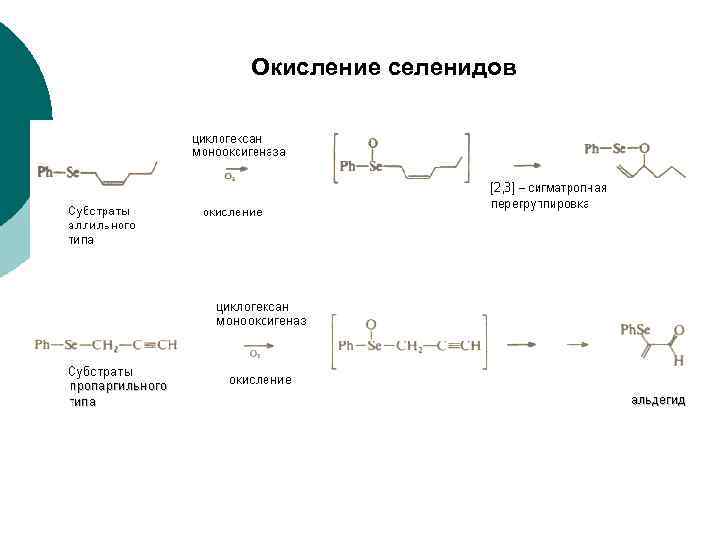
Окисление селенидов

Неспецифическое окисление

Ферменты лигнинпероксидазного комплекса лигнинпероксидаза или лигниназа; ¡ - Мn+2 -зависимая пероксидаза; ¡ - фенолокисляющие ферменты − фенолоксидаза, монооксигеназа и диоксигеназа; ¡ ферменты, генерирующие перекись водорода. ¡ 50

Пероксидазы как активная фармакологическая субстанция Появление на косметическом рынке нового депигментирующего агента — фермента лигнинперкосидазы (лигназы) — эксперты оценивают как прорыв в области разработки депигментирующих препаратов. Обнаруженный в 1984 году у дереворазрушающих грибов, этот фермент разрушает лигнин — полимерное вещество полифенольной природы, откладывающийся в оболочках растительных клеток, вызывающий их одревесение и повышающий прочность. Лигнинпероксидазу используют в бумажной промышленности с целью осветления древесной пульпы, идущей на производство бумаги. Недавно было обнаружено, что этот фермент способен разрушать эумеланин, который структурно близок к лигнину. Этот факт навел специалистов израильской компании Rakuto Bio Technologies Ltd. на мысль использовать лигнинпероксидазу в качестве депигментирующего агента, ликвидирующего уже сформированный пигмент и не влияющего на процесс меланогенеза как такового. Способ получения лигнинпероксидазы c помощью грибов Phanerochaete chrysosporium был запатентован (U. S. Patent and Trademark Office Patent Application 20060051305), а готовая к включению в косметическую рецептуру субстанция получила торговое название Melanozyme. 51

В настоящее время вследствие патентных ограничений Melanozyme используется только в одном косметическом бренде — ELURE, принадлежащем компании Syneron (Израиль).

Спасибо за внимание!
6.Окисление.ppt