 ОКИСЛЕНИЕ КРЕМНИЯ
ОКИСЛЕНИЕ КРЕМНИЯ
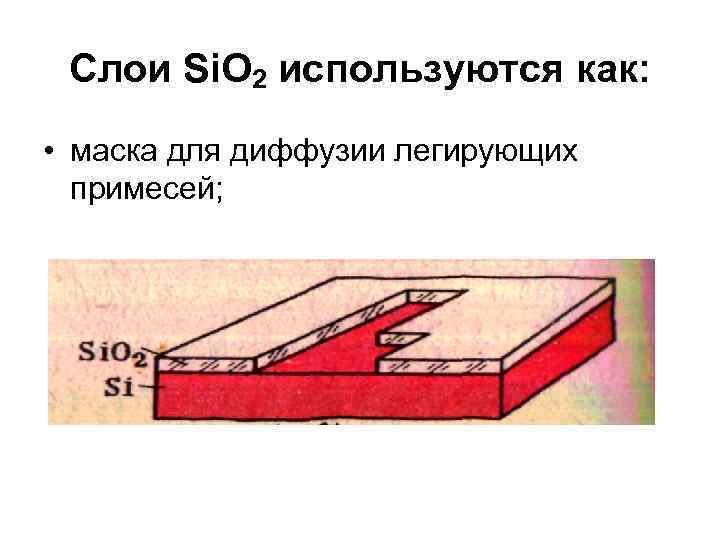 Слои Si. O 2 используются как: • маска для диффузии легирующих примесей;
Слои Si. O 2 используются как: • маска для диффузии легирующих примесей;
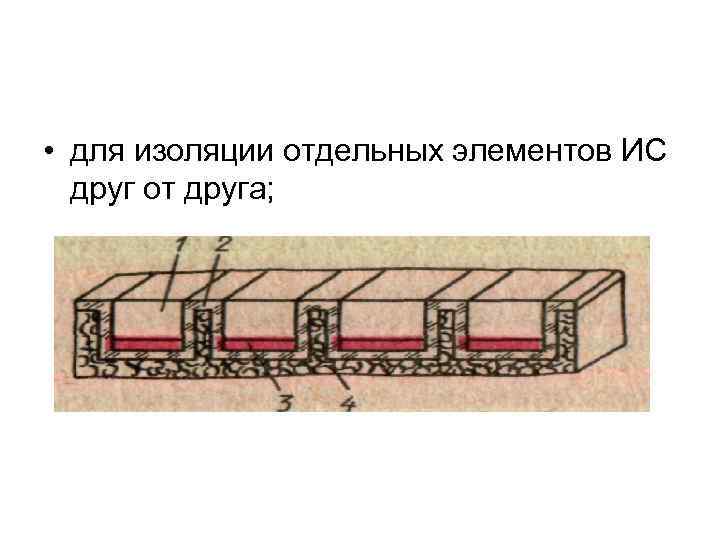 • для изоляции отдельных элементов ИС друг от друга;
• для изоляции отдельных элементов ИС друг от друга;
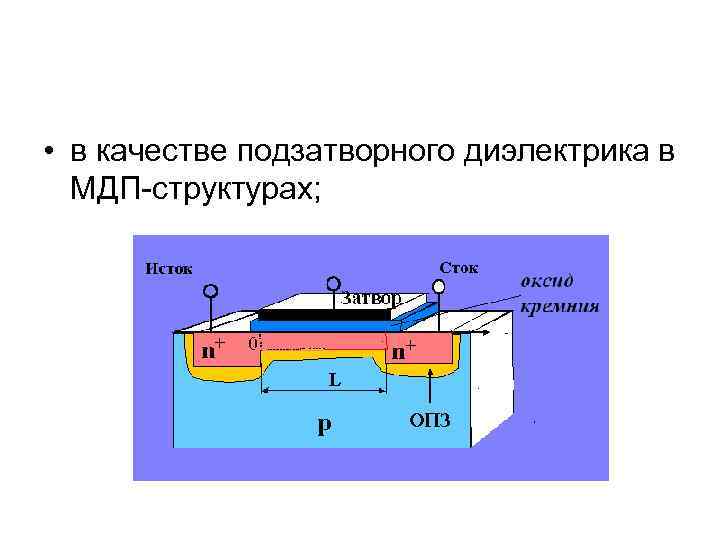 • в качестве подзатворного диэлектрика в МДП-структурах;
• в качестве подзатворного диэлектрика в МДП-структурах;
 СПОСОБЫ ПОЛУЧЕНИЯ ОКСИДА КРЕМНИЯ: • термическое окисление; • анодное окисление; • плазмохимическое окисление.
СПОСОБЫ ПОЛУЧЕНИЯ ОКСИДА КРЕМНИЯ: • термическое окисление; • анодное окисление; • плазмохимическое окисление.
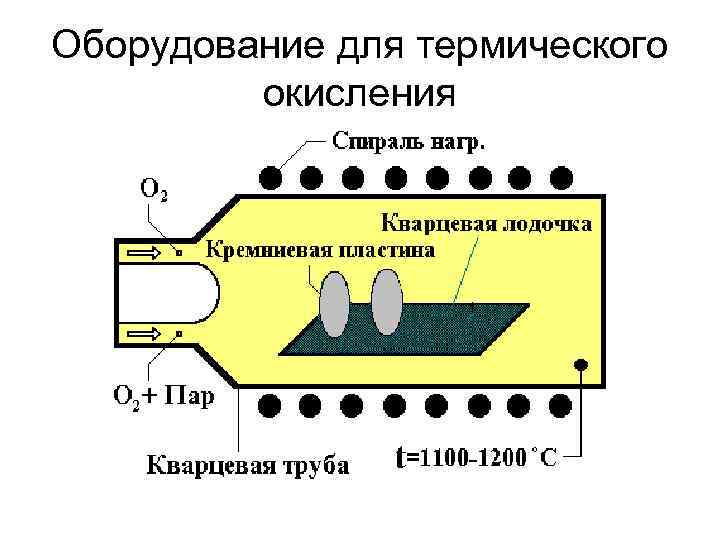 Оборудование для термического окисления
Оборудование для термического окисления
 Химическая реакция • окисление в атмосфере сухого кислорода (сухое окисление): Siтв. + O 2 = Si. O 2; • окисление в парах воды (влажное окисление): Siтв. +2 H 2 O = Si. O 2 + 2 H 2; • Время окисления в стандартных технологических процессах составляет 4 - 5 часов
Химическая реакция • окисление в атмосфере сухого кислорода (сухое окисление): Siтв. + O 2 = Si. O 2; • окисление в парах воды (влажное окисление): Siтв. +2 H 2 O = Si. O 2 + 2 H 2; • Время окисления в стандартных технологических процессах составляет 4 - 5 часов
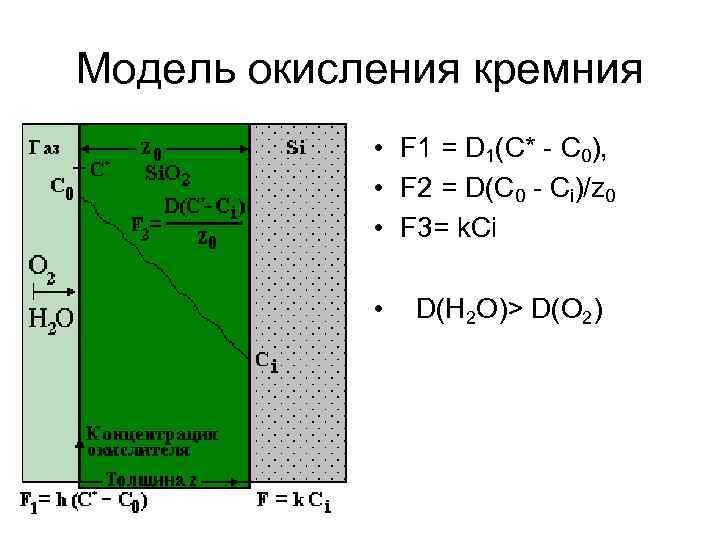 Модель окисления кремния • F 1 = D 1(C* - C 0), • F 2 = D(C 0 - Ci)/z 0 • F 3= k. Ci • D(H 2 O)> D(O 2)
Модель окисления кремния • F 1 = D 1(C* - C 0), • F 2 = D(C 0 - Ci)/z 0 • F 3= k. Ci • D(H 2 O)> D(O 2)
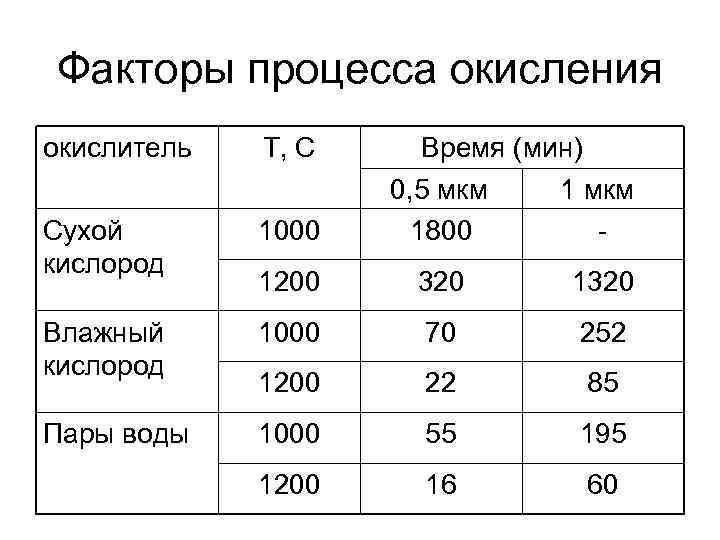 Факторы процесса окисления окислитель T, C Время (мин) 0, 5 мкм 1800 - Сухой кислород 1000 1200 320 1320 Влажный кислород 1000 70 252 1200 22 85 Пары воды 1000 55 195 1200 16 60
Факторы процесса окисления окислитель T, C Время (мин) 0, 5 мкм 1800 - Сухой кислород 1000 1200 320 1320 Влажный кислород 1000 70 252 1200 22 85 Пары воды 1000 55 195 1200 16 60
 Качество оксидных пленок • Сухой кислород (пленки более плотные, лучше сцепление с поверхностью, меньше скорость роста) • Пары воды ( более пористые, высокая скорость роста) • Комбинированный способ получения Сухой кислород - Влажный кислород - Сухой кислород
Качество оксидных пленок • Сухой кислород (пленки более плотные, лучше сцепление с поверхностью, меньше скорость роста) • Пары воды ( более пористые, высокая скорость роста) • Комбинированный способ получения Сухой кислород - Влажный кислород - Сухой кислород
 • Значительным достижением в совершенствовании технологии окисления кремния явилось добавление в окислительную среду в процессе окисления хлорсодержащих компонентов. Получают боле плотные качественные пленки, увеличивается скорость роста пленки.
• Значительным достижением в совершенствовании технологии окисления кремния явилось добавление в окислительную среду в процессе окисления хлорсодержащих компонентов. Получают боле плотные качественные пленки, увеличивается скорость роста пленки.
 • Рис. 1. 3 D-топография поверхности кремния с локальной пленкой оксида кремния.
• Рис. 1. 3 D-топография поверхности кремния с локальной пленкой оксида кремния.
 • изображение ямок травления оксидов
• изображение ямок травления оксидов
 Нитрид кремния • Si 3 N 4 используют для пассивирования поверхности полупроводниковых приборов (предохраняет от диффузии воды и ионов натрия, маска при локальном окислении кремния). • Химическое осаждение: при атмосферном давлении и температуре 700 - 900 °C 3 Si. H 4 + 4 NH 3 → Si 3 N 4 +12 H 2
Нитрид кремния • Si 3 N 4 используют для пассивирования поверхности полупроводниковых приборов (предохраняет от диффузии воды и ионов натрия, маска при локальном окислении кремния). • Химическое осаждение: при атмосферном давлении и температуре 700 - 900 °C 3 Si. H 4 + 4 NH 3 → Si 3 N 4 +12 H 2