f42ca708aea0cba81b3e73d91e6c69e6.ppt
- Количество слайдов: 26

OИсследование биоэквивалентности прерарата Стазекс (клопидогрель 75 мг), производства компании «Джи-Эм-Пи» , Грузия
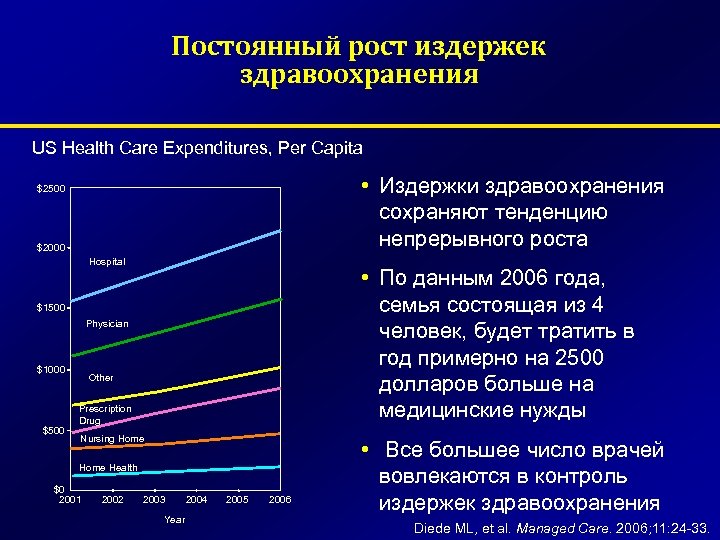
Постоянный рост издержек здравоохранения US Health Care Expenditures, Per Capita • Издержки здравоохранения сохраняют тенденцию непрерывного роста $2500 $2000 Hospital • По данным 2006 года, семья состоящая из 4 человек, будет тратить в год примерно на 2500 долларов больше на медицинские нужды $1500 Physician $1000 $500 Other Prescription Drug Nursing Home Health $0 2001 2002 2003 Year 2004 2005 2006 • Все большее число врачей вовлекаются в контроль издержек здравоохранения Diede ML, et al. Managed Care. 2006; 11: 24 -33.

Нужны ли генерические препараты? Доля генерических лекарственныч средств на фармацевтическом рынке: США - 25% , ГЕРМАНИЯ - 35%, ВЕЛИКОБРИТАНИЯ - 55%, ВЕНГРИЯ - 55%, ПОЛБША - 61%, СЛОВАКИЯ - 66%. РОССИЯ - 78% Общеизвестно, что исследование биоэквивалентности генерических препаратов является основным методом

Bioequivalence – Биоэквивалентность • Bioequivalence may be demonstrated through in vivo or in vitro test methods, comparative clinical trials, or pharmacodynamic studies • BБиоэквивалентность может быть продемонстрирована in vivo или in vitro методами изучения, сравнительными клиническими исследованиями или фармакодинамическими исследованиямию. Approved Drug Products With Therapeutic Equivalence Evaluations. 23 rd ed. 2003. FDA/CDER Web site. Available at: http: //www. fda. gov/cder/ob/docs/preface/ecpreface. htm#Therapeutic Equivalence. Related Terms. Accessed September 29, 2003.

Исследование биоэквивалентности с целью определения терапевтической эффективности • Существует четкая корреляция между фармакодинамикой одноразового приема препарата и его терапевтической эффективностью. • Фармакодинамика одноразового приема препарата не отличается от фармакодинамики при стабильном приеме лекарственного средства • Фармакокинетический профиль пациента полностью сопоставим с таковым у здорового добровольца • Разница в абсорбции – 20% + 25% (Cmax, AUC) не оказывает влияния на терапевтическую эффективность препарата Approved Drug Products With Therapeutic Equivalence Evaluations. 23 rd ed. 2003. FDA/CDER Web site. Available at: http: //www. fda. gov/cder/ob/docs/preface/ecpreface. htm#Therapeutic Equivalence-Related Terms. Accessed September 29, 2003. American Pharmaceutical Association. Substitution of Critical Dose Drugs: Issues, Analysis, and Decision Making. 2000. Available at: http: //www. pharmacist. com/pdf/critical_dose. pdf. Accessed October 7, 2003.

Pharmacokinetic Studies Healthy Volunteers Versus Patients – Фармакокинетические исследования – что предпочесть – здоровые добровольцы или пациенты • If 2 drug products perform the same in healthy volunteers, the assumption is made that they will perform the same in patients with the disease, except in the case of some drugs that are potentially toxic • Если 2 лекарственных средства одинаково действуют в случае здововых добровольцев, то можно утверждать, что их действие будет одинаковым и у пациентов (за исключением нескольких потенциально токсичных препаратов) Welage LS, et al. J Am Pharm Assoc. 2001; 41: 856 -867.
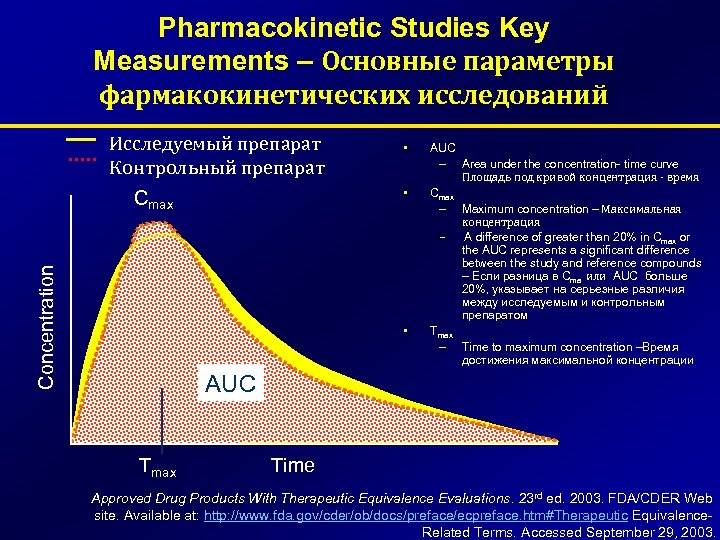
Pharmacokinetic Studies Key Measurements – Основные параметры фармакокинетических исследований Исследуемый препарат Контрольный препарат • Cmax Concentration • • AUC – Area under the concentration- time curve Площадь под кривой концентрация - время Cmax – Maximum concentration – Максимальная концентрация – A difference of greater than 20% in Cmax or the AUC represents a significant difference between the study and reference compounds – Если разница в Cma или AUC больше 20%, указывает на серьезные различия между исследуемым и контрольным препаратом Tmax – Time to maximum concentration –Время достижения максимальной концентрации AUC Tmax Time Approved Drug Products With Therapeutic Equivalence Evaluations. 23 rd ed. 2003. FDA/CDER Web site. Available at: http: //www. fda. gov/cder/ob/docs/preface/ecpreface. htm#Therapeutic Equivalence. Related Terms. Accessed September 29, 2003.

Этапы исследования биоэквивалентности 1. Клиническая часть 3. Статистическая часть 2. Лабораторная часть


Pharmacokinetic Reference Range FDA Requirements for Bioequivalence 125% 100% 80% Product A Bioequivalent Reference Drug Product B Not Bioequivalent • Product A is bioequivalent to the reference drug; its 90% confidence interval of the AUC falls within 80% to 125% of the reference drug • Product B is not bioequivalent to the reference drug; its 90% confidence interval of the AUC falls outside of 80% to 125% of the reference drug Approved Drug Products With Therapeutic Equivalence Evaluations. 23 rd ed. 2003. FDA/CDER Web site. Available at: http: //www. fda. gov/cder/ob/docs/preface/ecpreface. htm#Therapeutic Equivalence. Related Terms. Accessed September 29, 2003.

Подбор здоровых добровольцев • Письменное согласие на участие в исследовании • Карта страхования пациента • Полный физикальный осмотр • ЭКГ • Лабораторное исследование

Лабораторное исследование Перечень лабораторных анализов: Гематология гемоглобин гематокрит лейкоцитарная формула эритроциты тромбоциты СОЭ Электрокардиограмма* Биохимический анализ крови* BUN - с фракциями билирубина Креатинин Общий билирубин SGOT - АЛТ SGPT – АСТ LDH - ЛДГ натрий калий кальций фосфор глюкоза Анализ мочи* кислотность удельный вес белок глюкоза кетоны билирубин эритроциты нитриты уробилиноген микроскопическое исследование Анализ мочи на наркотики опияты Марихуана Бупренофрин Другие ВИЧ С и В гепатит RW. Тест на беременность повторяются по окончании исследования

Усредненный объем данных для лабораторного аналитза и статистической обработки количество проб , взятых у 1 добровольца за 1 период 13 Включая контрольную пробу - 26 количество проб , взятых у 1 добровольца за 2 периода 26 Включая контрольную пробу- 52 количество проб , взятых у 18 добровольцев за 2 периода 52 X 18 = 936

Процесс дозирования, взятия крови и подготовка исследуемого материала Основные принципы: Прием добровольцами исследуемого и контрольного препарата согласно списка рандомизации (двойное слепое исследование) Процесс взятия и подготовки должен быть максимально прослеживаемым, система маркироки должна обеспечивать возможность отследить пробу крови на каждом этапе исследования На подготовительном этапе производится. Замораживание биоматериала и егохранение для последующего аналитечского этапа.

Основные параметры Cmax : максимальная концентрация препарата в крови Cmin : минимальная концентрация препарата в крови Tmax : время до максимальной концентрации AUCt : площадь под кривой концентрация. время

• Точное определение концентрации лекарственного средства в крови, плазме или биологическом образце играет решающую роль в обработке и интерпретации исследований по биоэквивалентности

Методика анализа • Для количественного определения клопидогреля бисульфата в плазме крови был применен методвысоскоэффективной жидкой хроматографии на аппарате Agilent Technologies 1200 класса SL, (жидкостный хроматограф). Детекция производилась при помощи флюоресцентного детектора. M • Данные валидации биоаналитического метода • Процедура валидации аналитического метода подтвердила, что экстракция клоптдогреля из плязмы составила 86 -102%, а продуктивность рефкции колебалась в пределах 87 -90%-ов • Пределы валидации метода составили 10 -12, 000 pg/ml.

Хроматографический анализ • Проведение хроматографического анализа • Проверка чистоты пика в измерении 3 D • Перенесение результатов в таблицу статистической обработки

Проверка чистоты пика в измерении 3 DD

Результаты: • Данные на каждого добровольца сохранены в виде хроматограмм • Данные полученные в результате хроматографии переносятся в таблицу для статистической обработки
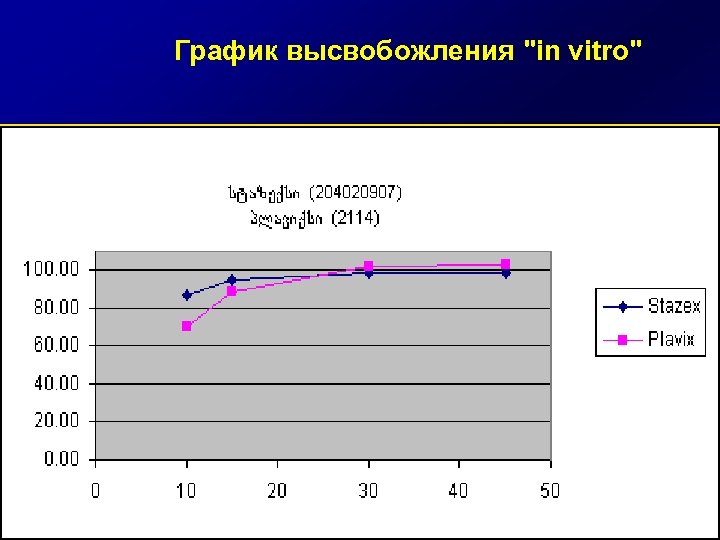
График высвобожления "in vitro"
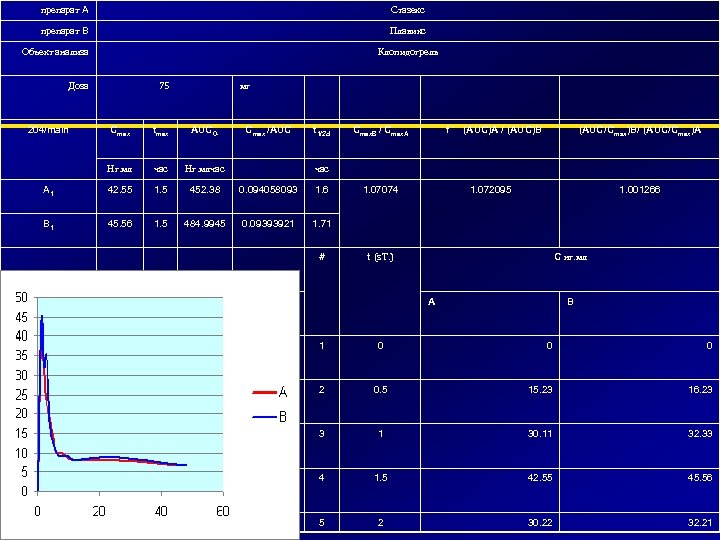
препарат A Стазекс препарат B Плавикс Объект анализа Клопидогрель 75 Доза 204/main мг Cmax tmax AUC 0 - Нг. мл час Нг. млчас A 1 42. 55 1. 5 B 1 45. 56 1. 5 Cmax /AUC t 1/2 el час 452. 38 0. 094058093 1. 6 484. 9945 0. 09393921 Cmax. B / Cmax. A (AUC/Cmax)B/ (AUC/Cmax)A 1. 71 # f ' (AUC)A / (AUC)B 1. 07074 1. 072095 1. 001266 t (s. T. ) C нг. мл A 1 0 2 B 0 0 0. 5 15. 23 16. 23 3 1 30. 11 32. 33 4 1. 5 42. 55 45. 56 5 2 30. 22 32. 21

Фармакокинетический анализ Cmax 1 – препарат А – 42. 55 нг/мл препарат В – 45. 56 нг/мл tmax 1 - препарат А – 1. 5 ч препарат В – 1. 5 ч AUC 0 -t (1) - препарат А – 452. 38 препарат В – 484. 9945 Cmax /AUC(1) – препарат А – 0. 09406 препарат В – 0. 0939

Сравнительный анализ основных фармакокинетических анализов Cmax. B / Cmax. A (1) – 1. 07 Cmax. B / Cmax. A (2) – 1. 04 Cmax. B / Cmax. A (3) – 0. 95 f ' (AUC)A / (AUC)B (1) – 1. 07 f ' (AUC)A / (AUC)B (2) – 1. 03 f ' (AUC)A / (AUC)B (3) – 1. 005 (AUC/Cmax)B/ (AUC/Cmax)A (1) – 1. 001 (AUC/Cmax)B/ (AUC/Cmax)A (2) – 0. 99 (AUC/Cmax)B/ (AUC/Cmax)A (3) – 1. 06 Данные подтверждают, что исследуемые препараты являются биоэквивалентными

Therapeutic Equivalents – Терапевтические эквиваленты • Лекарственные средства считаются терапевтическими эквивалентами, если они являются: – Фармацевтически эквивалентными – Биоэквивалентными – Безопасными и эффективными – Адекватно упакованы – Произведены согласно стандарту GMP • Терапевтические эквиваленты обладают тем же клиническим эффектом и профилем безопасности, что и оригиральный препарат. Approved Drug Products With Therapeutic Equivalence Evaluations. 23 rd ed. 2003. FDA/CDER Web site. Available at: http: //www. fda. gov/cder/ob/docs/preface/ecpreface. htm#Therapeutic Equivalence. Related Terms. Accessed September 29, 2003.

Благодарю за внимание
f42ca708aea0cba81b3e73d91e6c69e6.ppt