ОДНООСНОВНІ НЕНАСИЧЕНІ КАРБОНОВІ КИСЛОТИ можна розглядати як похідні

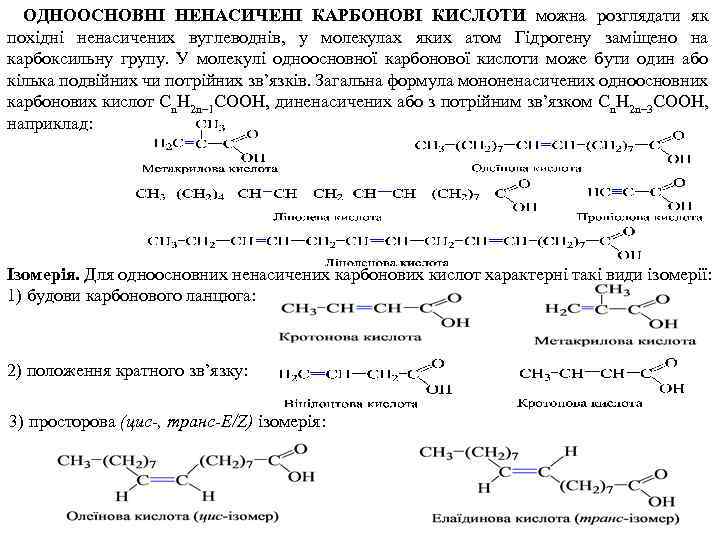
ОДНООСНОВНІ НЕНАСИЧЕНІ КАРБОНОВІ КИСЛОТИ можна розглядати як похідні ненасичених вуглеводнів, у молекулах яких атом Гідрогену заміщено на карбоксильну групу. У молекулі одноосновної карбонової кислоти може бути один або кілька подвійних чи потрійних зв’язків. Загальна формула мононенасичених одноосновних карбонових кислот Сn. Н 2 n– 1 COOH, диненасичених або з потрійним зв’язком Сn. Н 2 n– 3 COOH, наприклад: Ізомерія. Для одноосновних ненасичених карбонових кислот характерні такі види ізомерії: 1) будови карбонового ланцюга: 2) положення кратного зв’язку: 3) просторова (цис-, транс-E/Z) ізомерія:

Номенклатура. Для цих сполук широко вживані тривіальні назви (акрилова, кротонова кислоти). Номенклатура IUPAC складається згідно із загальними правилами. Нумерація починається з атома Карбону карбоксильної групи. Формула кислоти систематична назва тривіальна назва СН 2=СН–СООН СН 3–СН=СН–СООН СН 2=СН–СН 2–СООН СН 2=С(СН 3)–СООН СН 3–СН=СН–СООН Пропенова 2–Бутенова 3–Бутенова 2–Метил– 2–пропенова 2, 4 -Гексадієнова Акрилова Кротонова Вінілоцтова Метакрилова Сорбінова Способи одержання. 1. Реакції відщеплення: а) одержання з галогенокарбонових кислот дією спиртових розчинів лугів (особливо легко дегідрогалогенізуються α-галогенокарбонові кислоти): R–CH 2–CHCl–COOH + 2 Na. OH R–CH=CH–COONa + Na. Cl + H 2 O б) дегалогенування віцинальних дигалогенозаміщених карбонових кислот за допомогою цинкового пилу: R– CHCl–COOH + Zn R–CH=CH–COOH + Zn. Cl 2 2. Дегідратація β-гідроксикислот під час нагрівання: R–CH(OH)–CH 2–COOH R–CH=CH–COOH + H 2 O 3. Окиснення. Ненасичені монокарбонові кислоти утворюються в разі окиснення ненасичених спиртів або альдегідів за м’яких умов: R–CH=CH–(CH 2)n–CH 2 OH + 2[O] R–CH=CH–(CH 2)n–COOH + H 2 O R–CH=CH–(CH 2)n–CHO + 2[O] R–CH=CH–(CH 2)n–COOH За наявності спеціальних каталізаторів можливе також окиснення киснем повітря алкенів до карбонових ненасичених кислот.

4. Синтез з алкенів галогенуванням при 450 °С з наступною взаємодією галогеналкену з калій ціанідом та гідролізом нітрилу, що утворюється: H–(CH 2)n–CH=CH 2 + Cl 2 Cl–(CH 2)n–CH=CH 2 + HCl CH 2=CH–(CH 2)n–Cl + KC≡N CH 2=CH–(CH 2)n–C≡N + KCl CH 2=CH–(CH 2)n–C≡N + 2 H 2 O CH 2=CH–(CH 2)n–COOH + NH 3 5. Конденсація Кневенагеля відбувається під час взаємодії малонового естеру з карбоніловмісними сполуками за наявності піридину. Основа сприяє утворенню не тільки діаніона, але у невеликій кількості і трианіона за рахунок активної метиленової групи. Внаслідок цього відбувається конденсація за типом кротонової: Фізичні властивості. Ненасичені одноосновні кислоти – рідини або тверді речовини. Нижчі кислоти мають специфічний запах, розчинні у воді, вищі не мають запаху і нерозчинні у воді. Особливістю α-, β-ненасичених карбонових кислот є те, що вони мають кон’юговану систему, внаслідок чого виникає поляризація подвійного зв’язку. Хімічні властивості. Реакції карбоксильної групи аналогічні реакціям насичених одноосновних карбонових кислот. Реакції у вуглеводневому залишку визначаються наявністю подвійного зв’язку. Це реакції приєднання, окиснення, полімеризації. у ненасичених кислот, у яких наявна кон’югована система, у разі приєднання галогеноводнів атом Гідрогену приєднується до найменш гідрогенізованого атома Карбону:

У , - та ще більш віддаленими від СООН групи подвійними зв’язками, приєднання відбувається відповідно до правила Марковникова: Н 2 С=СН–СН 2–СООН + Н–Сl СН 3–СН(Сl)–(СН 2)2–СООН Пентен-4 -ова кислота 4 -Хлорпентанова кислота 2. Приєднання галогену. Наприклад: СН 3–СН=СН–СООН + Вr 2 СН 3–СН(Вr)–СООН Кротонова кислота 2, 3 -Дибромобутанова кислота 3. Приєднання водню. , -Ненасичені кислоти особливо легко приєднують водень, який утворюється реакцією амальгами натрію з водою: СН 2=СН–СООН + Н 2 СН 3–СН 2–СООН Вони також гідруються в рідкій фазі за присутності каталізаторів (Ni, Pt, Pd). 4. Приєднання води. Акрилова кислота та її гомологи ( , ‑ненасичені кислоти) за дії, наприклад, H 2 SO 4 приєднують воду з утворенням -гідроксикислот: СН 2=СН–СООН + Н 2 О СН 2(ОН)–СН 2–СООН -Гідроксипропіонова кислота 5. Приєднання амоніаку: , -ненасичені кислоти утворюють -амінокислоти: СН 2=СН–СООН + NН 3 NН 2–СН 2–СООН -Амінопропіонова кислота 6. Окисненням KMn. O 4 у лужному середовищі , -ненасичені кислоти перетворюються на дигідроксикислоти: СН 2=СН–СООН + [О] + Н 2 О СН 2(ОН)–СН(ОН)–СООН Більш енергійне окиснення призводить до розщеплення молекули кислоти за місцем подвійного зв’язку: +4 О СН 3–СН=СНСООН СН 3–СООН + НООС–СООН

Утворення солей. Ненасичені карбонові кислоти під час взаємодії з металами, оксидами і гідроксидами лужних та лужноземельних металів, карбонатами, амоніаком утворюють солі: Дія Н-нуклеофілів, тобто відновлення ненасичених карбонових кислот, відбувається під час використання комплексних гідридів, таких як Li. Al. H 4, Na. BH 4, які з надлишком реагенту і за жорсткіших умов відновлюються до первинних спиртів: 4 СH 2=CH–COOH + 3 Li. Al. H 4 → [(CH 3–CH 2 O)4 Al]Li + 2 Li. Al. O 2 [(CH 3–CH 2 O)4 Al]Li + 4 HCl → 4 CH 3–CH 2 OH + Al. Cl 3 + Li. Cl О-Нуклеофіли (реакція естерифікації). Спирти за наявності сильних мінеральних кислот утворюють естери карбонових кислот за загальною схемою:

N-Нуклеофіли (амоніак, аміни, гідразин) у разі взаємодії з карбоновими кислотами, як правило, утворюють амонієві карбоксилати і тільки за підвищених температур відбувається приєднання до карбонільної групи і утворюються аміди: RCOOH + H 2 N―R 1 → RCOO–[H 3 N+―R 1] → RCOHN―R 1 + H 2 O Нуклеофіли – галогенід-іони з карбоновими кислотами не реагують. Тільки у разі використання спеціальних реагентів (PCl 3, PCl 5, PBr 3, SOCl 2) здійснюється реакція, в якій утворюються ацилгалогеніди, наприклад: Утворення ангідридів відбувається під дією на карбонові кислоти водовідбирних засобів: 2 R–СOOH → (R–СO)2 O + HOH, Взаємодія з електрофільними реагентами відбувається, якщо активізувати карбоксильну групу, що здійснюється перетворенням її у карбоксилат-іон. У такому разі можна провести реакції алкілування та ацилування:
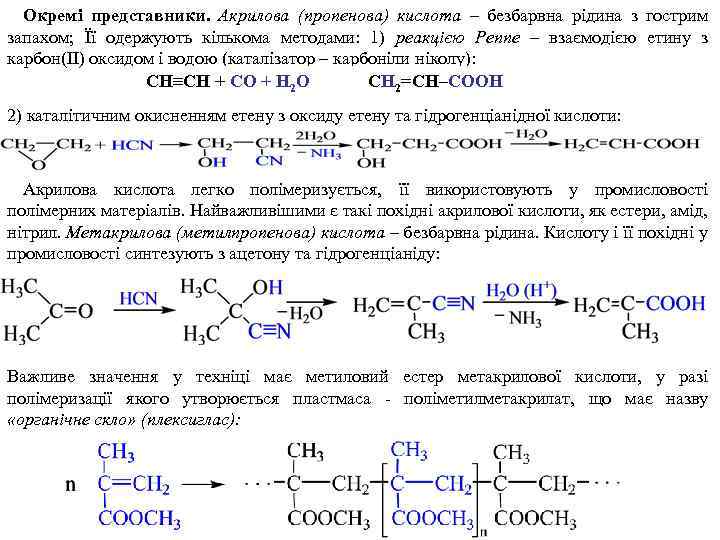
Окремі представники. Акрилова (пропенова) кислота – безбарвна рідина з гострим запахом; Її одержують кількома методами: 1) реакцією Реппе – взаємодією етину з карбон(ІІ) оксидом і водою (каталізатор – карбоніли ніколу): CH≡CH + CO + H 2 O CH 2=CH–COOH 2) каталітичним окисненням етену з оксиду етену та гідрогенціанідної кислоти: Акрилова кислота легко полімеризується, її використовують у промисловості полімерних матеріалів. Найважливішими є такі похідні акрилової кислоти, як естери, амід, нітрил. Метакрилова (метилпропенова) кислота – безбарвна рідина. Кислоту і її похідні у промисловості синтезують з ацетону та гідрогенціаніду: Важливе значення у техніці має метиловий естер метакрилової кислоти, у разі полімеризації якого утворюється пластмаса - поліметилметакрилат, що має назву «органічне скло» (плексиглас):

Сорбіонова (2, 4 -гексадієнова) кислота – кристалічна речовина, зовсім нетоксична, а тому є прекрасним антисептиком. Використовується для консервування м’ясних та рибних виробів, сиру, фруктових компотів, плодоягідних пюре, соків тощо. Олеїнова (Z-октадецен-9 -ова) кислота – масляниста безбарвна рідина, у присутності оксидів нітрогену перетворюється на тверду елаїдинову кислоту, яка є транс-ізомером: Олеїнова кислота Елаїдинова кислота Поширена у природі, міститься в оліях у вигляді гліцеридів (в олії арахісу – 50 -80, маслиновій – 70 -85 %. Синтезують гідролізом жирів. Естери олеїнової кислоти використовують у виробництві лаків та фарб, її солі – у виробництві мила. Лінолева (2, 2 -октадекадієн-9, 12 -ова) кислота – майже прозора масляниста рідина, нерозчинна у воді, добре розчинна у багатьох органічних розчинниках. Входить до складу гліцеридів, фосфоліпідів, конопляної, соєвої та кукурудзяної олії. Є незамінною кислотою, (не синтезується організмом людини і повинна входити до раціону харчування). Ненасичені кислоти з фрагментом такої будови – CH=CH–CН 2–CH=CH – необхідні для побудови клітинних стінок (мембран). Лінолева кислота легко окиснюється, а при контакті з повітрям – поступово автоокиснюється. Естери лінолевої кислоти використовують у виробництві лаків, фарб та емалей. Естери на повітрі поступово полімеризуються і утворюють прозорі плівки і тому належать до висихаючих олій. Ліноленова – (Z, Z, Z-октадекатриен-9, 12, 15 -ова) кислота – прозора масляниста рідина, входить до складу гліцеридів льняної олії. Є незамінною кислотою. Естери ліноленової кислоти використовують у виробництві лаків і фарб (висихаючі олії).
Nenasiheni-kislot-10.ppt
- Количество слайдов: 8

