 ОД ЕРЯ 2 5 ГЛК Ц И У Л Е
ОД ЕРЯ 2 5 ГЛК Ц И У Л Е



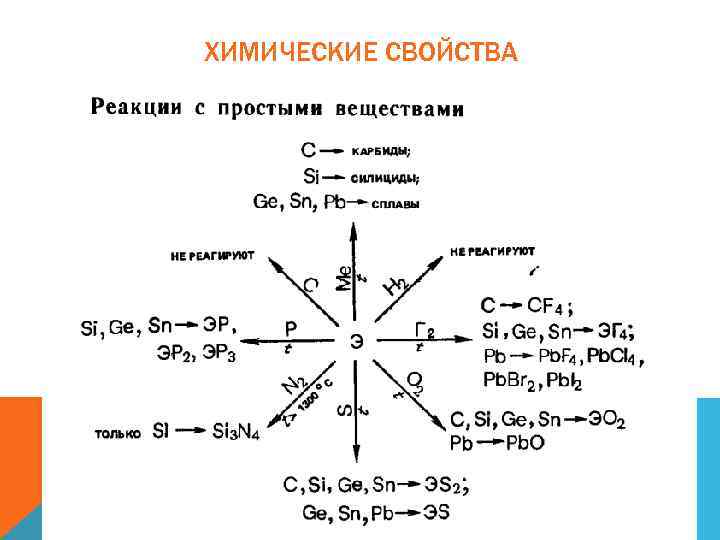 ХИМИЧЕСКИЕ СВОЙСТВА
ХИМИЧЕСКИЕ СВОЙСТВА

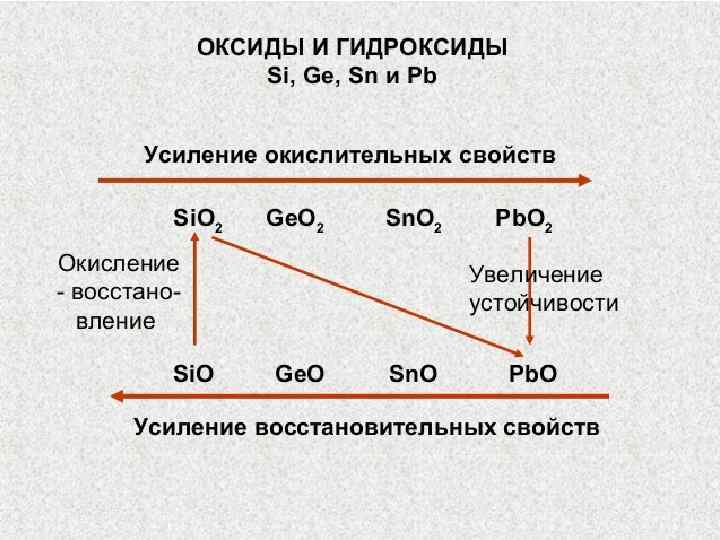
 СВОЙСТВА ГИДРОКСИДОВ IVА ГРУППЫ
СВОЙСТВА ГИДРОКСИДОВ IVА ГРУППЫ


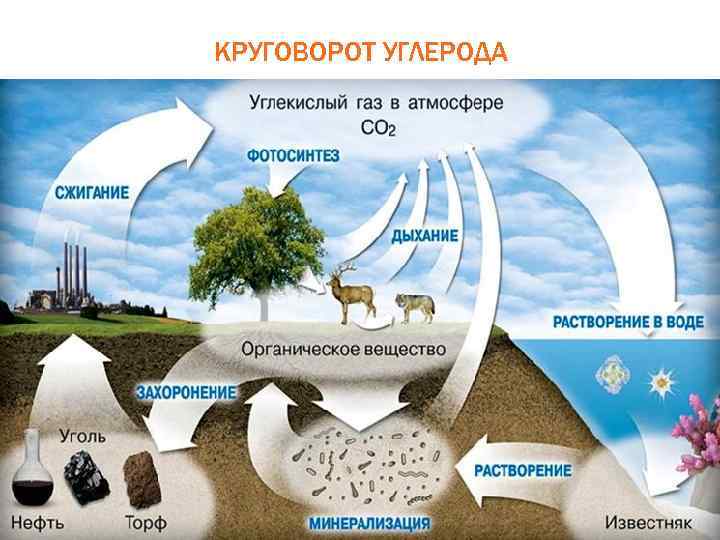 КРУГОВОРОТ УГЛЕРОДА
КРУГОВОРОТ УГЛЕРОДА


















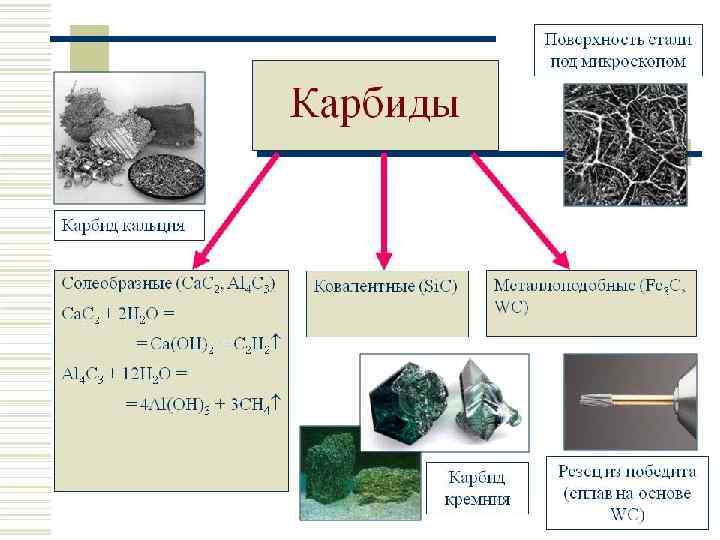
 ХИМИЧЕСКИЕ СВОЙСТВА УГЛЕРОДА 1) Образование карбидов: Ca + 2 C → Ca. C 2 (при нагревании) Ca. CO 3 + 4 C → Ca. C 2 + 3 CO↑ (при нагревании) 2) Взаимодействие с кислотами-окислителями: С + 4 HNO 3 (конц. ) → CO 2↑ + 4 NO 2↑ + 2 H 2 O (при нагревании)
ХИМИЧЕСКИЕ СВОЙСТВА УГЛЕРОДА 1) Образование карбидов: Ca + 2 C → Ca. C 2 (при нагревании) Ca. CO 3 + 4 C → Ca. C 2 + 3 CO↑ (при нагревании) 2) Взаимодействие с кислотами-окислителями: С + 4 HNO 3 (конц. ) → CO 2↑ + 4 NO 2↑ + 2 H 2 O (при нагревании)









 ОКИСЛЕНИЕ СЕРОУГЛЕРОДА Легко окисляется при небольшом нагревании: CS 2 + 3 O 2 → CO 2 + 2 SO 2
ОКИСЛЕНИЕ СЕРОУГЛЕРОДА Легко окисляется при небольшом нагревании: CS 2 + 3 O 2 → CO 2 + 2 SO 2








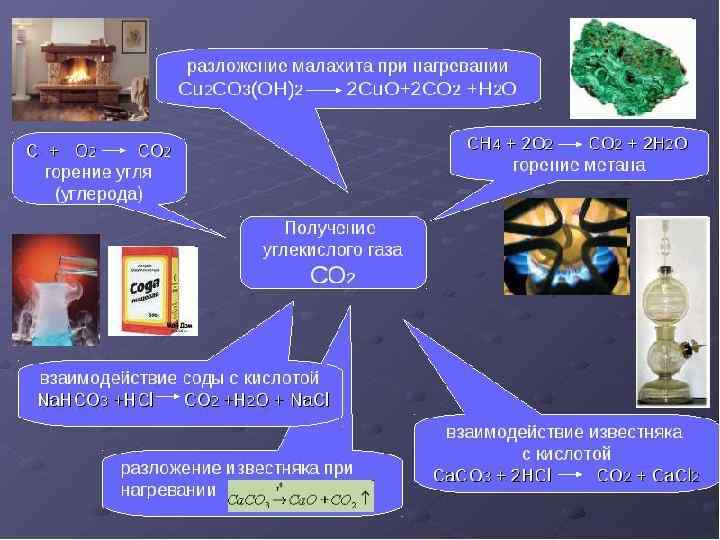




 ХИМИЧЕСКИЕ СВОЙСТВА УГЛЕКИСЛОГО ГАЗА 1) Восстановление раскаленным углем: CO 2 + C → 2 CO (при нагревании) 2) Взаимодействие с пероксидами металлов (регенерация воздуха): 2 Na 2 O 2 + 2 CO 2 → 2 Na 2 CO 3 + O 2↑
ХИМИЧЕСКИЕ СВОЙСТВА УГЛЕКИСЛОГО ГАЗА 1) Восстановление раскаленным углем: CO 2 + C → 2 CO (при нагревании) 2) Взаимодействие с пероксидами металлов (регенерация воздуха): 2 Na 2 O 2 + 2 CO 2 → 2 Na 2 CO 3 + O 2↑












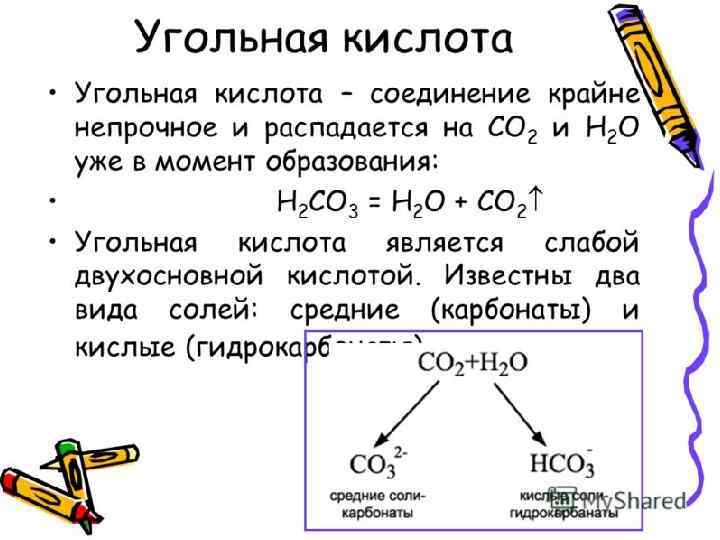


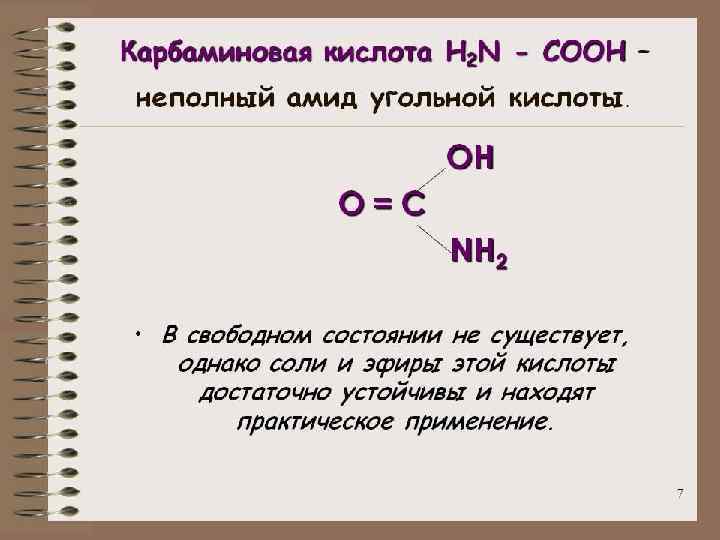

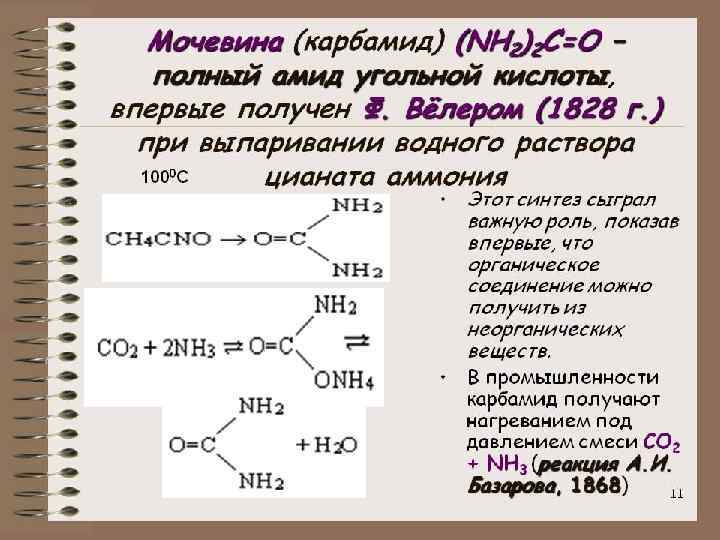
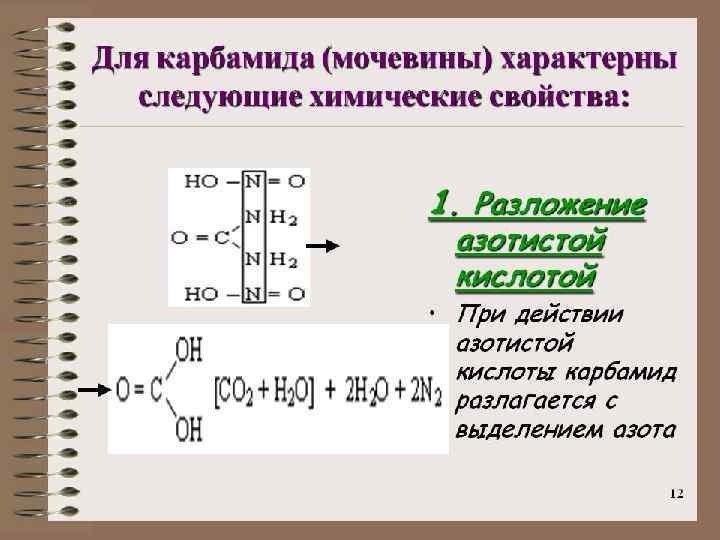
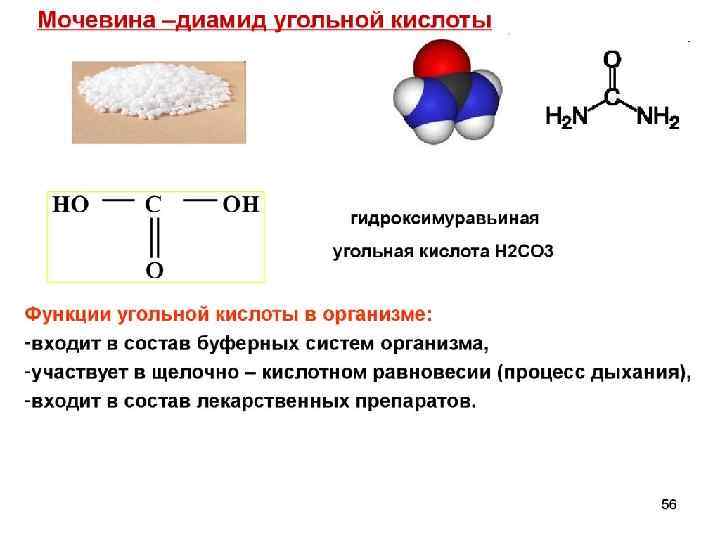










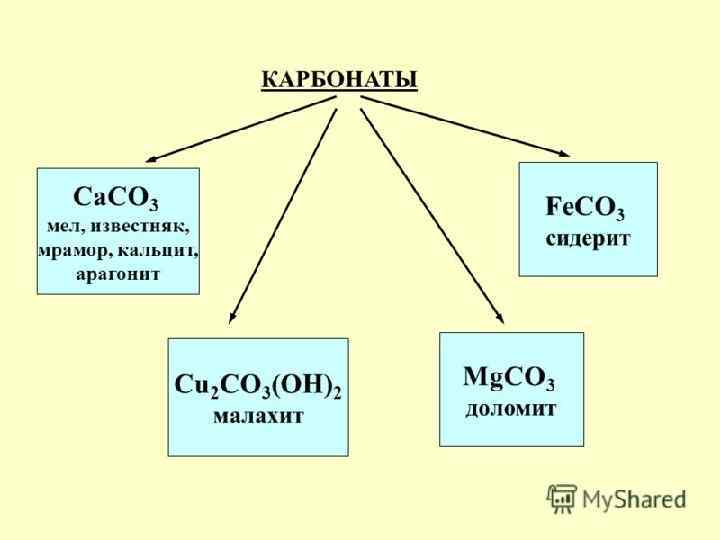






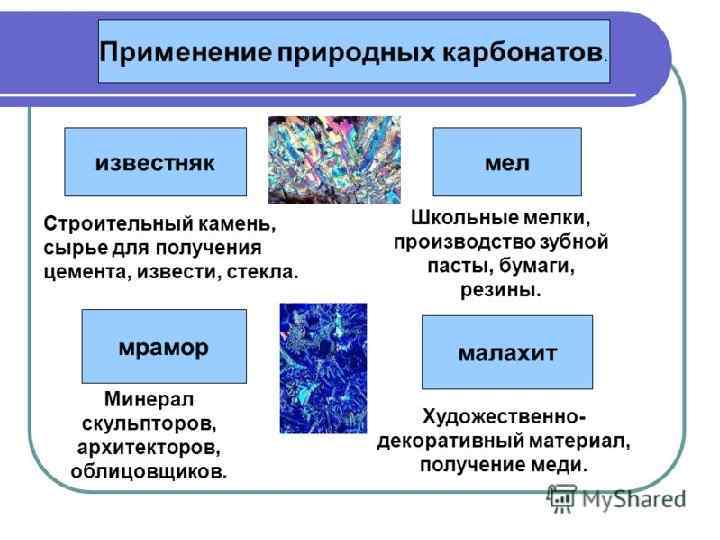















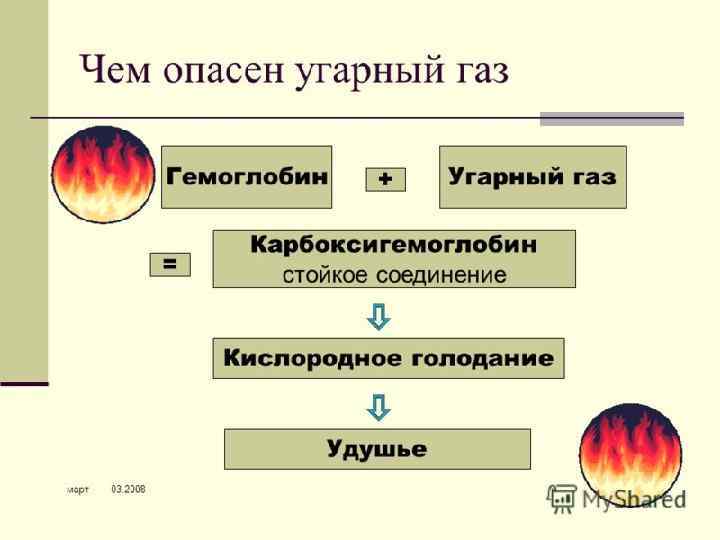
 ТРИВИАЛЬНЫЕ НАЗВАНИЯ Водяной газ – смесь СО и Н 2 СО – угарный газ Mg. CO 3 – магнезит, магнезия белая Ca. CO 3 ▪ Mg. CO 3 – доломит Ca. CO 3 – известняк, кальцит, мел, мрамор СО(NH 2)2 – карбамид, мочевина K 2 CO 3 - поташ Na 2 CO 3 ▪ 10 H 2 O – кристаллическая сода Na. HCO 3 – питьевая сода Na 2 CO 3 – кальцинированная сода (Cu. OH)2 CO 3 – малахит
ТРИВИАЛЬНЫЕ НАЗВАНИЯ Водяной газ – смесь СО и Н 2 СО – угарный газ Mg. CO 3 – магнезит, магнезия белая Ca. CO 3 ▪ Mg. CO 3 – доломит Ca. CO 3 – известняк, кальцит, мел, мрамор СО(NH 2)2 – карбамид, мочевина K 2 CO 3 - поташ Na 2 CO 3 ▪ 10 H 2 O – кристаллическая сода Na. HCO 3 – питьевая сода Na 2 CO 3 – кальцинированная сода (Cu. OH)2 CO 3 – малахит
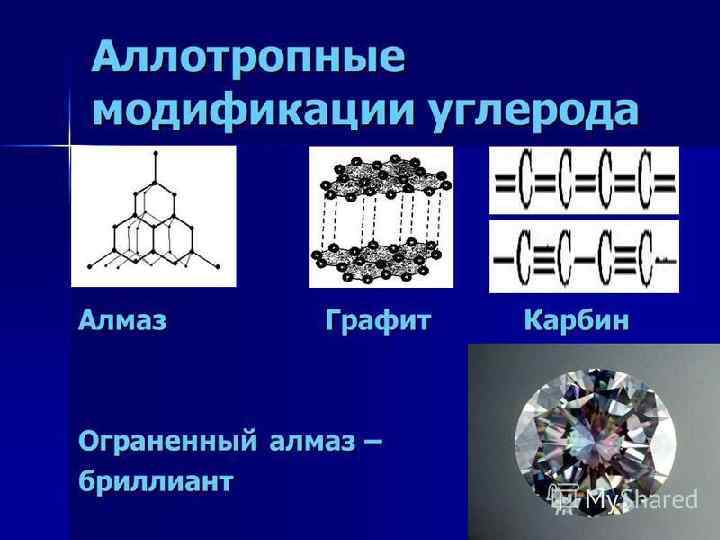
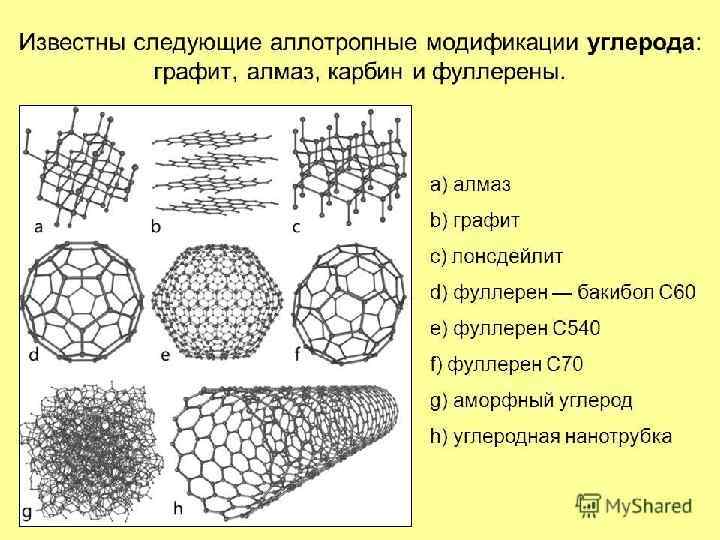
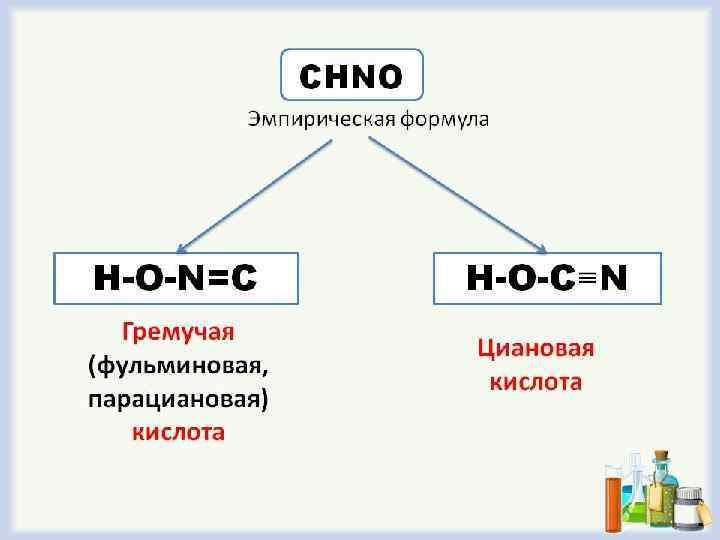
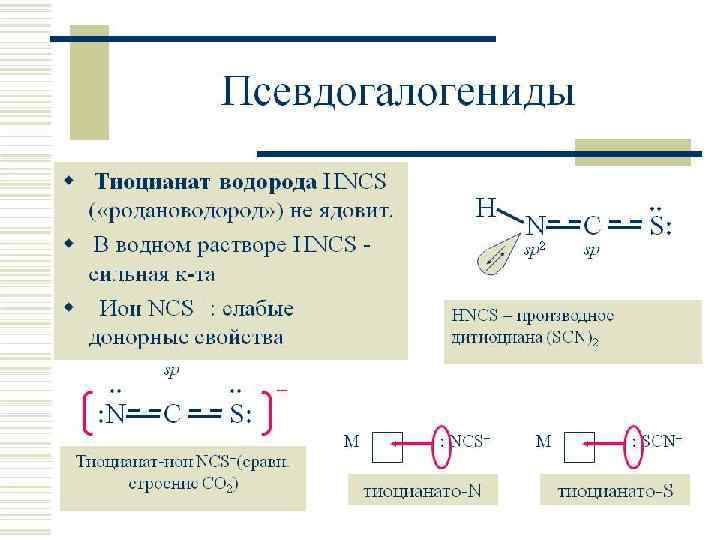
 ТРИВИАЛЬНЫЕ НАЗВАНИЯ СН 4 – болотный газ, рудничный газ СHI 3 – йодоформ Si. C – карборунд Роданиды (тиоцианаты) – соли роданистой (тиоциановой) кислоты HCNS – роданистая кислота, тиоциановая кислота HCN – синильная кислота COCl 2 - фосген Карбин – аллотропная модификация углерода, имеющая линейное строение Сажа – тонкодисперсный углерод С Сухой лед – твердый диоксид углерода СО 2 Углекислота – раствор диоксида углерода СО 2 в воде
ТРИВИАЛЬНЫЕ НАЗВАНИЯ СН 4 – болотный газ, рудничный газ СHI 3 – йодоформ Si. C – карборунд Роданиды (тиоцианаты) – соли роданистой (тиоциановой) кислоты HCNS – роданистая кислота, тиоциановая кислота HCN – синильная кислота COCl 2 - фосген Карбин – аллотропная модификация углерода, имеющая линейное строение Сажа – тонкодисперсный углерод С Сухой лед – твердый диоксид углерода СО 2 Углекислота – раствор диоксида углерода СО 2 в воде
 А! К ТИ К А ЕП Т РЬ Е РА П
А! К ТИ К А ЕП Т РЬ Е РА П


