Печкурова Н.Н..ppt
- Количество слайдов: 14
 ОЧИСТКА И РЕГУЛЯТОРНЫЕ ХАРАКТЕРИСТИКИ АКОНИТАТГИДРАТАЗЫ ИЗ ЩИТКОВ КУКУРУЗЫ (ZEA MAYS L. ) И ПРОРОСТКОВ СЕМЯН АМАРАНТА(AMARÁNTHUS CAUDATUS L. ). Дипломная работа Студентка: Печкурова Н. Н. Руководитель: профессор, д. б. н. Епринцев А. Т. Консультант: Сальников А. В. аспирант
ОЧИСТКА И РЕГУЛЯТОРНЫЕ ХАРАКТЕРИСТИКИ АКОНИТАТГИДРАТАЗЫ ИЗ ЩИТКОВ КУКУРУЗЫ (ZEA MAYS L. ) И ПРОРОСТКОВ СЕМЯН АМАРАНТА(AMARÁNTHUS CAUDATUS L. ). Дипломная работа Студентка: Печкурова Н. Н. Руководитель: профессор, д. б. н. Епринцев А. Т. Консультант: Сальников А. В. аспирант
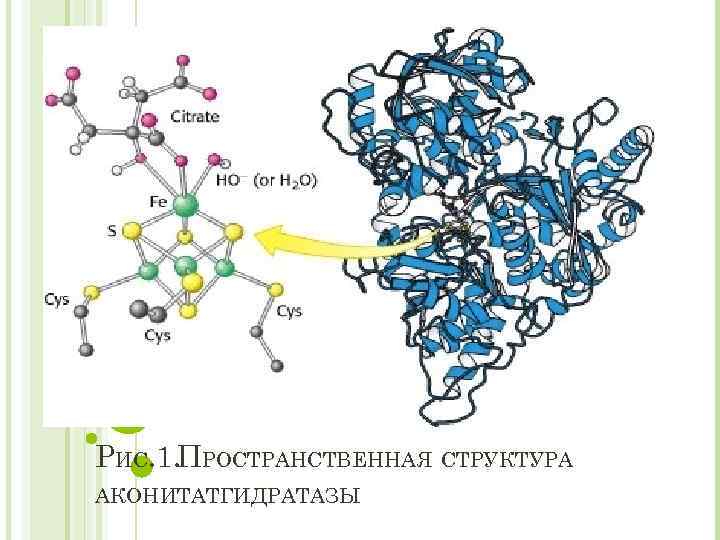 РИС. 1. ПРОСТРАНСТВЕННАЯ СТРУКТУРА АКОНИТАТГИДРАТАЗЫ
РИС. 1. ПРОСТРАНСТВЕННАЯ СТРУКТУРА АКОНИТАТГИДРАТАЗЫ
 ЦЕЛЬ И ЗАДАЧИ Целью исследования явилось получение цитоплазматической формы АГ из щитков кукурузы и проростков семян амаранта в высокоочищенном состоянии и изучение физикохимических и регуляторных свойств. Для выполнения цели были поставлены следующие задачи: 1. Изучить динамику активности АГ в щитках кукурузы и в семенах амаранта при прорастании семян. 2. Исследовать внутриклеточную локализацию аконитатгидратазы в щитках кукурузы и в проростках семян амаранта. 3. Получить гомогенные препараты цитоплазматической формы аконитазы из щитков кукурузы сорта «Воронежская « 76» и проростков семян амаранта сорта «Рыжик» . 4. Изучить физико-химические и регуляторные свойства аконитатгидратазы из щитков кукурузы и проростков семян амаранта.
ЦЕЛЬ И ЗАДАЧИ Целью исследования явилось получение цитоплазматической формы АГ из щитков кукурузы и проростков семян амаранта в высокоочищенном состоянии и изучение физикохимических и регуляторных свойств. Для выполнения цели были поставлены следующие задачи: 1. Изучить динамику активности АГ в щитках кукурузы и в семенах амаранта при прорастании семян. 2. Исследовать внутриклеточную локализацию аконитатгидратазы в щитках кукурузы и в проростках семян амаранта. 3. Получить гомогенные препараты цитоплазматической формы аконитазы из щитков кукурузы сорта «Воронежская « 76» и проростков семян амаранта сорта «Рыжик» . 4. Изучить физико-химические и регуляторные свойства аконитатгидратазы из щитков кукурузы и проростков семян амаранта.
 ОБЪЕКТЫ И МЕТОДЫ ИССЛЕДОВАНИЯ В качестве объекта исследования использовали щитки кукурузы сорта «Воронежская 76» и проростки семян амаранта сорта «Рыжик» , выращенные гидропонным способом при 25 о. С Активность фермента определяли спектрофотометрически на СФ-2000 при длине волны равной 240 нм. Субклеточную локализацию определяли с помощью дифференциального и изоплотностного центрифугирования в линейном градиенте плотности сахарозы. Определение количества белка осуществляли по методу Лоури. При окрашивании на белок использовали методику с кумасси. Специфическое проявление аконитазы осуществляли тетразолиевым методом.
ОБЪЕКТЫ И МЕТОДЫ ИССЛЕДОВАНИЯ В качестве объекта исследования использовали щитки кукурузы сорта «Воронежская 76» и проростки семян амаранта сорта «Рыжик» , выращенные гидропонным способом при 25 о. С Активность фермента определяли спектрофотометрически на СФ-2000 при длине волны равной 240 нм. Субклеточную локализацию определяли с помощью дифференциального и изоплотностного центрифугирования в линейном градиенте плотности сахарозы. Определение количества белка осуществляли по методу Лоури. При окрашивании на белок использовали методику с кумасси. Специфическое проявление аконитазы осуществляли тетразолиевым методом.
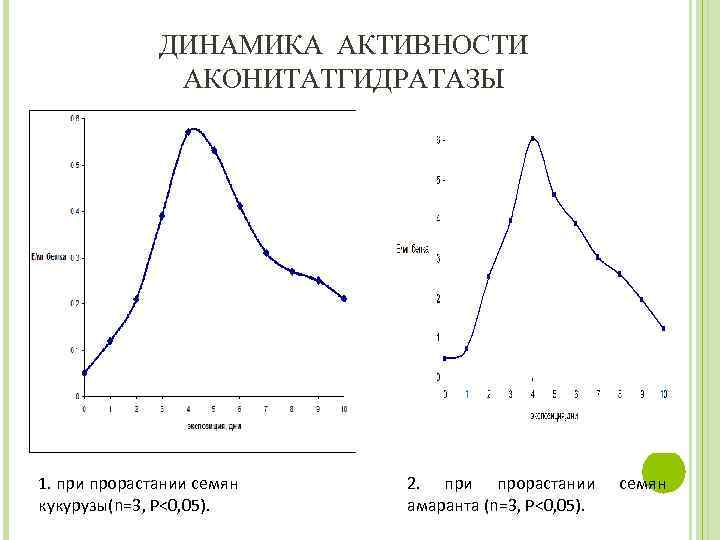 ДИНАМИКА АКТИВНОСТИ АКОНИТАТГИДРАТАЗЫ 1. при прорастании семян кукурузы(n=3, P<0, 05). 2. при прорастании амаранта (n=3, P<0, 05). семян
ДИНАМИКА АКТИВНОСТИ АКОНИТАТГИДРАТАЗЫ 1. при прорастании семян кукурузы(n=3, P<0, 05). 2. при прорастании амаранта (n=3, P<0, 05). семян
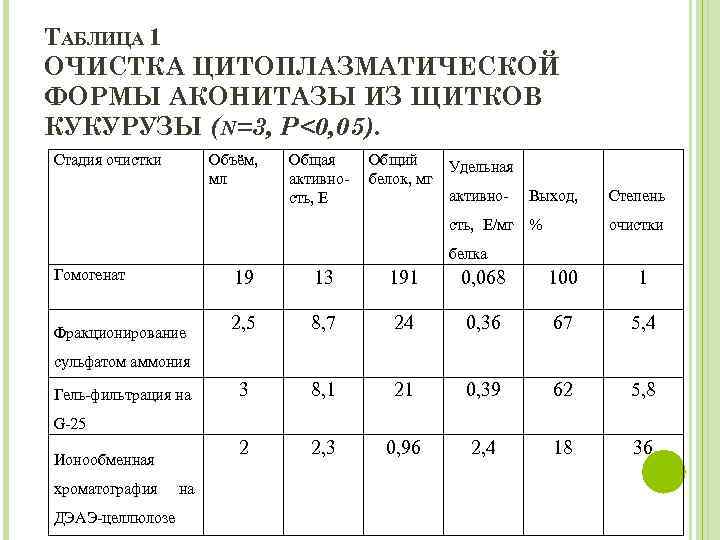 ТАБЛИЦА 1 ОЧИСТКА ЦИТОПЛАЗМАТИЧЕСКОЙ ФОРМЫ АКОНИТАЗЫ ИЗ ЩИТКОВ КУКУРУЗЫ (N=3, P<0, 05). Стадия очистки Объём, мл Общая активность, Е Общий белок, мг Удельная активно- Выход, сть, Е/мг % Степень очистки белка Гомогенат 19 13 191 0, 068 100 1 Фракционирование 2, 5 8, 7 24 0, 36 67 5, 4 3 8, 1 21 0, 39 62 5, 8 2 2, 3 0, 96 2, 4 18 36 сульфатом аммония Гель-фильтрация на G-25 Ионообменная хроматография ДЭАЭ-целлюлозе на
ТАБЛИЦА 1 ОЧИСТКА ЦИТОПЛАЗМАТИЧЕСКОЙ ФОРМЫ АКОНИТАЗЫ ИЗ ЩИТКОВ КУКУРУЗЫ (N=3, P<0, 05). Стадия очистки Объём, мл Общая активность, Е Общий белок, мг Удельная активно- Выход, сть, Е/мг % Степень очистки белка Гомогенат 19 13 191 0, 068 100 1 Фракционирование 2, 5 8, 7 24 0, 36 67 5, 4 3 8, 1 21 0, 39 62 5, 8 2 2, 3 0, 96 2, 4 18 36 сульфатом аммония Гель-фильтрация на G-25 Ионообменная хроматография ДЭАЭ-целлюлозе на
 РИС. 3. ЭЛЕКТРОФОРЕГРАММЫ ПРЕПАРАТОВ АКОНИТАТГИДРАТАЗЫ ИЗ ЩИТКОВ КУКУРУЗЫ I II N P F I – окрашивание кумасси; II – специфическое проявление. N – начало разделяющего геля; P – белковая полоса; F – фронт красителя
РИС. 3. ЭЛЕКТРОФОРЕГРАММЫ ПРЕПАРАТОВ АКОНИТАТГИДРАТАЗЫ ИЗ ЩИТКОВ КУКУРУЗЫ I II N P F I – окрашивание кумасси; II – специфическое проявление. N – начало разделяющего геля; P – белковая полоса; F – фронт красителя
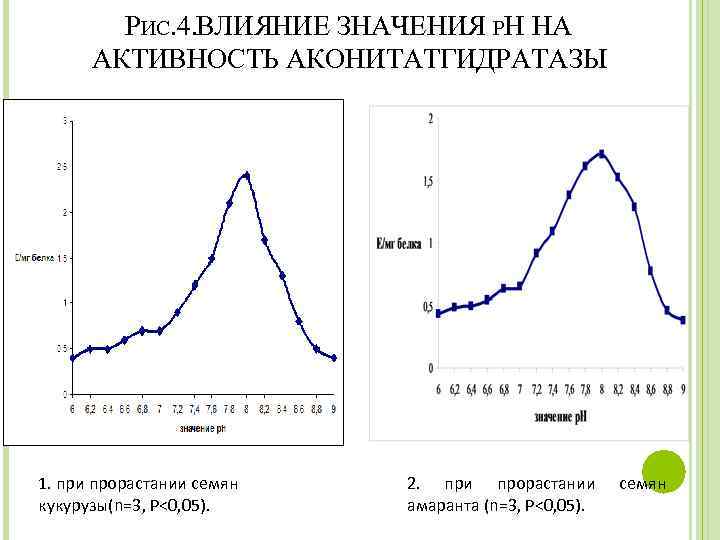 РИС. 4. ВЛИЯНИЕ ЗНАЧЕНИЯ РН НА АКТИВНОСТЬ АКОНИТАТГИДРАТАЗЫ 1. при прорастании семян кукурузы(n=3, P<0, 05). 2. при прорастании амаранта (n=3, P<0, 05). семян
РИС. 4. ВЛИЯНИЕ ЗНАЧЕНИЯ РН НА АКТИВНОСТЬ АКОНИТАТГИДРАТАЗЫ 1. при прорастании семян кукурузы(n=3, P<0, 05). 2. при прорастании амаранта (n=3, P<0, 05). семян
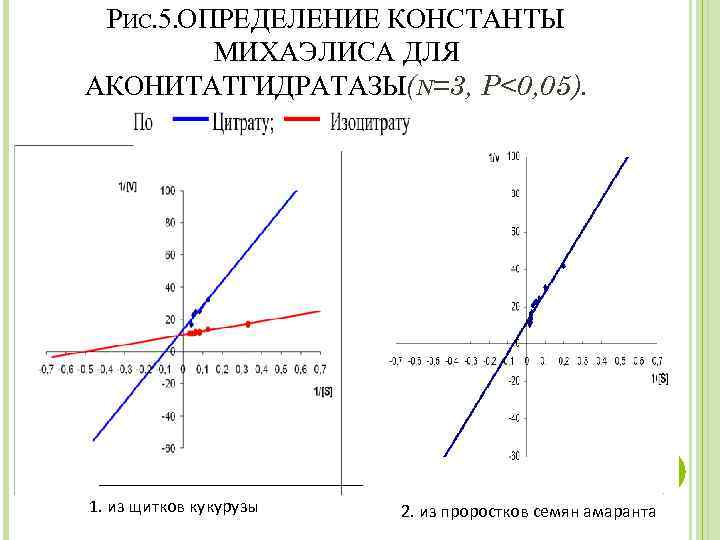 РИС. 5. ОПРЕДЕЛЕНИЕ КОНСТАНТЫ МИХАЭЛИСА ДЛЯ АКОНИТАТГИДРАТАЗЫ(N=3, P<0, 05). 1. из щитков кукурузы 2. из проростков семян амаранта
РИС. 5. ОПРЕДЕЛЕНИЕ КОНСТАНТЫ МИХАЭЛИСА ДЛЯ АКОНИТАТГИДРАТАЗЫ(N=3, P<0, 05). 1. из щитков кукурузы 2. из проростков семян амаранта
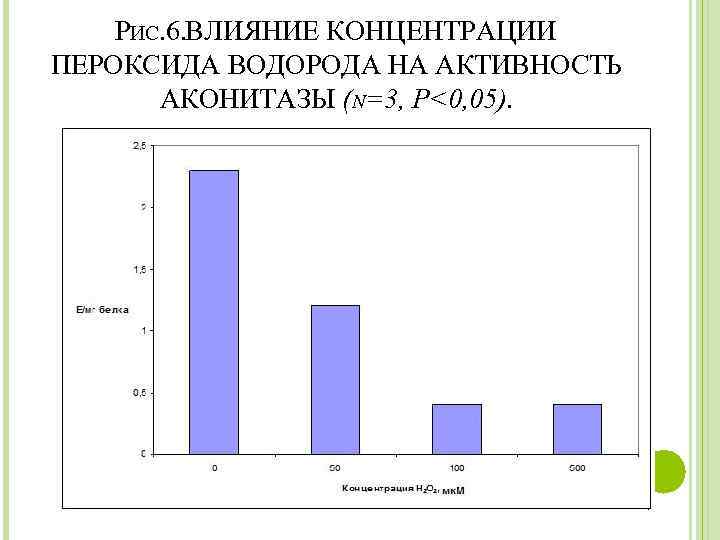 РИС. 6. ВЛИЯНИЕ КОНЦЕНТРАЦИИ ПЕРОКСИДА ВОДОРОДА НА АКТИВНОСТЬ АКОНИТАЗЫ (N=3, P<0, 05).
РИС. 6. ВЛИЯНИЕ КОНЦЕНТРАЦИИ ПЕРОКСИДА ВОДОРОДА НА АКТИВНОСТЬ АКОНИТАЗЫ (N=3, P<0, 05).
 ВЫВОДЫ Исследование динамики аконитазной активности позволило установить, что ее характер имеет сходство для амаранта и кукурузы. Максимальный уровень активности АГ обнаруживался на четвертый день прорастания семян обоих растений. Данные о субклеточной локализации свидетельствуют о том, что активность исследуемого фермента обнаруживается как в митохондриальной фракции, так и в цитоплазматической. Процентное соотношение между цитоплазматическим и митохондриальным компартментами составляет 87 и 13% соответственно. Применение четырехстадийной очистки позволило получить элекрофоретически гомогенные препараты АГ из щитков кукурузы и проростков семян амаранта. Удельная активность очищенных ферментов составила 2, 4 Е/мг белка для кукурузы и 1, 7 Е/мг белка для амаранта. Использование диск-электрофореза в ПААГ позволило установить гомогенность полученных препаратов из кукурузы и амаранта, при этом с помощью специфического проявления обнаружена их аконитазная активность. Исследованы каталитические свойства АГ из изучаемых объектов (р. Н оптимум, сродство к субстратам и др. ). Установлено, что значение Км зависит от применяемого субстрата. Сродство фермента значительно выше к изоцитрату по сравнению с цитратом.
ВЫВОДЫ Исследование динамики аконитазной активности позволило установить, что ее характер имеет сходство для амаранта и кукурузы. Максимальный уровень активности АГ обнаруживался на четвертый день прорастания семян обоих растений. Данные о субклеточной локализации свидетельствуют о том, что активность исследуемого фермента обнаруживается как в митохондриальной фракции, так и в цитоплазматической. Процентное соотношение между цитоплазматическим и митохондриальным компартментами составляет 87 и 13% соответственно. Применение четырехстадийной очистки позволило получить элекрофоретически гомогенные препараты АГ из щитков кукурузы и проростков семян амаранта. Удельная активность очищенных ферментов составила 2, 4 Е/мг белка для кукурузы и 1, 7 Е/мг белка для амаранта. Использование диск-электрофореза в ПААГ позволило установить гомогенность полученных препаратов из кукурузы и амаранта, при этом с помощью специфического проявления обнаружена их аконитазная активность. Исследованы каталитические свойства АГ из изучаемых объектов (р. Н оптимум, сродство к субстратам и др. ). Установлено, что значение Км зависит от применяемого субстрата. Сродство фермента значительно выше к изоцитрату по сравнению с цитратом.
 СПАСИБО ЗА ВНИМАНИЕ !!!
СПАСИБО ЗА ВНИМАНИЕ !!!

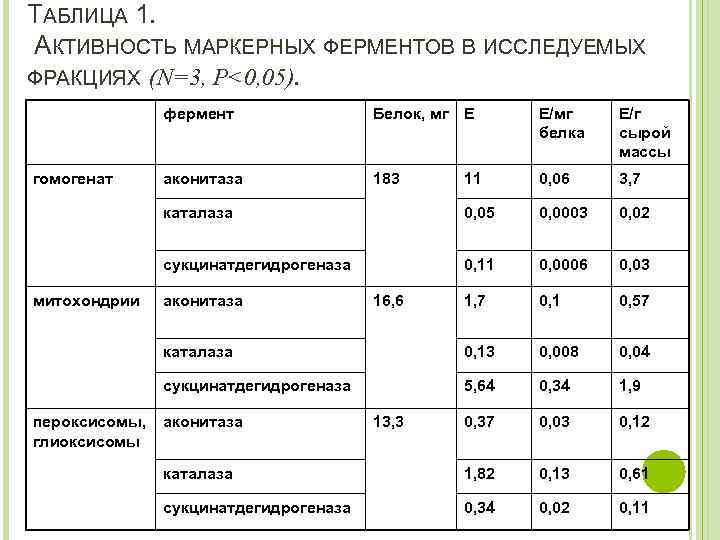 ТАБЛИЦА 1. АКТИВНОСТЬ МАРКЕРНЫХ ФЕРМЕНТОВ В ИССЛЕДУЕМЫХ ФРАКЦИЯХ (N=3, P<0, 05). фермент аконитаза 183 11 0, 06 3, 7 0, 05 0, 0003 0, 02 0, 11 0, 0006 0, 03 1, 7 0, 1 0, 57 каталаза 0, 13 0, 008 0, 04 сукцинатдегидрогеназа пероксисомы, глиоксисомы Е/г сырой массы сукцинатдегидрогеназа митохондрии Е/мг белка каталаза гомогенат Белок, мг Е 5, 64 0, 34 1, 9 0, 37 0, 03 0, 12 каталаза 1, 82 0, 13 0, 61 сукцинатдегидрогеназа 0, 34 0, 02 0, 11 аконитаза 16, 6 13, 3
ТАБЛИЦА 1. АКТИВНОСТЬ МАРКЕРНЫХ ФЕРМЕНТОВ В ИССЛЕДУЕМЫХ ФРАКЦИЯХ (N=3, P<0, 05). фермент аконитаза 183 11 0, 06 3, 7 0, 05 0, 0003 0, 02 0, 11 0, 0006 0, 03 1, 7 0, 1 0, 57 каталаза 0, 13 0, 008 0, 04 сукцинатдегидрогеназа пероксисомы, глиоксисомы Е/г сырой массы сукцинатдегидрогеназа митохондрии Е/мг белка каталаза гомогенат Белок, мг Е 5, 64 0, 34 1, 9 0, 37 0, 03 0, 12 каталаза 1, 82 0, 13 0, 61 сукцинатдегидрогеназа 0, 34 0, 02 0, 11 аконитаза 16, 6 13, 3


