552727c94bef6483b3a3f67b53d749e9.ppt
- Количество слайдов: 24

Оценка качества фармакотерапии в ЛПУ 21 ноября 2008 г Ассистент кафедры клинической фармакологии и фармакотерапии КГМА, к. м. н. Титаренко Альбина Фаритовна

Методы оценки качества фармакотерапии § Ретроспективный и Проспективный анализ качества фармакотерапии - контроль за использованием лекарственных средств, соблюдением совместимости § Карта экспертной оценки качества фармакотерапии, протокол консультации» (Приказом МЗ РФ от 22. 10. 2003 № 494, Приказ МЗ РТ № 55 от 13. 01. 2004 г. ) § Индикаторы использования лекарственных средств ВОЗ § Проведение фармакоэкономического анализа лекарственных средств с целью выбора наиболее эффективных и наименее затратных наименований § Мониторинг нежелательных лекарственных реакций (НЛР).

Фармакоэкономика призвана решать вопросы, связанные с § наиболее оптимальным путем использования имеющихся в наличии ресурсов § планированием дальнейшей политики их применения

История появления АВС анализа § 20 -е гг. ХХ в. – обсуждение в литературе проблемы разнесения косвенных затрат между различными изделиями § 30 -е гг. ХХ в. – «издержки нужно распределять между продуктами пропорционально усилиям, затрачиваемым на каждый продукт» § Конец 80 -х гг. ХХ в. – Гарвардская школа бизнеса, Robin Cooper, Robert S. Kaplan – АВС-метод как лучший способ калькуляции издержек

АВС метод. Общая постановка задачи § Данные анализа по традиционным показателям ЛПУ не позволяют адекватно оценивать качество лечения и эффективность затрат § Для реализации процессного подхода к управлению качеством лечения и повышению эффективности затрат требуется анализ стоимости бизнеспроцессов

Оценка рациональности закупок ЛС (АВС анализ) АВС анализ – метод оценки рационального использования денежных средств по трем классам в соответствии с их фактическим потреблением за определенный предыдущий период времени: - Класс А – 80% объема всех расходов (10 -20% наименований ЛС) - Класс В – 15% от всех расходов (20 -30% наименований ЛС) - Класс С – 5% общей суммы расходов (60 -80% наименований ЛС)

VEN-анализ § Метод оценки рационального использования лекарственных средств по трем категориям жизненной важности § Жизненно важные (V, Vital) – ЛС для лечения угрожающих жизни состояний, постоянно необходимые для поддержания жизни или имеющие опасный для жизни синдром отмены § Необходимые (E, Essential) – ЛС для лечения менее опасных, но серьезных заболеваний § Второстепенные (N, Non-essential) - ЛС для лечения легких заболеваний, ЛС сомнительной эффективности, дорогостоящие лекарства с симптоматическими показаниями
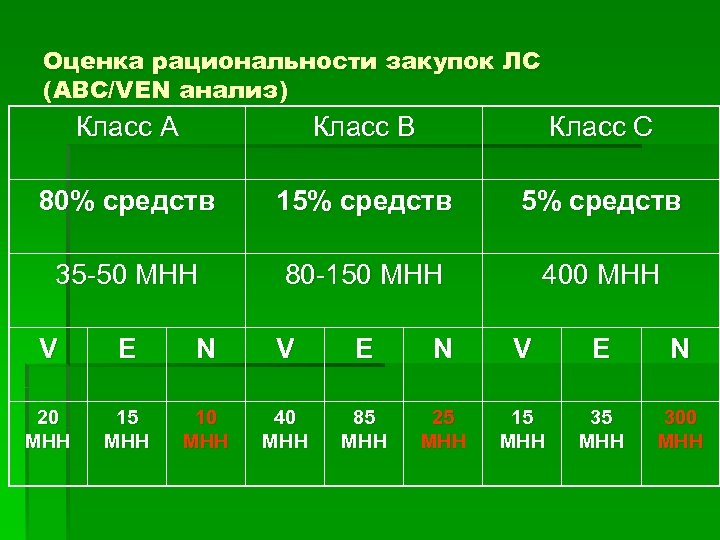
Оценка рациональности закупок ЛС (АВС/VEN анализ) Класс А Класс В Класс С 80% средств 15% средств 35 -50 МНН 80 -150 МНН 400 МНН V E N 20 МНН 15 МНН 10 МНН 40 МНН 85 МНН 25 МНН 15 МНН 300 МНН
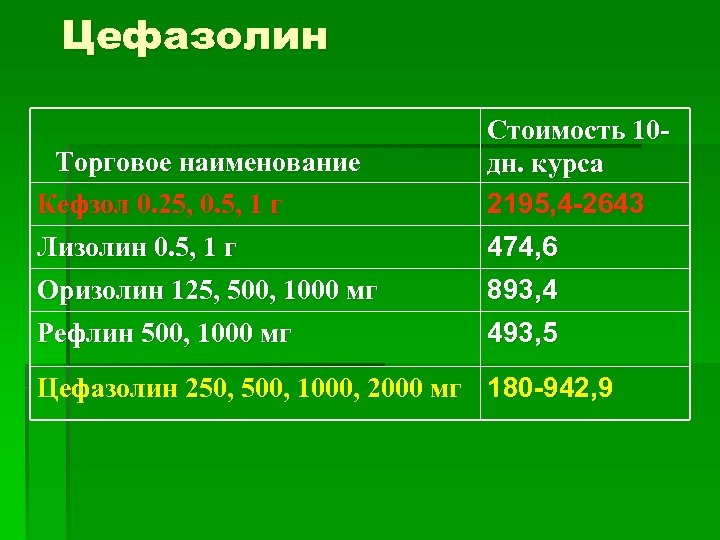
Цефазолин Торговое наименование Кефзол 0. 25, 0. 5, 1 г Лизолин 0. 5, 1 г Оризолин 125, 500, 1000 мг Рефлин 500, 1000 мг Стоимость 10 дн. курса 2195, 4 -2643 474, 6 893, 4 493, 5 Цефазолин 250, 500, 1000, 2000 мг 180 -942, 9
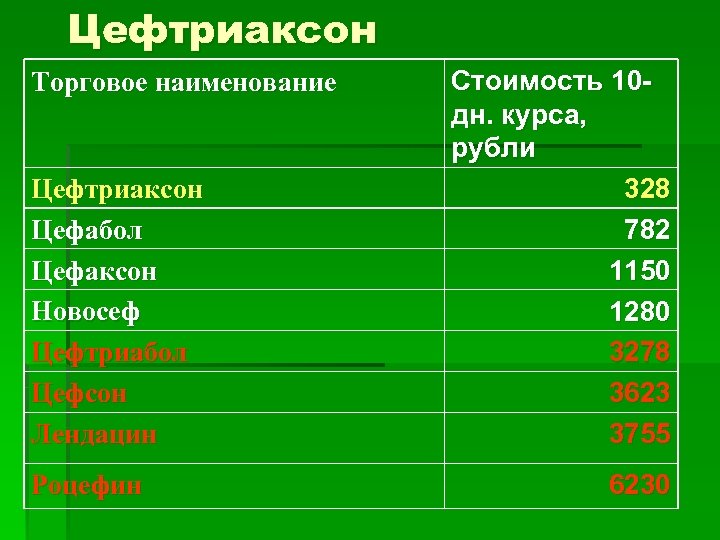
Цефтриаксон Торговое наименование Цефтриаксон Цефабол Цефаксон Новосеф Цефтриабол Цефсон Лендацин Роцефин Стоимость 10 дн. курса, рубли 328 782 1150 1280 3278 3623 3755 6230

ФЭА – в основе формирования формулярных и льготных перечней лекарственных средств Ницерголин Амп. 4 мг (8 мг/сутки) драже 10 мг (30 мг/сутки) Сермион Амп. 102, 2 -138, 4 руб. др. 72, 5 -88, 1 руб. Амп. 4 мг (8 Амп. – 5143 руб. мг/сутки) таб. 5 мг - 167, 8 -183, 4 таб. 5, 10, 30 мг руб. (30 мг/сутки) таб. 10 мг - 94, 5 -100, 7 руб. таб. 30 мг - 84, 3 руб.

Основные цели АВС – анализа § Оценка целесообразности финансовых затрат на лекарственные средства в конкретном ЛПУ § Разработка мероприятий по рационализации лекарственных закупок § Выбор препаратов для включения в формуляр и исключения из него § Анализ соответствия финансовых затрат данным анализа структуры заболеваемости

АВС-, VEN- и ФЭ-анализы § Систематизация и выделение объемов приоритетных затрат § Данные об избыточном или недостаточном использовании ЛС § Рациональное использование имеющихся средств

Мониторинг нежелательных лекарственных реакций

«Современные лекарства подобны атомной энергии. Они могут принести как огромную пользу, так и огромный вред» . Сер Деррик Данлоп Первый председатель Комитета по безопасности лекарств Великобритании

Побочные реакции не только серьезная медицинская, социальная, но также и экономическая проблема § Затраты, связанные с лекарственными осложнениями, составляют в США около 76 млрд. долларов в год

Нежелательные побочные реакции § В 2004 году около 10% от количества всех госпитализированных больных составляли больные с осложнениями лекарственной терапии: § в 33% случаев – серьезными и § в 2% случаев – летальными. (Статистика: Великобритания) § Ежегодно регистрируют около 2000 больных с кровотечениями из ЖКТ и 200 летальных исходов (на 11 млн. назначений) в результате применения НПВС.

Выявление и регистрация неблагоприятных побочных реакций § Россия – Минздравом РФ создан Федеральный центр по изучению НПР § В настоящее время на территории России функционирует 30 региональных центров по контролю безопасности ЛС § 1997 - Россия была официально принята в программу ВОЗ по международному мониторингу ЛС

Выявление и регистрация неблагоприятных побочных реакций § КЛИНИЧЕСКИЙ ФАРМАКОЛОГ (приказ Минздрава России № 131 05. 97). § Приказ Минздрава РФ от 22 октября 2003 г. № 494 «О совершенствовании деятельности врачейклинических фармакологов» . § Выявление случаев возникновения НПР и информационное обеспечение специалистов по вопросам эффективности и безопасности ЛС, зарегистрированных в России

Клиническая фармакология и мировое здравоохранение § Основные разделы: § Фармаконадзор (мониторинг и изучение безопасности лекарств) § Фармакокинетика § Метаболизм лекарств § Фармакоэпидемиология § Фармакоэкономика From the IUPHAR Clinical Pharmacology lecture given at the 8 th World Congress of Clinical Pharmacology and Therapeutics, Brisbane, Australia, August 2004. International Journal of Risk & safety in Medicine. 17: 65 -71 (2005) authored by Anthony J. Smith. Department of Clinical Pharmacology, University of Newcastle and WHO Collaborating Centre for training in Pharmaco-economics and Rational Pharmacotherapy, Australia. WHO Drug Information Vol 19, No. 3, 2005

Выявление и регистрация неблагоприятных побочных реакций § В России Федеральный закон «О лекарственных средствах» принят в 1998 г. § В пункте 1 статьи 43 «Закона о лекарственных средствах» указано, что «субьекты обращения ЛС обязаны сообщать федеральному органу исполнительной власти в сфере здравоохранения, органам исполнительной власти субъектов Российской Федерации в сфере здравоохранения, федеральному органу контроля качества ЛС и территориальным органам контроля качества ЛС о всех случаях побочных действий и об особенностях взаимодействия ЛС с другими ЛС, которые не соответствуют сведениям о ЛС, содержащимся в инструкциях по их применению» .

Выявление и регистрация неблагоприятных побочных реакций § В п. 2 этой статьи отмечается, что «за несообщение или сокрытие сведений, предусмотренных пунктом 1 настоящей статьи, лица, которым они стали известны по роду их профессиональной деятельности, несут дисциплинарную, административную или уголовную ответственность в соответствии с законодательством Российской Федерации» .

Выявление и регистрация неблагоприятных побочных реакций Приказ Минздрава РТ от 19 сентября 2005 г. № 881 § Положение об отделе мониторинга качества и безопасности лекарственной терапии. § Порядок приема и анализа сообщений о нежелательных лекарственных реакциях отделом мониторинга и безопасности лекарственной терапии.

Выявление и регистрация неблагоприятных побочных реакций § Учетная форма «Извещение о нежелательных лекарственных реакциях» и вложить в каждую историю болезни и в каждую амбулаторную карту. § Предоставление ежемесячно информации о всех случаях развития нежелательных лекарственных реакций с момента их выявления в отдел мониторинга качества и безопасности лекарственной терапии (ОМКИБЛТ) при ГУЗ «Республиканская клиническая психиатрическая больница им. акад. В. М. Бехтерева в электронном виде по адресу clinpharm 17@list. ru и факсу (843)273 -08 -02, 274 -92 -80 по форме карты-извещения «Извещение о нежелательных лекарственных реакциях.
552727c94bef6483b3a3f67b53d749e9.ppt