PF._Obzornaya_lekciya._Belokonova_N.A.ppt
- Количество слайдов: 68

Обзорная лекция и анкетирование

ИСТОРИЧЕСКАЯ СПРАВКА • XV-XVI в – швейцарский врач Парацельс Т. (1493 -1591) впервые стал успешно применять неорганические вещества для лечения больных и был убежден, что цель химии –изготовление лекарств, а не золота и серебра. • XVI-XVIII вв химия практически развивалась врачами, отделяясь от алхимии. • XVIII в – шведский фармацевт Шееле(1742 -1786), будучи помошником аптекаря, открыл кислоты растительного и животного происхождения – винную, лимонную, яблочную, мочевую. Наиболее важные его открытия – кислород и азот. • врач Майер(1814 -1878) и английский ученый Д. Джоуль( 1818 – 1889) стали основоположниками I начала термодинамики. • XIX в - русский врач И. М. Сеченов (1829 -1905) стал основоположником • XX в - немецкий бактериолог П. Эрлих(1854 -1915) впервые синтезировал внедрения физической химии в медицину соединения в качестве лекарственных средств и применил в области химиотерапии, за что ему присудили в 1908 г. Нобелевскую премию «Медик без довольного познания химии совершенен быть не может !» М. В. Ломоносов (1711 - 1765 )

1. ПРОНИКЛИСЬ ЛИ ВЫ ПОНИМАНИЕМ ЗНАЧИМОСТИ ХИМИИ ДЛЯ МЕДИЦИНЫ: 1. ДА 2. НЕТ

2. УРОВЕНЬ теоретического ПОНИМАНИЯ МАТЕРИАЛА: 2. 1. Химическая термодинамика – наука о взаимных превращениях одних форм энергии в другие.

Основные понятия термодинамики: ØСостояние системы определяется: параметрами: m(г, кг, моль), V(дм 3, м 3), Т (0 К), Р (атм, мм. рт. ст, Па, к. Па), и характеризуется функциями состояния: U(Дж/моль, к. Дж/моль)- внутренняя энергия, H(Дж/моль, к. Дж/моль)- энтальпия, S (Дж/моль)*K, к. Дж/моль*K)- энтропия, G (Дж/моль, к. Дж/моль)- энергия Гиббса Ø Процесс (обратимый, необратимый): • изохорный (V=const, ΔV=0), • изобарный (P=const, ΔP=0), • изотермический (T=const, ΔT=0)
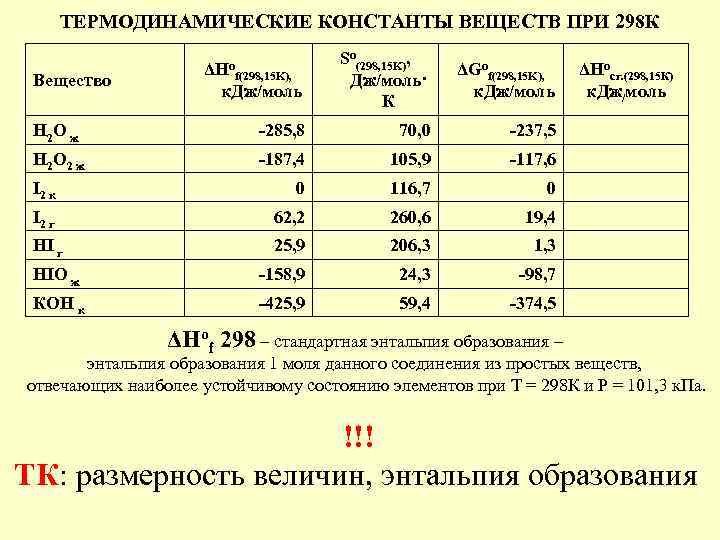
ТЕРМОДИНАМИЧЕСКИЕ КОНСТАНТЫ ВЕЩЕСТВ ПРИ 298 К Вещество ΔНо f(298, 15 K), к. Дж/моль So(298, 15 K), Дж/моль· К ΔGof(298, 15 K), к. Дж/моль Н 2 О ж -285, 8 70, 0 -237, 5 Н 2 О 2 ж -187, 4 105, 9 -117, 6 I 2 к 0 116, 7 0 I 2 г 62, 2 260, 6 19, 4 HI г 25, 9 206, 3 1, 3 HIO ж -158, 9 24, 3 -98, 7 КОН к -425, 9 59, 4 ΔНосг. (298, 15 К) к. Дж/моль -374, 5 ΔНоf 298 – стандартная энтальпия образования – энтальпия образования 1 моля данного соединения из простых веществ, отвечающих наиболее устойчивому состоянию элементов при Т = 298 К и Р = 101, 3 к. Па. !!! ТК: размерность величин, энтальпия образования

Типы задач: 1) количественные расчеты, характеризующие взаимодействия веществ : тепловой эффект, изменение энтальпии, энтропии, энергии Гиббса ( !!!Д. З: учет коэффициентов, правильность написания уравнений…. ), 2) определение направления химической реакции при определенных условиях, 3) рассчитать условия равновесного состояния в системе
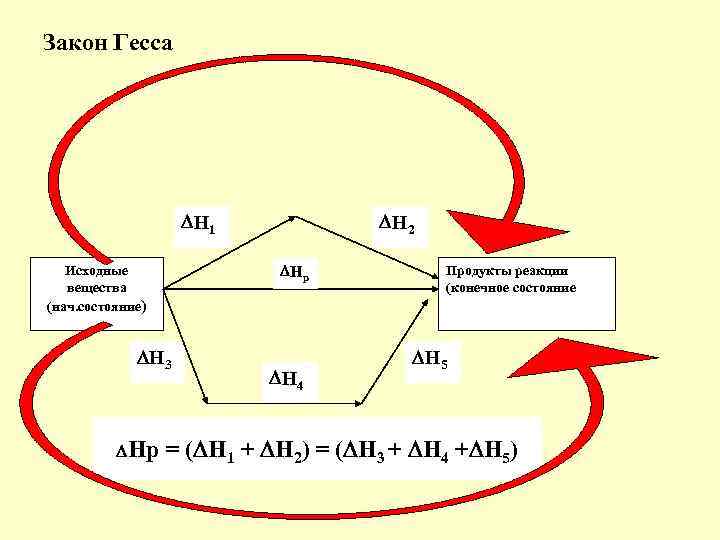
Закон Гесса Н 2 Н 1 Нр Исходные вещества (нач. состояние) Н 3 Нр Н 4 Продукты реакции (конечное состояние Н 5 = ( Н 1 + Н 2) = ( Н 3 + Н 4 + Н 5)

Следствия из закона Гесса: Ø 1 -ое следствие - Закон Лавуазье-Лапласа: ΔНоразл = - ΔНообр. Ø 2 -ое следствие: стандартная энтальпия реакции равна разности между суммой стандартных энтальпий образования продуктов реакции и суммой стандартных энтальпий образования исходных веществ (с учетом стехиометрических коэффициентов): !!! ΔSрo, ΔGрo ΔНор-и = ∑ νiΔНоf 298 прод. - ∑ νi ΔНоf 298 исх. Ø 3 -ье следствие: стандартная : энтальпия реакции равна разности между суммой стандартных энтальпий сгорания исходных веществ и суммой стандартных энтальпий сгорания продуктов реакции (с учетом стехиометрических коэффициентов). !!! См. табл. ΔНо 298 р-и = ∑ νi ΔНо сг. 298 (исх. в-в) - ∑ νi ΔНо сг. 298 (прод. р-и). Задача: По какому следствию можно рассчитать изменение энтальпии реакции: С 2 Н 4 + 3 О 2 = 2 СО 2 +2 Н 2 О
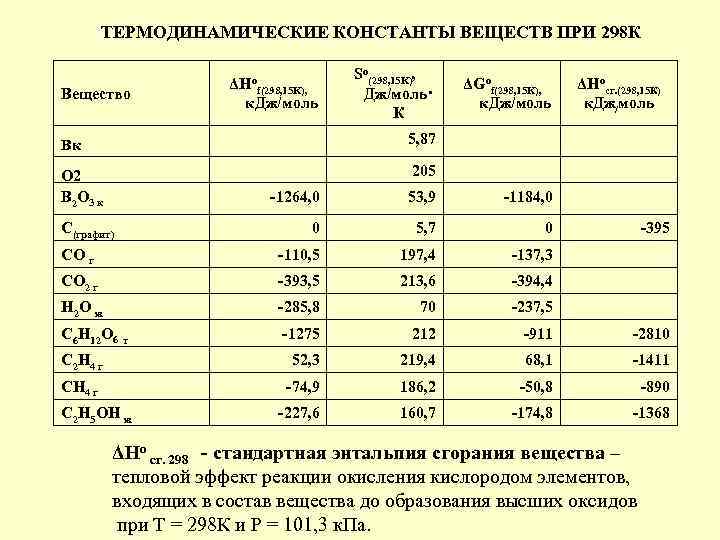
ТЕРМОДИНАМИЧЕСКИЕ КОНСТАНТЫ ВЕЩЕСТВ ПРИ 298 К Вещество ΔНоf(298, 15 K), к. Дж/моль So(298, 15 K), Дж/моль· К Вк ΔНосг. (298, 15 К) к. Дж/моль 5, 87 О 2 В 2 О 3 к ΔGof(298, 15 K), к. Дж/моль 205 -1264, 0 53, 9 -1184, 0 0 5, 7 0 СО г -110, 5 197, 4 -137, 3 СО 2 г -393, 5 213, 6 -394, 4 Н 2 О ж -285, 8 70 -237, 5 С 6 Н 12 О 6 т -1275 212 -911 -2810 С 2 Н 4 г 52, 3 219, 4 68, 1 -1411 СН 4 г -74, 9 186, 2 -50, 8 -890 -227, 6 160, 7 -174, 8 -1368 С(графит) С 2 Н 5 ОН ж -395 ΔНо сг. 298 - стандартная энтальпия сгорания вещества – тепловой эффект реакции окисления кислородом элементов, входящих в состав вещества до образования высших оксидов при Т = 298 К и Р = 101, 3 к. Па.

Алгоритм решения задач 1 и 2 типа: ШПравильно списать справочные данные ШВыбрать метод решения: алгебраический, графический ШНаписать уравнение процесса ШОбосновать расчет: указать закон или следствие, на основании которого выполняется ШПодставить в формулу данные с учетом коэффициентов и выполнить расчет ШВыводы

Задачи: 1)Вычислите энтальпию образования В 2 О 3, если известно: 2 В(к) + N 2(к) = 2 BN(к) + 507, 5 к. Дж 2 BN(к) + 3/2 О 2 = В 2 О 3 (к) + N 2(Г)+ 754 к. Дж 2)Возможна ли реакция при 298 К : 2 B(к) + 3/2 О 2 = В 2 О 3 (к) 3) Возможно ли состояние равновесия в системе 2 B(к) + 3/2 О 2 = В 2 О 3 (к)
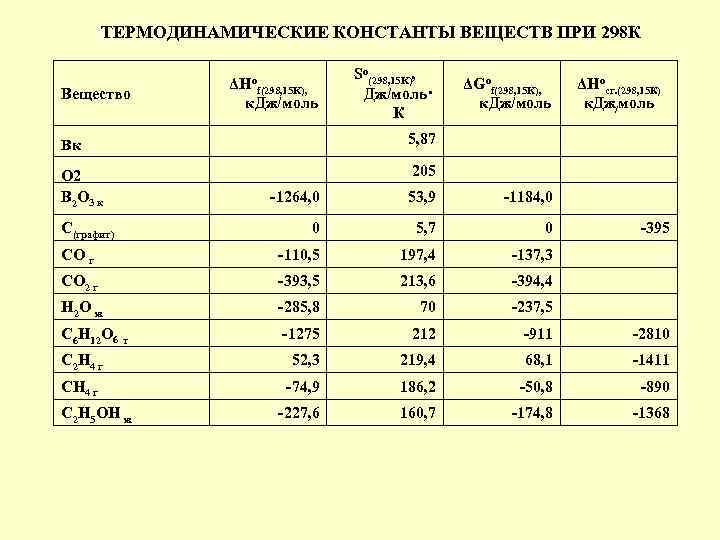
ТЕРМОДИНАМИЧЕСКИЕ КОНСТАНТЫ ВЕЩЕСТВ ПРИ 298 К Вещество ΔНоf(298, 15 K), к. Дж/моль So(298, 15 K), Дж/моль· К Вк ΔНосг. (298, 15 К) к. Дж/моль 5, 87 О 2 В 2 О 3 к ΔGof(298, 15 K), к. Дж/моль 205 -1264, 0 53, 9 -1184, 0 0 5, 7 0 СО г -110, 5 197, 4 -137, 3 СО 2 г -393, 5 213, 6 -394, 4 Н 2 О ж -285, 8 70 -237, 5 С 6 Н 12 О 6 т -1275 212 -911 -2810 С 2 Н 4 г 52, 3 219, 4 68, 1 -1411 СН 4 г -74, 9 186, 2 -50, 8 -890 -227, 6 160, 7 -174, 8 -1368 С(графит) С 2 Н 5 ОН ж -395
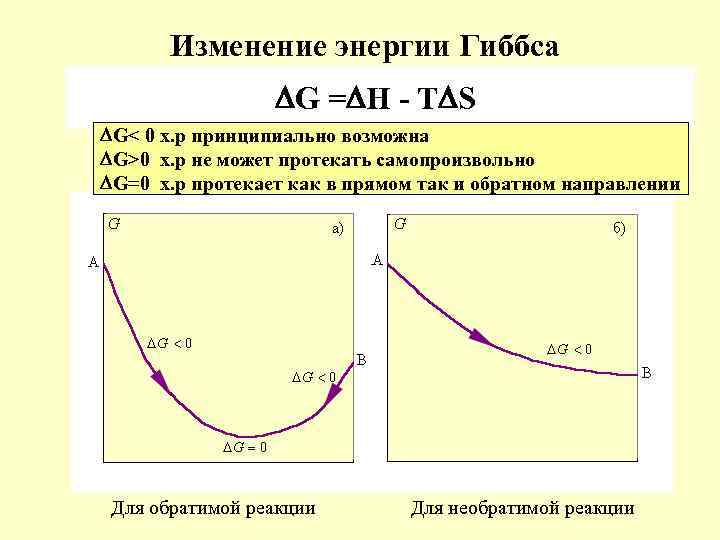
Изменение энергии Гиббса G = H - T S G< 0 х. р принципиально возможна G>0 х. р не может протекать самопроизвольно G=0 х. р протекает как в прямом так и обратном направлении Для обратимой реакции Для необратимой реакции
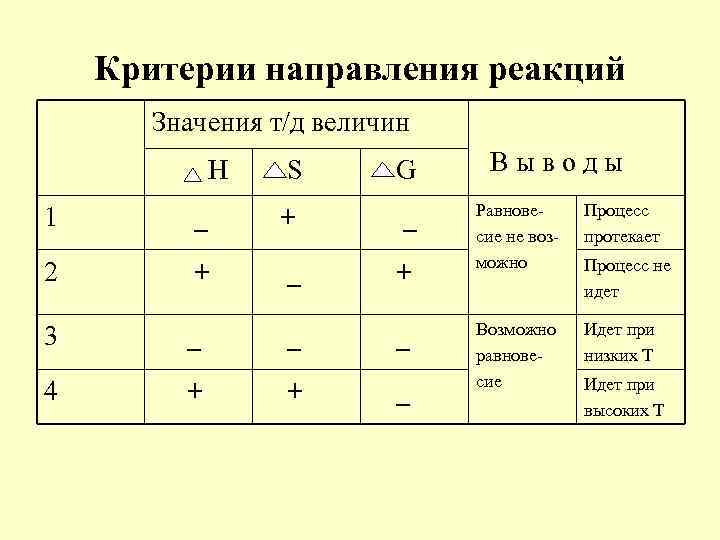
Критерии направления реакций Значения т/д величин Н S G 1 _ + _ 2 + _ + 3 _ _ _ 4 + + _ Выводы Равновесие не возможно Процесс протекает Возможно равновесие Идет при низких Т Процесс не идет Идет при высоких Т

УРОВЕНЬ теоретического ПОНИМАНИЯ МАТЕРИАЛА: 2. 1. Химическая термодинамика 1. не слушал(а) 2. не успевал(а) вникать. Только запись 3. понимаю меньше половины 4. все понятно

2. 2. Химическая кинетика Равновесие Химическая кинетика - учение о скорости химических реакций и о зависимости ее от различных факторов !!! Закон действующих масс Закон Вант-Гоффа Принцип Ле-Шателье

а. А(г) + b. B(г) ↔ l. L(г) + d. D(г) . Закон действующих масс для равновесия:
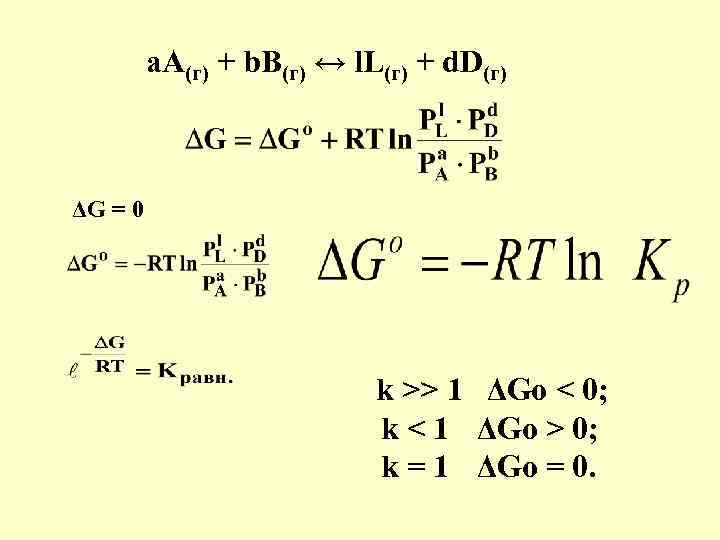
а. А(г) + b. B(г) ↔ l. L(г) + d. D(г) ΔG = 0 k >> 1 ΔGo < 0; k < 1 ΔGo > 0; k = 1 ΔGo = 0.

Закон Вант-Гоффа γ – температурный коэффициент скорости реакции.

Задачи: 1) На сколько градусов необходимо повысить температуру, чтобы скорость реакции увеличилась в 16 раз. Температурный коэффициент равен 2. 2) При 1000 С реакция заканчивается за 32 минуты. Определить время реакции при температуре 1500 С. Температурный коэффициент равен 2.

Принцип Ле-Шателье: если на равновесную систему оказывать внешнее воздействие, то равновесие смещается в сторону, противодействующую этому воздействию.

Задачи: 1)Определить направление смещения равновесия в системе: 2 SO 2 + O 2 2 SO 3 + 192, 7 к. Дж при повышении температуры, увеличении давления и содержания кислорода 2) Как изменится скорость прямой и обратной реакции. Куда сместится равновесие ? 3) Реакции в растворах электролитов: изменится ли значение р. Н раствора при добавлении солей Nа. CI или СН 3 СООNa к раствору уксусной кислоты СН 3 СООН СН 3 СОО- + Н+ 4) Гетерогенные равновесия: Ш выпадет ли осадок, если: дана концентрация ионов в растворе, объемы и концентрация растворов, которые смешиваются и т. д. Ш концентрация ионов в насыщенном растворе трудно растворимого соединения составляет…. . Ш Растворится ли осадок, если к нему добавить….

УРОВЕНЬ ПОНИМАНИЯ теоретического МАТЕРИАЛА: 2. 2. Химическая кинетика. Равновесие 1. не слушал(а) 2. не успевал(а) вникать. Только запись 3. понимаю меньше половины 4. все понятно

УРОВЕНЬ ПОНИМАНИЯ теоретического МАТЕРИАЛА: 2. 3. Свойства растворов электролитов слабые ( 3 %); средние (3 < 33 %); сильные ( > 33 %). Сильные: Na. Cl Na+ + Cl. HCl H+ + Cl- Слабые: CН 3 СООН Н+ + CН 3 СОО- Закон Оствальда !!! р. Н = - lg C H+ р. Н = 0, 5( р. К + р. Ск )

Типы задач 1) Рассчитайте С Н+ и р. Н следующих растворов: а) 0, 01 М НС 1; б) 0, 01 М СН 3 СООН. Как изменится р. Н при 100 кратном разбавлении? , р. К = 4, 76. Решение: а) НС 1 → Н+ + С 1 - (кислота сильная), = 1 р. Н 1 = р. Ск = -lg 0, 01 = 2 При разбавлении раствора в 100 раз Ск в 100 раз уменьшается. р. Н 2 = р. Ск = -lg 10 -4 = 4 Ответ: р. Н увеличится на 2 единицы. б) СН 3 СООН ↔ Н+ + СН 3 СООС Н+ = ∙Ск р. Н 1 =1/2( р. К + р. Ск ) = 1/2 (4, 76 + lg 0, 01) = 3, 4 р. Н 2 = 1/2(4, 76 + lg 10 -4) = 4, 4 При разбавлении в 100 раз Ск в 100 раз уменьшится. Ответ: р. Н увеличится на единицу.

2. 3. Свойства растворов электролитов 1. не слушал(а) 2. не успевал(а) вникать. Только запись 3. понимаю меньше половины 4. все понятно

КОС кислотно-основное состояние определяет соотношение кислоты и щелочи в каком-либо растворе и характеризуется показателем р. Н
Системы, поддерживающие постоянство КОС Выделительная система Буферная система Дыхательная система Кислотнощелочное равновесие

УРОВЕНЬ теоретического ПОНИМАНИЯ МАТЕРИАЛА: 2. 4. Буферные системы

2. 4. Буферные системы 1. не слушал(а) 2. не успевал(а) вникать. Только запись 3. понимаю меньше половины 4. все понятно

Буферные системы 1 типа: слабая кислота+соль сл. к-ты. 2 типа: слабое основание+соль сл. осн.
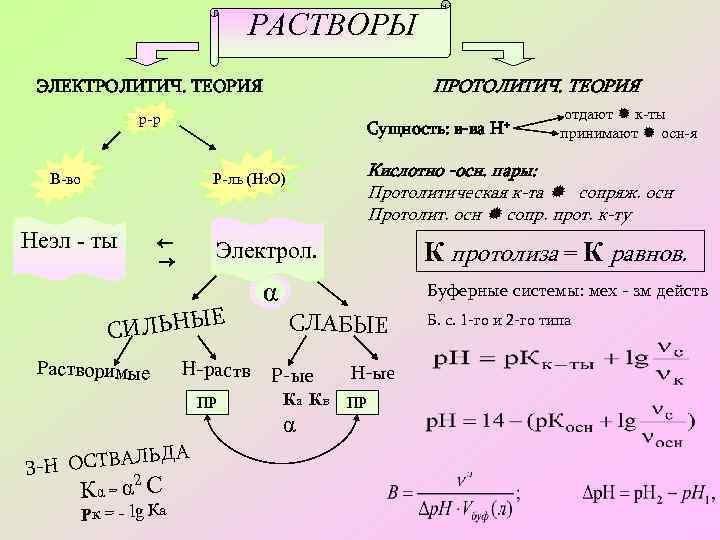
РАСТВОРЫ ПРОТОЛИТИЧ. ТЕОРИЯ ЭЛЕКТРОЛИТИЧ. ТЕОРИЯ р-р Сущность: в-ва В-во Е СИЛЬНЫ Растворимые Н-раств ПР ЛЬД З-Н ОСТВА 2 Кα = α С Рк = - lg Ка К протолиза = К равнов. Электрол. А α отдают к-ты принимают осн-я Кислотно -осн. пары: Протолитическая к-та сопряж. осн Протолит. осн сопр. прот. к-ту Р-ль (H 2 O) Неэл - ты Н+ Буферные системы: мех - зм действ СЛАБЫЕ Р-ые Н-ые Ка Кв ПР α Б. с. 1 -го и 2 -го типа

(2 семестр) УРОВЕНЬ теоретического ПОНИМАНИЯ МАТЕРИАЛА: 2. 5. Поверхностные явления. Адсорбция
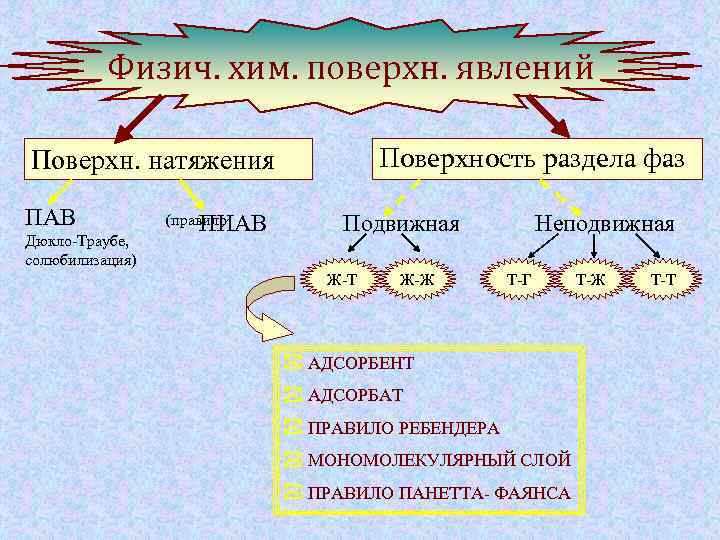
Физич. хим. поверхн. явлений Поверхность раздела фаз Поверхн. натяжения ПАВ Дюкло-Траубе, солюбилизация) (правило ПИАВ Подвижная Ж-Т Ж-Ж Неподвижная Т-Г АДСОРБЕНТ АДСОРБАТ ПРАВИЛО РЕБЕНДЕРА МОНОМОЛЕКУЛЯРНЫЙ СЛОЙ ПРАВИЛО ПАНЕТТА- ФАЯНСА Т-Ж Т-Т

Адсорбция зависит от : Øприроды растворенного вещества, Øконцентрации растворенного вещества, Øтемпературы раствора Изотермы адсорбции Изотермы поверхностного натяжения Для веществ одного и того же гомологического ряда адсорбция и поверхностное натяжение изменяются в соответствии с правилом Дюкло-Траубе
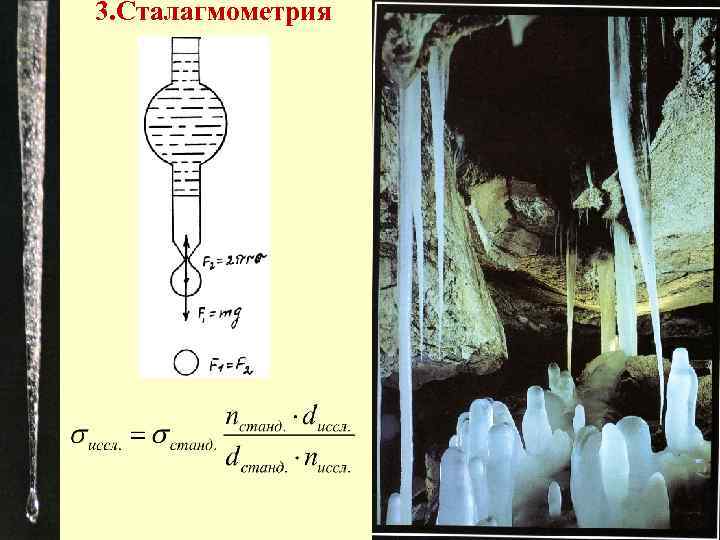
3. Сталагмометрия
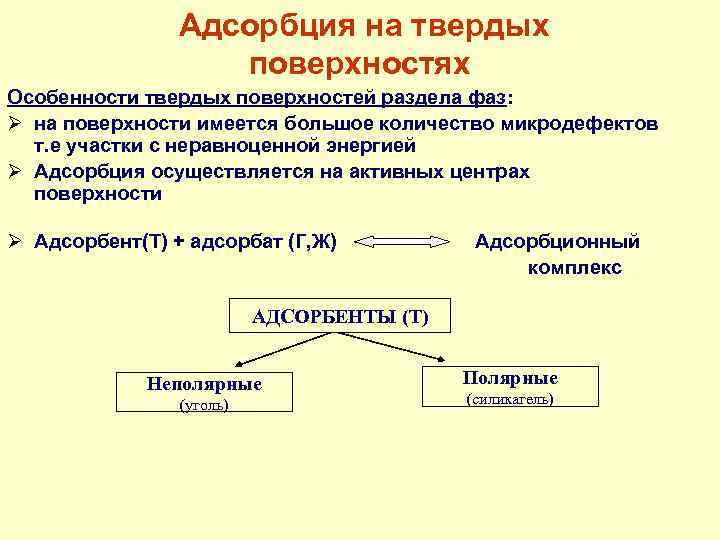
Адсорбция на твердых поверхностях Особенности твердых поверхностей раздела фаз: Ø на поверхности имеется большое количество микродефектов т. е участки с неравноценной энергией Ø Адсорбция осуществляется на активных центрах поверхности Ø Адсорбент(Т) + адсорбат (Г, Ж) Адсорбционный комплекс АДСОРБЕНТЫ (Т) Неполярные (уголь) Полярные (силикагель)
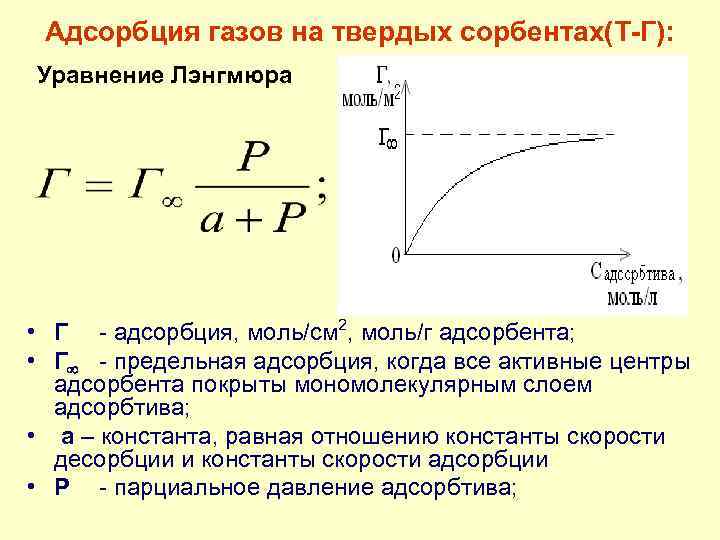
Адсорбция газов на твердых сорбентах(Т-Г): Уравнение Лэнгмюра • Г - адсорбция, моль/см 2, моль/г адсорбента; • Г - предельная адсорбция, когда все активные центры адсорбента покрыты мономолекулярным слоем адсорбтива; • а – константа, равная отношению константы скорости десорбции и константы скорости адсорбции • Р - парциальное давление адсорбтива;
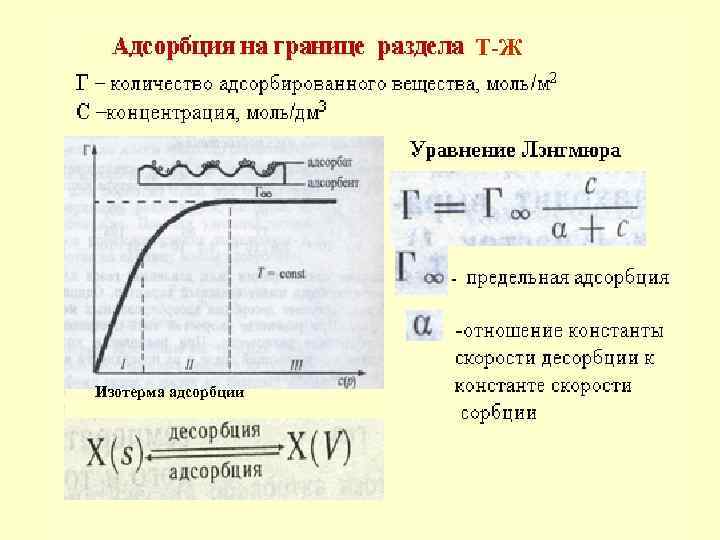
Т-Ж Изотерма адсорбции
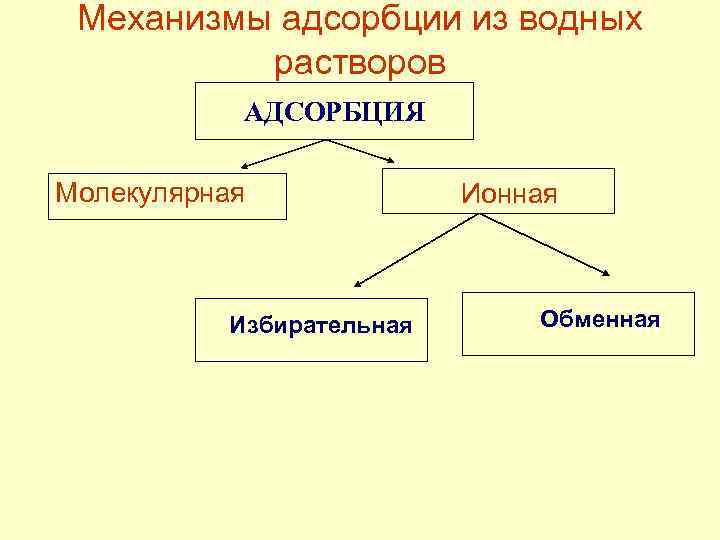
Механизмы адсорбции из водных растворов АДСОРБЦИЯ Молекулярная Избирательная Ионная Обменная
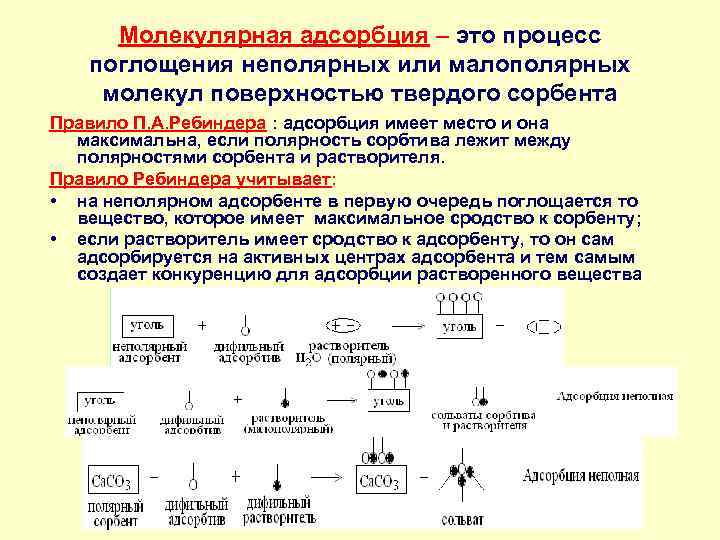
Молекулярная адсорбция – это процесс поглощения неполярных или малополярных молекул поверхностью твердого сорбента Правило П. А. Ребиндера : адсорбция имеет место и она максимальна, если полярность сорбтива лежит между полярностями сорбента и растворителя. Правило Ребиндера учитывает: • на неполярном адсорбенте в первую очередь поглощается то вещество, которое имеет максимальное сродство к сорбенту; • если растворитель имеет сродство к адсорбенту, то он сам адсорбируется на активных центрах адсорбента и тем самым создает конкуренцию для адсорбции растворенного вещества

Ионная адсорбция – это процесс поглощения ионов электролитов на полярных адсорбентах. Избирательная - характерна для сильных электролитов и наблюдается тогда, когда адсорбция какого-либо вещества значительно превосходит адсорбцию других данным сорбентом. Избирательная адсорбция подчиняется правилу Панета-Фаянса: • на поверхности твердого полярного сорбента преимущественно адсорбируются те ионы, которые входят в состав кристаллической решетки адсорбента или близкие к ним по природе и свойствам; • на заряженной поверхности сорбента могут дополнительно поглощаться противоположные по знаку ионы. Схема адсорбции: Ионообменная – ионы растворенного вещества эквивалентно обмениваются на ионы того же знака из сорбента: R OH + Cl- ↔ R Cl + OH 2 R Na + Ca 2+ ↔ R 2 Ca + 2 Na+

УРОВЕНЬ теоретического ПОНИМАНИЯ МАТЕРИАЛА: 2. 5. Поверхностные явления. Адсорбция 1. не слушал(а) 2. не успевал(а) вникать. Только запись 3. понимаю меньше половины 4. все понятно

УРОВЕНЬ теоретического ПОНИМАНИЯ МАТЕРИАЛА: 2. 6. Дисперсные системы. Физико-химические свойства

Классификация дисперсных систем Дисперсная система – это система, состоящая из дисперсной фазы (ДФ) дисперсионной среды (ДС): • Ø • • • ДФ: Размер частиц: ГДС: >10 -7 м, КДС: 10 -7 – 10 -9 м Истинные растворы НМС(М<5000 г/моль): 10 -10 – 10 -12 м; ВМС(М>5000 г/моль): 10 -7 – 10 -9 м Ø Структурные свойства: • ДФ-подвижна (свободнодисперсные системы): суспензии, эмульсии, кровь, аэрозоли(туман, дым, пыль) • ДФ-неподвижна (связанодисперсные): студни, волокнистые и пористые капиллярные системы, костная ткань, биологические мембраны, вещество мозга, мышцы. ДФ + ДС ДФ+ДС: Ø Характер взаимодействия: • Лиофобные (греч. «лиос» -жидкость, «фобио» -ненавижу)- слабое взаимодействие (термодинамически неустойчивы, требуется стабилизатор), • Лиофильные (греч. «филио» -люблю) сильное взаимодействие, образуются самопроизвольно, термодинамически устойчивы, стабилизатор не требуется (растворы белков, полинуклеиновых кислот) Ø Агрегатное состояние ДФ / ДС: • Т/Т, Ж, Г, • Ж/Т, Ж, Г • Г/Т, Ж Истинные растворы – это однофазные гомогенные системы, состоящие из двух и более компонентов

Факторы, влияющие на набухание: Ø Природа ВМС: плохо набухают полимеры с небольшой молекулярной массой и сферическими молекулами Ø Температура: на 1 ст. – выделяется тепло, поэтому процесс лучше идет при низких температурах, 2 ст. – повышение температуры способствует набуханию Ø р. Н: минимальное набухание в ИЭТ Ø Электролиты: если ионы электролитов, связывающие «свободную» воду в собственных гидратных оболочках, не адсорбируются на макромолекулах, например, F- или Li+, то они уменьшают набухание или даже дегидратируют макромолекулы. Напротив, слабо гидратирующиеся и адсорбирующиеся вместе со своими гидратными оболочками ионы, такие как I- и CNS-, увеличивают гидратацию макромолекул и благоприятствуют набуханию

Физико-химические свойства студней(гелей): Ø Тиксотропия- способность разжижаться при механическом воздействии и самопроизвольно восстанавливать свои свойства в состоянии покоя (сотрясение мозга) Ø Синерезис – необратимый процесс старения, который сопровождается сжатием сетки и выделением из нее растворителя (мясо старых животных плотнее) Ø Периодические реакцииобусловлены наличием пространственной сетки, которая препятствует перемешиванию, поэтому Если образуются нерастворимые соли, то они Располагаются в виде колец(кольца Лизеганга) (слоистые камни в почках, печени и. т. д. )
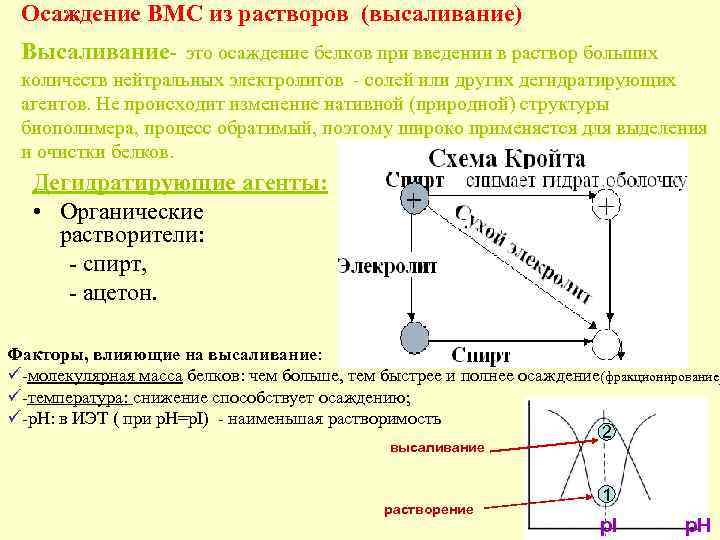
Осаждение ВМС из растворов (высаливание) Высаливание- это осаждение белков при введении в раствор больших количеств нейтральных электролитов - солей или других дегидратирующих агентов. Не происходит изменение нативной (природной) структуры биополимера, процесс обратимый, поэтому широко применяется для выделения и очистки белков. Дегидратирующие агенты: • Органические растворители: - спирт, - ацетон. • Растворы солей Факторы, влияющие на высаливание: ü-молекулярная масса белков: чем больше, тем быстрее и полнее осаждение(фракционирование) ü-температура: снижение способствует осаждению; ü-р. Н: в ИЭТ ( при р. Н=р. I) - наименьшая растворимость 2 высаливание растворение 1 pl p. H
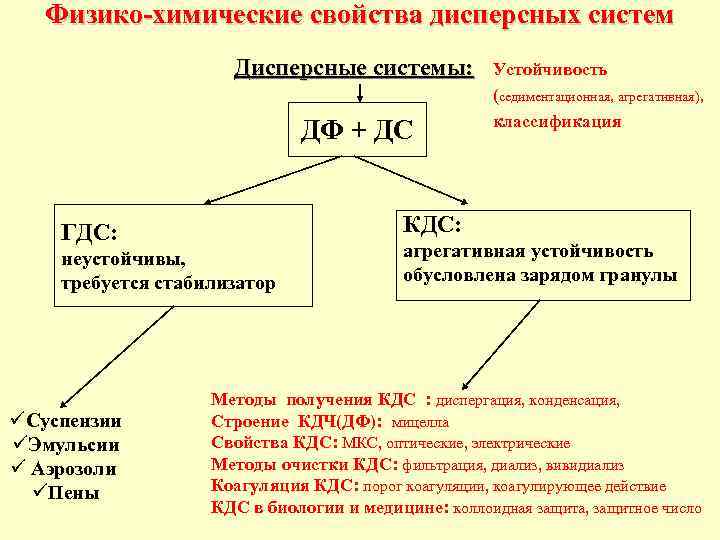
Физико-химические свойства дисперсных систем Дисперсные системы: ДФ + ДС КДС: ГДС: неустойчивы, требуется стабилизатор üСуспензии üЭмульсии ü Аэрозоли üПены Устойчивость (седиментационная, агрегативная), классификация агрегативная устойчивость обусловлена зарядом гранулы Методы получения КДС : диспергация, конденсация, Строение КДЧ(ДФ): мицелла Свойства КДС: МКС, оптические, электрические Методы очистки КДС: фильтрация, диализ, вивидиализ Коагуляция КДС: порог коагуляции, коагулирующее действие КДС в биологии и медицине: коллоидная защита, защитное число
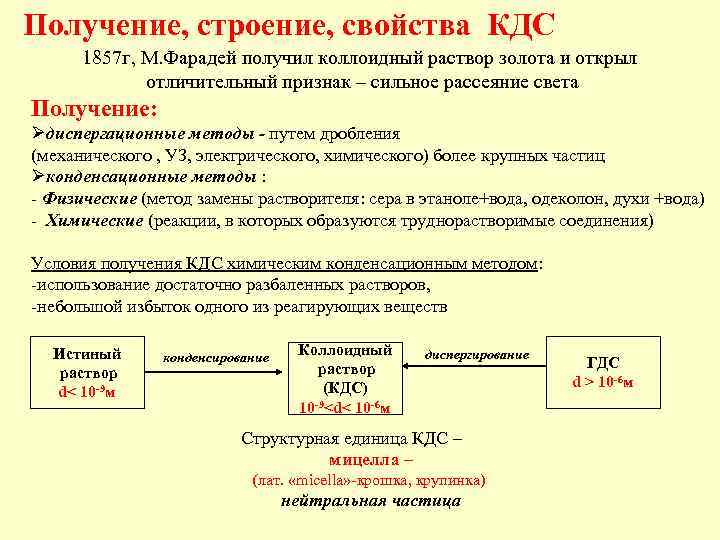
Получение, строение, свойства КДС 1857 г, М. Фарадей получил коллоидный раствор золота и открыл отличительный признак – сильное рассеяние света Получение: Øдиспергационные методы - путем дробления (механического , УЗ, электрического, химического) более крупных частиц Øконденсационные методы : - Физические (метод замены растворителя: сера в этаноле+вода, одеколон, духи +вода) - Химические (реакции, в которых образуются труднорастворимые соединения) Условия получения КДС химическим конденсационным методом: -использование достаточно разбаленных растворов, -небольшой избыток одного из реагирующих веществ Истиный раствор d< 10 -9 м конденсирование Коллоидный раствор (КДС) -9<d< 10 -6 м 10 диспергирование Структурная единица КДС – мицелла – (лат. «micella» -крошка, крупинка) нейтральная частица ГДС d > 10 -6 м
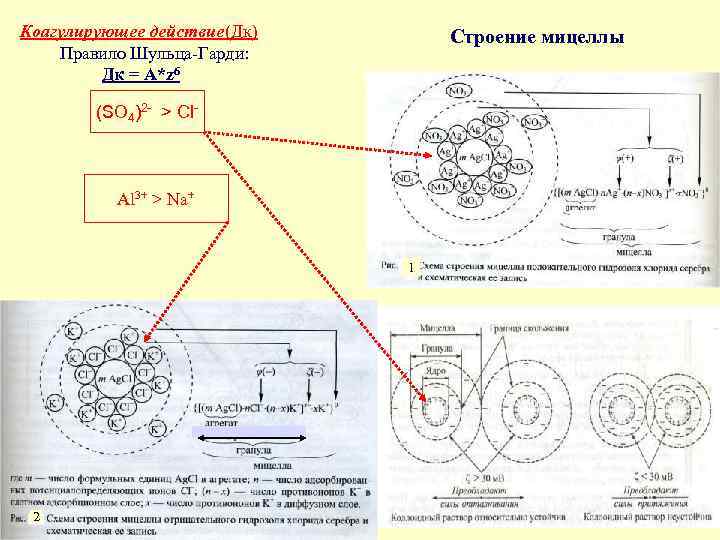
Коагулирующее действие(Дк) Правило Шульца-Гарди: Дк = А*z 6 Строение мицеллы (SO 4)2 - > Cl- Al 3+ > Na+ 1 2

Физико-химические свойства дисперсных систем Коллигативные свойства – это свойства дисперсных систем, которые зависят от концентрации, величины и формы частиц, но не зависят от природы частиц дисперсной фазы

Осмос в дисперсных системах • Осмос – это диффузия растворителя через полупроницаемую мембрану в раствор с большей концентрацией • Осмотическое давление это величина гидравлического давления, которое необходимо приложить к раствору, чтобы осмос прекратился. Уравнение Вант-Гоффа: π = C∙R∙T (для неэлектролитов) 2 - концентрированный раствор 3 - растворитель 4 - мембрана π – осмотическое давление, н/м 2 (Па); С– молярная концентрация, моль/л; R– газовая постоянная(8, 3 Дж/моль∙К); Т– температура, К.

Для электролитов: π = i∙C∙R∙T i - изотонический коэффициент i = 1 + α(n – 1) α – степень ионизации электролита n – число частиц, которые образуются при ионизации

Кипение и замерзание растворов. Закон Рауля. Следствия из закона Рауля Ро > Р Закон Рауля: относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества ΔР = Ро - Р

Следствия из закона Рауля: Первое Ø Для неэлектролитов: Δtкип. = Кэб∙b, Ø для электролитов: Δtкип. = i Kэб. ∙b, b – моляльная концентрация растворенного вещества, моль/кг; i – изотонический коэффициент, Kэб. – эбулиоскопическая константа, К∙кг∙моль-1 Второе Ø Для неэлектролитов: Δtзам. = Ккр. ∙b, Ø для электролитов: Δtзам. = i∙Kкр. ∙b, Δtзам. – понижение температуры замерзания (иногда называют депрессией); i – изотонический коэффициент; Ккр. – криоскопическая константа, К∙кг∙моль-1

УРОВЕНЬ ПОНИМАНИЯ теоретического МАТЕРИАЛА: 2. 6. Дисперсные системы. Физико-химические свойства 1. не слушал(а) 2. не успевал(а) вникать. Только запись 3. понимаю меньше половины 4. все понятно

УРОВЕНЬ теоретического ПОНИМАНИЯ МАТЕРИАЛА: 2. 7. Электрохимические методы исследования в медицине и санитарии • Электрохимические методы исследования: потенциометрия и кондуктометрия. Эти методы используются в медицине для определения различных метаболитов, р. Н биологических жидкостей, в санитарии – для токсикологического контроля и анализа воды (питьевой, для инъекций, очищенной).
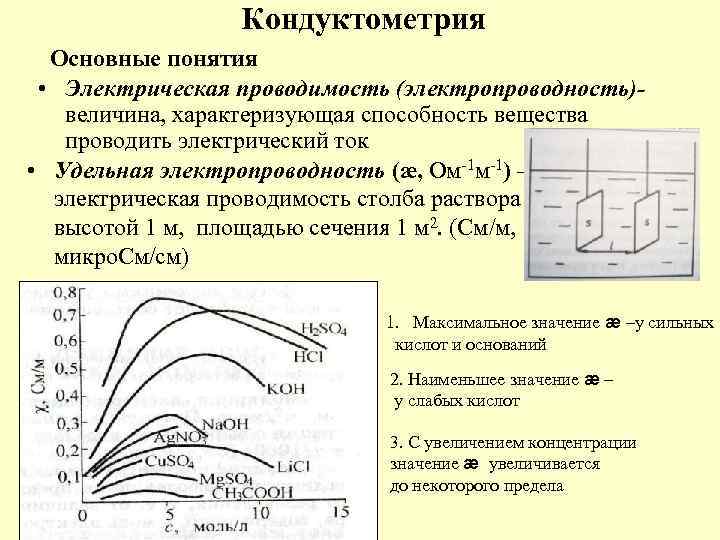
Кондуктометрия Основные понятия • Электрическая проводимость (электропроводность)величина, характеризующая способность вещества проводить электрический ток • Удельная электропроводность (æ, Ом-1 м-1) – электрическая проводимость столба раствора высотой 1 м, площадью сечения 1 м 2. (См/м, микро. См/см) 1. Максимальное значение æ –у сильных кислот и оснований 2. Наименьшее значение æ – у слабых кислот 3. С увеличением концентрации значение æ увеличивается до некоторого предела

Закон Кольрауша: предельная молярная электрическая проводимость данного электролита равна сумме предельных молярных проводимостей ионов, входящих в его состав λ∞ = λК + λА • Предельная молярная электрическая проводимость иона – это количество электричества , перенесенное 1 моль ионов данного типа в бесконечно разбавленном растворе в однородном электрическом поле напряженностью 1 В/м через поперечное сечение раствора площадью 1 м 2 за 1 с. λК = uк*z*q*Na = uк*z*F = 96500*uк*z U – предельная подвижность иона, м 2/(В с); Z - заряд иона; q= 1, 6 *10 -19 Кл – величина элементарного заряда; Na = 6, 02*1023 моль -1 число Авогадро; F= 96 500 Кл/моль – число Фарадея


Потенциометрия- физико-химический метод анализа, позволяющий определять активности(концентрации) ионов на основании измерения э. д. с. гальваническо цепи, состоящей из электрода сравнения и электрода определения, опущенных в исследуемый раствор Классификация электродов по назначению: ü Стандартные или электроды сравнения ü Индикаторные или электроды определения

Электрические явления при химических реакциях. Потенциометрия Механизмы возникновения потенциалов Ø Электродный Ø Окислительно-восстановительный (редокс потенциал) Ø Диффузионный Ø Мембранный

Иономер «Анион -4100»

УРОВЕНЬ ПОНИМАНИЯ теоретического МАТЕРИАЛА: 2. 7. Электрохимические методы исследования в медицине и санитарии 1. не слушал(а) 2. не успевал(а) вникать. Только запись 3. понимаю меньше половины 4. все понятно

3. СЧИТАЕТЕ ЛИ ВЫ НЕОБХОДИМЫМ ПРИМЕНЕНИЕ МУЛЬТИМЕДИЙНЫХ СРЕДСТВ В ЛЕКЦИЯХ: 1. да, лекция должна быть полностью в виде презентации 2. нет, традиционная форма «мел-доска» лучше 3. сочетание: слайды и традиционная форма «мел-доска»

4. ВАШИ ПОЖЕЛАНИЯ ПО ПОВОДУ СОВЕРШЕНСТВОВАНИЯ ЛЕКЦИОННОГО КУРСА:
PF._Obzornaya_lekciya._Belokonova_N.A.ppt