Обзор свойств металлов I II III.ppt
- Количество слайдов: 38

Обзор свойств s- и dэлементов I, III группы ПС.

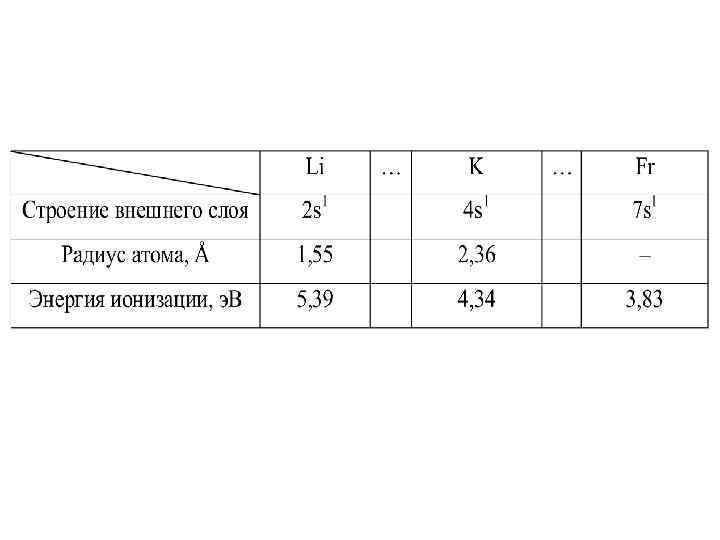
Металлы первой группы главной • Металлы первой группы главной подгруппы называются щелочными. • Гидрооксиды калия и натрия называются щелочами. • Металлы первой группы имеют на внешнем электронном слое один электрон.


Применение металлов. • Литий применяется в ядерной энергетике в качестве теплоносителя. Литий легко соединяется с водородом, азотом, кислородом, серой, и его применяют для удаления следов этих элементов из металлов и сплавов. Литий также применяется в керамике, стекольной промышленности. • Натрий применяют в качестве теплоносителя в ядерной промышленности, а также в металлургии и органическом синтезе. Из соединений натрия самый важный продукт основной химии это гидроксид натрия. Его применяют в мыловарении, в бумажной, текстильной и других отраслях промышленности. Получают Na. OH электролизом раствора Na. Cl. • Калий это аналог натрия. Из соединений калия KOH – используют в синтезе очень ограничено по причине дороговизны. Калий получают электролизом их карналлита (KCl·Mg. Cl 2· 6 H 2 O). Соли калия используют в качестве удобрений.

Окрашивание пламени: Li Алый Na Желтый K Синефиолет овый Бледноголубой Темнокрасны й Cs Rb

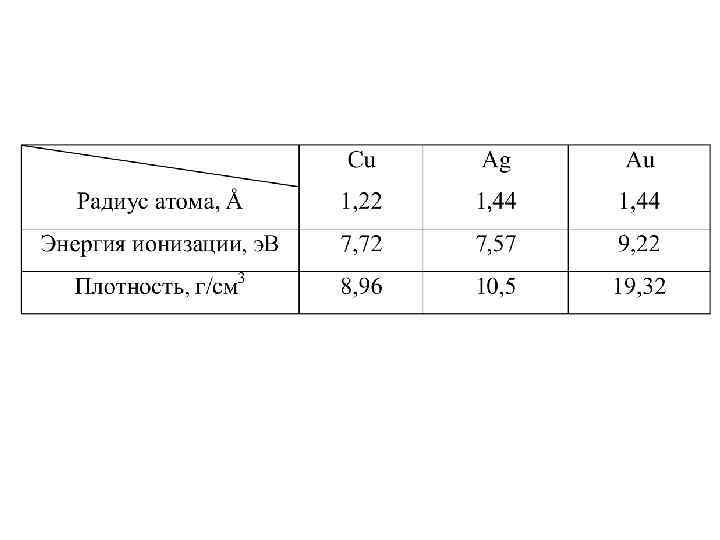
Подгруппа меди (медь, серебро, золото). • Структура двух внешних оболочек атомов изображается формулой: (n-1)s 2(n-1)p 6(n-1)d 10 ns 1 , где n – номер периода. • Все элементы подгруппы меди, на предпоследнем слое имея d электроны, способны образовывать комплексные соединения.

Распространение в земной коре: • медь 0, 01% (вес. ). Иногда в природе встречается в виде самородков; • чаще в виде минералов: медный блеск – Cu 2 S, халькоперит – Cu. Fe. S 2, малахит – (Cu. OH)2 CO 3.
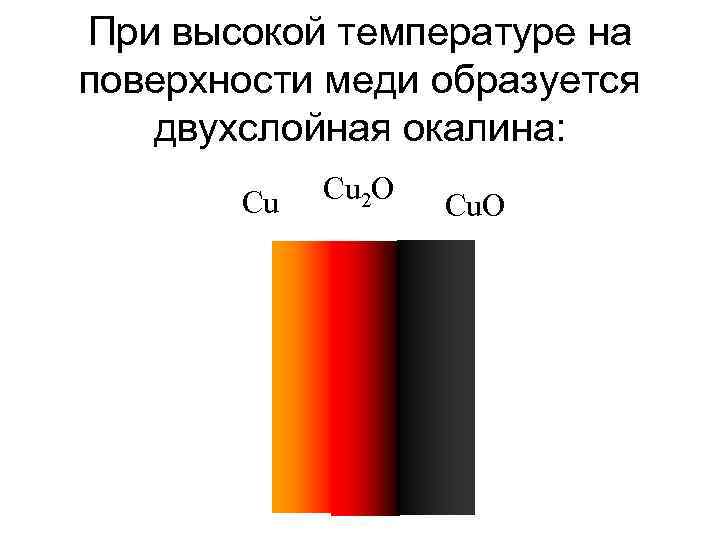
При высокой температуре на поверхности меди образуется двухслойная окалина: Cu Cu 2 O Cu. O

Важнейшие сплавы: • бронза – Cu-Sn (древний сплав), современная бронза с добавками Al, Be; • латунь – Cu-Zn; (Zn 45%) применяются для изготовления труб; • томпак – Cu-Ag; (Cu 80%) имеет цвет золота, применяется для ювелирных изделий; • мельхиор – Cu-Ni; (Ni 20 -30%) применяется для бытовых целей (коррозионно-устойчив); • капель – Cu-Ni-Mn; (Ni 45%, Mn 0, 5%) используется для изготовления термопар.

Свойства меди: • Медь не вытесняет водород из кислот; • в присутствии кислорода воздуха медь растворяется в кислотах по реакции: 2 Cu + 4 HCl + O 2 = 2 Cu. Cl 2 + 2 H 2 O.

Применение: • Все соли меди – ядовиты, поэтому медную посуду покрывают оловом (лудят). • Золото можно растворить в царской водке (смесь соляной и азотной кислот 1: 3): Au + HCl +HNO 3 → H[Au. Cl 4]. • Некоторые композиты из соединений меди, серебра и золота применяют для изготовления катализаторов.
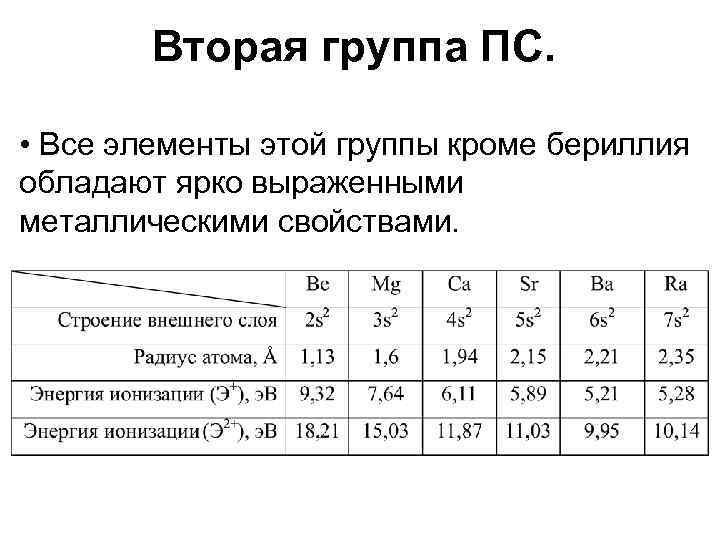
Вторая группа ПС. • Все элементы этой группы кроме бериллия обладают ярко выраженными металлическими свойствами.

Свойства: • Бериллий получают электролизом расплавов его соединений. • Применяют в качестве легирующей добавки в сплавы для придания коррозионной устойчивости. • Соли бериллия – токсичны. • Гидроксид бериллия обладает амфотерными свойствами.

Магний • Магний в природе встречается в виде карбонатов: магнезит – Mg. CO 3; доломит – Mg. CO 3·Ca. CO 3; карналлит – KCl·Mg. Cl 2· 6 H 2 O. • Магний получают электролизом расплава хлористого магния. • Щелочи на магний не действуют • Из кислот магний вытесняет водород. • Магний используется для изготовления сплавов, самый известный сплав – электрон (Mg-Al-Zn). Этот сплав имеет малую плотность 1, 8 г/см 3, применяется в ракетной технике и авиастроении. Чистый магний используется в металлургии для получения титана по реакции: Ti. Cl 4 + 2 Mg = Ti + 2 Mg. Cl 2.


Кальций





Жесткость природных вод. • углекислый газа и вода взаимодействует с известняком по реакции: Ca. CO 3 + CO 2 + H 2 O = Ca 2+ + HCO 3–. • Присутствие ионов кальция и магния определяют жесткость воды – как свойство природной воды.
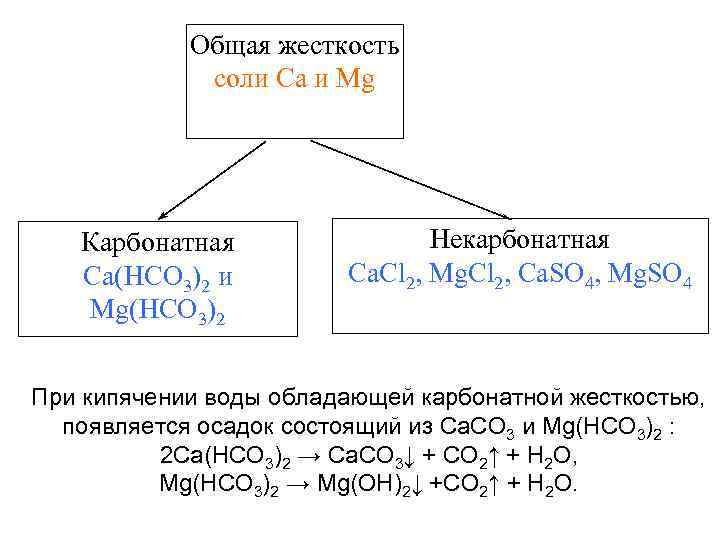
Общая жесткость соли Ca и Mg Карбонатная Ca(HCO 3)2 и Mg(HCO 3)2 Некарбонатная Ca. Cl 2, Mg. Cl 2, Ca. SO 4, Mg. SO 4 При кипячении воды обладающей карбонатной жесткостью, появляется осадок состоящий из Ca. CO 3 и Mg(HCO 3)2 : 2 Ca(HCO 3)2 → Ca. CO 3↓ + CO 2↑ + H 2 O, Mg(HCO 3)2 → Mg(OH)2↓ +CO 2↑ + H 2 O.
Методы умягчение воды. Методы умягчения воды Реагентный метод Ионообменный метод

Реагентный метод основан на удалении ионов кальция и магния в виде осадков Ca. CO 3 и Mg(OH)2.

Метод ионного обмена. • Марки ионитов: АБ 16, АБ 27, КУ-2, пермутит. • Метод ионного обмена применяется, как для умягчения воды, так и для полного ее обессоливание. • Применяется на подводных лодках и в бытовой технике.
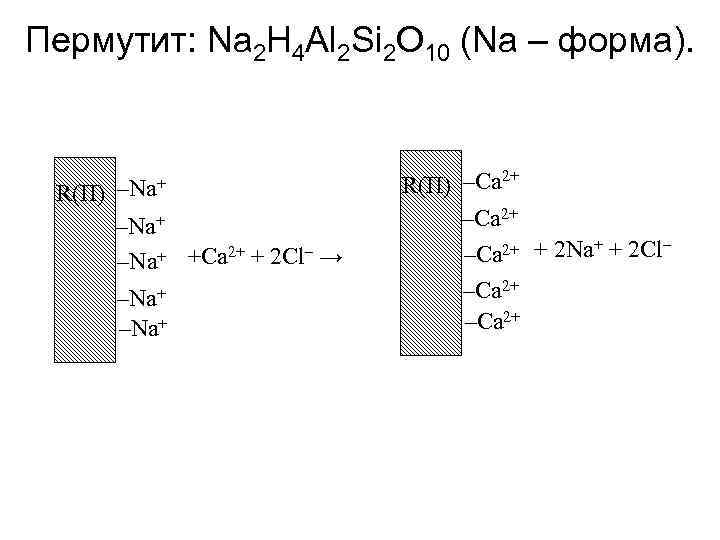
Пермутит: Na 2 H 4 Al 2 Si 2 O 10 (Na – форма). R(П) –Na+ 2+ – –Na+ +Сa + 2 Cl → –Na+ R(П) –Ca 2+ + – –Ca 2+ + 2 Na + 2 Cl –Ca 2+
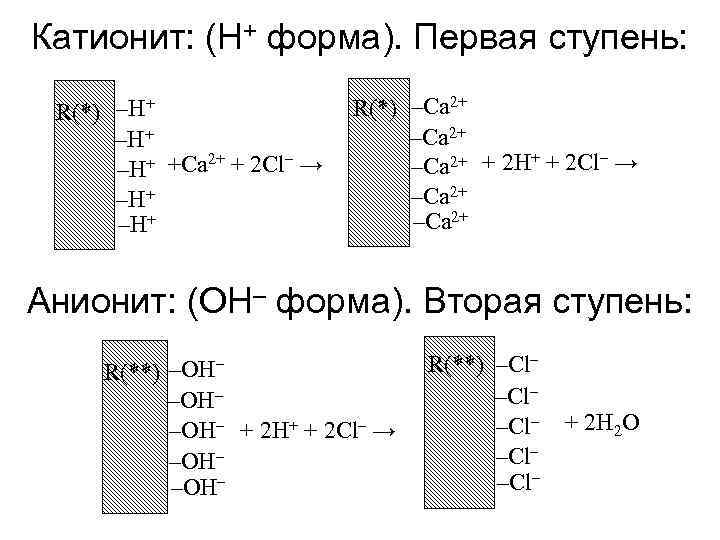
Катионит: (H+ форма). Первая ступень: R(*) –H+ 2+ – –H+ +Сa + 2 Cl → –H+ R(*) –Ca 2+ + 2 H+ + 2 Cl– → –Ca 2+ Анионит: (OH– форма). Вторая ступень: R(**) –OH– + 2 H+ + 2 Cl– → –OH– R(**) –Cl– –Cl– + 2 H 2 O

Третья группа ПС. • Элементы главной группы: B, Al, Ga, In, Tl – имеют электронную формулу ns 2 np 1, где n – номер периода. • В группу входят лантаноиды (57 -71), актиноиды (89 -103). В наружном слое этих элементов три электрона, общая форма оксидов – R 2 O 3.

Бор. • Важные природные соединения – бура (Na 2 B 4 O 7· 10 H 2 O), борная кислота – H 3 BO 3 встречается в минеральной воде. • Получают бор по реакции: B 2 O 3 + 3 Mg = 2 B + 3 Mg. O. • Бор образует не прямым синтезом различные соединения с водородом.
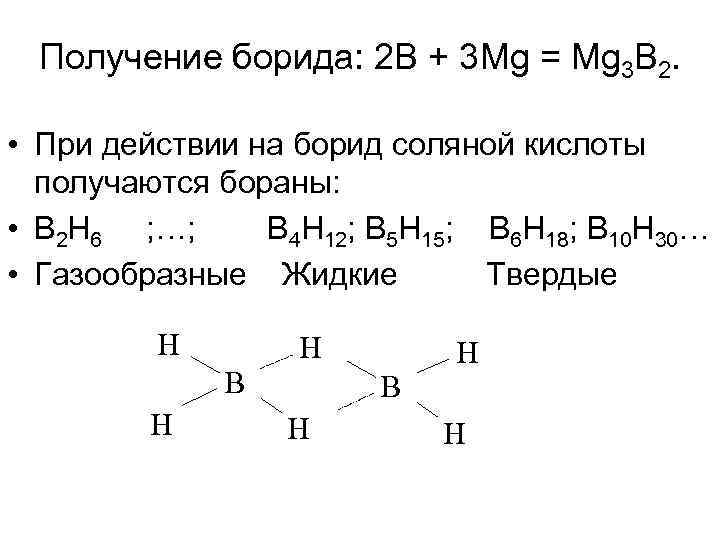
Получение борида: 2 B + 3 Mg = Mg 3 B 2. • При действии на борид соляной кислоты получаются бораны: • B 2 H 6 ; …; B 4 H 12; B 5 H 15; B 6 H 18; B 10 H 30… • Газообразные Жидкие Твердые H B H H H

• При прокаливании бора с углем образуется карбид бора – B 4 C. Его механическая прочность сохраняется при высокой температуре (2350 о. С) обладает высокой твердостью и химической стойкостью. • В промышленности карбид бора называют эльбор. • Применяют для обработки твердых сплавов. • Используется в качестве материала для форсунок в пескоструйках, так как стоек против эрозии.

Алюминий. • Самый распространенный металл в природе – 8%вес. в земной коре. • Основным сырьем для производства алюминия служит боксит, содержащий 32 -60% глинозема (Al 2 O 3). • Металлический алюминий впервые получил Велер в 1827 г. по реакции: 3 K + Al. Cl 3 = Al + 3 KCl.

Алюминий получают из расплава оксида алюминия и криолита (3 Na. F·Al. F 3). • При электролизе на катоде: Al 3+ +3ē → Al. • На угольных анодах происходит разряд ионов кислорода и выделяется свободный кислород по реакции: 2 O 2– – 4ē → O 2. Кислород окисляет углерод анода до CO и CO 2. • При получении алюминия расходуется глинозем, угольные электроды и электричество в количестве 17 -18 тыс. к. Вт ч. на 1 тонну алюминия.

Механизм растворения алюминия в щелочи: 1. стадия. Растворяется защитная пленка по реакции: Al 2 O 3 +2 OH– = 2 Al. O 2– + H 2 O. 2. стадия. Алюминий лишенный защитной пленки взаимодействует с водой по реакции: 2 Al + 6 H 2 O = 2 Al(OH)3 + 3 H 2↑. • Суммарный процесс: 2 Al + Na. OH + 6 H 2 O = 2 Na[Al(OH)4] + 3 H 2↑.

Газобетон. • При взаимодействии алюминиевого порошка с цементным раствором и с известковым раствором получается газобетон по следующей реакции: 2 Al +2 Ca(OH)2 + 6 H 2 O = 3 Ca. O·Al 2 O 3· 6 H 2 O + 3 H 2↑.

Алюмотермия. • Используется для получения металлов Cr, Mn, V из оксидов. В сварочном производстве используется следующая реакция: Fe 2 O 3 + 2 Al = 2 Fe + Al 2 O 3 + 800 ккал. • Алюминий используется в виде сплавов. По объему сплавы алюминия занимают второе место после стали. • Легкие и прочные, коррозионные устойчивые сплавы – дуралюмин (Al-Mg-Cu), силумин – (Al-Si).
Обзор свойств металлов I II III.ppt