RE-NOVATE_RE-MODEL_исследования в ортопедии.ppt
- Количество слайдов: 49

Обзор клинической программы RE-VOLUTION

RE-VOLUTION – Обзор клинической программы Первичная профилактика ВТЭ Лечение ВТЭ Вторичная профилактика кардиальных осложнений у пациентов с ОКС* Профилактика инсульта у пациента с фибрилляцией предсердий Включено более 34 000 пациентов *Фаза II

Введение Дабигатрана этексилат – это новый пероральный, прямой ингибитор тромбина. Он характеризуется: Предсказуемым антикоагулянтным эффектом 1 -3 Возможностью применения в фиксированной дозе Отсутствием необходимости в мониторинге терапии 1 -3 Он представляет собой пролекарство активного компонента дабигатрана, который напрямую связывается с тромбином с высокой афинностью и специфичностью4 -5 1. Eriksson BI et al. Journal of Thrombosis and Haemostasis 2004; 2: 1573– 1580 2. Eriksson BI et al. Journal of Thrombosis and Haemostasis 2005; 3: 103– 111 3. Wallentin L et al. European Heart Journal 2005; 26(suppl): 482. 4. Stassen JM et al. 28 th Congress of the International Society on Thrombosis and Haemostasis; Paris July 6 -12, 2001 5. Hauel NH et al. J Med Chem 2002; 45: 1757 -66

Введение Без проведения профилактики обширные хирургические операции связаны с высоким риском венозных тромбоэмболических осложнений (ВТЭ) Симптомные и бессимптомные тромбозы глубоких вен (ТГВ) после обширных ортопедических операций без проведения профилактики диагностируются до 60% случаев 1 У пациентов, подвергающихся операциям по полной замене тазобедренного сустава (ПЗТС), частота развития ТГВ несмотря на лечение антикоагулянтами в течение 5 -11 дней достигает 20%. 1 Среднее время до развития ВТЭ составляет 9, 7 дней после ПЗКС и 21, 5 дней после ПЗТС 2 По результатам анализа, который включал 43 645 пациентов, ВТЭ были диагностированы после выписки из стационара у 76% больных после замены тазобедренного сустава и у 47% после замены коленного сустава (ПЗКС) р<0, 001). 3 1 2 Warwick D et al. J Bone Joint Surg [Br] 2007; 89: 799 -807 ; Geerts WH et al. Chest 2004; 126: 338 -400; RH et al. Arch Intn Med 1998; 158: 1525 -1531 3 White

Введение По результатам мета-анализа продленная профилактика (30 -42 дня) статистически значимо снижает частоту развития симптомных ВТЭ после ПЗТС 1 Рекомендации АССР (Американская коллегия торакальных врачей) предлагают2: проводить антикоагулянтную профилактику в течение минимум 5 дней после ПЗТС проводить продленную профилактику в течение 28 -35 дней после ПЗТС Неудобства, связанные с инъекциями низкомолекулярного гепарина в домашних условиях, и узкая терапевтическая широта варфарина приводят к тому, что после выписки из стационара лечение оказывается неадекватным Для улучшения качества лечения и профилактики тромбоэмболических осложнений требуются новые антикоагулянты 1 Eikelboom JW et al. Lancet 2001; 358: 9 -15; 2 Geerts WH et al. Chest 2004; 126: 338 -400

Исследование RE-NOVATE Сравнение дабигатрана этексилата и эноксапарина для профилактики венозных тромбоэмболических осложнений после полной замены тазобедренного сустава: рандомизированное, двойное, слепое исследование на эквивалентную эффективность Eriksson BI et al Lancet 2007; 370: 949 -56

Содержание Введение Дизайн Методы Пациенты Процедуры Статистический анализ Распределение пациентов Результаты Эффективность Безопасность Заключение

Дизайн исследования RE-NOVATE - рандомизированное, двойное, слепое исследование на Эноксапарин эквивалентную эффективность Начало вечером накануне операции R Начало через 1 -4 часа после операции 40 мг 1 р. /сут. Дабигатрана этексилат 75 / 150 мг 1 р. /сут. 110 / 220 мг 1 р. /сут. Рандомизация Венография Наблюдение в через 28 – 35 течение 12 -14 дней недель Дабигатрана этексилат и эноксапарин назначали в течение 28 -35 дней после операции Все результаты, связанные с эффективностью и безопасностью, оценивала центральная экспертная комиссия Eriksson BI et al Lancet 2007; 370: 949 -56

Методы – пациенты Критерии включения: Пациенты в возрасте от 18 лет и старше Масса тела минимум 40 кг Пациенты, у которых планируется операция по односторонней полной замене тазобедренного сустава Критерии исключения : Геморрагические диатезы Острые внутричерепные кровоизлияния или геморрагический инсульт в анамнезе Обширные хирургические вмешательства, травмы, неконтролируемая артериальная гипертензия или ИМ в течение предыдущих 3 месяцев Кровотечения из ЖКТ или мочеполового тракта, или язвенная болезнь в течение предшествующих 6 месяцев Тяжелые заболевания печени Уровни АЛТ или АСТ больше 2 х. ВГН в течение предыдущего месяца Тяжелая почечная недостаточность (Cr. Cl<30 мл/мин) Использование НПВП длительного действия Беременность и лактация Аллергические реакции на радиофармпрепараты или гепарин 370: 949 -56 Eriksson BI et al Lancet 2007;

Методы – процедуры Исследование RE-NOVATE проводилось в 115 центрах Европы, Австралии и Южной Африки Первичная конечная точка, характеризующая эффективность: Комбинированный показатель, включающий общее число тромбоэмболических осложнений (ВТЭ) (симптомные или выявленные при венографии ТГВ или симптомная тромбоэмболия легочной артерии [ТЭЛА]) и летальность от любых причин в процессе лечения • Запланированные вторичные конечные точки, характеризующие эффективность: Комбинированный показатель, включающий тяжелые венозные тромбоэмболии (проксимальные ТГВ и ТЭЛА) и летальность, обусловленную тромбоэмболиями Проксимальные ТГВ Отдельные компоненты первичной конечной точки, характеризующей эффективность Eriksson BI et al Lancet 2007; 370: 949 -56

Методы - процедуры Билатеральная венография проводилась в течение 24 часов последнего приема пероральной дозы исследуемого препарата Диагноз ТГВ подтверждали по выявлению стабильного дефекта заполнения в просвете сосуда минимум на двух венограммах Диагноз ТЭЛА подтверждали методами вентиляционноперфузионной сцинтиграфии, ангиографии легких, спиральной КТ грудной клетки или при аутопсии При наличии симптомных ТГВ диагноз подтверждали методом компрессионной ультрасонографии или венографии Результаты диагностических тестов оценивала независимая центральная экспертная комиссия, члены которой не знали о распределении пациентов по группам лечения* *Амстердам, Голландия. Eriksson BI et al Lancet 2007; 370: 949 -56

Методы - процедуры Первичная конечная точка, характеризующая безопасность: Частота развития геморрагических осложнений в процессе лечения Большие геморрагические осложнения, клинически значимые не большие кровотечения и минимальные геморрагические осложнения, включая кровотечения, возникшие во время или после хирургического вмешательства, в соответствии с общепринятыми рекомендациями Оценкой осложнений занималась независимая экспертная комиссия Особое внимание при оценке безопасности уделяли функции Eriksson BI et al Lancet 2007; 370: 949 -56

Определение больших кровотечений * Фатальные кровотечения Кровотечения в жизненно важные органы Клинически значимое снижение уровня гемоглобина более чем на 20 г/л Клинически значимое кровотечение, потребовавшее трансфузии двух или более доз эритроцитной массы или цельной крови Кровотечения, потребовавшие окончания лечения Кровотечения, потребовавшие повторного оперативного вмешательства Включая кровотечения из операционной раны *Определение соответствует рекомендациям Комитета по патентованным лекарственным препаратам. Вопросы к рассмотрению при проведении клинических исследований лекарственных препаратов для профилактики интра- и послеоперационных венозных тромбоэмболических осложнений. Лондон: Европейское агентство по оценке лекарственных препаратов, 29 июня 2000 год. Рекомендации № CPMP/EWP/707/98

Методы – статистический анализ Основывались на предположении, что частота первичной конечной точки, характеризующей эффективность, одинакова в трех группах Согласно расчетам, абсолютное различие в частоте между группами эноксапарина и плацебо составляет 32 -38% (95% ДИ 23, 2 -42, 6) На основании этого, пороговое значение для критерия не меньшей эффективности (noninferiority margin) при оценке различий в риске для первичной конечной точки, характеризующей эффективность, для обеих доз дабигатрана этексилата по сравнению с эноксапарином был установлен на уровне 7, 7%. Eriksson BI et al Lancet 2007; 370: 949 -56
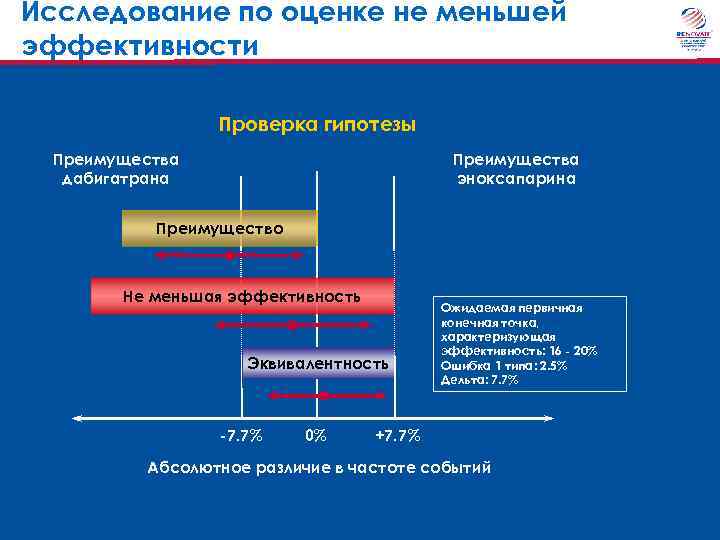
Исследование по оценке не меньшей эффективности Проверка гипотезы Преимущества дабигатрана Преимущества эноксапарина Преимущество Не меньшая эффективность Эквивалентность -7. 7% 0% Ожидаемая первичная конечная точка, характеризующая эффективность: 16 - 20% Ошибка 1 типа: 2. 5% Дельта: 7. 7% +7. 7% Абсолютное различие в частоте событий
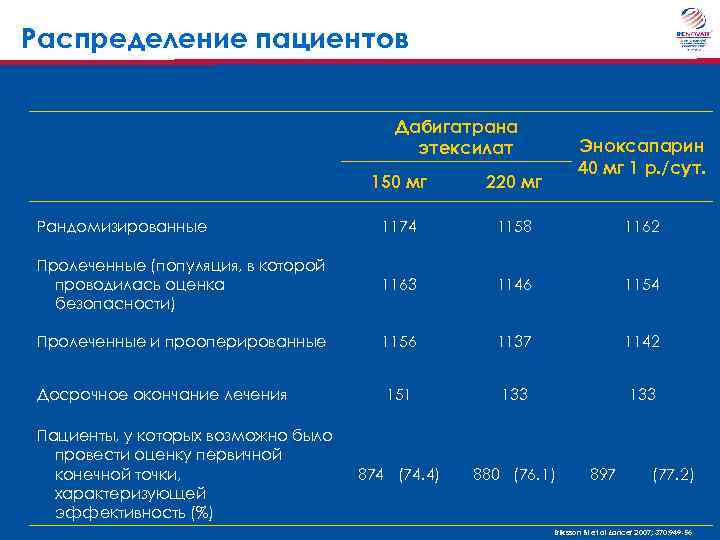
Распределение пациентов Дабигатрана этексилат Эноксапарин 40 мг 1 р. /сут. 150 мг 220 мг Рандомизированные 1174 1158 1162 Пролеченные (популяция, в которой проводилась оценка безопасности) 1163 1146 1154 Пролеченные и прооперированные 1156 1137 1142 Досрочное окончание лечения 151 133 874 (74. 4) 880 (76. 1) Пациенты, у которых возможно было провести оценку первичной конечной точки, характеризующей эффективность (%) 897 (77. 2) Eriksson BI et al Lancet 2007; 370: 949 -56

Исходные характеристики Дабигатрана этексилат 150 мг 220 мг N=1163 Эноксапари н N=1146 40 мг 1 р. /сут. N=1154 Характеристики пациентов Возраст (средний) - годы Женщины - % Все (средний) - кг 63. 4 57 79 64. 6 56 79 63. 8 56 79 24 26 24 Анестезия* Общая - % Назначение исследуемого препарата* Время до первого приема 3. 5 3. 3 3. 4‡ пероральной дозы† (среднее) – ч Длительность пребывания в 9 9 9 стационаре§ (медиана) – дни Длительность лечения (медиана) 33 32 33 - дни * Пролеченная и прооперированная популяция; † После завершения операции; ‡ Доза плацебо; § Время от операции до выписки, данные были получены у 1136, 1155 и 1140 пациентов соответственно. Eriksson BI et al Lancet 2007; 370: 949 -56

Первичная конечная точка, характеризующая эффективность Дабигатрана этексилат Конечная точка 150 мг Эноксапари н 220 мг 40 мг 1 р. /сут. Общая частота ВТЭ и летальность от любых причин 75/874 (8. 6 %) Абсолютное различие в риске по сравнению с эноксапарином 1. 9 % -0. 7 % (-0. 6, 4. 4) (-2. 9, 1. 6) < 0. 0001 (95% ДИ) Значение Р для критерия не меньшей эффективности по сравнению с эноксапарином 53/880 %) (6. 0 60/897 (6. 7 %) - - Eriksson BI et al Lancet 2007; 370: 949 -56

Первичная конечная точка, характеризующая эффективность Пациенты (%) Общая частота ВТЭ или летальности от любых причин P<0. 0001 для критерия не меньшей эффективности Дабигатрана этексилат Статистически значимых различий между обеими дозами дабигатрана этексилата и эноксапарином при сравнении профилактики ВТЭ и частоты летальных исходов от любых причин установлено не et al Lancet 2007; 370: 949 -56 было Eriksson BI

Первичная конечная точка, характеризующая эффективность Преимущество дабигатрана этексилата Преимущество эноксапарина -7. 7% +7. 7% -0. 7 220 мг +1. 9 150 мг Эквивалентность -8% -6% -4% -2% 0 2% 4% 6% 8% Различия в абсолютном риске (дабигатрана этексилат – эноксапарин) Eriksson BI et al Lancet 2007; 370: 949 -56
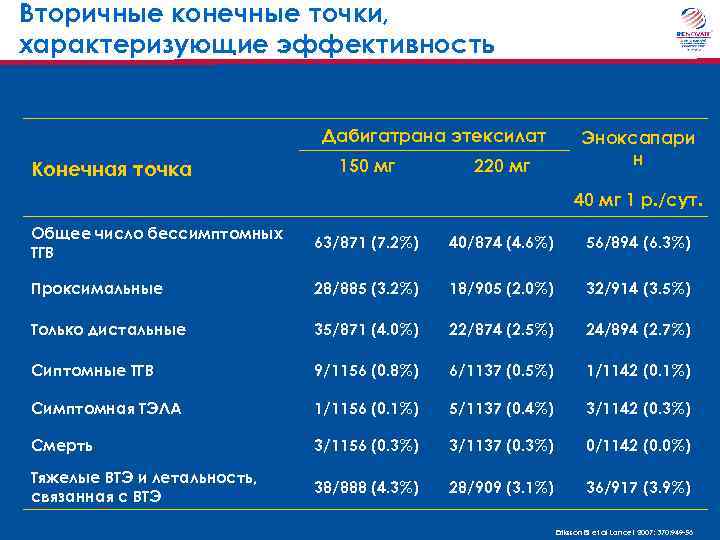
Вторичные конечные точки, характеризующие эффективность Дабигатрана этексилат Конечная точка 150 мг 220 мг Эноксапари н 40 мг 1 р. /сут. Общее число бессимптомных ТГВ 63/871 (7. 2%) 40/874 (4. 6%) 56/894 (6. 3%) Проксимальные 28/885 (3. 2%) 18/905 (2. 0%) 32/914 (3. 5%) Только дистальные 35/871 (4. 0%) 22/874 (2. 5%) 24/894 (2. 7%) Сиптомные ТГВ 9/1156 (0. 8%) 6/1137 (0. 5%) 1/1142 (0. 1%) Симптомная ТЭЛА 1/1156 (0. 1%) 5/1137 (0. 4%) 3/1142 (0. 3%) Смерть 3/1156 (0. 3%) 3/1137 (0. 3%) 0/1142 (0. 0%) Тяжелые ВТЭ и летальность, связанная с ВТЭ 38/888 (4. 3%) 28/909 (3. 1%) 36/917 (3. 9%) Eriksson BI et al Lancet 2007; 370: 949 -56
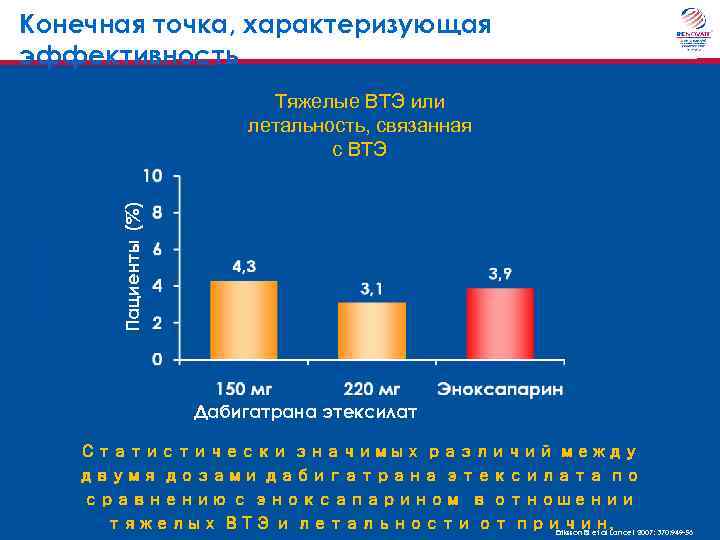
Конечная точка, характеризующая эффективность Пациенты (%) Event Rate (%) Тяжелые ВТЭ или летальность, связанная с ВТЭ Дабигатрана этексилат Статистически значимых различий между двумя дозами дабигатрана этексилата по сравнению с эноксапарином в отношении тяжелых ВТЭ и летальности от причин, 2007; 370: 949 -56 Eriksson BI et al Lancet

характеризующая безопасность – большие кровотечения Пациенты (%) Большие кровотечения Дабигатрана этексилат Статистически достоверных различий между двумя дозами дабигатрана по сравнению с эноксапарином в отношении геморрагических осложнений выявлено не было. Eriksson BI et al Lancet 2007; 370: 949 -56

Конечные точки, характеризующие безопасность – большие кровотечения* Дабигатрана этексилат Конечная точка Эноксапар ин 40 мг 1 р. /сут. 150 мг 220 мг N=1163 N=1146 Большие кровотечения 15 (1. 3%) 23 (2. 0%) 18 (1. 6%) (95% ДИ) (0. 7, 2. 1) (1. 3, 3. 0) (0. 9, 2. 5) Фатальные - n 1 1 0 Кровоизлияния в жизненно важные органы - n 0 0 0 Потребовавшие повторной операции- n 3 2 3 Потребовавшие окончания применения исследуемого препарата- n 1 1 1 Клинически значимое снижение уровне Hb ≥ 2 г/дл - n 12 18 12 Клинически значимое кровотечение, потребовавшее трансфузии ≥ 2 доз - n 8 21 16 *Включая кровотечения из послеоперационной раны Для всех геморрагических осложнений статистически значимых различий между обеими дозами дабигатрана этексилата и эноксапарином выявлено не было N=1154 Eriksson BI et al Lancet 2007; 370: 949 -56

Конечная точка, характеризующая безопасность – большие кровотечения В 51 из 56 случаев (91%) большие кровотечения развились в области послеоперационной раны Большие кровотечения развились до применения первой пероральной дозы препарата у 47% пациентов в группе, где дабигатрана этексилат назначался в дозе 150 мг, у 57% пациентов в группе, где назначалась доза 220 мг, и у 44% пациентов из группы эноксапарина Eriksson BI et al Lancet 2007; 370: 949 -56

Дополнительные конечные точки, характеризующие безопасность Обе дозы дабигатрана характеризуются сходным профилем побочных эффектов по сравнению с эноксапарином Умеренное повышение уровней АЛТ (>3 х. ВГН*) после исходной оценки наблюдалось несколько чаще в группе эноксапарина по сравнению с обеими дозами дабигатрана этексилата Дабигатрана этексилат 150 мг Пациенты (%) 220 мг Эноксапарин 3% 3% 5% Острые коронарные осложнения наблюдались у: Дабигатрана этексилат Пациенты 150 мг 220 мг Эноксапарин В процессе лечения 8 5 9 Наблюдение (после окончания лечения) 0 0 3 *-верхняя граница нормы Eriksson BI et al Lancet 2007; 370: 949 -56

Заключение: У пациентов после полной замены тазобедренного сустава, обе дозы перорального прямого ингибитора тромбина дабигатрана этексилата примени в среднем в течение 33 дней были такими же эффективными, как и назначение эноксапарина для профилактики венозных тромбоэмболических осложнений и обладали сравнимым с эноксапарином профилем безопасности. Было доказано, что дабигатрана этексилат является не менее эффективным по сравнению с эноксапарином при назначении в течение одинакового периода времени для снижения риска всех случаев ВТЭ и летальности от любых причин после операций по полной замене тазобедренного сустава Была показана низкая частота геморрагических осложнений, сходная с эноксапарином Было выявлено отсутствие различий в частоте повышения уровней печеночных ферментов по сравнению с эноксапарином Острые коронарные осложнения возникали редко, и частота их не отличалась от таковой применении эноксапарина, в частности, после окончания лечения Дабигатрана этексилат является новым эффективным, безопасным и удобным методом лечения как в условиях стационара, так и в амбулаторных условиях Eriksson BI et al Lancet 2007; 370: 949 -56

Исследование RE-MODEL Сравнение дабигатрана этексилата и эноксапарина для профилактики венозных тромбоэмболических осложнений после полной замены тазобедренного сустава: рандомизированное исследование RE-MODEL Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.

Содержание Введение Дизайн Методы Пациенты Процедуры Статистический анализ Распределение пациентов Результаты Эффективность Безопасность Заключение
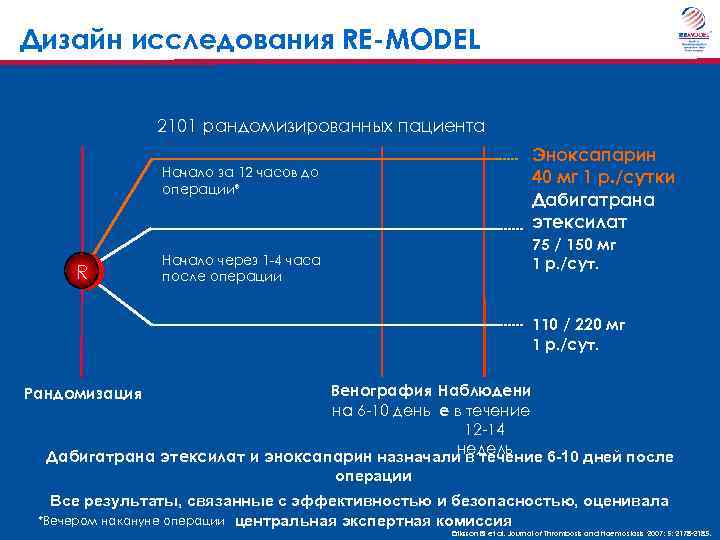
Дизайн исследования RE-MODEL 2101 рандомизированных пациента Начало за 12 часов до операции* R Начало через 1 -4 часа после операции Эноксапарин 40 мг 1 р. /сутки Дабигатрана этексилат 75 / 150 мг 1 р. /сут. 110 / 220 мг 1 р. /сут. Венография Наблюдени на 6 -10 день е в течение 12 -14 недель Дабигатрана этексилат и эноксапарин назначали в течение 6 -10 дней после операции Рандомизация Все результаты, связанные с эффективностью и безопасностью, оценивала *Вечером накануне операции центральная экспертная комиссия Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.

Методы – пациенты Критерии включения: Пациенты в возрасте от 18 лет и старше Масса тела минимум 40 кг Пациенты, у которых планируется операция по односторонней полной замене коленного сустава Критерии исключения : Геморрагические диатезы Острые внутричерепные кровоизлияния или геморрагический инсульт в анамнезе Обширные хирургические вмешательства, травмы, неконтролируемая артериальная гипертензия или ИМ в течение предыдущих 3 месяцев Кровотечения из ЖКТ или мочеполового тракта, или язвенная болезнь в течение предшествующих 6 месяцев Тяжелые заболевания печени Уровни АЛТ или АСТ больше 2 х. ВГН в течение предыдущего месяца Тяжелая почечная недостаточность (Cr. Cl<30 мл/мин) Использование НПВП длительного действия Беременность и лактация Прогрессирующие злокачественные опухоли Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.

Методы – процедуры Исследование RE-MODEL проводилось в 105 центрах Европы, Австралии и Южной Африки Первичная конечная точка, характеризующая эффективность: Комбинированный показатель, включающий общее число тромбоэмболических осложнений (ВТЭ) (симптомные или выявленные при венографии ТГВ или симптомная тромбоэмболия легочной артерии [ТЭЛА]) и летальность от любых причин в процессе лечения • Запланированные вторичные конечные точки, характеризующие эффективность: Комбинированный показатель, включающий тяжелые венозные тромбоэмболии (проксимальные ТГВ и ТЭЛА) и летальность, обусловленную тромбоэмболиями Проксимальные ТГВ Общая частота ВТЭ и летальность от любых причин в процессе Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185. наблюдения

Методы - процедуры Билатеральная венография проводилась в течение 24 часов последнего приема пероральной дозы исследуемого препарата Диагноз ТГВ подтверждали по выявлению стабильного дефекта заполнения в просвете сосуда минимум на двух венограммах Диагноз ТЭЛА подтверждали методами вентиляционноперфузионной сцинтиграфии, ангиографии легких, спиральной КТ грудной клетки или при аутопсии При наличии симптомных ТГВ диагноз подтверждали методом компрессионной ультрасонографии или венографии Результаты диагностических тестов оценивала независимая центральная экспертная комиссия, члены которой не знали о распределении пациентов по группам лечения* *Экспертная комиссия работала в г. Гетенбург, Швеция Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.

Методы - процедуры Первичная конечная точка, характеризующая безопасность: Частота развития геморрагических осложнений в процессе лечения Большие кровотечения, клинически значимые небольшие кровотечения и минимальные геморрагические осложнения, включая кровотечения, возникшие во время или после хирургического вмешательства, в соответствии с общепринятыми рекомендациями Оценкой осложнений занималась независимая экспертная комиссия Особое внимание при оценке безопасности уделяли функции печени Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185

Определение больших кровотечений * Фатальные кровотечения Кровотечения в жизненно важные органы Клинически значимое снижение уровня гемоглобина более чем на 20 г/л Клинически значимое кровотечение, потребовавшее трансфузии двух или более доз эритроцитной массы или цельной крови Кровотечения, потребовавшие окончания лечения Кровотечения, потребовавшие повторного оперативного вмешательства Включая кровотечения из послеоперационной раны *Определение соответствует рекомендациям Комитета по патентованным лекарственным препаратам. Вопросы к рассмотрению при проведении клинических исследований лекарственных препаратов для профилактики интра- и послеоперационных венозных тромбоэмболических осложнений. Лондон: Европейское агентство по оценке лекарственных препаратов, 29 июня 2000 год. Рекомендации № CPMP/EWP/707/98

Методы – статистический анализ Основывались на предположении, что частота первичной конечной точки, характеризующей эффективность, на 1% меньше применении дабигатрана этексилата по сравнению с эноксапарином Частота ВТЭ применении эноксапарина составляет 3048% На основании этого, для оценки первичной конечной точки эффективности для обеих доз дабигатрана этексилата по сравнению с эноксапарином была Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.
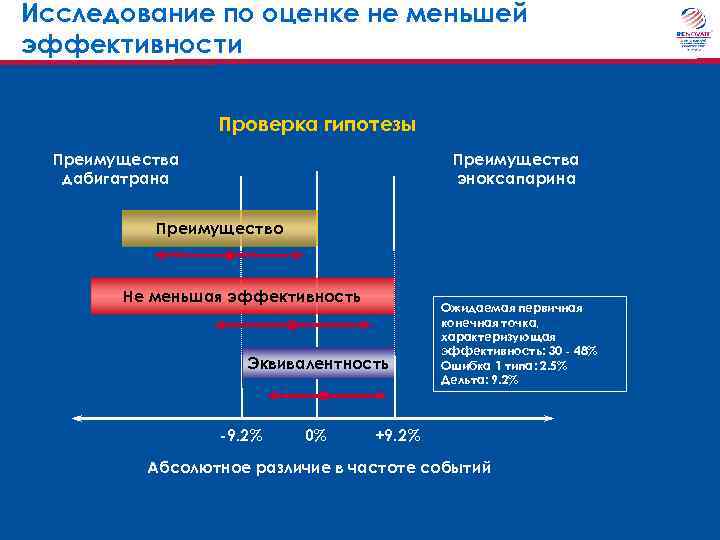
Исследование по оценке не меньшей эффективности Проверка гипотезы Преимущества дабигатрана Преимущества эноксапарина Преимущество Не меньшая эффективность Эквивалентность -9. 2% 0% Ожидаемая первичная конечная точка, характеризующая эффективность: 30 - 48% Ошибка 1 типа: 2. 5% Дельта: 9. 2% +9. 2% Абсолютное различие в частоте событий

Распределение пациентов Дабигатрана этексилат Эноксапарин 40 мг 1 р. /сут. 150 мг 220 мг Рандомизированные 708 694 699 Пролеченные (популяция, в которой проводилась оценка безопасности) 703 679 694 Пролеченные и прооперированные 696 675 685 Досрочное окончание лечения 526 (74. 3) 503 (72. 5) 512 (73. 2) Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.
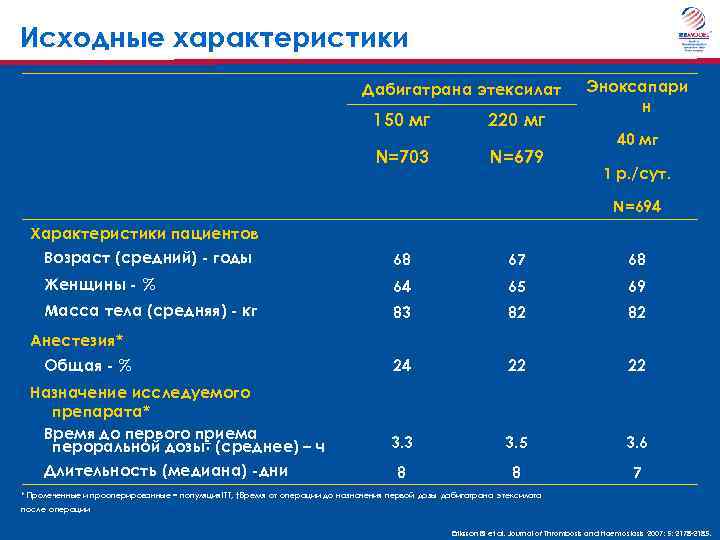
Исходные характеристики Дабигатрана этексилат 150 мг 220 мг N=703 N=679 Эноксапари н 40 мг 1 р. /сут. N=694 Характеристики пациентов Возраст (средний) - годы 68 67 68 Женщины - % 64 65 69 Масса тела (средняя) - кг 83 82 82 24 22 22 3. 3 3. 5 3. 6 8 8 7 Анестезия* Общая - % Назначение исследуемого препарата* Время до первого приема пероральной дозы† (среднее) – ч Длительность (медиана) -дни * Пролеченные и прооперированные = популяция ITT, †Время от операции до назначения первой дозы дабигатрана этексилата после операции Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.

Первичная конечная точка, характеризующая эффективность Дабигатрана этексилат Конечная точка 150 мг Эноксапарин 220 мг 40 мг 1 р. /сут. Общая частота ВТЭ и летальность от любых причин 213/526 (40. 5%) 183/503 (36. 4%) Абсолютное различие в риске по сравнению с эноксапарином 2. 8 % -1. 3 % (-3. 1, 8. 7) (-7. 6, 4. 6) < 0. 017 < 0. 0003 (95% ДИ) Значение Р для критерия не меньшей эффективности по сравнению с эноксапарином 193/512 (37. 7%) - - Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.

Первичная конечная точка, характеризующая эффективность Общая частота ВТЭ или летальности от любых причин P<0. 017 для критерия не меньшей эффективности Пациенты (%) P<0. 0003 для критерия не меньшей эффективности Дабигатрана этексилат Статистически значимых различий между обеими дозами дабигатрана этексилата и эноксапарином при сравнении профилактики ВТЭ и частоты летальных исходов от любых причин установлено не было Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.
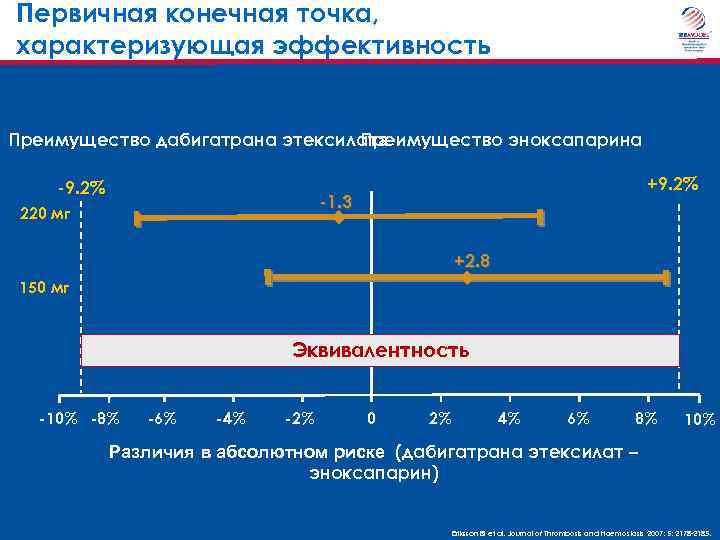
Первичная конечная точка, характеризующая эффективность Преимущество дабигатрана этексилата Преимущество эноксапарина -9. 2% +9. 2% -1. 3 220 мг +2. 8 150 мг Эквивалентность -10% -8% -6% -4% -2% 0 2% 4% 6% 8% 10% Различия в абсолютном риске (дабигатрана этексилат – эноксапарин) Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.

Вторичные конечные точки, характеризующие эффективность Дабигатрана этексилат Конечная точка 150 мг 220 мг Эноксапари н 40 мг 1 р. /сут. Общее число бессимптомных ТГВ 208/524 (39. 7%) 181/503 (36. 0%) 184/511 (36. 0%) 18/525 (3. 4%) 13/506 (2. 6%) 16/510 (3. 1%) 190/524 (36. 3%) 168/503 (33. 4%) 168/511 (32. 9%) Сиптомные ТГВ 3/696 (0. 4%) 1/675 (0. 1%) 8/685 (1. 2%) Симптомная ТЭЛА 1/696 (0. 1%) 0/675 (0. 0%) 1/685 (0. 1%) Смерть 1/696 (0. 1%) 1/675(0. 1%) 1/685 (0. 1%) Тяжелые ВТЭ и летальность, связанная с ВТЭ 20/527 (3. 8%) 13/506 (2. 6%) 18/511 (3. 5%) Проксимальные Только дистальные Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.
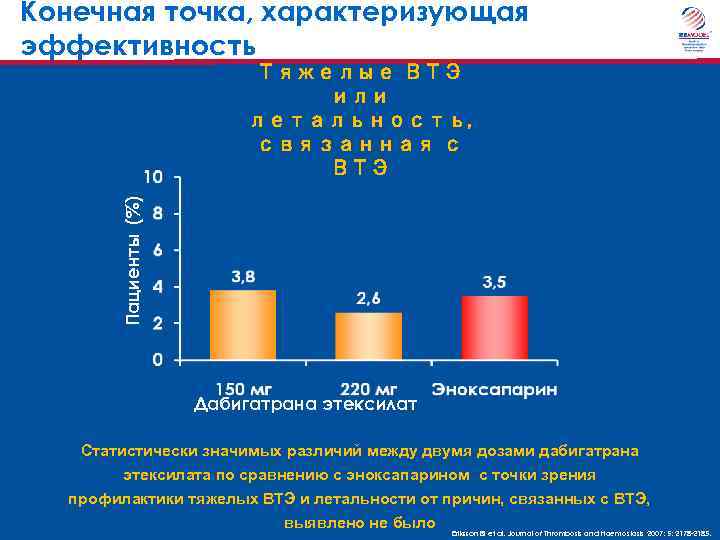
Конечная точка, характеризующая эффективность Пациенты (%) Тяжелые ВТЭ или летальность, связанная с ВТЭ Дабигатрана этексилат Статистически значимых различий между двумя дозами дабигатрана этексилата по сравнению с эноксапарином с точки зрения профилактики тяжелых ВТЭ и летальности от причин, связанных с ВТЭ, выявлено не было Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.
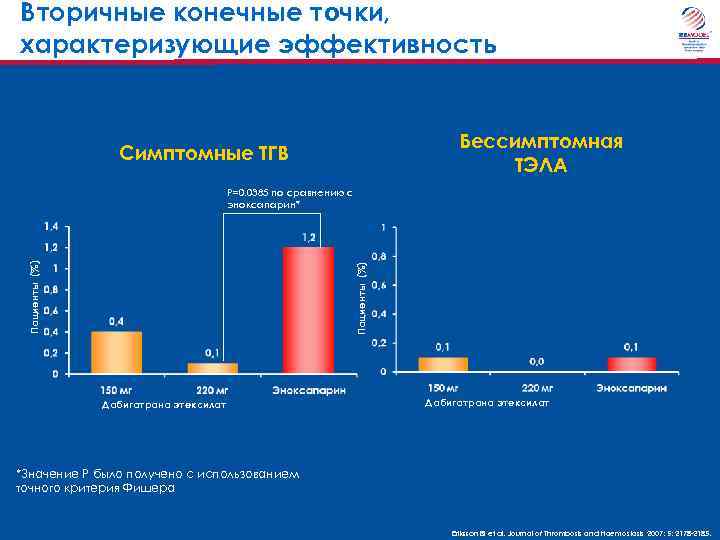
Вторичные конечные точки, характеризующие эффективность Бессимптомная ТЭЛА Симптомные ТГВ Пациенты (%) P=0. 0385 по сравнению с эноксапарин* Дабигатрана этексилат *Значение P было получено с использованием точного критерия Фишера Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.
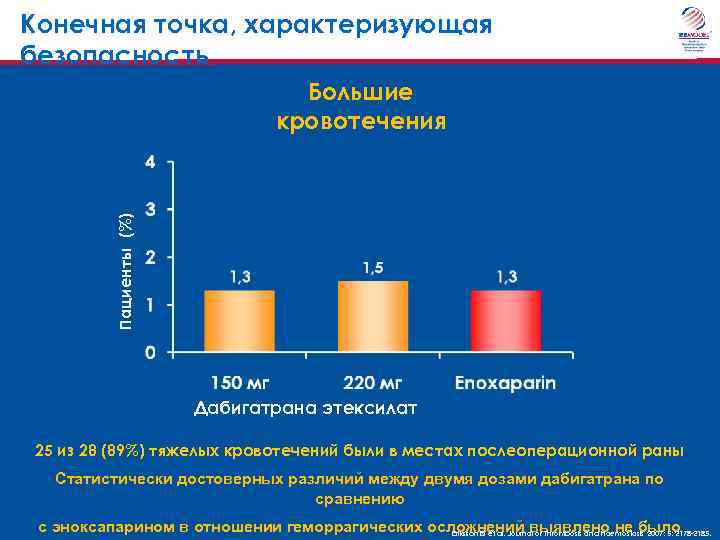
Конечная точка, характеризующая безопасность Пациенты (%) Большие кровотечения Дабигатрана этексилат 25 из 28 (89%) тяжелых кровотечений были в местах послеоперационной раны Статистически достоверных различий между двумя дозами дабигатрана по сравнению с эноксапарином в отношении геморрагических осложнений выявлено не было Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.

Конечные точки, характеризующие безопасность – большие кровотечения * Дабигатрана этексилат 150 мг 220 мг N= 703 Конечная точка N= 679 Эноксапари н 40 мг 1 р. /сут. N= 694 Большие кровотеченияŦ 9 (1. 3%) 10 (1. 5%) 9 (1. 3%) (95% ДИ) (0. 6, 2. 4) (0. 7, 2. 7) (0. 6, 2. 4) 0 0 0 Кровоизлияния в жизненно важные органы - n 1† 0 0 Потребовавшие повторной операции- n 1 3 1 Потребовавшие окончания применения исследуемого препарата- n 0 2 0 Клинически значимое снижение уровне Hb ≥ 2 г/дл - n 7 7 7 Клинически значимое кровотечение, потребовавшее трансфузии ≥ 2 доз - n 6 8 5 Фатальные - n Для всех геморрагических осложнений статистически значимых различий между обеими дозами дабигатрана этексилата и эноксапарином выявлено не было. Включая кровотечения из послеоперационной раны Ŧ 89% тяжелых кровотечений развились в области послеоперационной раны †лекарственный препарат не назначался * Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.
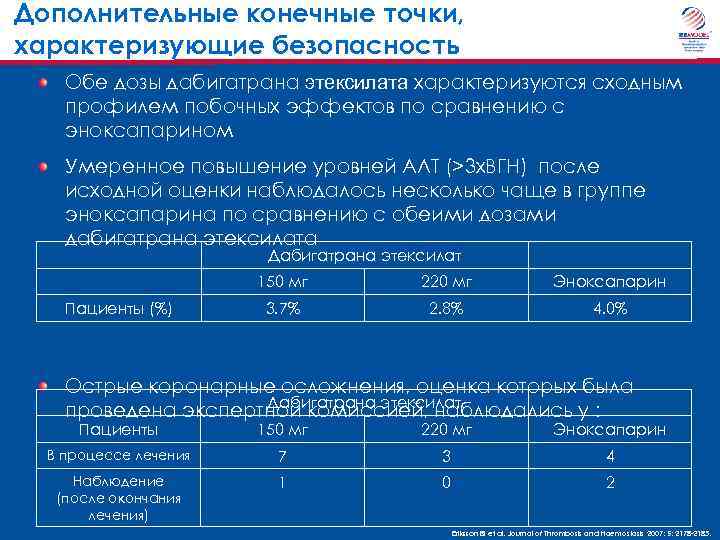
Дополнительные конечные точки, характеризующие безопасность Обе дозы дабигатрана этексилата характеризуются сходным профилем побочных эффектов по сравнению с эноксапарином Умеренное повышение уровней АЛТ (>3 х. ВГН) после исходной оценки наблюдалось несколько чаще в группе эноксапарина по сравнению с обеими дозами дабигатрана этексилата Дабигатрана этексилат 150 мг Пациенты (%) 220 мг Эноксапарин 3. 7% 2. 8% 4. 0% Острые коронарные осложнения, оценка которых была Дабигатрана этексилат проведена экспертной комиссией, наблюдались у : Пациенты 150 мг 220 мг Эноксапарин В процессе лечения 7 3 4 Наблюдение (после окончания лечения) 1 0 2 Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.

Заключение: У пациентов поcле полной замены коленного сустава, обе дозы перорального прямого ингибитора тромбина дабигатрана этексилата примени в течение 6 -10 дней были такими же эффективными, как и назначение эноксапарина для профилактики венозных тромбоэмболических осложнений и обладали сравнимым с эноксапарином профилем безопасности. Было доказано, что дабигатрана этексилат является не менее эффективным по сравнению с назначением эноксапарина в дозе 40 мг 1 р. /сут. на ночь до операции для профилактики ВТЭ после полной замены коленного сустава Была показана низкая частота геморрагических осложнений, сходная с эноксапарином Было выявлено отсутствие различий в частоте повышения уровней печеночных ферментов по сравнению с эноксапарином Острые коронарные осложнения возникали редко, и частота их не отличалась от таковой применении эноксапарина, в частности, после окончания лечения Возможно пероральное применение дабигатрана этексилата в фиксированных дозах без контроля антикоагулянтного эффекта Дабигатрана этексилат является хорошей альтернативой эноксапарину для профилактики ВТЭ после полной замены коленного сустава, которая характеризуется хорошей переносимостью Eriksson BI et al. Journal of Thrombosis and Haemostasis 2007; 5: 2178 -2185.
RE-NOVATE_RE-MODEL_исследования в ортопедии.ppt