ОБЩИЕ ТРЕБОВАНИЯ GMP К КВАЛИФИКАЦИИ И ВАЛИДАЦИИ Директор


ОБЩИЕ ТРЕБОВАНИЯ GMP К КВАЛИФИКАЦИИ И ВАЛИДАЦИИ Директор по качеству – Уполномоченное лицо Заболотная Элла Вадимовна ГП «Межведомственный научный центр криобиологии и криомедицины НАН и АМН МОЗ Украины»

ЦЕЛИ Название предприятия и отдела 2 2 Основы квалификации и валидации Виды валидации и основные общие требования Введение в валидацию очистки Валидация компьютеризированных систем

ВАЛИДАЦИЯ Отдел проверки соответствия GMP 3 ■ Принцип Доказательства, в соответствии с принципами надлежащей производственной практики, что все методики, процессы, действия персонала, функционирование систем действительно отвечают своему предназначению и ведут к ожидаемым результатам. Гарантия постоянного рутинного производства лекарственных средств надлежащего качества в соответствии со спецификациями

КВАЛИФИКАЦИЯ Отдел проверки соответствия GMP 4 ■ Принцип Доказательство того, что все оборудование и системы обеспечения надлежащим образом смонтированы, правильно функционируют и действительно приводят к ожидаемым результатам. Квалификация является частью валидации

КВАЛИФИКАЦИЯ, ВАЛИДАЦИЯ Отдел проверки соответствия GMP 5 ■ Сфера применения ● оборудование ● помещения ● системы ● технологический процесс ● процедуры очистки ● аналитические методики ● компьютеризированные системы

ВАЛИДАЦИЯ Отдел проверки соответствия GMP 6 ■ Когда необходима валидация ● Внедрение новых средств производства, контроля качества, систем обеспечения производства ● Внедрение новых лекарственных средств ● Изменения в средствах производства, системах обеспечения, технологии, методиках ● Переодическая проверка функционирования (критическая ревалидация)

ВАЛИДАЦИЯ Отдел проверки соответствия GMP 7 ♦ Подход ▪ оценка рисков ▪ Фармацевтическая разработка ▪ Подбор средств для валидации ▪ Планирование

ВАЛИДАЦИЯ Отдел проверки соответствия GMP 8 ■ Планирование ● Охват всей деятельности, связанной с валидацией ● Составление основного плана валидации предприятия (мастер-план) ● Составление планов валидации для отдельных составляющих

ВАЛИДАЦИЯ Отдел проверки соответствия GMP 9 ●Планирование. Основной план валидации ● Общая информация (вступление) ♦политика валидации ♦цель данного плана ♦общие сведения о предмете валидации (предприятие, участок, система и т.д.) ● Организационная структура деятельности, связанной с валидацией ♦персонал (ответственность, распределение обязанностей, составление документации, согласование, утверждение)

ВАЛИДАЦИЯ Отдел проверки соответствия GMP 10 ●Основной план валидации ♦описание технических средств, Систем, оборудования, процессов, которые подлежат валидации (виды валидации, описание, критерии приемлемости) ▪Помещения ▪ Технологическое оборудование, технологические системы ▪ Основные и вспомогательные системы обеспечения производства ▪ Технологические процессы ▪ Контроль качества, аналитические методики очистки

ВАЛИДАЦИЯ Отдел проверки соответствия GMP 11 Основной план валидации Формы документации (форма, содержание, оформление, подписание и утверждение) План Протоколы Отчеты Планирование, графики, схемы Порядок проведения Сроки Контроль изменений, отклонения, несоответствия Документация, перекрестные ссылки, сокращения

ВАЛИДАЦИЯ Документация Виды Основной план Протоколы Методики проведения валидационных испытаний Отчеты Отдел проверки соответствия GMP 12

ВАЛИДАЦИЯ Оформление документации Предусмотреть СОП на СОП Соответствие оформления общей системе документации предприятия Соответствующие методики, регламентирующие форму, порядок оформления, подписания, утверждения Прослеживаемость Внутренняя кодификация Ссылки в основном плане План – протоколы и методики - отчеты Отдел проверки соответствия GMP 13

ВАЛИДАЦИЯ Документация Содержание протокола Объект валидации Состав валидационной группы Оборудование, системы, процессы Документация и литература Планирование хода валидации (квалификации) Валидационные испытания Формы для регистрации хода валидационных испытаний и полученных результатов Отдел проверки соответствия GMP 14

ВАЛИДАЦИЯ Документация Содержание протокола Формы для регистрации хода валидационных испрытаний и полученных результатов Цель испытаний Методы испытаний Критерии приемлемости Анализ испытаний Место для внесения результатов и наблюдений Ссылки на необходимые приложения Выводы Отдел проверки соответствия GMP 15

ВАЛИДАЦИЯ Документация Содержание протокола Согласование и утверждение Валидаторы Руководитель группы валидаторов Руководители других структурных подразделений (соответственно с компетенцией) Лицо, которое отвечает за валидацию на предприятии Отдел проверки соответствия GMP 16

ВАЛИДАЦИЯ Документация Отчет ( форма), его согласование и утверждение Подтверждение в отчете выполнения всех запланированных испытаний Виды отчетов Для от дельных испытаний Для отдельных участков, систем Заключительный обобщающий Отдел проверки соответствия GMP 17

ВАЛИДАЦИЯ Документация Содержание заключительного отчета по валидации Объекты Состав группы валидаторов Перекрестные ссылки на соответствующие документы Описание хода валидации Этапы валидации для отдельных объектов (IQ, OQ, PQ) Анализ отклонений Общие выводы Рекомендации в отношении валидации Отдел проверки соответствия GMP 18

ВАЛИДАЦИЯ Документация Отклонения, внесение изменений, расхождения несоответствия Не выполненные испытания Получение негативного результата Осуществление испытаний не в соответствии с прописанными методиками Дополнительные испытания Отдел проверки соответствия GMP 19

ВАЛИДАЦИЯ Составляющие Квалификация проекта (DQ) Квалификация монтажа (IQ) Квалификация функционирования (OQ) Квалификация эксплуатации (PQ) Валидация технологического процесса (PV) Валидация аналитических методик (АV) Валидация методик очистки (СV) Квалификация и валидация работы систем Ревалидация Отдел проверки соответствия GMP 20
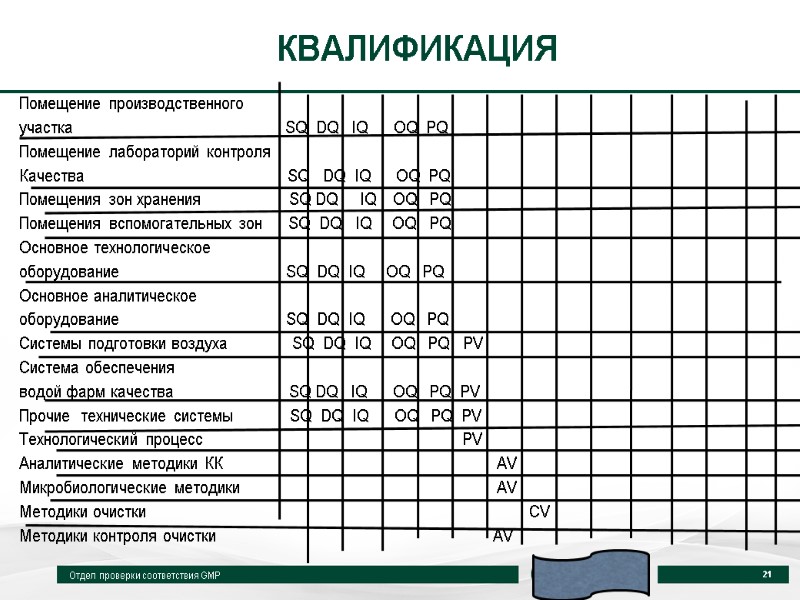
КВАЛИФИКАЦИЯ Помещение производственного участка SQ DQ IQ OQ PQ Помещение лабораторий контроля Качества SQ DQ IQ OQ PQ Помещения зон хранения SQ DQ IQ OQ PQ Помещения вспомогательных зон SQ DQ IQ OQ PQ Основное технологическое oборудование SQ DQ IQ OQ PQ Основное аналитическое oборудование SQ DQ IQ OQ PQ Системы подготовки воздуха SQ DQ IQ OQ PQ PV Система обеспечения водой фарм качества SQ DQ IQ OQ PQ PV Прочие технические системы SQ DQ IQ OQ PQ PV Технологический процесс PV Аналитические методики КК AV Микробиологические методики AV Методики очистки CV Методики контроля очистки AV Отдел проверки соответствия GMP 21

КВАЛИФИКАЦИЯ СПЕЦИФИКАЦИЙ (SQ) SQ (specification qualification), основные задачи Оценка технического задания на проектирование или реконструкцию новых технических средств, систем, оборудования, техническое переоснащение (спецификации требований пользователя – URS, user requirement specification) Предусмотреть возможность соблюдения требований GMP, обеспеченности и надлежащего функционирования технических систем, возможности обеспечения качества продукции Анализ концепции технического задания Оценка полноты информации для возможности последующего правильного и полного проектирования Оценка обеспечения требований GMP при последующем проектировании, монтаже, эксплуатации Отдел проверки соответствия GMP 22

КВАЛИФИКАЦИЯ ПРОЕКТА DQ (design qualification), основные задачи Валидация новых технических средств, систем оборудования Соответствие проекта требованиям GMP, основные элементы Анализ концепции проекта Оценка обеспечения требований GMP после принятия в эксплуатацию Выявление недостатков, неточностей, несоответствий проекта и оценки их влияния на соответствие GMP Отдел проверки соответствия GMP 23

ПРИЕМКА ТЕХНИЧЕСКИХ СИСТЕМ Этапы приемки FAT – factory acceptance tests Заводские приемочные испытания у производителя технической системы SAT – site acceptance tests Приемочные испытания у заказчика Монтаж, квалификация при монтаже (IQ) Использование (внедрение) новых технических средств, систем, оборудования Модификация технических средств, систем, оборудования Позволяет определиться с составлением собственной технической документацией (паспорта0 Отдел проверки соответствия GMP 24

КВАЛИФИКАЦИЯ МОНАЖА (1) Использование (внедрение) новых технических средств, систем, оборудования Модификация технических средств, систем, оборудования Отдел проверки соответствия GMP 25

КВАЛИФИКАЦИЯ МОНТАЖА (2) Основные элементы Документальное подтверждение правильности установки оборудования и систем (в соответствии с проектом), Документальное подтверждение комплектности оборудования (паспортам, проектно-конструкторской документации и т.п.) Подтверждение наличия и достаточности документации на оборудование и системы обеспечения производства, Подтверждение наличия всех необходимых контрольно-измерительных приборов, наличия на них сертификатов калибровки или поверки, Подтверждение соответствия материалов рабочих поверхностей Отдел проверки соответствия GMP 26

КВАЛИФИКАЦИЯ ФУНКЦИОНИРОВАНИЯ (1) Знание процессов, систем, оборудования Основные элементы Испытания на основе знаний Охват верхнего и нижнего пределов рабочих параметров («наихудший случай») Отдел проверки соответствия GMP 27

КВАЛИФИКАЦИЯ ФУНКЦИОНИРОВАНИЯ (2) Основные элементы Проверка функциональных возможностей (параметров) оборудования, Проверка работы элементов управления оборудованием, Проверка работы аварийных систем, Проверка правильности работы оборудования и его систем, Проверка правильности показателей контрольно-измерительных приборов, Проверка производительной мощности, Проверка наличия и правильность составления инструкций по обслуживанию и эксплуатации оборудования Отдел проверки соответствия GMP 28

КВАЛИФИКАЦИЯ ФУНКЦИОНИРОВАНИЯ (3) ■ Предназначение и выводы по результатам квалификации Составление и оформление методик Выполнение процессов Калибровка Очистка Обучение операторов Определение требований к обслуживанию и эксплуатации оборудования Отдел проверки соответствия GMP 29

КВАЛИФИКАЦИЯ ЭКСПЛУАТАЦИИ Знание процессов, систем, оборудования Основные элементы Проверка возможности обеспечения производства продукции необходимого качества или необходимого качества работы систем (проверка качества работы оборудования – качество продукции, которая производится на данном оборудовании) Испытания с использованием материалов, которые используются в производстве или способных моделировать их свойства Испытания с охватом верхнего и нижнего пределов ▪Совмещение с квалификацией функционирования и валидацией технологического процесса Отдел проверки соответствия GMP 30

ВАЛИДАЦИЯ ПРОЦЕССА (1) Классификация Новые технологические процессы Валидация при внесении изменений Ревалидация Отдел проверки соответствия GMP 31

ВАЛИДАЦИЯ ПРОЦЕССА (2) Виды валидации Перспективная валидация (до реализации выпущенной продукции) Сопутствующая валидапция (во время серийного выпуска продукции) Ретроспективная валидация (процессы выполняются в течение какого-то времени, берется от 10 до 30 последовательных серий) Отдел проверки соответствия GMP 32

ВАЛИДАЦИЯ ПРОЦЕССА (3) Общие требования и принципы Технические средства, системы, оборудование должны быть проквалифицированы Аналитические методики должны быть провалидированы Обученный персонал, который принимает участие в валидационных испытаниях Обеспечение периодичности оценки технических средств, систем, оборудования, процессов для подтверждения их правильного функционирования Отдел проверки соответствия GMP 33

ВАЛИДАЦИЯ ПРОЦЕССА (4) Основные элементы Подтверждение правильности регламентированных параметров технологических процессов – обеспечение качества продукции во время выполнения операций техпроцесса; Подтверждение правильности методик (инструкций) по осуществлению операций техпроцесса (соответствие возможностям и предназначению оборудования); Подтверждение возможности оборудования обеспечить соблюдение всех параметров ведения техпроцессов и качества продукта; Подтверждение возможности (способности) персонала обеспечить выполнение (соблюдения) операций техпроцесса; Воспроизводимость (точность воспроизведения) параметров техпроцесса и обеспечение при этом необходимых показателей качества Отдел проверки соответствия GMP 34

ВАЛИДАЦИЯ АНАЛИТИЧЕСКИХ МЕТОДИК (1) Цель Гарантия того, что избранная аналитическая методика обеспечивает воспроизводимые и достоверные результаты, которые отвечают заданной цепи Нормативные требования: ГФУ (ЕР) Правила управления лекарственными средствами в ЕС, том 3А (3АQ13a) Validation of Analytical Procedures used in the Examination of Pharmaceutical Materials (WHO Technical Report Series, N823) Отдел проверки соответствия GMP 35

ВАЛИДАЦИЯ АНАЛИТИЧЕСКИХ МЕТОДИК (2) Виды аналитических методик Идентификация Количественное определение Примеси Отдел проверки соответствия GMP 36

ВАЛИДАЦИЯ АНАЛИТИЧЕСКИХ МЕТОДИК (3) Валидационные характеристики Правильность Точность Сходимость Внутрилабораторная точность Специфичность Предел обнаружения Предел количественного определения Линейность Диапазон применения Отдел проверки соответствия GMP 37

ВАЛИДАЦИЯ АНАЛИТИЧЕСКИХ МЕТОДИК (4) Типичные изменения, которые требуют ревалидации Синтез активных фармацевтических субстанций Состав готовой лекарственной формы Изменение методик И зменение хроматографических колонок Режим (время экстрагирования, температура, скорость подвижной фазы и т.п) Определение состава, рН,и т.п. Отдел проверки соответствия GMP 38

ВАЛИДАЦИЯ ОЧИСТКИ (1) Цель Подтверждение эффективности процедуры очистки Минимизация аналитического контроля Принцип Документированное доказательство того, что методика обеспечивает необходимую чистоту оборудования, с помощью которого осуществляется производство лекарственных средств Рекомендации PIC/S (PI 006-3) Отдел проверки соответствия GMP 39

ВАЛИДАЦИЯ ОЧИСТКИ (2) Требования Чувствительность методик, возможность выявления Валидация аналитической методики Внимание к поверхностям, которые контактируют и не контактируют с продуктом Промежутки времени между эксплуатацией и очисткой и между очисткой и последующей эксплуатацией Количество последовательно выполненных процедур очистки для подтверждения валидации Моделирование токсичных веществ Отдел проверки соответствия GMP 40

ВАЛИДАЦИЯ ОЧИСТКИ (3) Основные элементы Подтверждение эффективности методик во избежание контаминации последующего продукта предыдущим, микробной контаминации и другими видами контаминантов, Подтверждение воспроизводимости методики, Подтверждение возможности (способности) персонала обеспечить точное выполнение прописанных процедур Отдел проверки соответствия GMP 41

ВАЛИДАЦИЯ ОЧИСТКИ (4) Планирование Валидация очистки для каждого препарата Определение групп препаратов с определением «наихудшего случая» и проведение валидации для репрезентативного ряда препаратов Определение ряда препаратов по группам риска Отдел проверки соответствия GMP 42

ВАЛИДАЦИЯ ОЧИСТКИ (5) Планирование Определение пределов В максимальной суточной дозе препарата – не больше 0,1% средней терапевтической дозы другого препарата Не более10 ppm Не должно быть видимых остатков Аллергены, пенициллины, сильнодействующие стероиды, цитостатики и др. – предел обнаружения ниже предела возможного обнаружения Отдел проверки соответствия GMP 43

ВАЛИДАЦИЯ ОЧИСТКИ (6) Документация Основной план валидации План валидации очистки Методика очистки (СОП) Протокол валидации очистки Отчет Отдел проверки соответствия GMP 44

РЕВАЛИДАЦИЯ ЦЕЛЬ Периодичность оценки технических средств, систем, оборудования. Процессов (включая очистку) для подтверждения того, что они остаются в том состоянии, в котором были утверждены Осуществление Изменения оборудования, систем, продукции, процессов Периодическая ревалидация Отдел проверки соответствия GMP 45

ВАЛИДАЦИЯ КОМПЬЮТЕРИЗИРОВАННЫХ СИСТЕМ Жизненный цикл компьютеризированной системы (КС) включает этапы: Планирование, Установление спецификаций, Программирования, Тестирования, Настройки, Документирования, Эксплуатации, Контроля, модификации Отдел проверки соответствия GMP 46

КОМПЬЮТЕРИЗИРОВАННЫЕ СИСТЕМЫ Валидация КС – часть полного жизненного цикла Отдел проверки соответствия GMP 47

КОМПЬЮТЕРИЗИРОВАННЫЕ СИСТЕМЫ Необходимо составить и постоянно актуализировать подробное описание КС (включая при необходимости схемы). В нем должны быть описаны принципы, цели, меры безопасности и область применения системы, основные особенности той области, где используется компьютер, а также взаимодействие этой системы с другими системами и процедурами (GMP, Annex 11, p.4) Отдел проверки соответствия GMP 48

КОМПЬЮТЕРИЗИРОВАННЫЕ СИСТЕМЫ Валидация Все компьютеризированные системы должны пройти документированную процедуру перспективной валидации или квалификации Отдел проверки соответствия GMP 49

Полезные ссылки по компьютеризированным системам: 1. EU Annex 11 the EU guidelines of Good Manufacturing Practice for Medicinal Products. http://ec.europa.eu/enterprise/pharmaceuticals/ 2. Annex 11 to PIC/S Guide to Good Manufacturing Practice for Medicinal Products, Document PH 1/97 (Rev.3) 3. GOOD PRACTICES FOR COMPUTERISED SYSTEMS IN REGULATED “GXP” ENVIRONMENTS PIC/S GUIDANS PI 011-3 http://www.picscheme.org 4. GAMP Guide for Validation of Automated Systems, GAMP4 (ISPE Forum), 2001 http://www.ispe.org 5. Validation of computerized systems. WHO TRS 937, 2006, Annex 4 (Appendix 5) http://www.who.int Отдел проверки соответствия GMP 50

Современные требования GMP EC Отдел проверки соответствия GMP 51 Спасибо за внимание!
14906-lektsia_5_obsch_treb_gmp_kval_valid.ppt
- Количество слайдов: 51

