Общие свойства металло.ppt
- Количество слайдов: 20

Общие свойства металлов

УМК «ХИМИЯ» Тема лекции: Общие свойства металлов Лектор – Иванов М. Г.

Цель лекции: изложение основных понятий физических и химических свойств металлов в рамках современной химической теории Компетенции, формируемые у студента: Умения: q прогнозировать на основе современных представлений о строении атомов и химической связи, физические и химические свойства металлов.

СОДЕРЖАНИЕ Нахождение в природе Физические свойства металлов Металлическая связь Основные типы кристаллических решеток Химические свойства металлов Взаимодействие с простыми веществами Электрохимический ряд напряжений металлов Взаимодействие с кислотами С концентрированной серной кислотой С концентрированной азотной кислотой С разбавленной азотной кислотой Взаимодействие с водными растворами щелочей Литература

Нахождение в природы содержание Mn. O 2 Si. O 2 Al 2 O 3 Fe. S 2 Ag 2 S Cu. Fe. S 2 Mn. Si. O 3 Cu. CO 3(OH)2 Ca. SO 4. 2 H 2 O Оксиды - Fe 3 O 4, Mn. O 2 Сульфиды - Zn. S, Fe. S 2 Соли- Mn. Si. O 3, Cu. CO 3(OH)2, Ca. SO 4. 2 H 2 O

Нахождение в природы содержание Cu В свободном виде (смородки)- Au, Pt, Ag, Cu Au Pt

Физические свойства металлов Пластичноость Блеск, обычно серый цвет и непрозрачность Электропроводность Теплопроводность Твердость Плотность Температуры плавления и кипения содержание
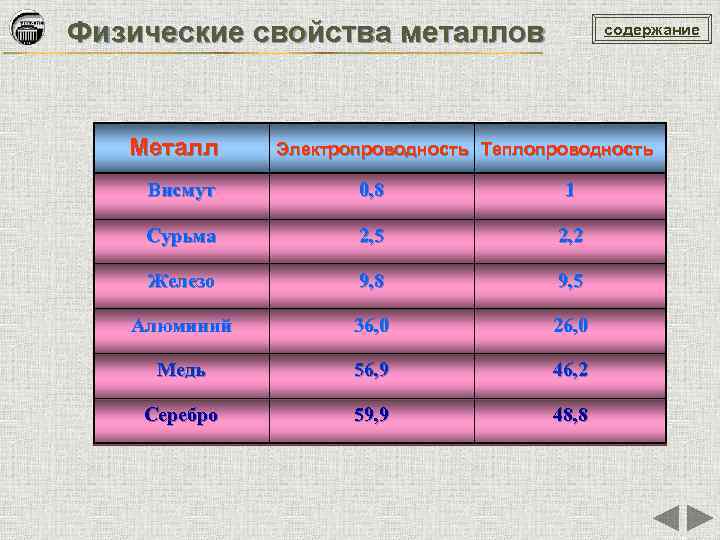
Физические свойства металлов Металл содержание Электропроводность Теплопроводность Висмут 0, 8 1 Сурьма 2, 5 2, 2 Железо 9, 8 9, 5 Алюминий 36, 0 26, 0 Медь 56, 9 46, 2 Серебро 59, 9 48, 8
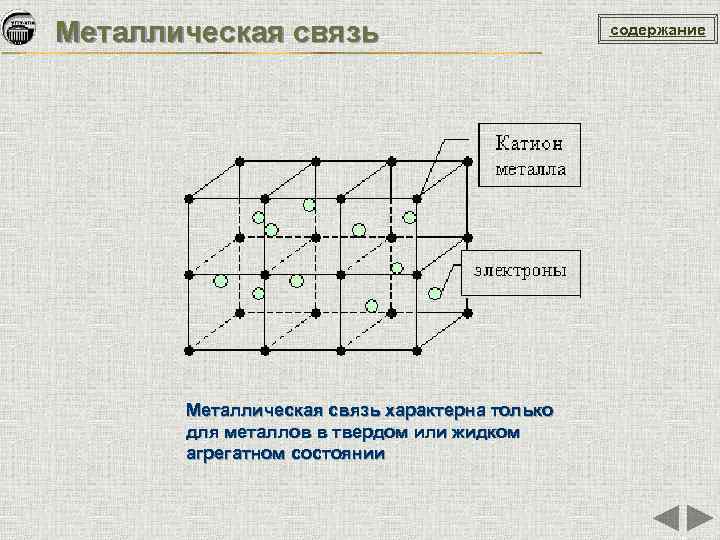
Металлическая связь характерна только для металлов в твердом или жидком агрегатном состоянии содержание
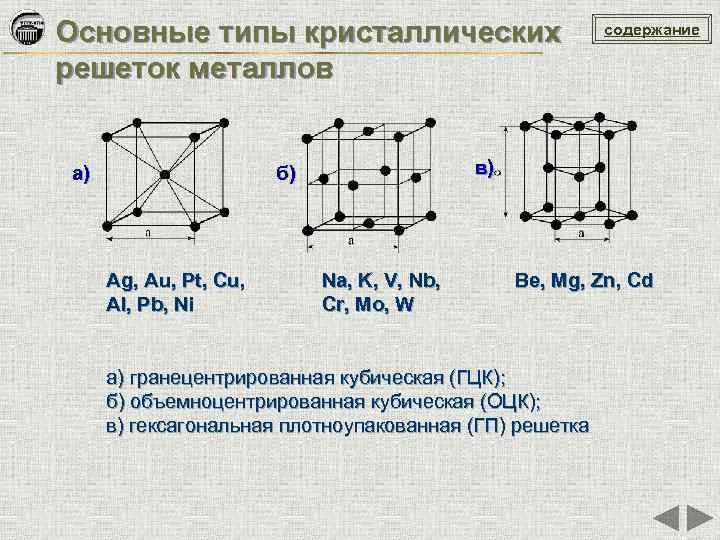
Основные типы кристаллических решеток металлов а) в) б) Ag, Au, Pt, Cu, Al, Pb, Ni содержание Na, K, V, Nb, Cr, Mo, W Be, Mg, Zn, Cd а) гранецентрированная кубическая (ГЦК); б) объемноцентрированная кубическая (ОЦК); в) гексагональная плотноупакованная (ГП) решетка

Химические свойства металлов содержание По своим химическим свойствам все металлы являются восстановителями Взаимодействие с простыми веществами с кислородом 4 Li + O 2 = 2 Li 2 O 4 Al + 3 O 2 = 2 Al 2 O 3 с серой Zn + S = Zn. S Hg + S = Hg. S с галогенами Cu + Cl 2 = Cu. Cl 2 Ni + Cl 2 = Ni. Cl 2 с водородом 2 Na + H 2 = 2 Na. H 2 Li + H 2 = 2 Li. H с азотом 3 Mg + N 2 = Mg 3 N 2 3 Ca + N 2 = Ca 3 N 2 с углеродом 4 Al + 3 C = Al 3 C 4 с фосфором 3 Ca + 2 P = Ca 3 P 2 интерметаллические соединения 3 Cu + Au = Cu 3 Au

Электрохимический ряд напряжений металлов содержание Электрохимический ряд напряжений металлов Li, K, Ca, Na, Mg, Al, Zn, Cr, Fe, Pb, H 2, Cu, Ag, Hg, Au Gо = - ∆Еоn. F где F - число Фарадея (96485 Кл); n - число электронов на один перенесенный ион. ∆Ео - разность стандартных потенциалов системы, В
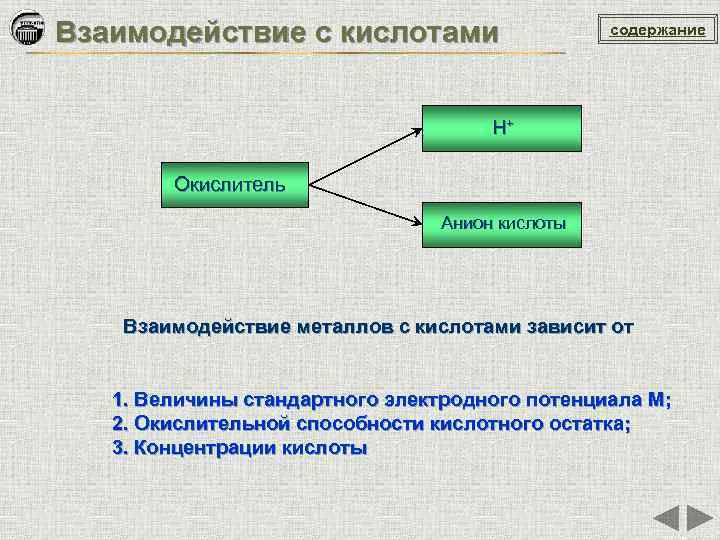
Взаимодействие с кислотами содержание Н+ Окислитель Анион кислоты Взаимодействие металлов с кислотами зависит от 1. Величины стандартного электродного потенциала М; 2. Окислительной способности кислотного остатка; 3. Концентрации кислоты
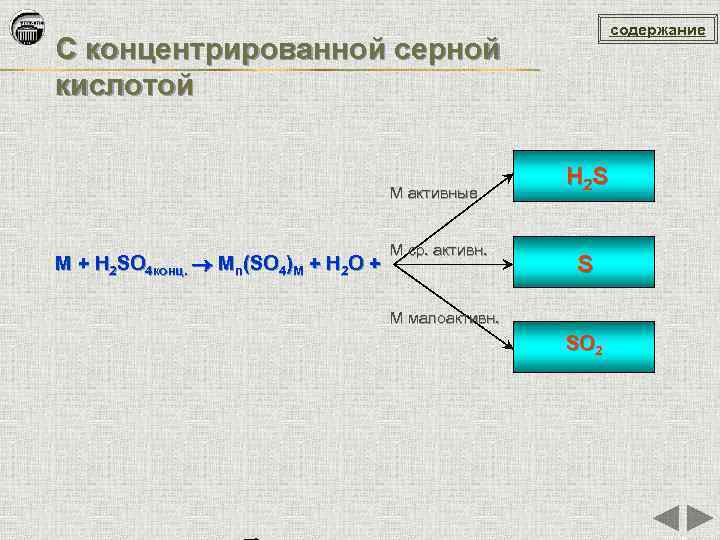
содержание С концентрированной серной кислотой М активные М + H 2 SO 4 конц. Мn(SO 4)M + H 2 O + М ср. активн. H 2 S S М малоактивн. SO 2

С концентрированной азотной кислотой М + HNO 3 конц. М(NO 3)M + H 2 O + NO 2 3 Re + 7 HNO 3 = 3 HRe. O 4 + 7 NO + 2 H 2 O Au + HNO 3 + 4 HCl = H[Au. Cl 4 ] + NO + 2 H 2 O «царская водка» содержание
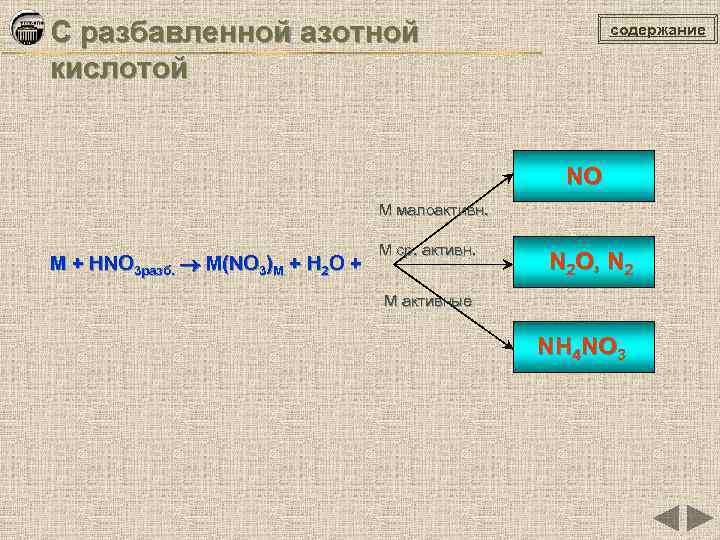
С разбавленной азотной кислотой содержание NO М малоактивн. М + HNO 3 разб. М(NO 3)M + H 2 O + М ср. активн. N 2 O, N 2 М активные NH 4 NO 3

Взаимодействие с водой при p. H = 7 M + H 2 O M(OH)n + H 2 окислитель Явление глубокого торможения окисления металла, обусловленное наличием на его поверхности защитных оксидных пленок, называется пассивацией. содержание

Взаимодействие с водными растворами щелочей при p. H = 14 окислитель в растворах щелочей растворяются металлы, потенциалы которых меньше -0, 83 В, склонные к образованию гидроксокомплексов типа [Me(OH)4 ]n- то есть металлы, чьи гидроксиды являются амфотерными: Ве(OH)2, (Al(OH)3, Zn(OH)2, Sn(OH)2, Рb(OH)2, Cr(OH)3 и др. содержание

Выводы и заключения n n содержание Химия металлов является важнейшей является частью неорганической химии. Знание законов Фарадея, а также понятие электродного потенциала позволяет охарактеризовать электрохимические процессы, проходящие с участием свободных металлов.

Список литературы n n n содержание 1. Ахметов Н. С. Общая и неорганическая химия. М. : Высшая школа. 2002. 2. О. М. Полторак, Л. М. Ковба. «Физико-химические основы неорганической химии» . М. : МГУ, 1994. 3. В. И. Горшков, И. А. Кузнецов. «Физическая химия» . М. : МГУ, 1993. 4. А. Джонсон. Термодинамические аспекты в курсе неорганической химии. М. : Мир. 1985. 5. Анорганикум. Под ред. Л. Кольдица. М. Мир. 1984. Т. 1. 6. Хьюи Дж. Неорганическая химия. Строение вещества и реакционная способность. М. , Химия, 1987. 7. Фичини Ж. , Ламброзо-Бадер Н. , Депезе Ж. -К. Основы физической химии. М. Мир. 1972. стр. 276 -283. 8. Дж. Кемпбел. Современная общая химия. М. : Мир. 1975 г. Т. 2. стр. 90. гл. 20. , Т 3. 9. Дикерсон Р. , Грей Г. , Хейт Дж. Основные законы химии. М. : Мир, 1982. Т. 2. 10. Б. Б. Дамаскин, О. А. Петрий. Электрохимия. М: Высшая школа, 1987. 11. CRC Hand book of Chemistry and Physics. 82 издание. 2001 -2002
Общие свойства металло.ppt