Программа курса.pptx
- Количество слайдов: 7

Общие представления, понятия, структура. Курс химии в МИРЭА читается в соответствии с ГОСТом по специальностям и направлениям подготовки специалистов высшего профессионального образования Российской Федерации. 1. 1 Цели и задачи курса. 1. 1. 1 Цель изучения дисциплины. Получение фундаментальных знаний, умений и навыков, необходимых как для изучения смежных и специальных дисциплин, так и для последующей практической деятельности будущего специалиста. 1. 1. 2 Задачи изучения дисциплины. Освоить современные представления о строении вещества. Научиться использовать основные законы химической термодинамики и кинетики для наиболее оптимального проведения различных процессов (молекулярных, ионных, каталитических, электрохимических) в различных средах, в том числе и в растворах. Возможность самостоятельного выполнения химических экспериментов и обобщения наблюдаемых фактов. Для достижения поставленных целей и задач используются: химические эксперименты, обучающие и контролирующие программы, демонстрационные опыты, таблично-графическое представление данных и их обработка, решение типовых задач, работа с литературой, создание электронного обучающего курса.

Программа курса 1. 2. 1 Общие представления о химии. Структура дисциплины. Место химии в естествознании. Основные понятия, законы и определения. 1. 2. 2. Строение атома. Волновые свойства электрона. Квантовые числа. Формы орбиталей. Многоэлектронные атомы. Принцип Паули, правило Гунда, правила Клечковского. 1. 2. 3. Периодический закон и система Д. И. Менделеева. Атомные радиусы. Потенциал ионизации и сродство к электрону. Электроотрицательность. 1. 2. 4. Химическая связь. Виды химических связей. Метод валентных связей. Насыщаемость, направленность, полярность. Метод молекулярных орбиталей. Связывающие и разрыхляющие орбитали. Порядок связи. Межмолекулярные взаимодействия. 1. 2. 5 Термодинамика. 1 -ый закон термодинамики. Энтальпия. Тепловой эффект химической реакции. Закон Гесса. Энтропия. 2 -ое начало термодинамики. Энергия Гиббса. Определение направления химической реакции. 1. 2. 6. Химическая кинетика. Скорость химических реакций. Гомогенные и гетерогенные реакции. Закон действующих масс. Порядок и молекулярность. Влияние температуры на скорость реакции. Правило Вант- Гоффа. Энергия активации. Уравнение Аррениуса. Катализ. Химическое равновесие. Константа равновесия. Принцип Ле- Шателье.

Программа курса 1. 2. 7. Химические равновесия в растворах электролитов. Сильные и слабые электролиты. Константа диссоциации и степень диссоциации. Ионное произведение воды. Водородный показатель. Ионные равновесия в растворах электролитов. 1. 2. 8. Дисперсные системы. Основные виды дисперсных систем. Коллоиды. Основные свойства коллоидных растворов. Полимеры, их основные свойства. Фазовые равновесия. Правило фаз Гиббса. Диаграммы состояния. 1. 2. 9. Электрохимические процессы. Электродные потенциалы и гальванические элементы. Максимальная работа и э. д. с. Уравнение Нернста. Поляризационные явления в гальванических элементах. Коррозия металлов. Химическая коррозия. Защитные пленки на поверхности металлов. Электрохимическая коррозия. Анодные и катодные процессы. Катодная деполяризация. Зависимость коррозии от внешних условий. Защита от коррозии. Электрохимические способы защиты. Электролиз. Анодное окисление и катодное восстановление. Последовательность разряда ионов. Электролиз с растворимым и нерастворимым анодом. Напряжение разложения. Перенапряжение.
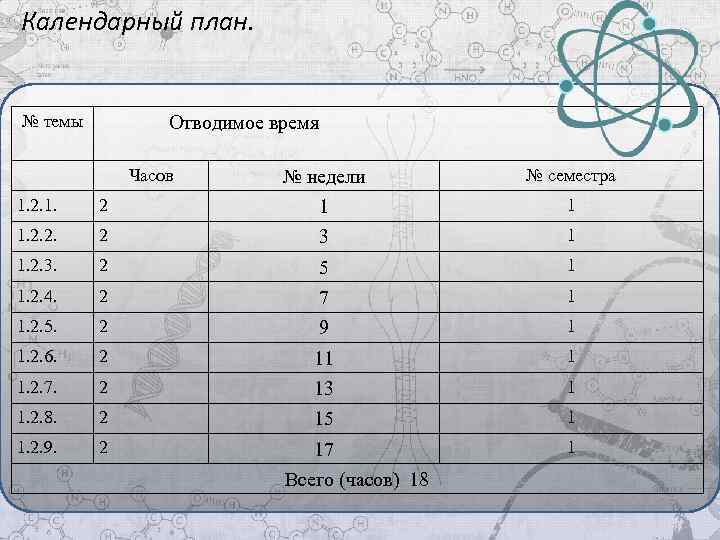
Календарный план. № темы Отводимое время Часов № недели № семестра 1. 2. 1. 2 1 1 1. 2. 2. 2 3 1 1. 2. 3. 2 5 1 1. 2. 4. 2 7 1 1. 2. 5. 2 9 1 1. 2. 6. 2 11 1 1. 2. 7. 2 13 1 1. 2. 8. 2 15 1 1. 2. 9. 2 17 1 Всего (часов) 18
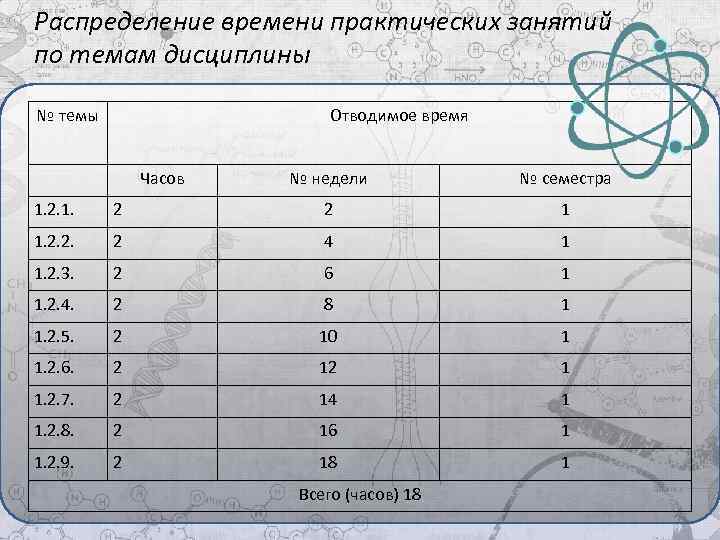
Распределение времени практических занятий по темам дисциплины № темы Отводимое время Часов № недели № семестра 1. 2. 1. 2 2 1 1. 2. 2. 2 4 1 1. 2. 3. 2 6 1 1. 2. 4. 2 8 1 1. 2. 5. 2 10 1 1. 2. 6. 2 12 1 1. 2. 7. 2 14 1 1. 2. 8. 2 16 1 1. 2. 9. 2 18 1 Всего (часов) 18

Определение дисциплины Одно из первых определений химии дал М. В. Ломоносов (1741): Наука о качествах и изменениях тел. Здесь под качеством надо понимать свойства вещества, а под их изменением – химическое превращение, то есть изменение электронной подсистемы атомов или молекул (при изменении ядерной подсистемы протекают ядерные процессы – объект изучения ядерной физики). Тогда современное определение химии можно представить так: Наука о свойствах и превращениях веществ в результате изменения их электронной подсистемы.
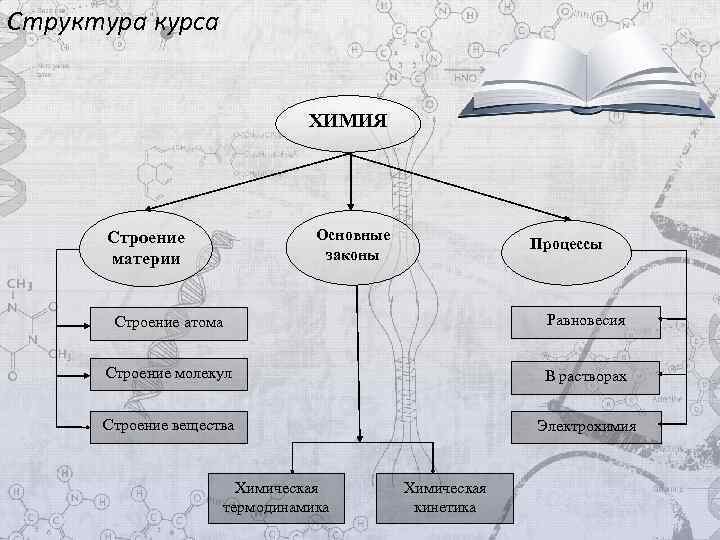
Структура курса ХИМИЯ Основные законы Строение материи Процессы Строение атома Равновесия Строение молекул В растворах Строение вещества Электрохимия Химическая термодинамика Химическая кинетика
Программа курса.pptx