Общие положения ТКП – теория кристаллического


Общие положения ТКП – теория кристаллического поля (Бете, 1929) 1. Рассматриваются соединения, состоящие из катиона d-металла и лигандов, связанных электростатическим взаимодействием (лиганды – ионы или диполи). 2. Лиганды рассматриваются только как точечные заряды, являющиеся источником электростатического поля. Может учитываться радиус, но не структура. 3. Взаимодействие центрального атома с лигандами рассматривается, напротив, подробно: с учетом всех особенностей d- (и f-) орбиталей центрального атома и распределения электронов на них.

2
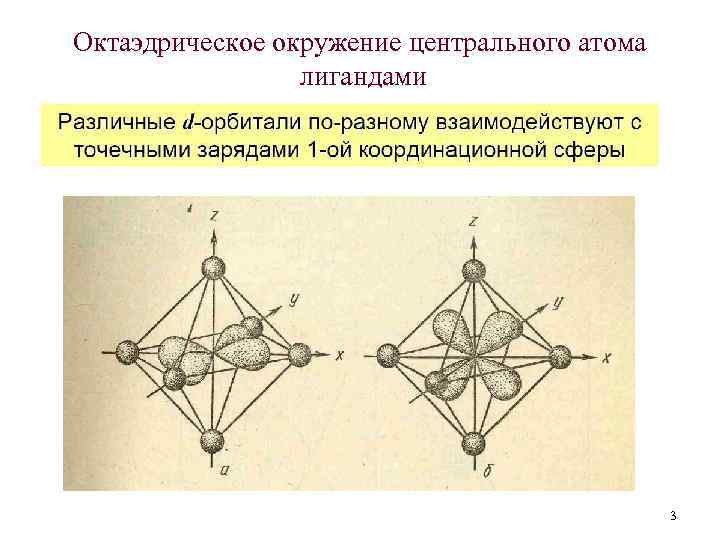
Октаэдрическое окружение центрального атома лигандами 3
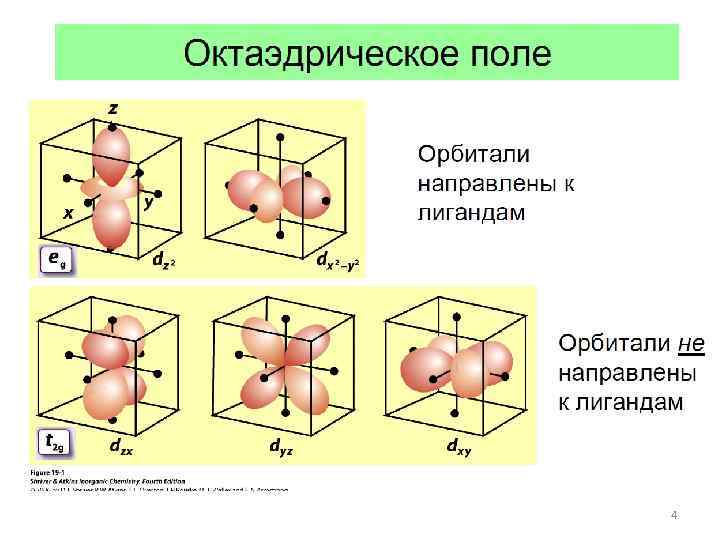
4
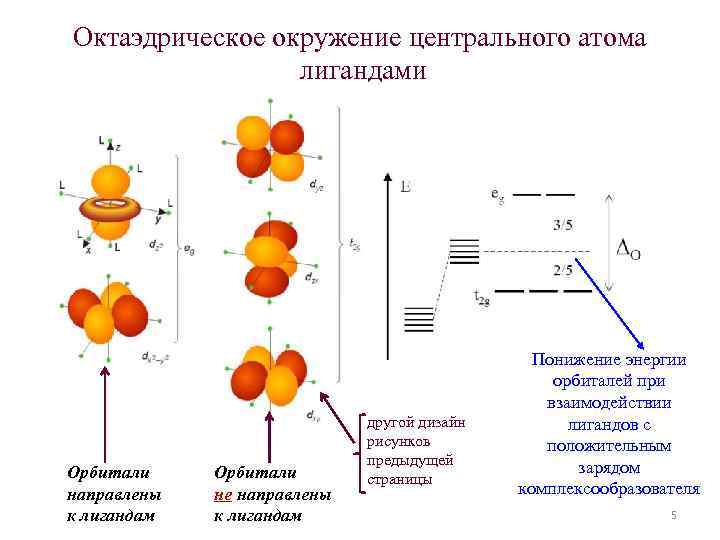
Октаэдрическое окружение центрального атома лигандами Понижение энергии орбиталей при взаимодействии другой дизайн лигандов с рисунков положительным предыдущей зарядом Орбитали страницы направлены не направлены комплексообразователя к лигандам 5

Сильное и слабое октаэдрическое поле Борьба двух противоположных тенденций: 1. Стремление к максимальному спину 2. Стремление к минимуму энергии 6
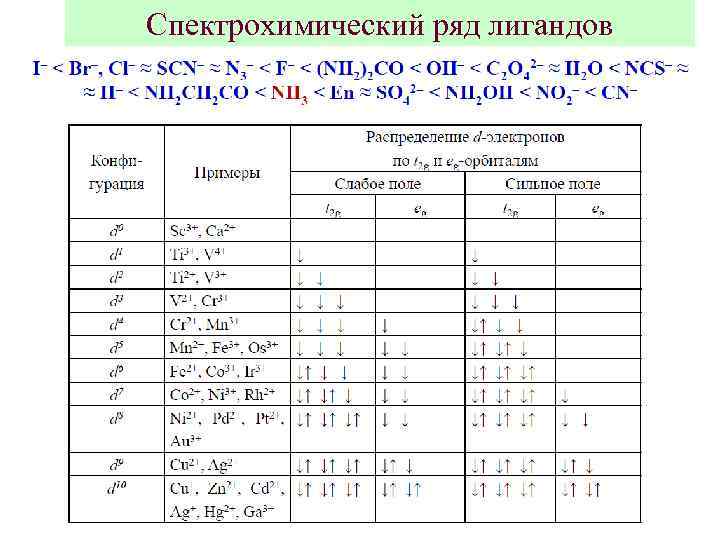
Спектрохимический ряд лигандов 7
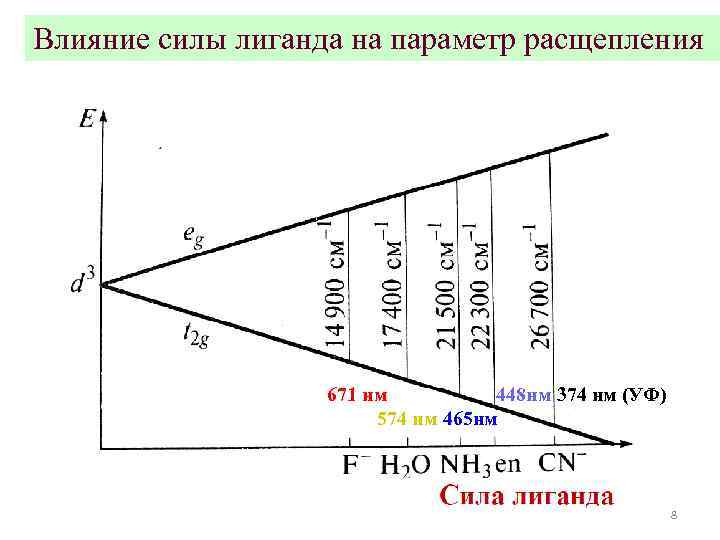
Влияние силы лиганда на параметр расщепления 671 нм 448 нм 374 нм (УФ) 574 нм 465 нм 8

Пример расщепления в октаэдрических комплексах Ni 2+ Красный Оранж. -желт. Желтый 9
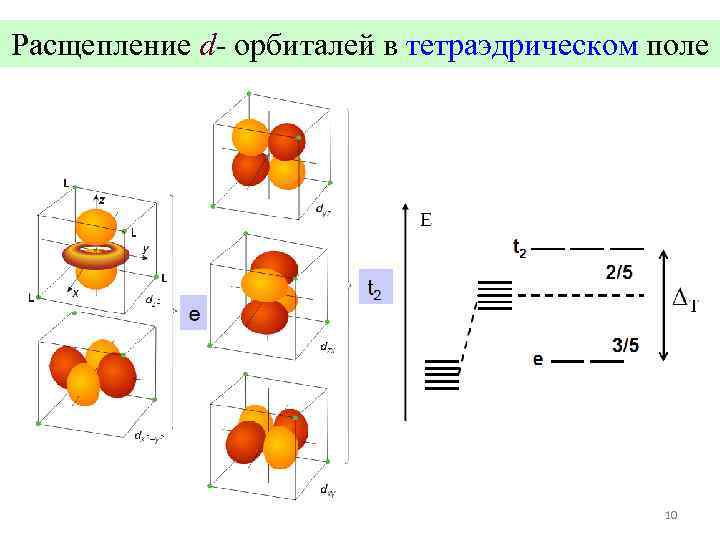
Расщепление d- орбиталей в тетраэдрическом поле 10
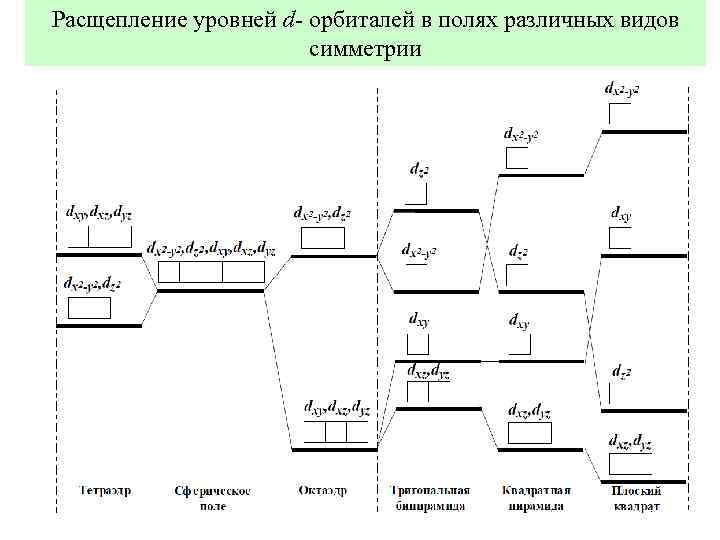
Расщепление уровней d- орбиталей в полях различных видов симметрии 11
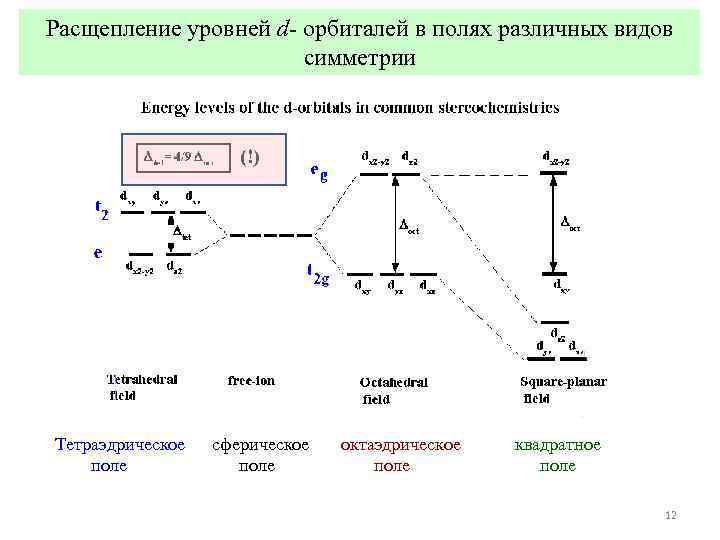
Расщепление уровней d- орбиталей в полях различных видов симметрии (!) Тетраэдрическое сферическое октаэдрическое квадратное поле 12

ЭСКП Энергия стабилизации кристаллическим полем В октаэдре: ЭСКП = [2/5 n(t 2 g) – 3/5 n(eg)]ΔO – nспар. P Энергия: Дж/моль, э. В или см– 1 ΔO – энергия расщепления октаэдрическим полем P – энергия спаривания электронов (P вычитается только тогда, когда это спаривание происходит). nспар. – количество спарившихся электронов 13
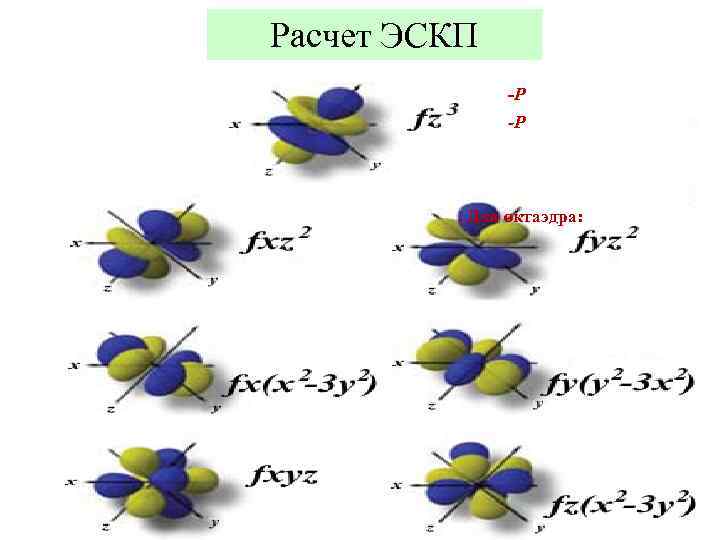
Расчет ЭСКП -P . Для октаэдра: 14

ЭСКП ΔO >P – сильное поле ΔO < P – слабое поле Для конфигурации d 4 (Cr 2+, Mn 3+) в октаэдрическом поле: Слабое поле: (t 2 g)3(eg)1: ЭСКП= (2/5· 3 – 3/5· 1)ΔO= 3/5ΔO Сильное поле: (t 2 g)4: ЭСКП = (2/5· 4 – 0)ΔO – P = 8/5ΔO – P 15
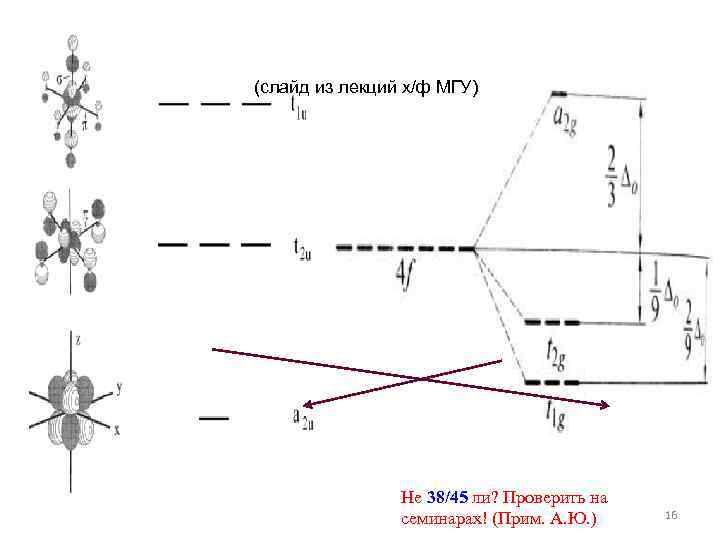
(слайд из лекций х/ф МГУ) Не 38/45 ли? Проверить на семинарах! (Прим. А. Ю. ) 16

f- орбитали и их расщепление 17
![Расщепление f- орбиталей в октаэдрическом поле (комплексы типа K 3[Ln 3+Cl 6]; Ln = Расщепление f- орбиталей в октаэдрическом поле (комплексы типа K 3[Ln 3+Cl 6]; Ln =](https://present5.com/presentation/3/190141580_377211381.pdf-img/190141580_377211381.pdf-18.jpg)
Расщепление f- орбиталей в октаэдрическом поле (комплексы типа K 3[Ln 3+Cl 6]; Ln = Ce, Pr, …, Lu) Zbiri et al. , Chem. Phys. Lett. , 397 (2004) 441 18
19

20
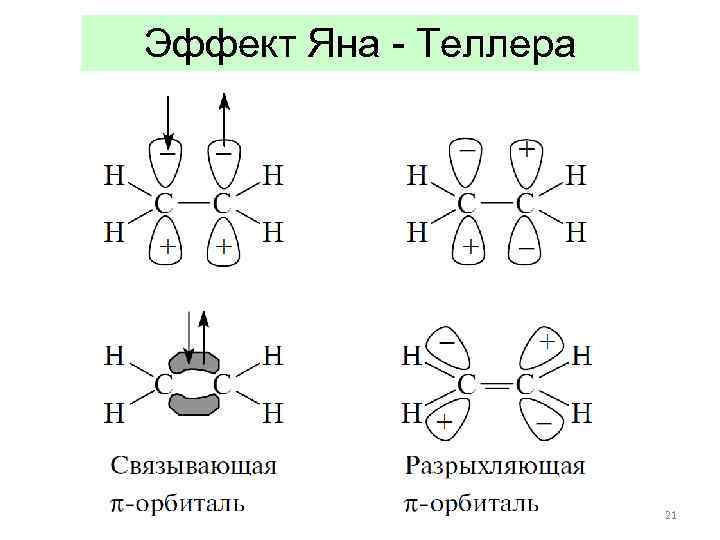
Эффект Яна - Теллера 21
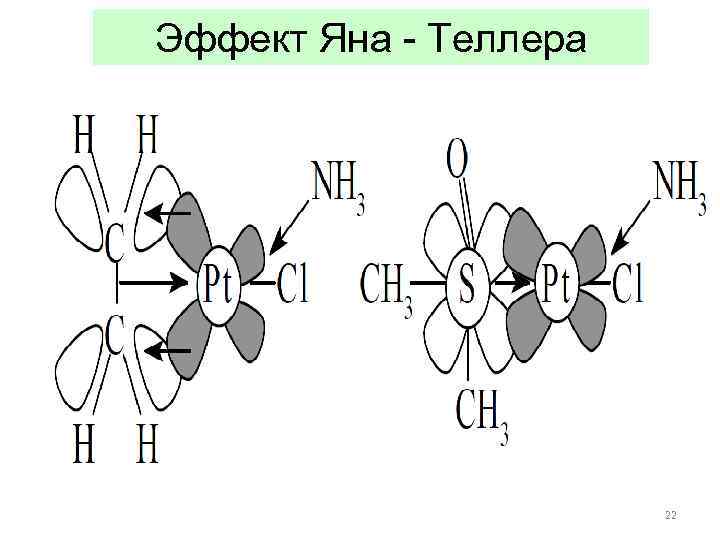
Эффект Яна - Теллера 22

Основы ММО для комплексов Ван Флек, 30 -40 гг. XX в. • Образование комплекса и снятие вырождения d- орбиталей происходит не только за счет электростатического взаимодействия, но и за счет перекрывания орбиталей ЦА и лигандов (ковалентного взаимодействия) • Уитываются не только d-орбитали ЦА, но и s, p… • Учитывается строение лигандов • Взаимодействие двух АО (ЦА и лиганда) приводит к образованию 2 МО. Связывающая МО лежит ниже АО, разрыхляющая – выше. (МО ЛКАО) • Взаимодействуют только АО, одинаковые по симметрии. Если симметрия не совпадает – несвязывающие орбитали • Соблюдается принцип Паули и правила Хунда 23

24

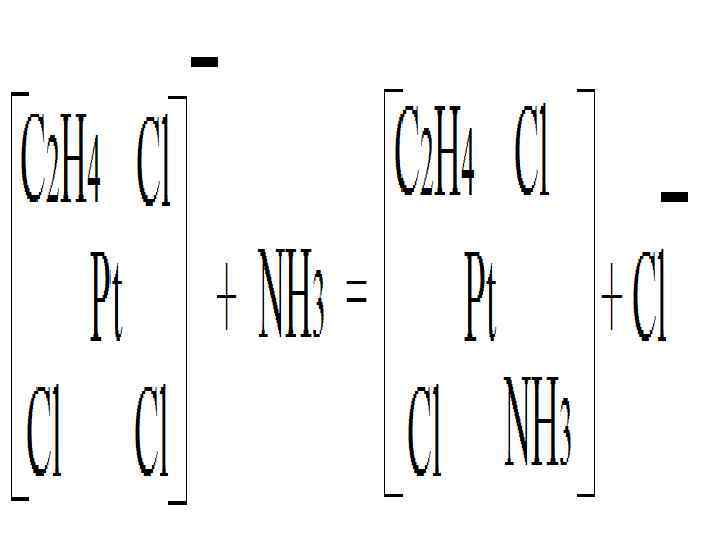
Эффект транс-влияния Черняева Для квадратных и октаэдрических комплексов, скорость реакции замещения лиганда L определяется природой заместителя X (тоже лиганда), занимающего противоположный конец диагонали L-Me-X ( Me – атом комплексобразователя, находящийся в центре квадрата или октаэдра). 25

26

Эффект транс-влияния Черняева 27

Эффект транс-влияния Черняева (еще один пример) Cl NH 3 K 2 [ Pt ] + 2 NH 3 = [ Pt ] + 2 KCl Cl Cl NH 3 Cl NH 3 [ Pt ] Cl 2 + 2 HCl = [ Pt ] + 2 NH 4 Cl NH 3 Cl 28
Лекция_3_4_Комплексы.ppt
- Количество слайдов: 28

