8 функциональный анализ.pptx
- Количество слайдов: 64

ОБЩИЕ МЕТОДЫ АНАЛИЗА ОРГАНИЧЕСКИХ ЛЕКАСТВЕННЫХ СРЕДСТВ ФУНКЦИОНАЛЬНЫЙ АНАЛИЗ
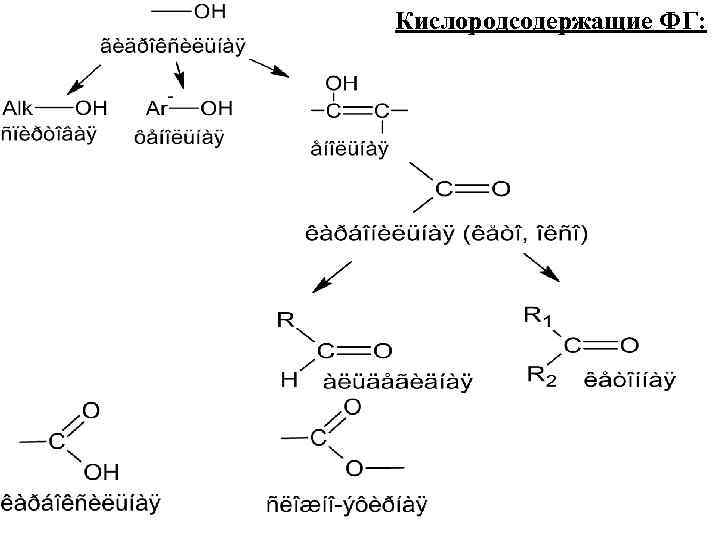
Кислородсодержащие ФГ:
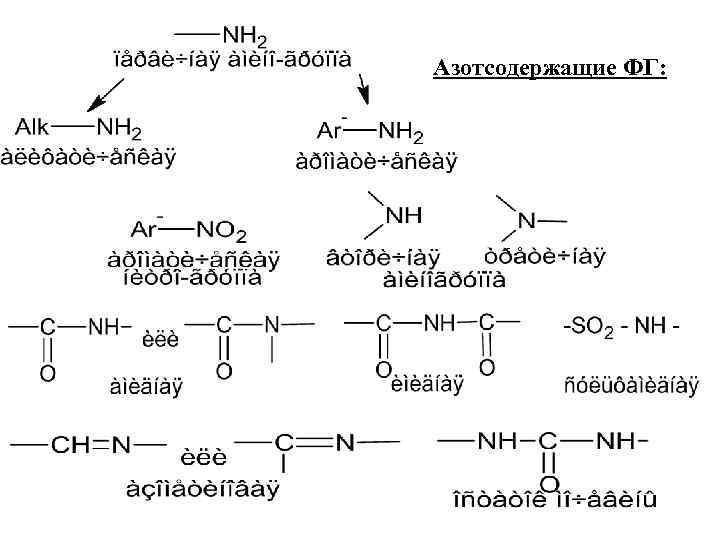
Азотсодержащие ФГ:

ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВОЙ ГИДРОКСИЛ. Реакция этерификации. + CH 3 COOH + ментол кип. 2 ч пиридин уксусный ангидрид белый кристаллический осадок, Т°пл
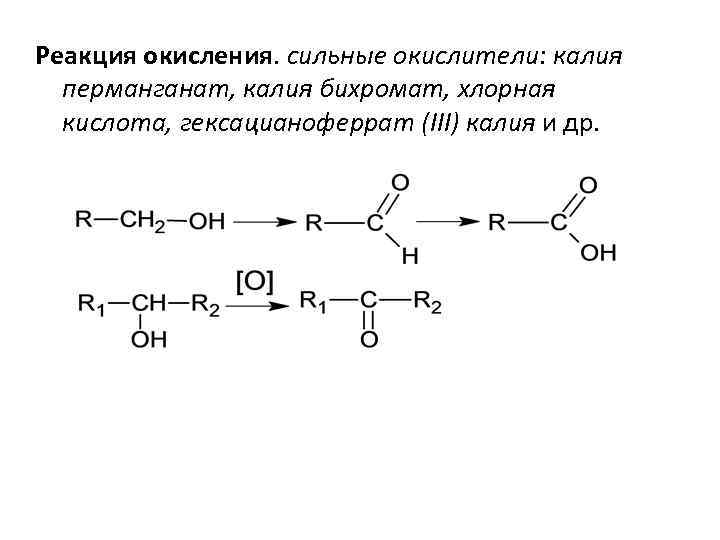
Реакция окисления. сильные окислители: калия перманганат, калия бихромат, хлорная кислота, гексацианоферрат (III) калия и др.

окисление первичных спиртов реакция «йодоформной» пробы: характерна не только для этанола, но и для веществ, содержащих этокси-группу (-ОС 2 Н 5), альдегидную (-СОН ) и ацето-группу (-CОСН 3).
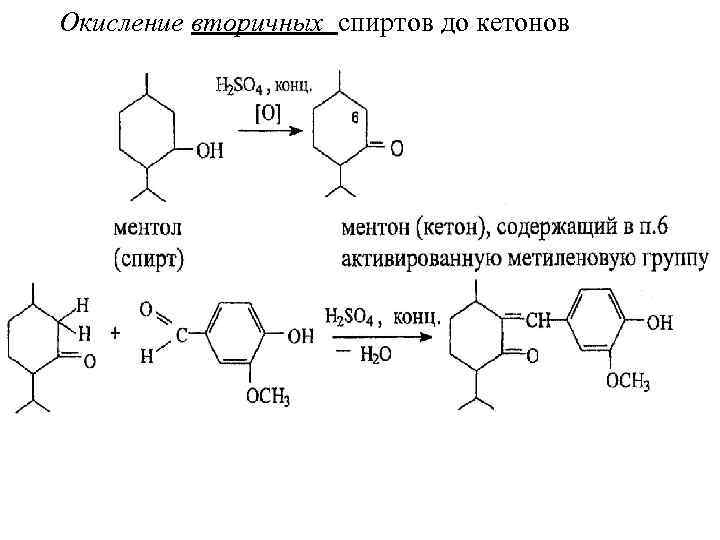
Окисление вторичных спиртов до кетонов
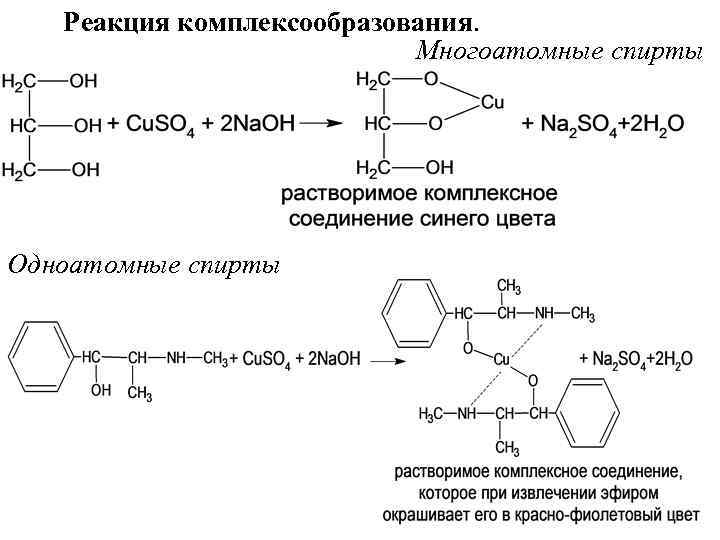
Реакция комплексообразования. Многоатомные спирты Одноатомные спирты

ЛВ, СОДЕРЖАЩИЕ КАРБОНИЛЬНУЮ ГРУППУ Типы реакций для идентификации альдегидов: 1. Реакции окисления 2. Реакции нуклиофильного присоединения (конденсации). 2. 1 Конденсации 2. 2 Замещения 2. 3 Присоединения 3. Полимеризации. 1. Реакции окисления. а) Реакция с аммиачным раствором нитрата серебра (реакция серебряного зеркала) Ag. NO 3 + 2 NH 4 OH → [Ag(NH 3)2]NO 3 +2 H 2 O НСОН + 2[Ag(NH 3)2]NO 3 + H 2 O → HCOONH 4 + 2 Ag↓+ 2 NH 4 NO 3+ NH 3↑

б) Реакция с реактивом Фелинга (комплексное соединение меди (II) с калий-натриевой солью винной кислоты). 2 Cu. OH 4 + Na 2 Cu. OH↓ → Cu 2 O↓ + H 2 O Желтый осадок кирпично-красный осадок + 2 H 2 O

Пример Суммарная реакция на глюкозу в) Реакция с реактивом Несслера (щелочной раствор тетрайодмеркурата (II) калия). R-COH + K 2[Hg. I 4] +3 KOH → R-COOK + 4 KI + черный. Hg↓ +2 H 2 O
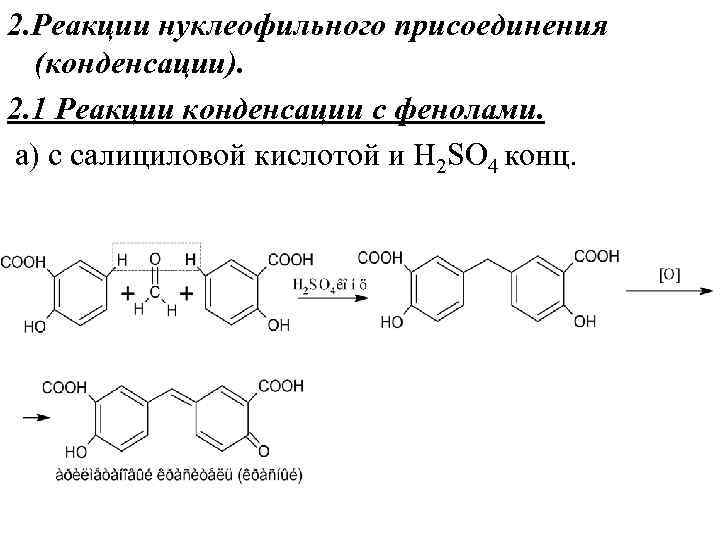
2. Реакции нуклеофильного присоединения (конденсации). 2. 1 Реакции конденсации с фенолами. а) c салициловой кислотой и H 2 SO 4 конц.
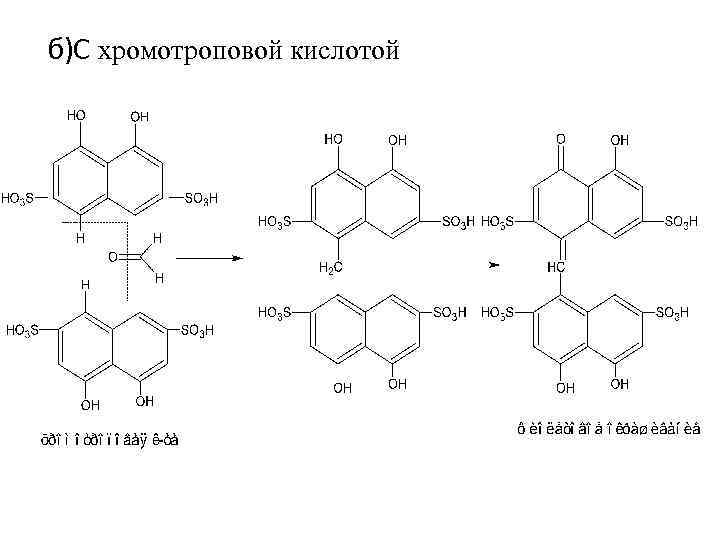
б)С хромотроповой кислотой

2. 2 Реакции замещения ( конденсации) с аминами и их производными Реактивы: а) соединения с первичной ароматической и алифатической аминогруппой – п-аминобензолсульфамид (стрептоцид) и гидроксиламин; б)производные гидразина – семикарбазид, 2, 4 – динитрофенилгидразин, фенилгидразин. Продукты реакции: | с азометиновой связью – C = N – основания Шиффа, оксимы, гидразоны, семикарбазоны
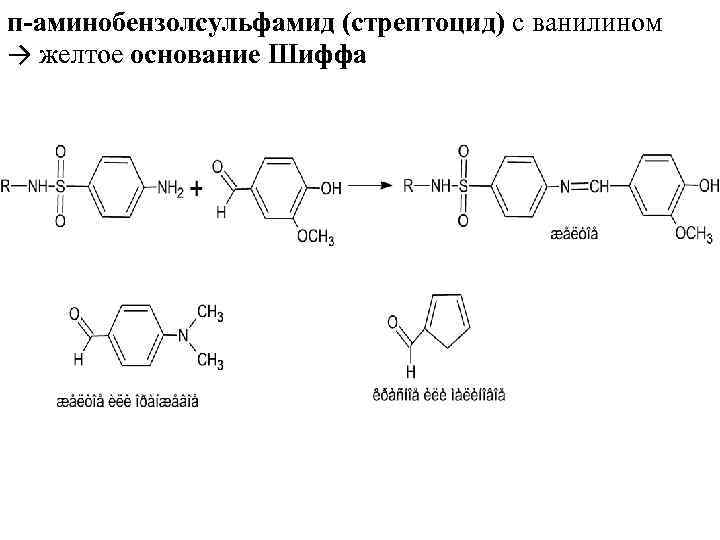
п-аминобензолсульфамид (стрептоцид) с ванилином → желтое основание Шиффа
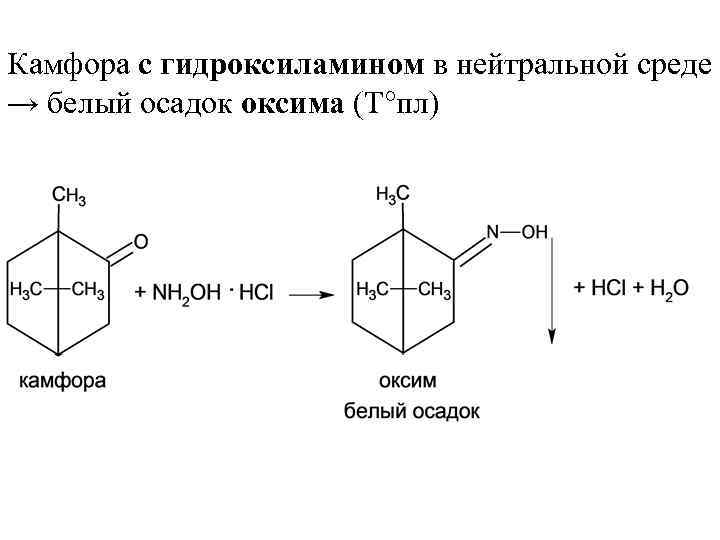
Камфора с гидроксиламином в нейтральной среде → белый осадок оксима (Т°пл)
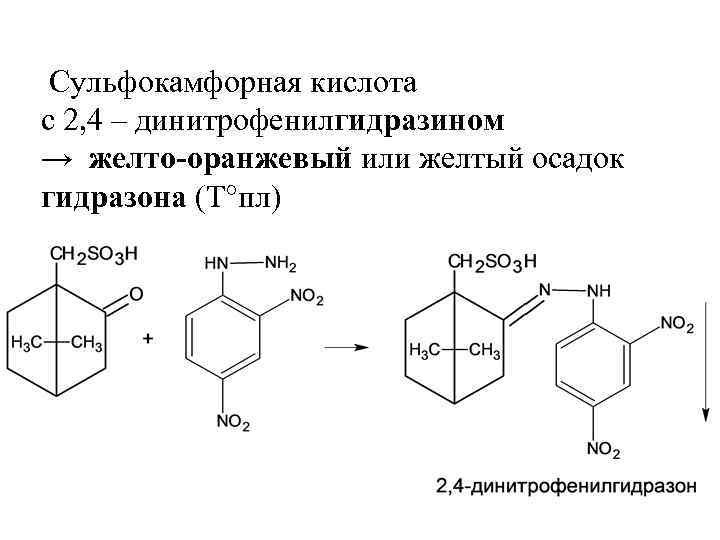
Сульфокамфорная кислота с 2, 4 – динитрофенилгидразином → желто-оранжевый или желтый осадок гидразона (Т°пл)
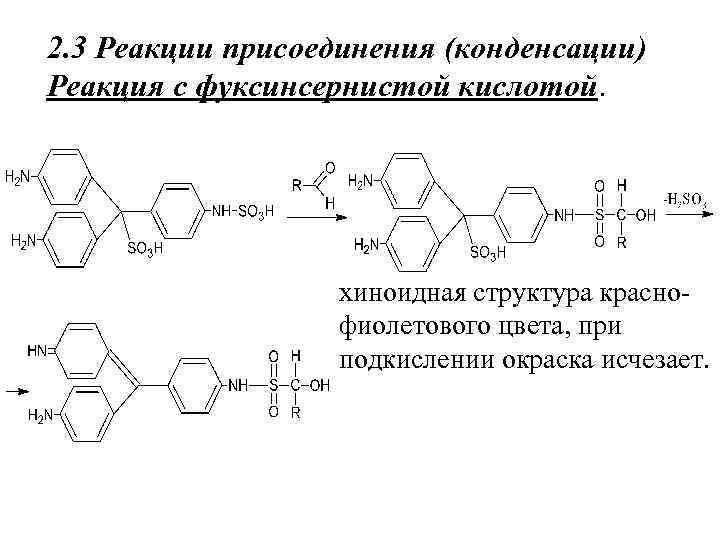
2. 3 Реакции присоединения (конденсации) Реакция с фуксинсернистой кислотой. хиноидная структура краснофиолетового цвета, при подкислении окраска исчезает.
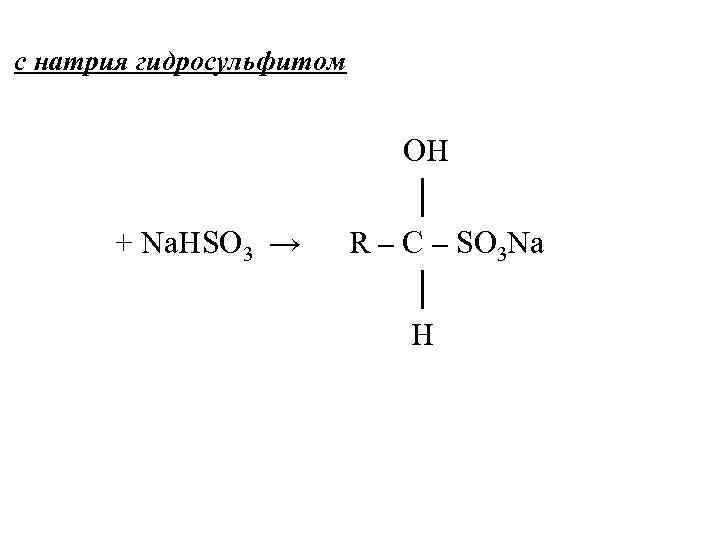
с натрия гидросульфитом + Na. HSO 3 → OH │ R – C – SO 3 Na │ H

ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ КАРБОКСИЛЬНУЮ ГРУППУ кислотные свойства R-COOH → R-COO- + H+ 1. Реакции с солями тяжелых металлов Взаимодействие с ионами железа (III) или меди (II) ) с образованием простых или комплексных солей
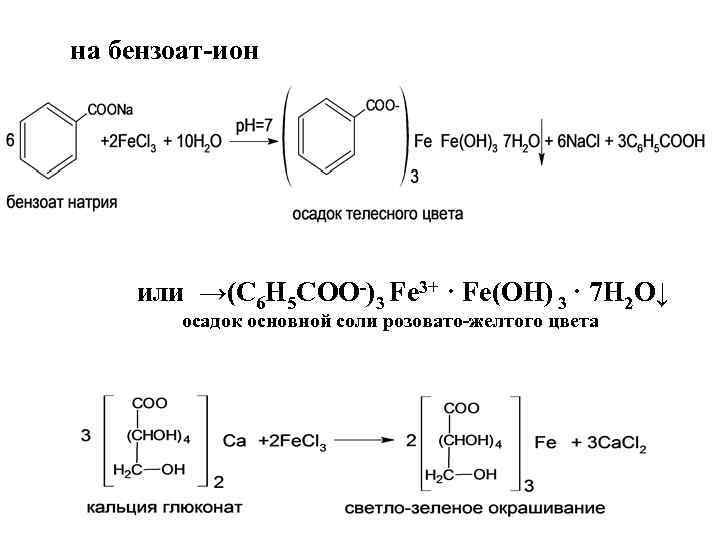
на бензоат-ион или →(С 6 Н 5 СОО-)3 Fе 3+ · Fе(ОН) 3 · 7 Н 2 О↓ осадок основной соли розовато-желтого цвета

2. Реакция этерификации Т°пл
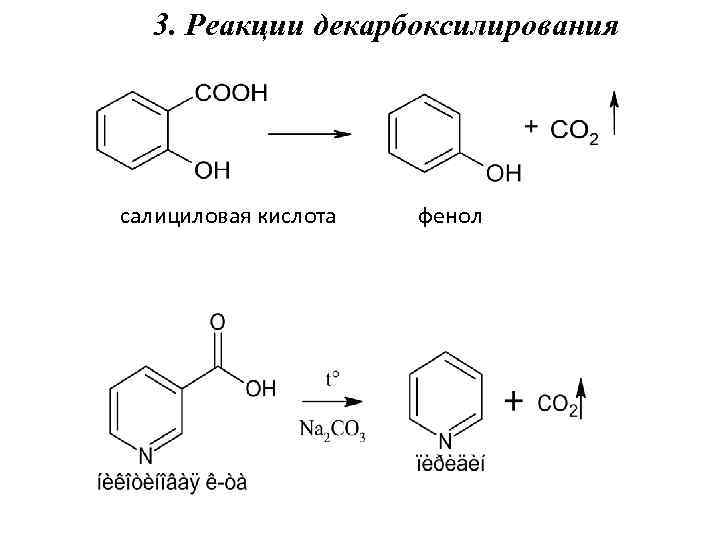
3. Реакции декарбоксилирования салициловая кислота фенол
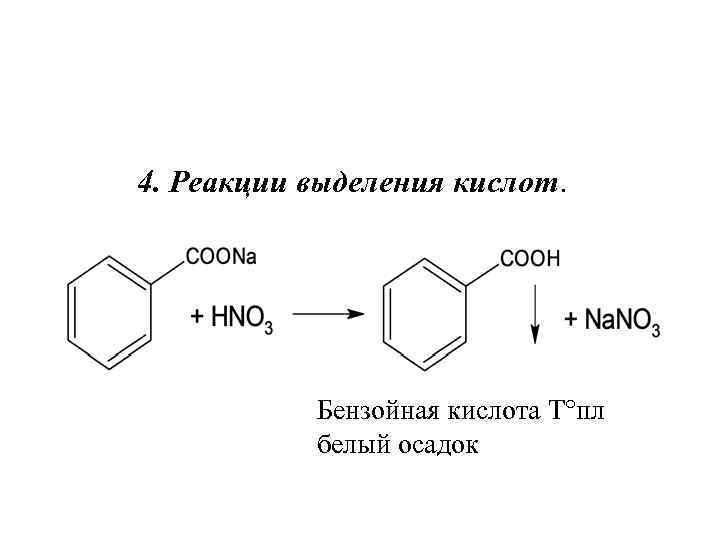
4. Реакции выделения кислот. Бензойная кислота Т°пл белый осадок

ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ ФЕНОЛЬНЫЙ ГИДРОКСИЛ используют следующие реакции: 1. комплексообразование 2. окисление 3. электрофильного замещения • галогенирование (бромирование) • нитрование • азосочетание с солями диазония • конденсация (с альдегидами) синий
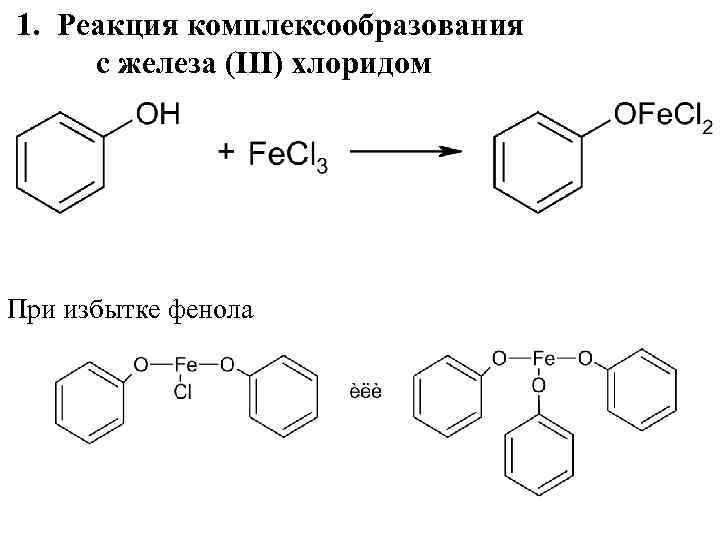
1. Реакция комплексообразования с железа (III) хлоридом При избытке фенола
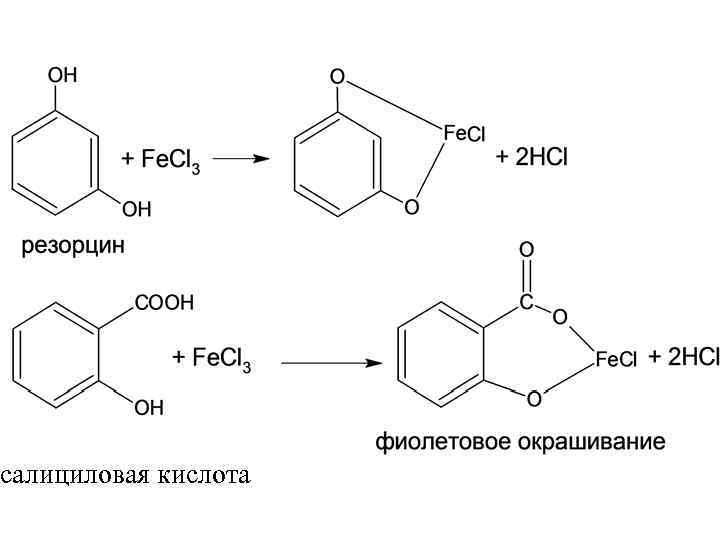
салициловая кислота
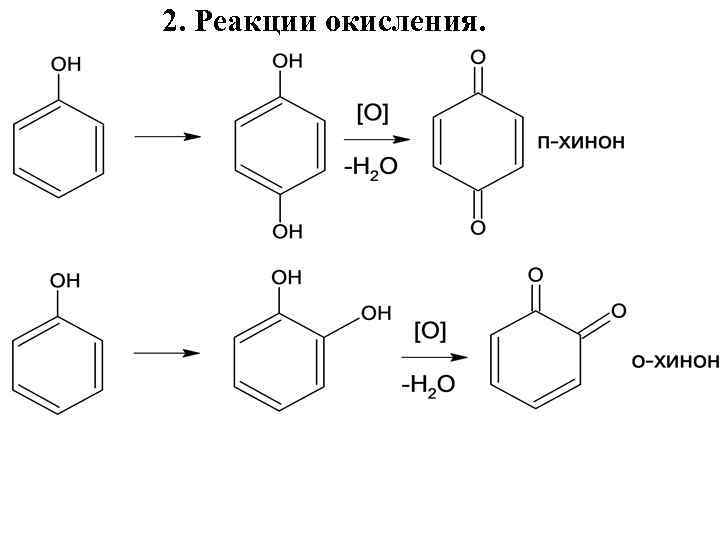
2. Реакции окисления.

Реакции образования индофенолового красителя а) с аммиаком или аминопроизводным и избытком фенола б) для веществ, образующих в результате гидролиза п-аминофенол - образование индоамина в) нитрозореакция Либермана для фенолов, не имеющих в о- и п-положениях заместителей (нитрит натрия в кислой среде )
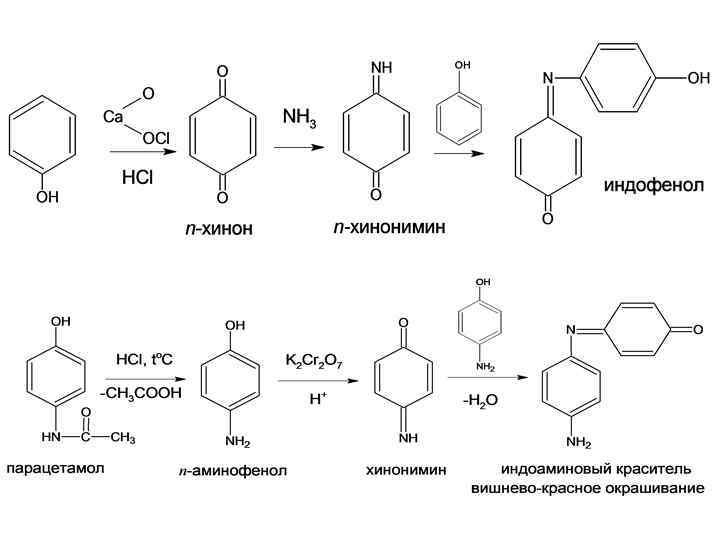
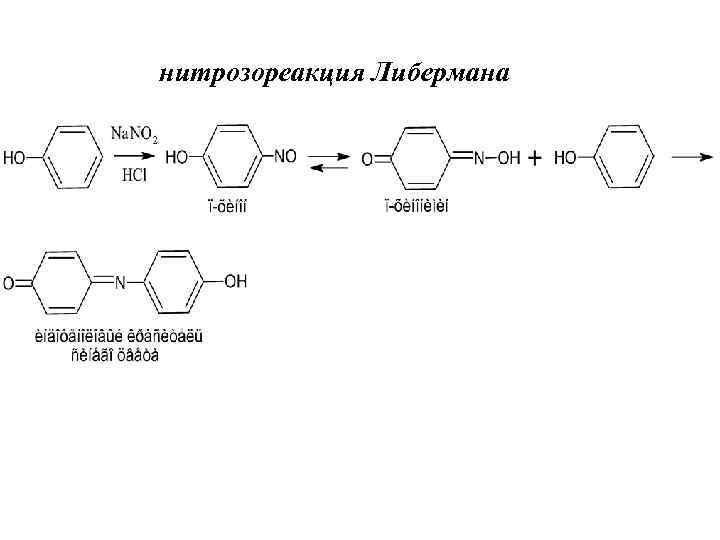
нитрозореакция Либермана
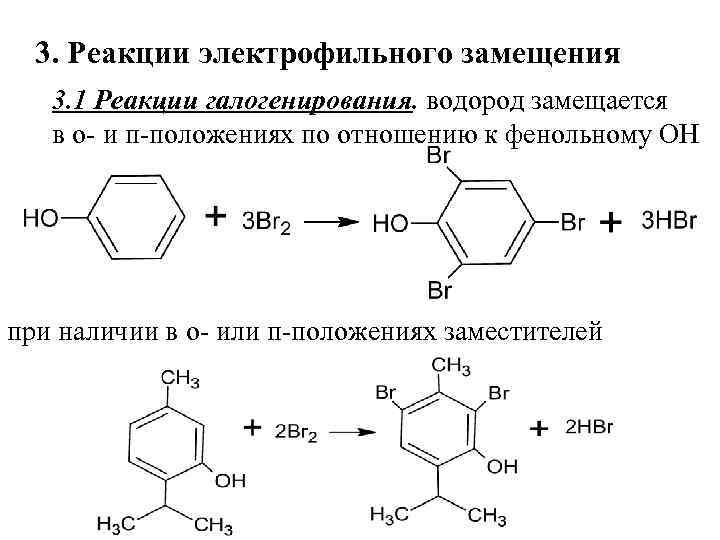
3. Реакции электрофильного замещения 3. 1 Реакции галогенирования. водород замещается в о- и п-положениях по отношению к фенольному ОН при наличии в о- или п-положениях заместителей
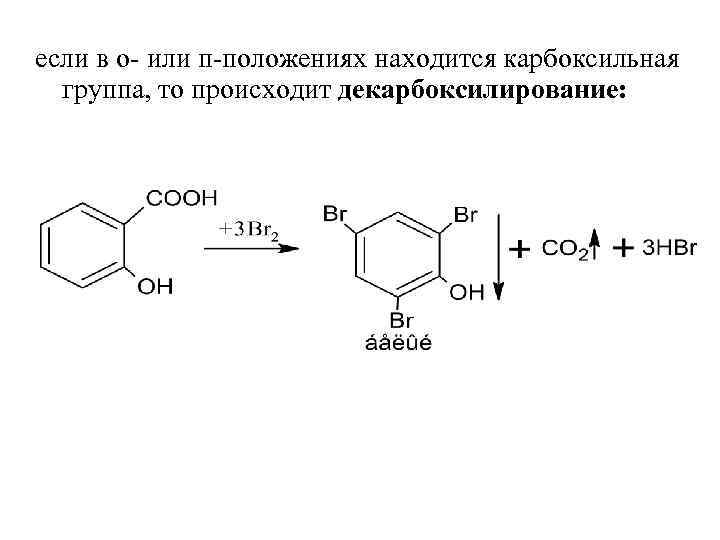
если в о- или п-положениях находится карбоксильная группа, то происходит декарбоксилирование:
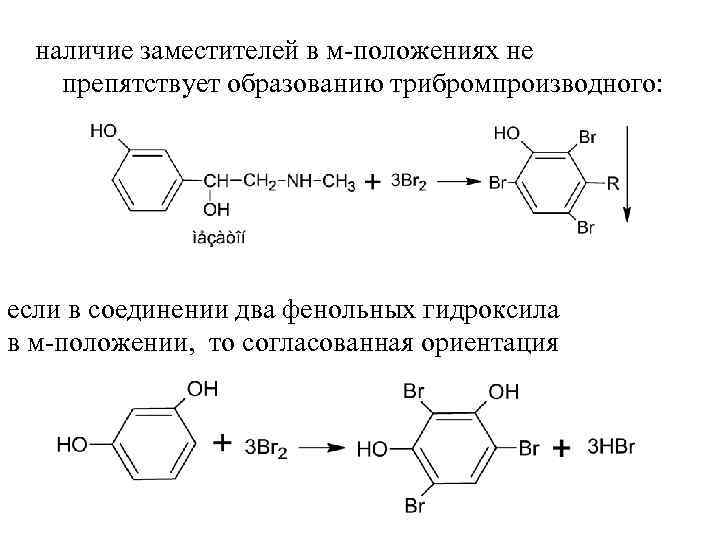
наличие заместителей в м-положениях не препятствует образованию трибромпроизводного: если в соединении два фенольных гидроксила в м-положении, то согласованная ориентация
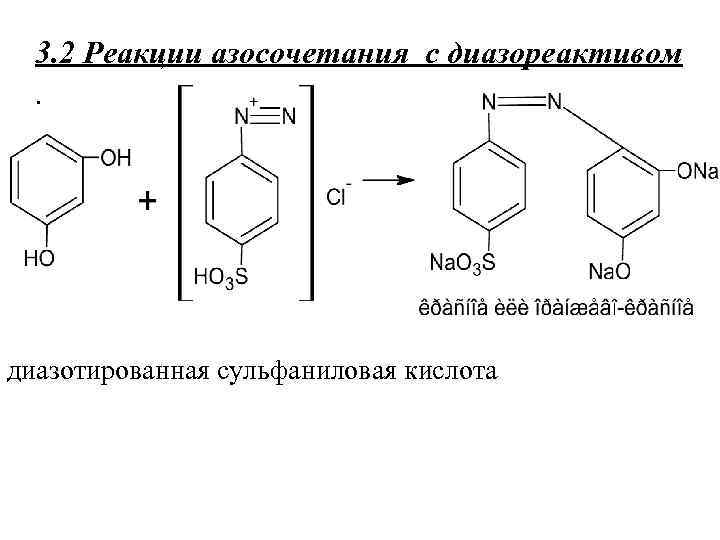
3. 2 Реакции азосочетания с диазореактивом. диазотированная сульфаниловая кислота
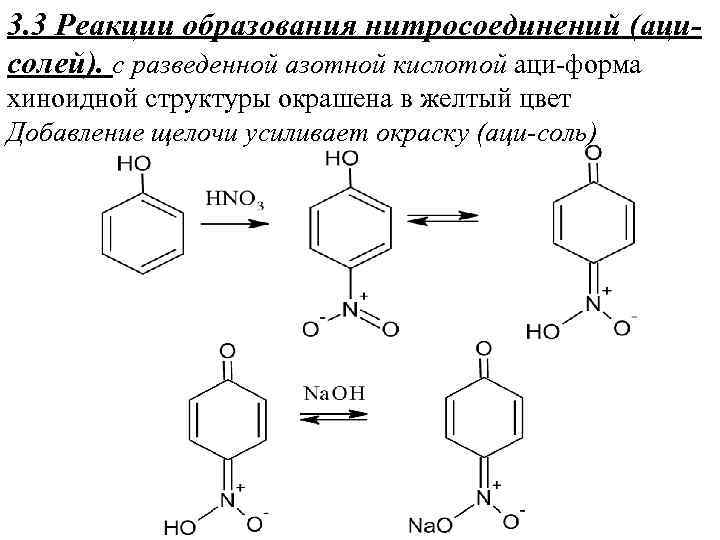
3. 3 Реакции образования нитросоединений (ацисолей). с разведенной азотной кислотой аци-форма хиноидной структуры окрашена в желтый цвет Добавление щелочи усиливает окраску (аци-соль)
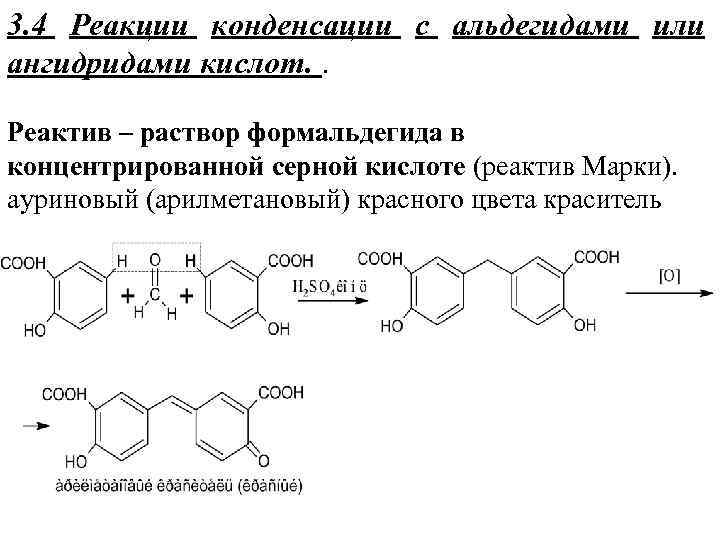
3. 4 Реакции конденсации с альдегидами или ангидридами кислот. . Реактив – раствор формальдегида в концентрированной серной кислоте (реактив Марки). ауриновый (арилметановый) красного цвета краситель
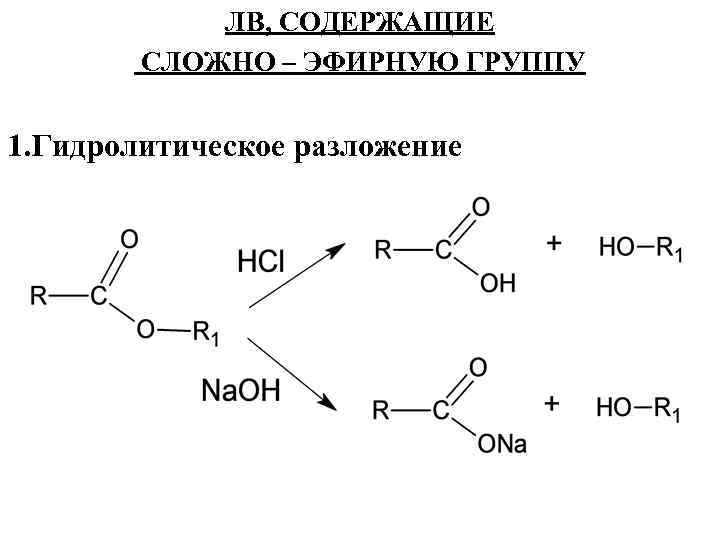
ЛВ, СОДЕРЖАЩИЕ СЛОЖНО – ЭФИРНУЮ ГРУППУ 1. Гидролитическое разложение
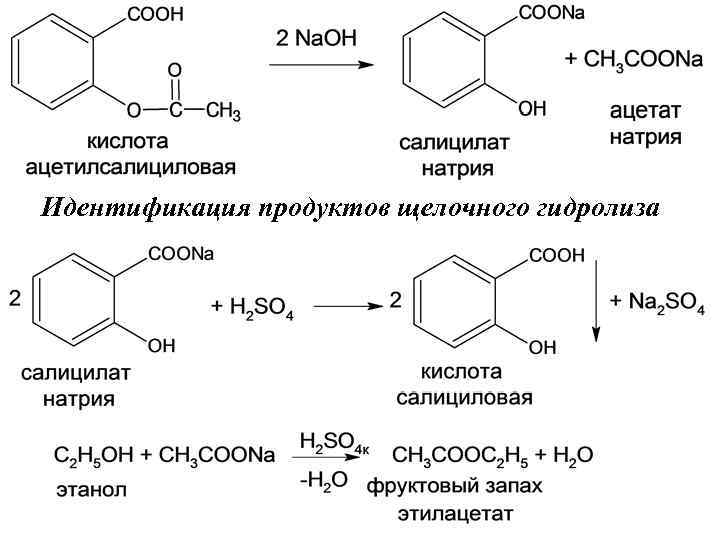
Идентификация продуктов щелочного гидролиза
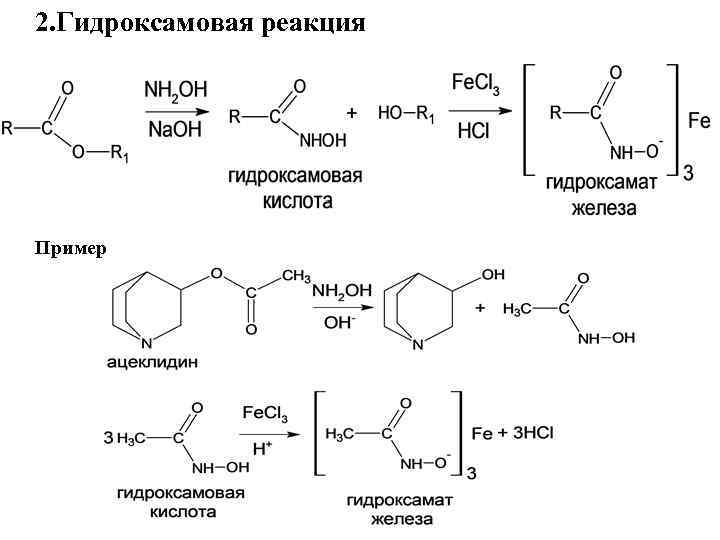
2. Гидроксамовая реакция Пример
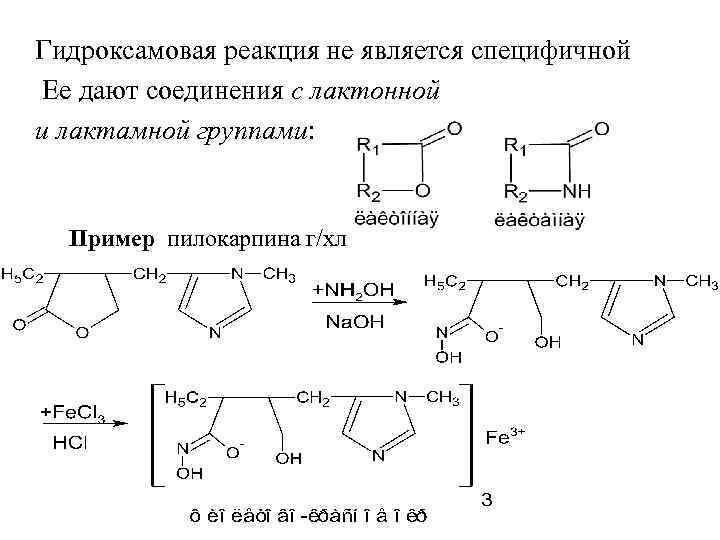
Гидроксамовая реакция не является специфичной Ее дают соединения с лактонной и лактамной группами: Пример пилокарпина г/хл

ЛВ, СОДЕРЖАЩИЕ ПЕРВИЧНУЮ АРОМАТИЧЕСКУЮ АМИНОГРУППУ для анализа используют реакции: 1. Реакция диазотирования с последующим азосочетанием 2. Окисление 3. Конденсация 4. Галогенирование 1. Реакция образования азокрасителя 1 стадия с нитритом натрия в кислой среде → бесцветные или светло-желтого цвета растворимые соли диазония:
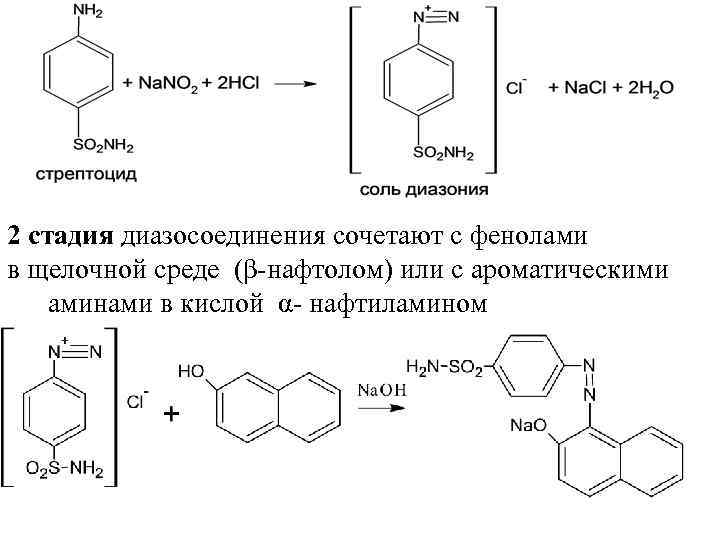
2 стадия диазосоединения сочетают с фенолами в щелочной среде (β-нафтолом) или с ароматическими аминами в кислой α- нафтиламином
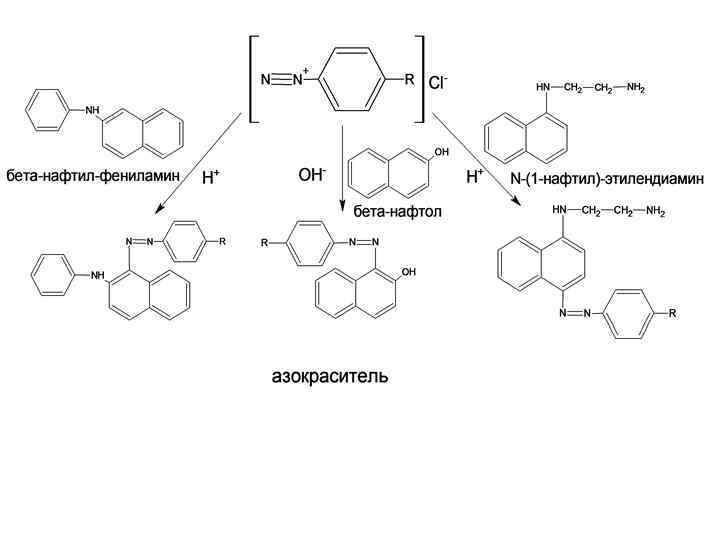
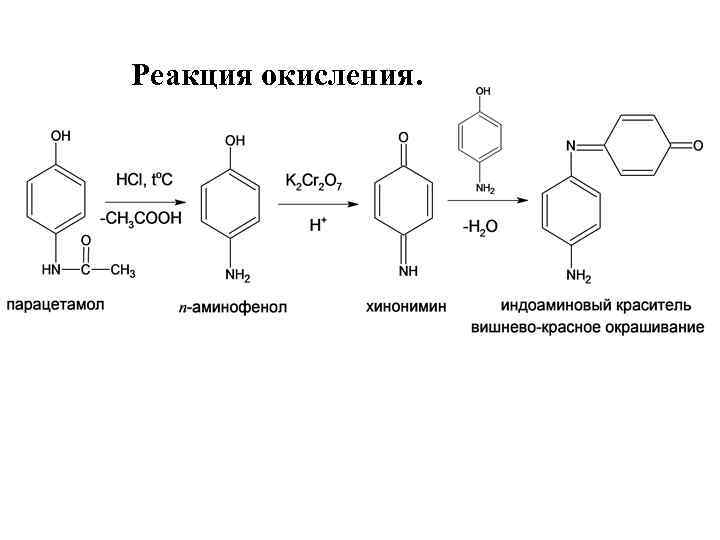
Реакция окисления.
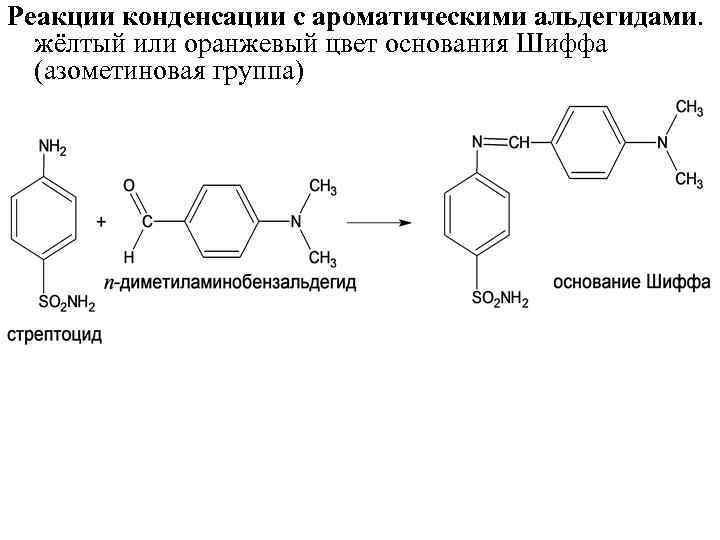
Реакции конденсации с ароматическими альдегидами. жёлтый или оранжевый цвет основания Шиффа (азометиновая группа)
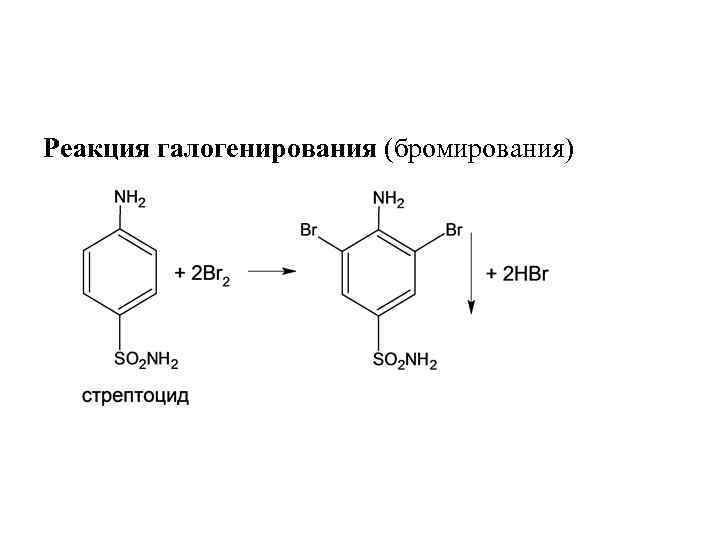
Реакция галогенирования (бромирования)
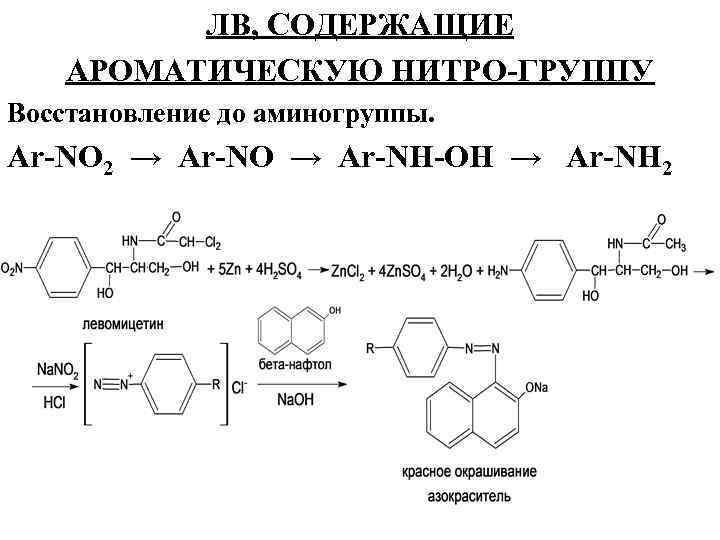
ЛВ, СОДЕРЖАЩИЕ АРОМАТИЧЕСКУЮ НИТРО-ГРУППУ Восстановление до аминогруппы. Ar-NO 2 → Ar-NO → Ar-NH-OH → Ar-NH 2
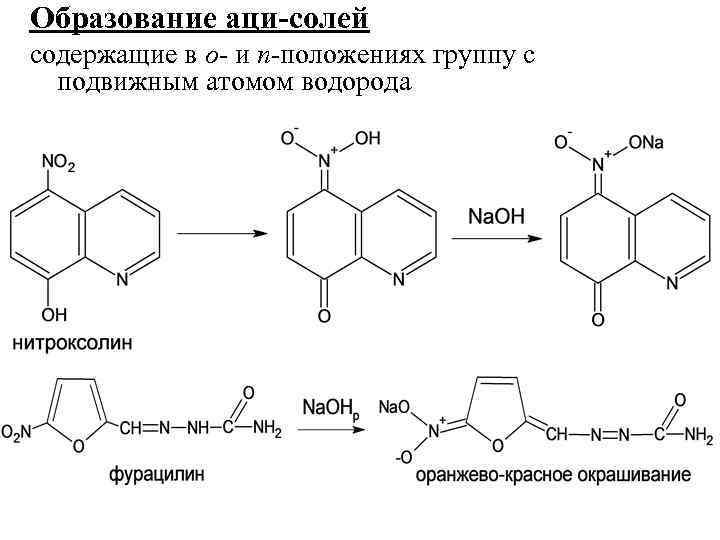
Образование аци-солей содержащие в о- и п-положениях группу с подвижным атомом водорода
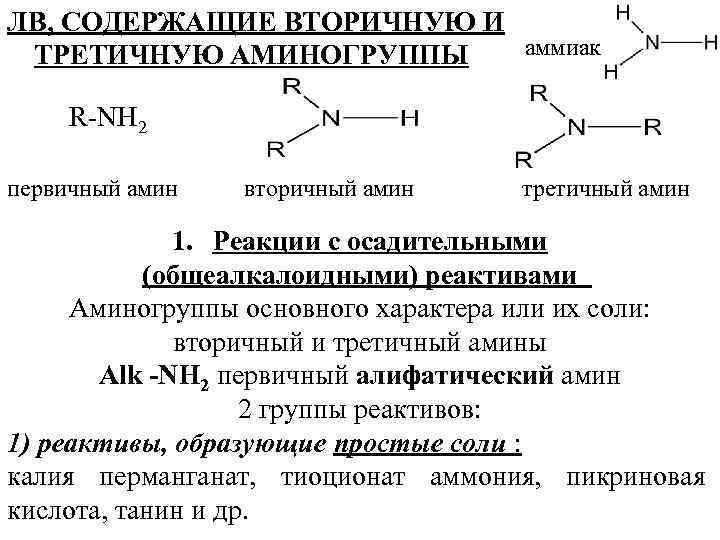
ЛВ, СОДЕРЖАЩИЕ ВТОРИЧНУЮ И аммиак ТРЕТИЧНУЮ АМИНОГРУППЫ R-NH 2 первичный амин вторичный амин третичный амин 1. Реакции с осадительными (общеалкалоидными) реактивами Аминогруппы основного характера или их соли: вторичный и третичный амины Alk -NH 2 первичный алифатический амин 2 группы реактивов: 1) реактивы, образующие простые соли : калия перманганат, тиоционат аммония, пикриновая кислота, танин и др.
![2. )реактивы, образующие комплексные соли Р-р I 2 в КI → [ KI 3] 2. )реактивы, образующие комплексные соли Р-р I 2 в КI → [ KI 3]](https://present5.com/presentation/55362899_22881121/image-51.jpg)
2. )реактивы, образующие комплексные соли Р-р I 2 в КI → [ KI 3] – реактив Бушарда, Вагнера, Люголя (отличаются концентрациями йода и калия йодида) Р-р Bi. I 3 в КI → K[Bi. I 4] – реактив Драгендорфа. Р-р Hg. I 2 в КI → K 2[Hg. I 4]– реактив Майера. Фосфорномолибденовая кислота H 3 PO 4 • 12 Mo. O 3 • 3 H 2 O– реактив Зонненштейна. Фосфорновольфрамовая кислота H 3 PO 4 • 12 Wo. O 3 • 3 H 2 O – реактив Шейблера
![1) [R 3 H+]Cl- + KMn. O 4 → [R 3 H+]Mn. O 4 1) [R 3 H+]Cl- + KMn. O 4 → [R 3 H+]Mn. O 4](https://present5.com/presentation/55362899_22881121/image-52.jpg)
1) [R 3 H+]Cl- + KMn. O 4 → [R 3 H+]Mn. O 4 - + KCl 2) R 3 N • HCl + n. I 2 + KI → R 3 N • n. I 2 • HI↓ + KCl R 3 N • HCl + KBi. I 4 → [R 3 N] • HBi. I 4 ↓ + KCl
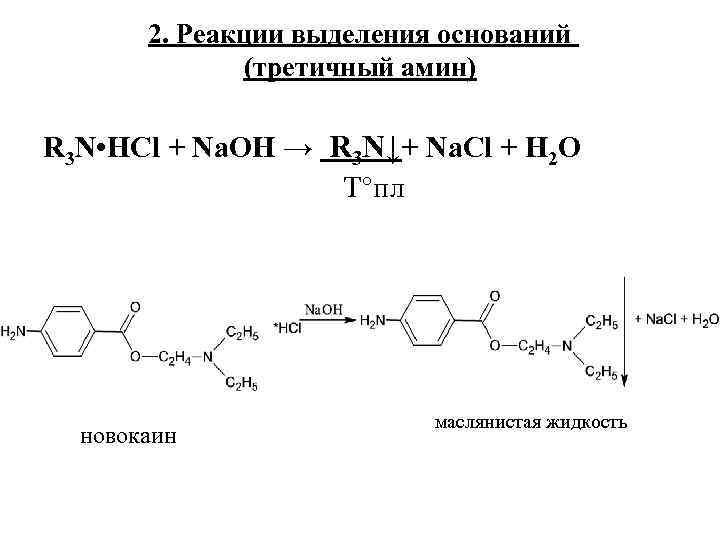
2. Реакции выделения оснований (третичный амин) R 3 N • HCl + Na. OH → R 3 N↓+ Na. Cl + H 2 O Т°пл новокаин маслянистая жидкость
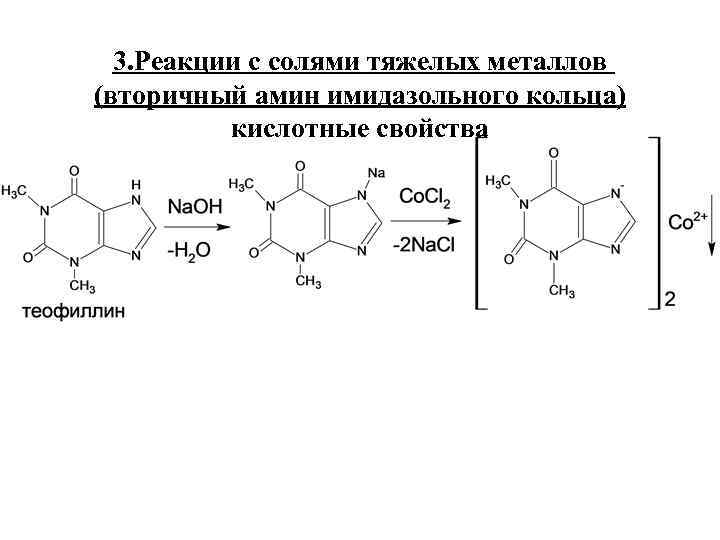
3. Реакции с солями тяжелых металлов (вторичный амин имидазольного кольца) кислотные свойства

ЛВ С КОВАЛЕНТНО СВЯЗАННЫМИ ГАЛОГЕНАМИ 1. гидролитическое разложение водным (бромизовал) или спиртовым (хлорэтил) раствором щелочи 2. восстановительная минерализация водородом в момент выделения (металлический цинк в щелочной среде, цинк в уксусной кислоте) – бромкамфора 3. сжигание в колбе с кислородом (для всех) 4. прокаливание со смесью для спекания (все, кроме фторсодержащих) 5. проба Бельштейна 6. специальные способы для йодсодержащих (нагревание в сухой пробирке, действие конц кислот) 7. непосредственное взаимодействие с реагентом, осаждающим галогенид-ионы (йодоформ с нитратом серебра).
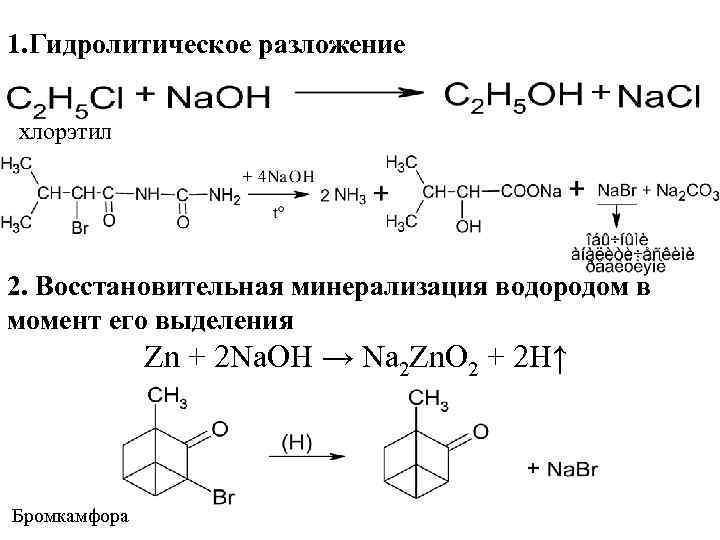
1. Гидролитическое разложение хлорэтил 2. Восстановительная минерализация водородом в момент его выделения Zn + 2 Na. OH → Na 2 Zn. O 2 + 2 H↑ Бромкамфора
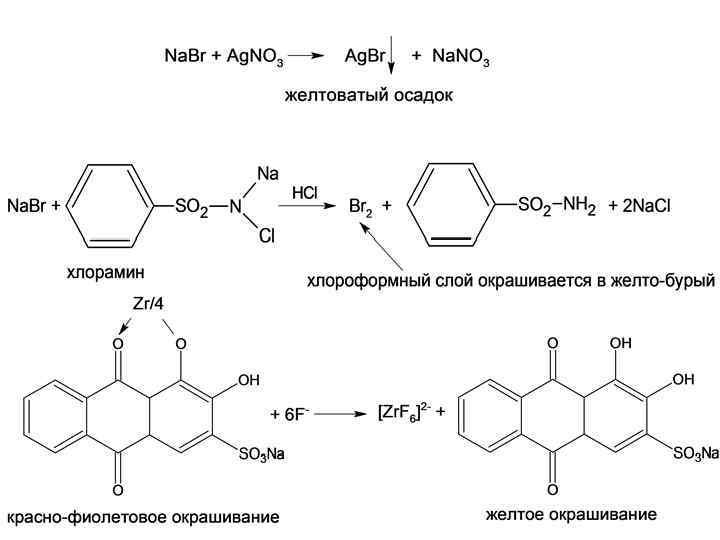
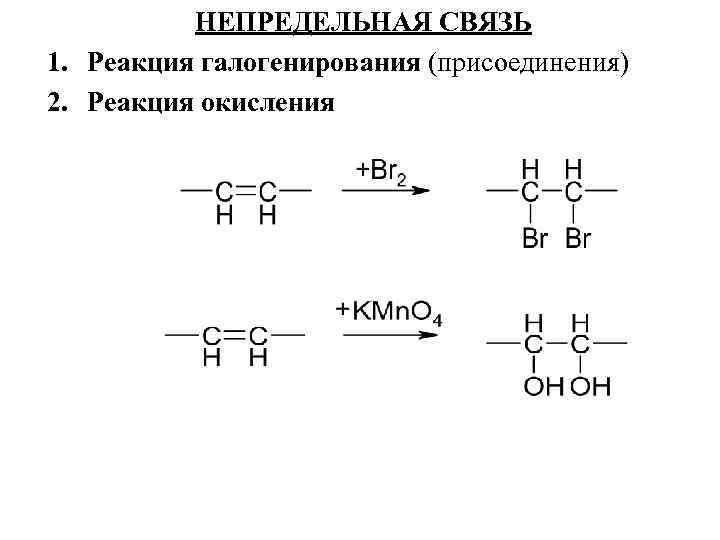
НЕПРЕДЕЛЬНАЯ СВЯЗЬ 1. Реакция галогенирования (присоединения) 2. Реакция окисления
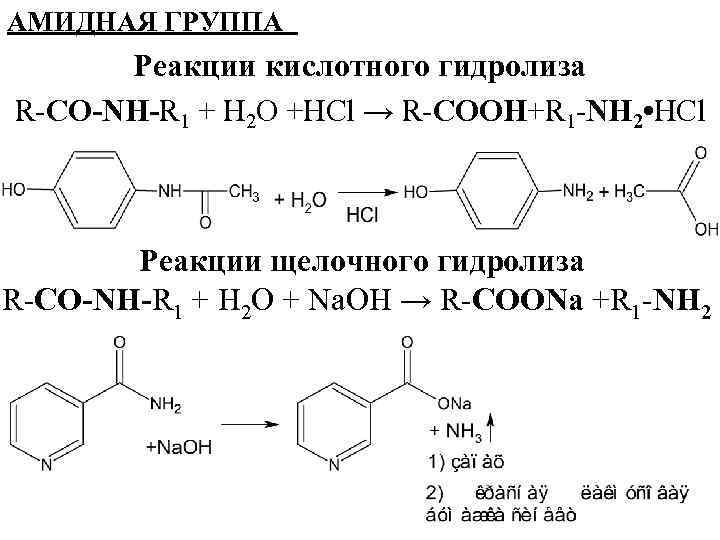
АМИДНАЯ ГРУППА Реакции кислотного гидролиза R-CO-NH-R 1 + H 2 O +HCl → R-COOH+R 1 -NH 2 • HCl Реакции щелочного гидролиза R-CO-NH-R 1 + H 2 O + Na. OH → R-COONa +R 1 -NH 2

ЛВ, СОДЕРЖАЩИЕ КОВАЛЕНТНО СВЯЗАННУЮ СЕРУ 1. окисление до сульфата (окислительная минерализация) Pb(CH 3 COO)2 + Na 2 S Pb. S↓ + 2 CH 3 COOH 2. восстановление до сульфида (восстановительная минерализация) Pb(CH 3 COO)2 + Na 2 S Pb. S↓ + 2 CH 3 COOH
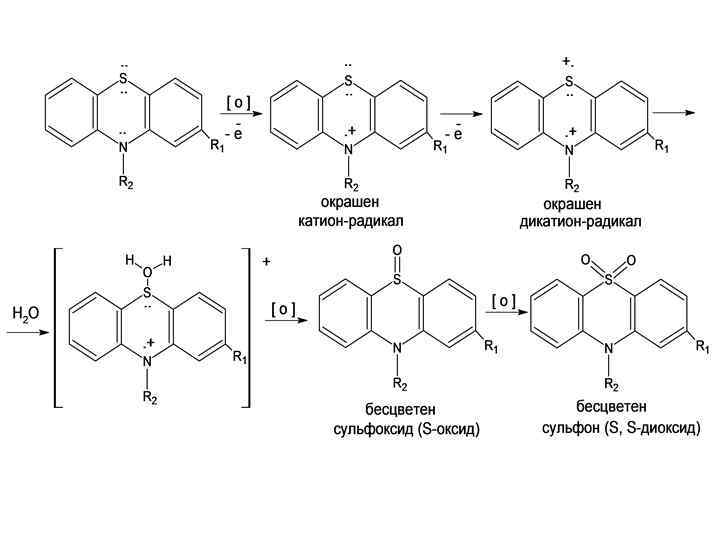
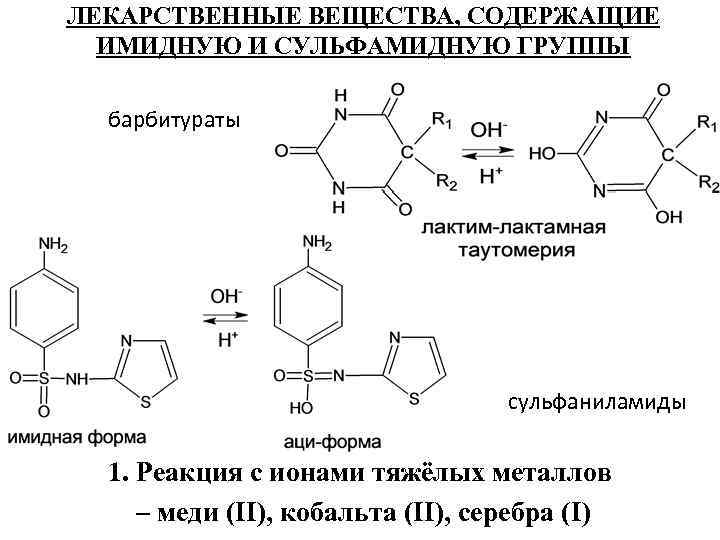
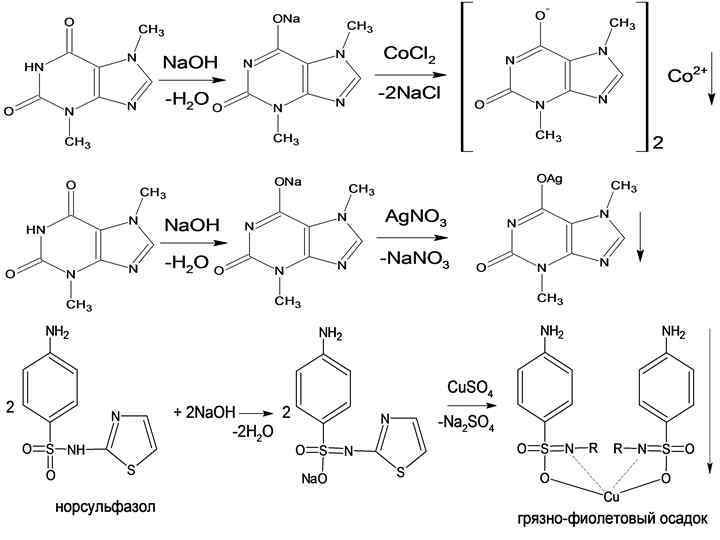
ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ ИМИДНУЮ И СУЛЬФАМИДНУЮ ГРУППЫ барбитураты сульфаниламиды 1. Реакция с ионами тяжёлых металлов – меди (II), кобальта (II), серебра (I)
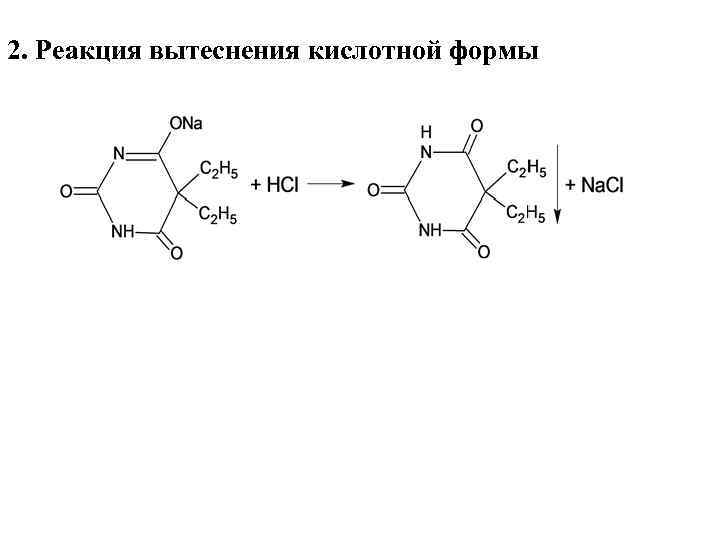
2. Реакция вытеснения кислотной формы
8 функциональный анализ.pptx