харак VIA гр.pptx
- Количество слайдов: 9

Общая характеристика халькогенов − элементов Положение в ПСХЭ

Халькогены — «рождающие руды» — химические элементы главной подгруппы VI группы

Положение халькогенов в ПСХЭ Элементы главной подгруппы VI (VI-А) группы «Халькогены» − рождающие руды (O, S, Se, Te, Po) Элемент Кислород Сера Селен Теллур Полоний ЭО Окислительная Неметалличность Радиус активность атома

Распространенность элемента кислорода в природе. • Кислород – самый распространенный элемент на нашей планете; • На долю кислорода приходится приблизительно половина всей массы земной коры; • В почвах , грунтовых , речных и морских водах кислород выступает настоящим геохимическим диктатором.

Распространенность элемента серы в природе • Относится к весьма распространенным химическим элементам; • Встречается в свободном состоянии (самородная сера); • Встречается в виде соединений - сульфидов, полисульфидов, сульфатов; • Вода морей и океанов содержит сульфаты натрия, магния, кальция; • Известно более 200 минералов Серы, образующихся при эндогенных процессах; • В биосфере образуется свыше 150 минералов Серы (преимущественно сульфатов)

Основное состояние атома кислорода 2 p 2 s ↑↓ ↑ ↑ ↑↓ ОVIA =… 2 s 22 р4 В основном (невозбужденном) состоянии кислород двухвалентен потому, что у него на двух p-орбиталях (из трех имеющихся) находится по одному электрону, переход в возбужденное состояние не выгоден 2 d подуровень не существует
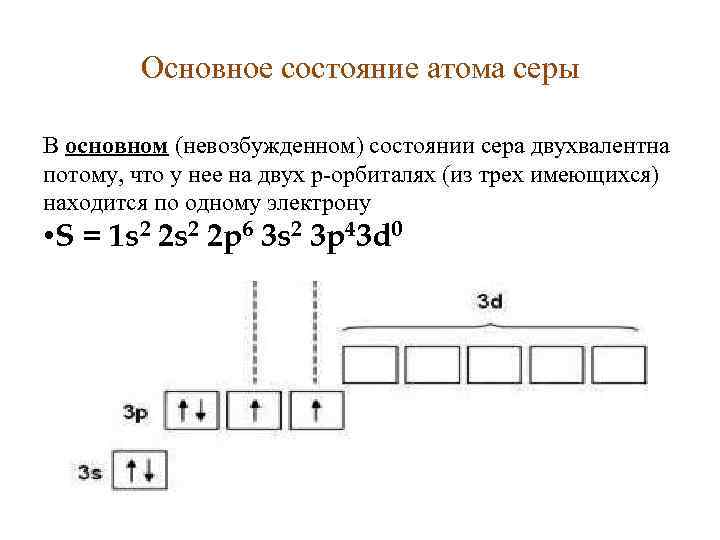
Основное состояние атома серы В основном (невозбужденном) состоянии сера двухвалентна потому, что у нее на двух p-орбиталях (из трех имеющихся) находится по одному электрону • S = 1 s 2 2 p 6 3 s 2 3 p 43 d 0
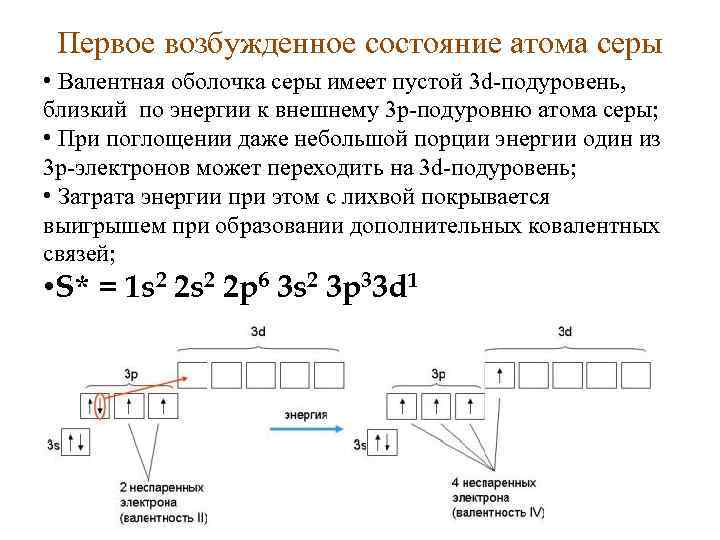
Первое возбужденное состояние атома серы • Валентная оболочка серы имеет пустой 3 d-подуровень, близкий по энергии к внешнему 3 p-подуровню атома серы; • При поглощении даже небольшой порции энергии один из 3 p-электронов может переходить на 3 d-подуровень; • Затрата энергии при этом с лихвой покрывается выигрышем при образовании дополнительных ковалентных связей; • S* = 1 s 2 2 p 6 3 s 2 3 p 33 d 1
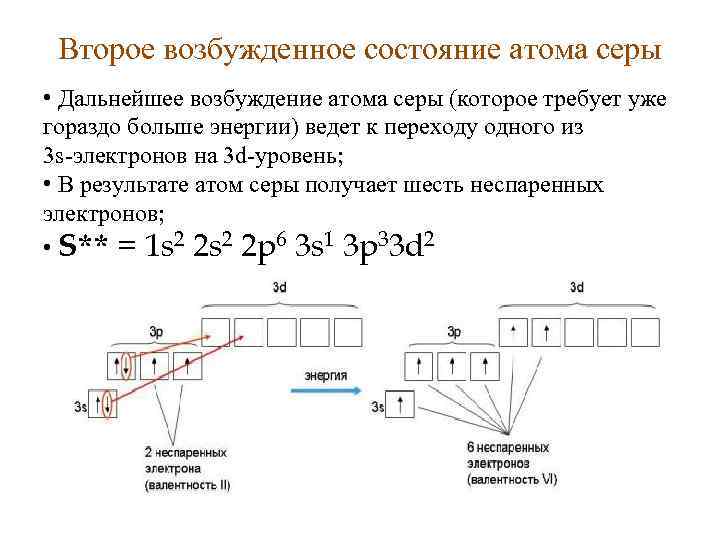
Второе возбужденное состояние атома серы • Дальнейшее возбуждение атома серы (которое требует уже гораздо больше энергии) ведет к переходу одного из 3 s-электронов на 3 d-уровень; • В результате атом серы получает шесть неспаренных электронов; • S** = 1 s 2 2 p 6 3 s 1 3 p 33 d 2
харак VIA гр.pptx