Обмен углеводов.ppt
- Количество слайдов: 122


Общая характеристика углеводов Углеводы – органические соединения, содержащие альдегидную или кетонную группу и несколько гидроксильных групп. Их элементарный состав выражается формулой Cm(H 2 O)n, но она не совсем верна, т. к. существуют соединения в которых водород и кислород содержатся в несколько иной пропорции. Например, дезоксирибоза – С 5 Н 10 О 4. В 1927 г. Международная комиссия по реформе химической номенклатуры предложила термин «углеводы» заменить термином «глициды» (или «глюциды» ). глициды

Функции углеводов в организме Канонические (общие) функции: Ø Энергетическая Ø Структурная (пластическая) Ø Метаболическая Неканонические функции: Ø Защитная (Пример: мукополисахариды) Ø Регуляторная (Пример: клетчатка) Ø Обеспечение специфичности групп крови (Групповые вещества крови – гликопротеины) Ø Рецепторные функции Ø Информационная

Процессы углеводного обмена 1. Расщепление поли- и дисахаридов до моносахаридов в ЖКТ. Всасывание моносахаридов из кишечника в кровь. 2. Синтез и распад гликогена в тканях (в печени). 3. Анаэробное и аэробное расщепление глюкозы: глюкозы • анаэробный путь – гликолиз (дихотомический путь); • аэробный путь – пентозофосфатный цикл (апотомический путь). 4. Взаимопревращение гексоз 5. Аэробный метаболизм ПВК 6. Глюконеогенез – образование углеводов из неуглеводных веществ.


Переваривание начинается в ротовой полости. Гидролиз крахмала ускоряется амилазами: амилазами ü -амилаза Ускоряет гидролиз 1, 4 -гликозидных связей в молекуле крахмала без какого-либо определенного порядка, в результате чего сначала возникают олигосахариды (следовательно -амилаза – эндоамилаза). Конечным продуктом ее действия является -мальтоза.

ü -амилаза Отщепляет от молекулы крахмала остатки мальтозы начиная с нередуцирующего конца молекулы крахмала (следовательно амилаза – экзоамилаза). Ее действие прекращается в местах разветвлений в молекуле крахмала.

ü γ-амилаза (глюкоамилаза) Последовательно отщепляет остатки глюкозы от невосстанавливающего конца молекулы крахмала или гликогена, олиго- и даже дисахаридов (мальтозы). Действие ее прекращается в местах разветвления молекулы полисахарида.
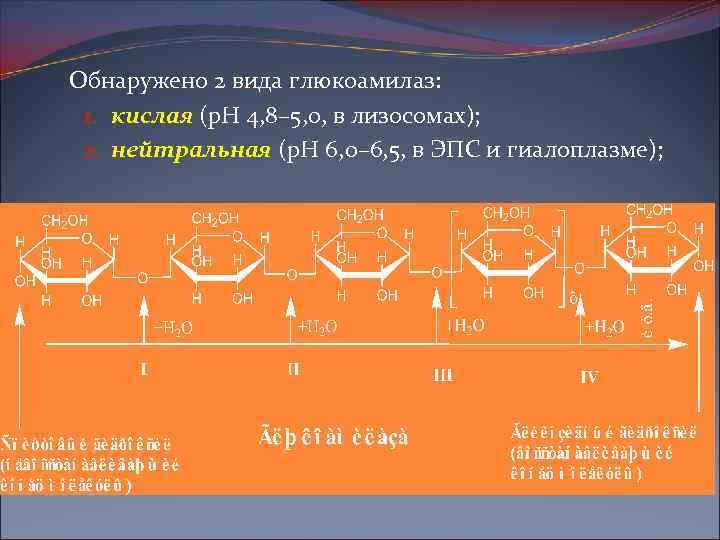
Обнаружено 2 вида глюкоамилаз: 1. кислая (р. Н 4, 8– 5, 0, в лизосомах); 2. нейтральная (р. Н 6, 0– 6, 5, в ЭПС и гиалоплазме);

ü амило-1, 6 -глюкозидаза Ускоряет реакцию гидролиза 1, 6 связей в молекуле крахмала (амилопектина), расщепляя, таким образом, молекулу крахмала в точках разветвления полиглюкозидпой цепи и образуя олигосахариды с тем или иным числом остатков α-D-глюкозы
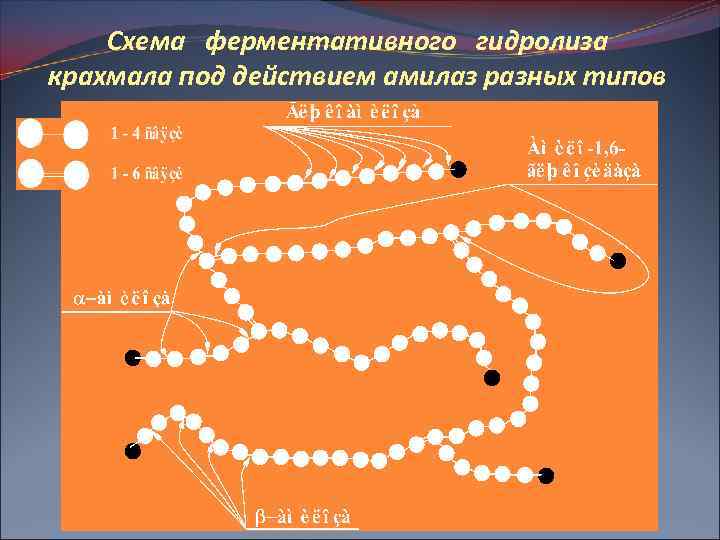
Схема ферментативного гидролиза крахмала под действием амилаз разных типов

Для амилаз характерно отсутствие абсолютной специфичности
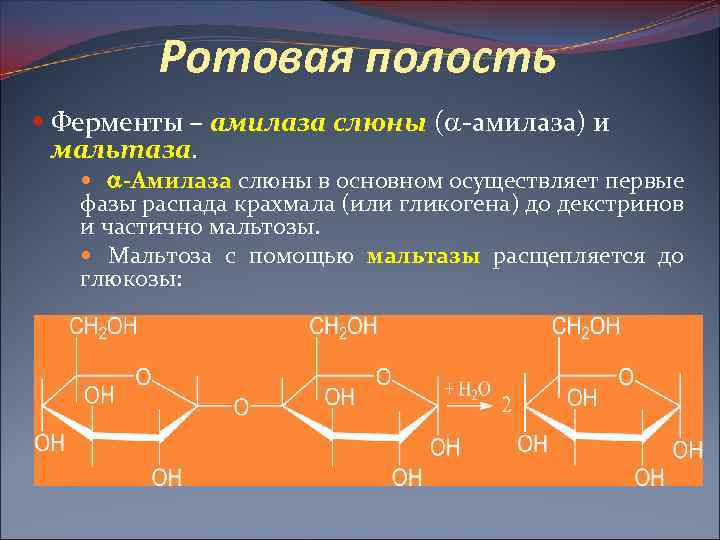
Ротовая полость Ферменты – амилаза слюны ( -амилаза) и мальтаза -Амилаза слюны в основном осуществляет первые фазы распада крахмала (или гликогена) до декстринов и частично мальтозы. Мальтоза с помощью мальтазы расщепляется до глюкозы:

Желудок Желудочный сок не содержит ферменты, расщепляющие сложные углеводы, а амилаза слюны инактивируется кислой средой (р. Н желудочного сока 1, 5– 2, 5, тогда как оптимум р. Н -амилазы 6, 8– 7, 2). Однако в более глубоких слоях пищевого комка, куда не сразу проникает желудочный сок, действие амилазы слюны некоторое время продолжается и происходит расщепление полисахаридов до декстринов и мальтозы.

Двенадцатиперстная кишка Крахмал (и гликоген) расщепляется под действием панкреатической -амилазы р. Н близок к нейтральному, поэтому -амилаза панкреатического сока максимально активна. Этот фермент завершает превращение крахмала (и гликогена) в мальтозу. 1, 6 -гликозидные связи гидролизуются амило 1, 6 -гликозидазой Мальтоза гидролизуется до глюкозы под влиянием мальтазы
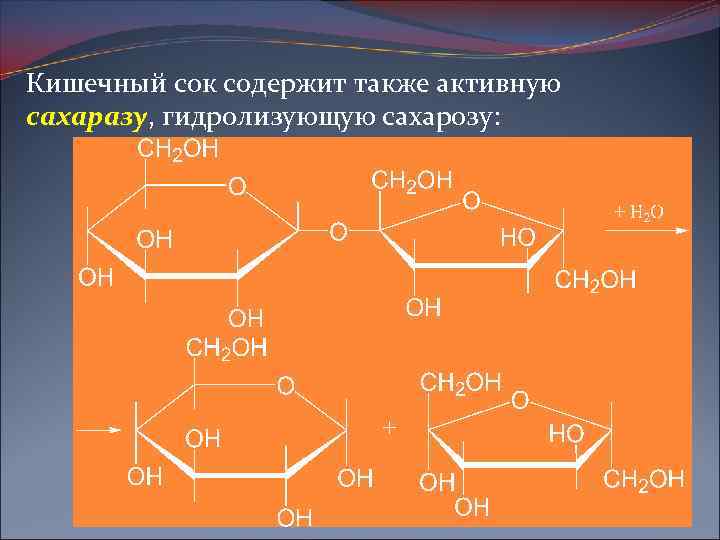
Кишечный сок содержит также активную сахаразу, гидролизующую сахарозу: сахаразу
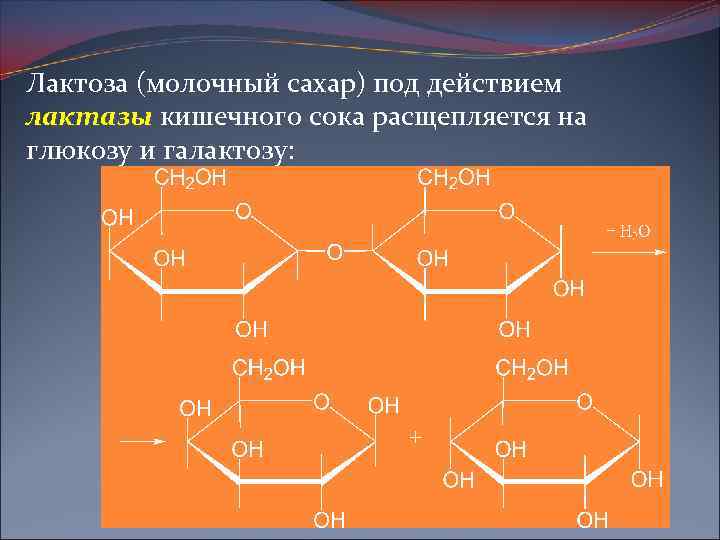
Лактоза (молочный сахар) под действием лактазы кишечного сока расщепляется на глюкозу и галактозу:

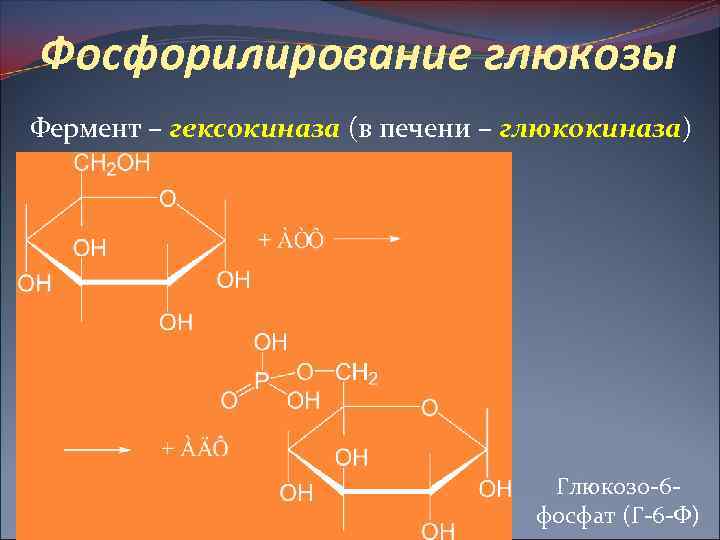
Фосфорилирование глюкозы Фермент – гексокиназа (в печени – глюкокиназа) Глюкозо-6 фосфат (Г-6 -Ф)
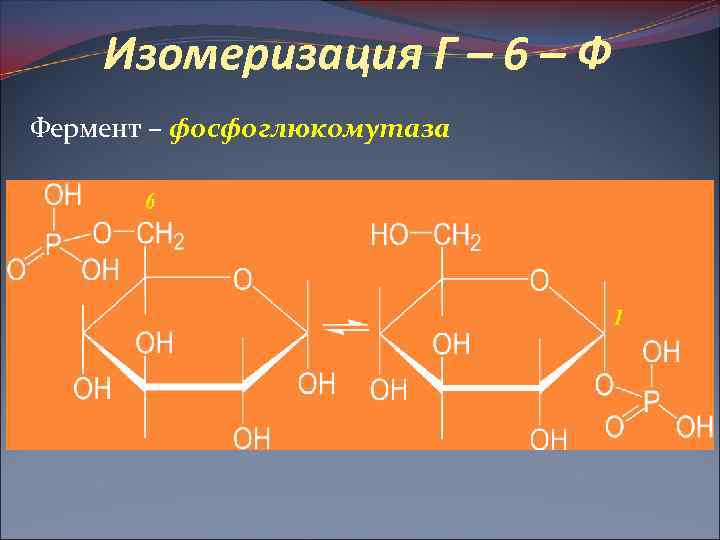
Изомеризация Г – 6 – Ф Фермент – фосфоглюкомутаза

I стадия синтеза гликогена Г-1 -Ф взаимодействует с уридинтрифосфатом (УТФ) с образованием уридиндифосфатглюкозы (УДФ-глюкозы) и пирофосфата. Фермент – глюкозо-1 -фосфат-уридилилтрансфераза (УДФГ-пирофосфатаза):
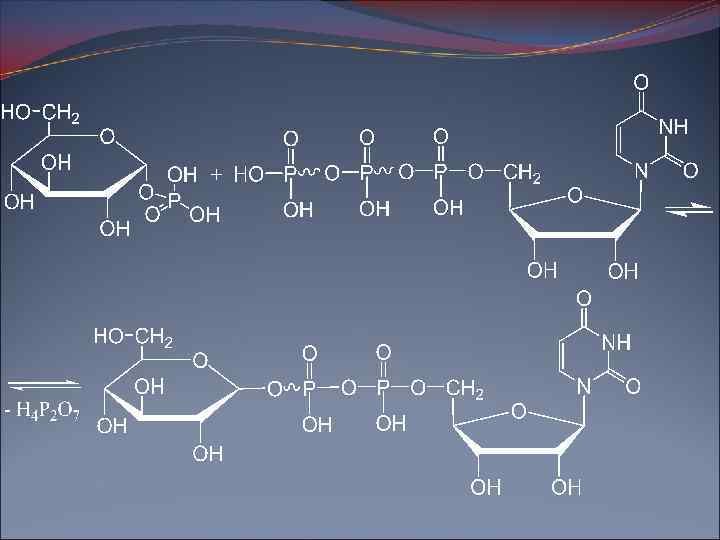

II стадия синтеза гликогена Перенос глюкозного остатка, входящего в состав УДФ-глюкозы, на глюкозидную цепь гликогена; При этом образуется (1– 4)-гликозидная связь между атомом С 1 добавляемого остатка глюкозы и гидроксильной группой атома С 4 остатка глюкозы растущей цепи. Фермент – гликогенсинтаза: гликогенсинтаза УДФ-глюкоза + (С 6 Н 10 О 5)n → УДФ + (С 6 Н 10 О 5)n+1. УДФ вновь фосфорилируется в УТФ за счет АТФ, и цикл превращения Г-1 -Ф начинается сначала.
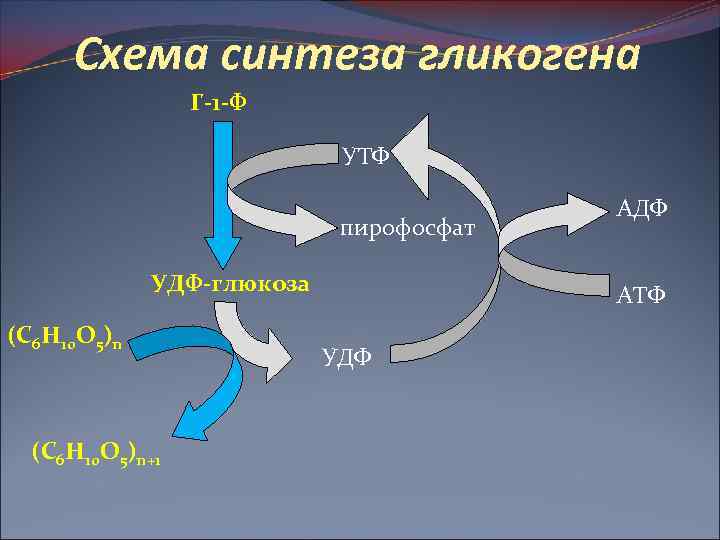
Схема синтеза гликогена Г-1 -Ф УТФ пирофосфат УДФ-глюкоза (С 6 Н 10 О 5)n+1 АДФ АТФ УДФ

Образование 1, 6 -гликозидных связей происходит с помощью гликогенветвящего фермента Благодаря способности к отложению гликогена (в печени, мышцах и др. ) создаются условия для накопления в норме некоторого резерва углеводов.


Главным в распаде гликогена является процесс фосфоролиза, а не гидролиза. фосфоролиза Фосфоролиз происходит под действием ферментов фосфорилаз, которые переводят фосфорилаз полисахариды из запасной формы в метаболически активную. В присутствии фосфорилазы гликоген распадается с образованием Г-1 -Ф: (С 6 Н 10 О 5)n + Н 3 РО 4 → (С 6 Н 10 О 5)n– 1 + Г-1 -Ф.

Регуляция активности фосфорилазы Активность фосфорилаз, как и, следовательно, процесс фосфоролиза в целом, тонко регулируется
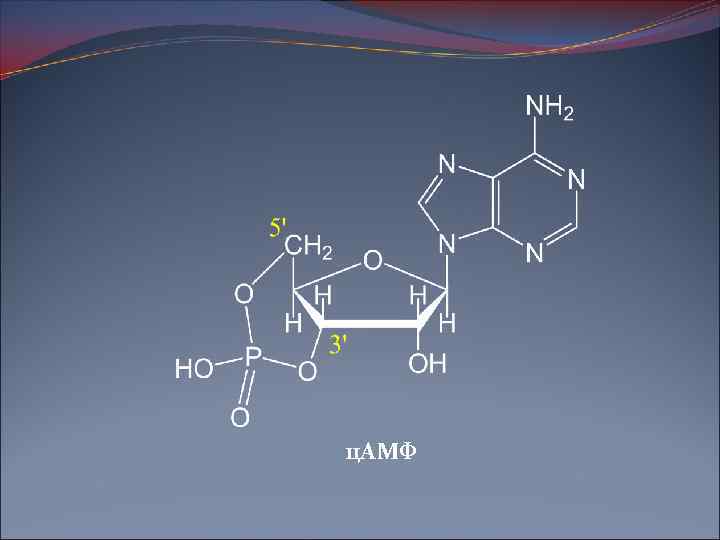
ц. АМФ

Глюкогенез Фосфорилаза а отщепляет остатки глюкозы от периферического конца наружных ветвей молекулы гликогена При приближении к 1, 6 -связям начинает работать фермент амило-1, 6 -глюкозидаза, после чего фосфорилаза а продолжает действовать до новой точки ветвления. Образовавшийся Г-1 -Ф превращается в Г-6 -Ф под действием фосфоглюкомутазы, которая активируется глюкозо-1, 6 -дифосфатом (Г-1, 6 -д. Ф), выполняющим функцию кофермента. Образование глюкозы из Г-6 -Ф в печени происходит под влиянием глюкозо-6 -фосфатазы: Г-6 -Ф + Н 2 О → С 6 Н 12 О 6 + Н 3 РО 4.


Сохранение постоянства концентрации сахара в крови есть прежде всего результат одновременного протекания двух процессов: • поступления глюкозы в кровь из печени • потребления ее из крови тканями, где она используется как источник энергии (в первую очередь).

Превращение моносахаридов В дальнейшем обмене используются только фосфорные эфиры моносахаридов, свободные же монозы фосфорилируются. Фосфорилирование моносахаридов часто рассматривается как реакция активирования. Фосфорилирование моносахаридов осуществляется при взаимодействии их с АТФ и ускоряется ферментами фосфотрансферазами (киназами). Важнейшей особенностью фосфорных эфиров моносахаридов является их способность к изомеризации, что дает возможность перехода от одной гексозы или пентозы к другой, изомерной ей.


Гликолиз – сложный ферментативный процесс превращения глюкозы, протекающий в тканях человека и животных без потребления кислорода. Гликолиз является первым, а в анаэробных условиях основным этапом на пути использования глюкозы и других углеводов для обеспечения биоэнергетических потребностей живых организмов. На промежуточных стадиях гликолиза образуются трехуглеродные фрагменты, используемые для биосинтеза ряда веществ. У ряда микроорганизмов процессами, аналогичными гликолизу, являются различные виды брожения. Процесс гликолиза катализируется 11 -ю ферментами и протекает в гиалоплазме клеток.
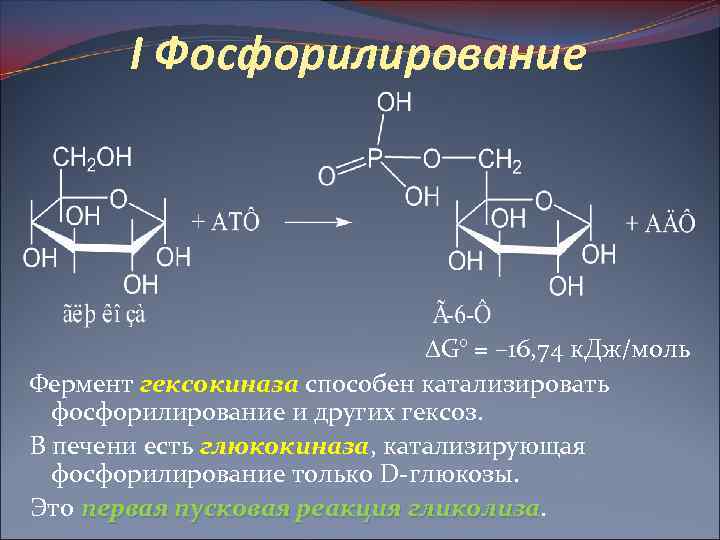
I Фосфорилирование G° = – 16, 74 к. Дж/моль Фермент гексокиназа способен катализировать фосфорилирование и других гексоз. В печени есть глюкокиназа, катализирующая фосфорилирование только D-глюкозы. Это первая пусковая реакция гликолиза
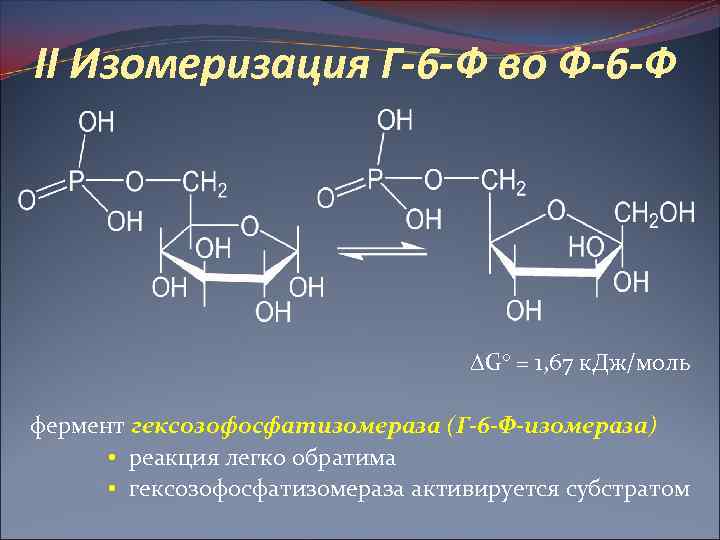
II Изомеризация Г-6 -Ф во Ф-6 -Ф G° = 1, 67 к. Дж/моль фермент гексозофосфатизомераза (Г-6 -Ф-изомераза) • реакция легко обратима • гексозофосфатизомераза активируется субстратом
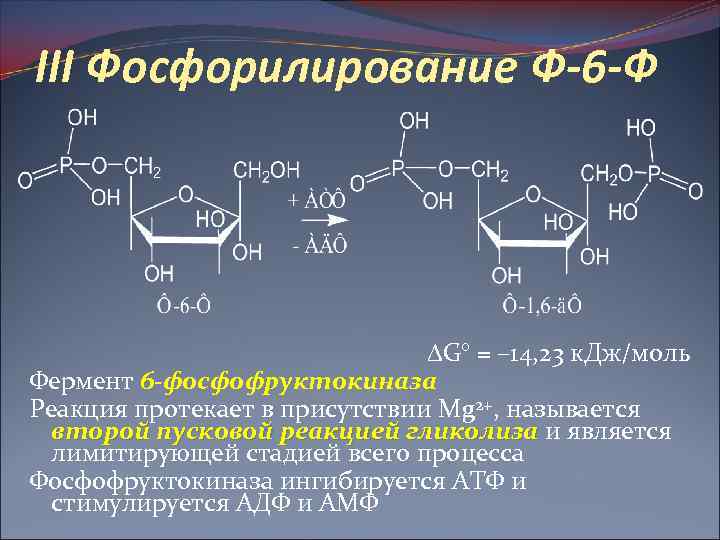
III Фосфорилирование Ф-6 -Ф G° = – 14, 23 к. Дж/моль Фермент 6 -фосфофруктокиназа Реакция протекает в присутствии Mg 2+, называется второй пусковой реакцией гликолиза и является лимитирующей стадией всего процесса Фосфофруктокиназа ингибируется АТФ и стимулируется АДФ и АМФ
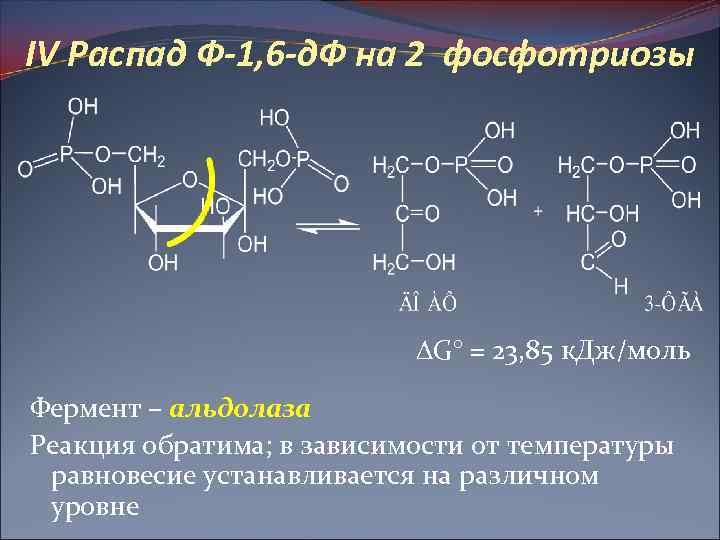
IV Распад Ф-1, 6 -д. Ф на 2 фосфотриозы G° = 23, 85 к. Дж/моль Фермент – альдолаза Реакция обратима; в зависимости от температуры равновесие устанавливается на различном уровне
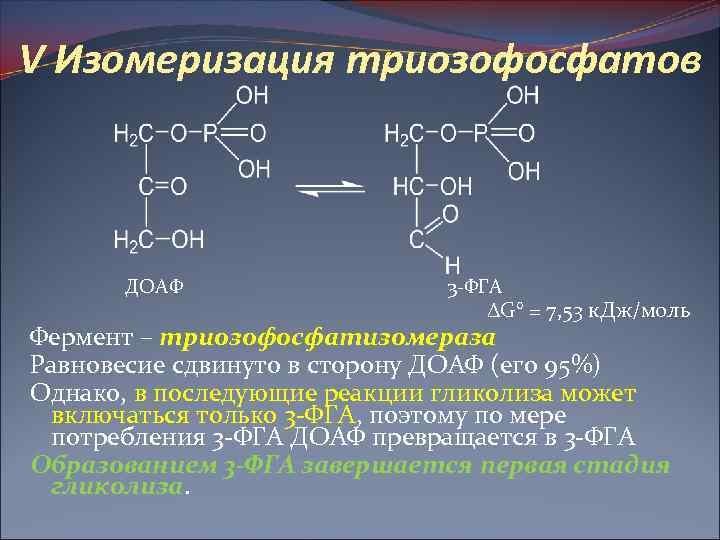
V Изомеризация триозофосфатов ДОАФ 3 -ФГА G° = 7, 53 к. Дж/моль Фермент – триозофосфатизомераза Равновесие сдвинуто в сторону ДОАФ (его 95%) Однако, в последующие реакции гликолиза может включаться только 3 -ФГА, поэтому по мере потребления 3 -ФГА ДОАФ превращается в 3 -ФГА Образованием 3 -ФГА завершается первая стадия гликолиза.

VI Окисление 3 -ФГА 1, 3 -д. ФГК G° = 6, 28 к. Дж/моль Фермент - глицеральдегид-3 -фосфатдегидрогеназа (кофермент – НАД) 1, 3 -д. ФГК – макроэргическое соединение

VI Окисление 3 -ФГА 1, 3 -д. ФГК Реакция происходит через промежуточное образование тиоэфира между окисляемой альдегидной группой и группой –SН остатка цистеина, входящего в активный центр фермента. Эта связь затем подвергается фосфоролизу с регенерацией активного центра и образованием смешанного ангидрида 3 -фосфоглицериновой и фосфорной кислот: Е–SН + ОНС–СН(ОН)–СН 2–О–РО(ОН)2 + НАД ⇄ ⇄ Е–S СО–СН(ОН)–СН 2–О–РО(ОН)2 + НАДН 2; Е–S СО–СН(ОН)–СН 2–О–РО(ОН)2 + Н 3 РО 4 ⇄ ⇄ Е–SН + (ОН)2 РО О–СО–СН(ОН)–СН 2–О–РО(ОН)2
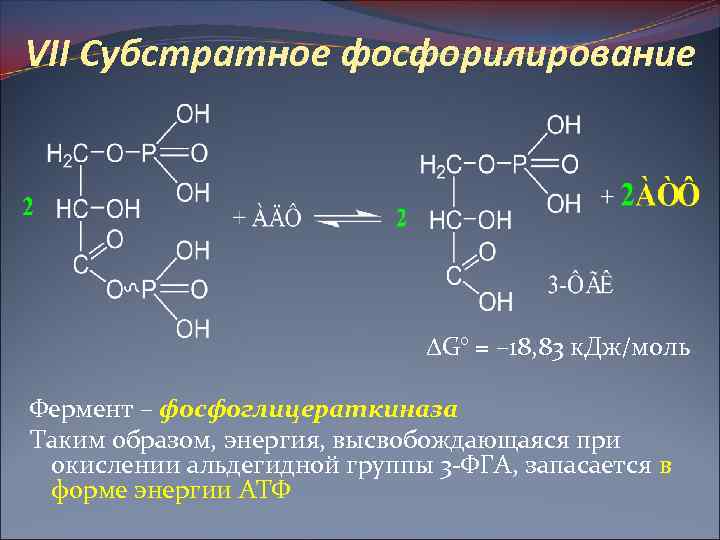
VII Субстратное фосфорилирование G° = – 18, 83 к. Дж/моль Фермент – фосфоглицераткиназа Таким образом, энергия, высвобождающаяся при окислении альдегидной группы 3 -ФГА, запасается в форме энергии АТФ
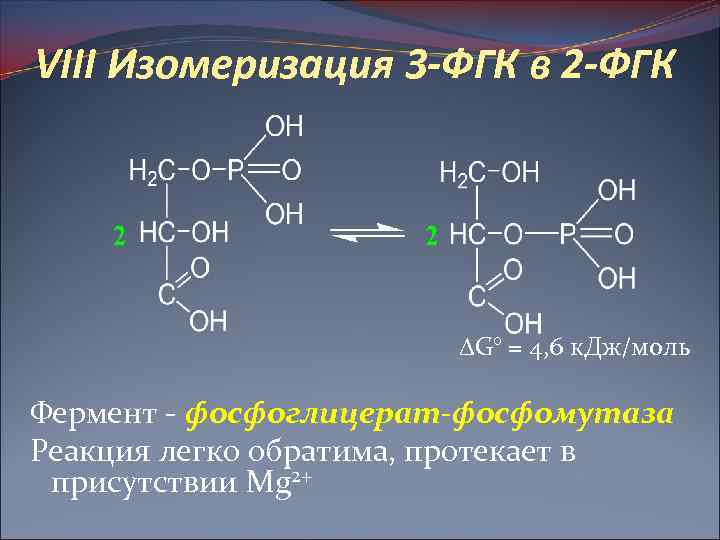
VIII Изомеризация 3 -ФГК в 2 -ФГК G° = 4, 6 к. Дж/моль Фермент - фосфоглицерат-фосфомутаза Реакция легко обратима, протекает в присутствии Mg 2+
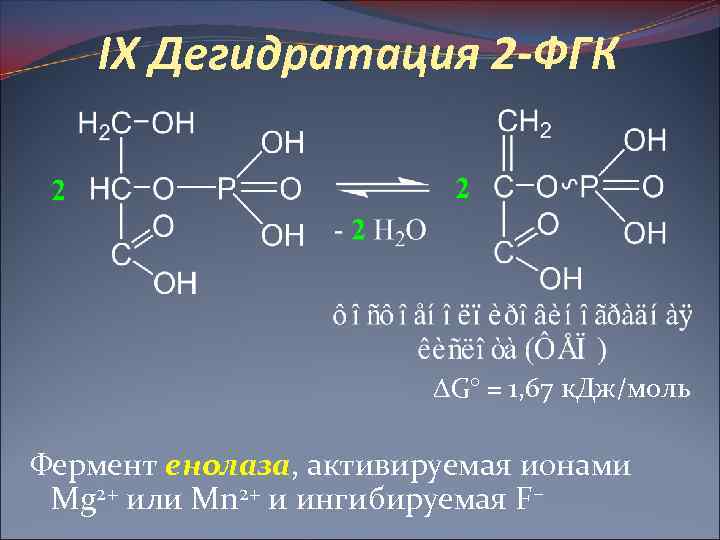
IX Дегидратация 2 -ФГК G° = 1, 67 к. Дж/моль Фермент енолаза, активируемая ионами Mg 2+ или Mn 2+ и ингибируемая F–
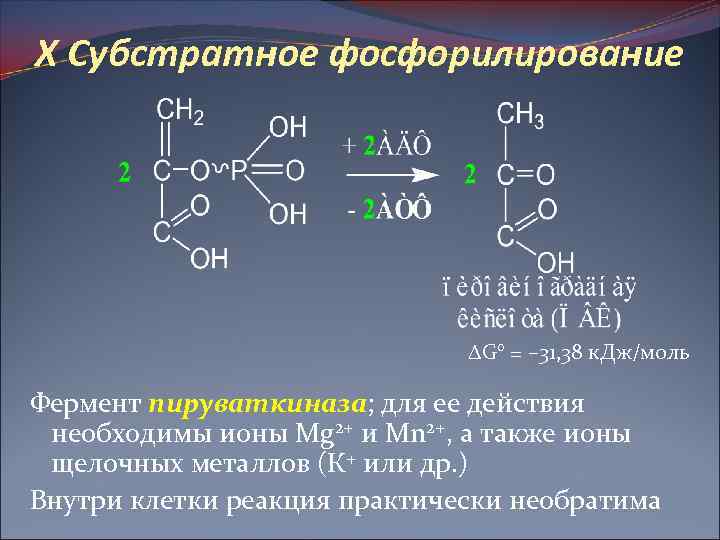
X Субстратное фосфорилирование G° = – 31, 38 к. Дж/моль Фермент пируваткиназа; для ее действия необходимы ионы Mg 2+ и Mn 2+, а также ионы щелочных металлов (К+ или др. ) Внутри клетки реакция практически необратима

Схема гликолиза

Суммарное уравнение гликолиза С 6 Н 12 О 6 + 2 НАД + 2 АДФ + 2 Н 3 РО 4 → → 2 СН 3–СО–СООН + 2 НАДН 2 + 2 АТФ 6 АТФ 8 АТФ

Биологическое значение процесса гликолиза заключается прежде всего в образовании макроэргических соединений. В первой стадии гликолиза затрачиваются 2 АТФ; во второй стадии образуются 4 АТФ. Таким образом, энергетическая эффективность гликолиза составляет 2 молекулы АТФ на 1 молекулу глюкозы Если гликолиз начинается не с глюкозы, а с гликогена или крахмала (гликогенолиз), то накапливаются не 2, а 3 молекулы АТФ (т. к. на образование Г-6 -Ф не тратится АТФ). Однако в энергетическом плане гликолиз и гликогенолиз практически равноценны, т. к. на синтез гликогена в тканях расходуется АТФ.


Анаэробные условия • Восстановление до молочной кислоты (молочнокислое брожение, окончание гликолиза); • Спиртовое брожение; • другие виды брожения.

I В анаэробных условиях – восстановление до молочной кислоты Фермент – лактатдегидрогеназа Другие названия процесса – молочнокислое брожение, окончание гликолиза (в зависимости от локализации)

Молочная кислота накапливается при активной мышечной работе и вызывает утомление мышц. Часть молочной кислоты в аэробных условиях окисляется до СО 2 и Н 2 О (1/5 – 1/6) или идет на ресинтез гликогена. G° 310 расщепления глюкозы до молочной кислоты (С 6 Н 12 О 6 → 2 С 3 Н 6 О 3) составляет ~210 к. Дж/моль. Из этого количества энергии ~126 к. Дж рассеивается в виде тепла, а ~84 к. Дж накапливается в форме АТФ. Концевая макроэргическая связь АТФ соответствует примерно 33, 6– 42, 0 к. Дж/моль. Таким образом, КПД гликолиза (до молочной кислоты) составляет около 0, 4. Молочнокислое брожение осуществляется

II В анаэробных условиях – спиртовое брожение Осуществляется дрожжеподобными организмами и некоторыми плесневыми грибами: С 6 Н 12 О 6 → 2 СО 2 + 2 С 2 Н 5 ОН. По механизму близко к гликолизу. При спиртовом брожении ПВК вначале подвергается декарбоксилированию под действием фермента пируватдекарбоксилазы, которая требует наличия Mg 2+ и кофермента тиаминпирофосфата: СН 3–СО–СООН → СН 3–СНО + СО 2 Затем уксусный альдегид восстанавливается в этанол при участии фермента алкогольдегидрогеназы: СН 3–СНО + НАДН 2 → СН 3–СН 2–ОН + НАД Существуют и другие виды брожения, отличающиеся конечными продуктами

III В аэробных условиях – окислительное декарбокислирование (дыхание) ПВК подвергается окислительному декарбоксилированию с образованием ацетил. Ко. А, который затем может окисляться до СО 2 и Н 2 О. СН 3–СО–СООН + НАД + НSКо. А → → СО 2 + СН 3–СО SКо. А + НАДН 2 Мультиэнзимный комплекс – пируватдегидрогеназный
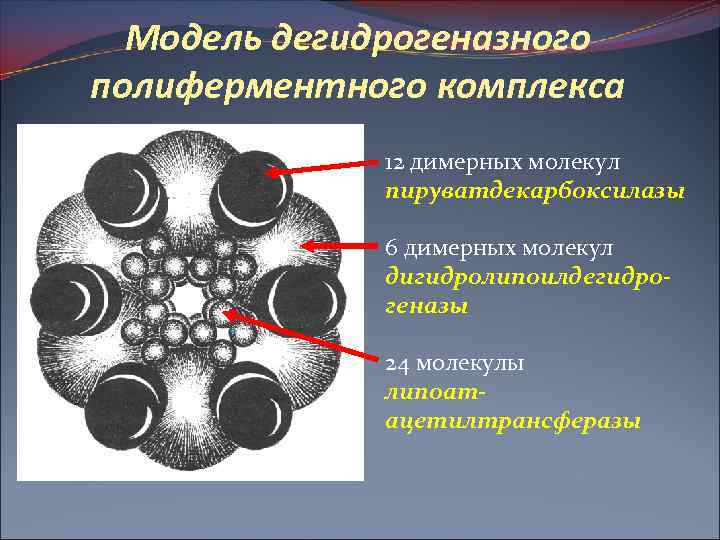
Модель дегидрогеназного полиферментного комплекса 12 димерных молекул пируватдекарбоксилазы 6 димерных молекул дигидролипоилдегидрогеназы 24 молекулы липоатацетилтрансферазы
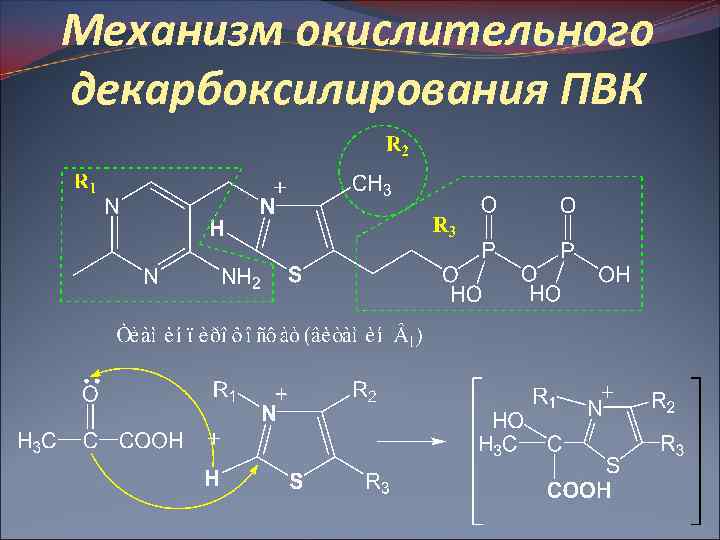
Механизм окислительного декарбоксилирования ПВК
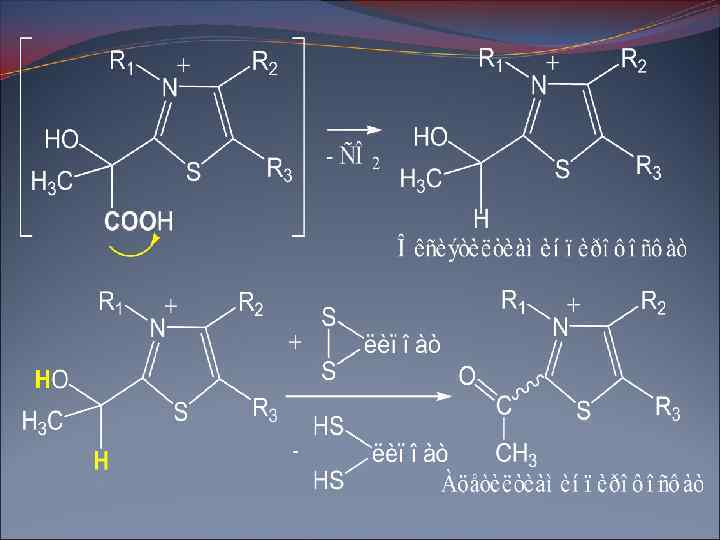
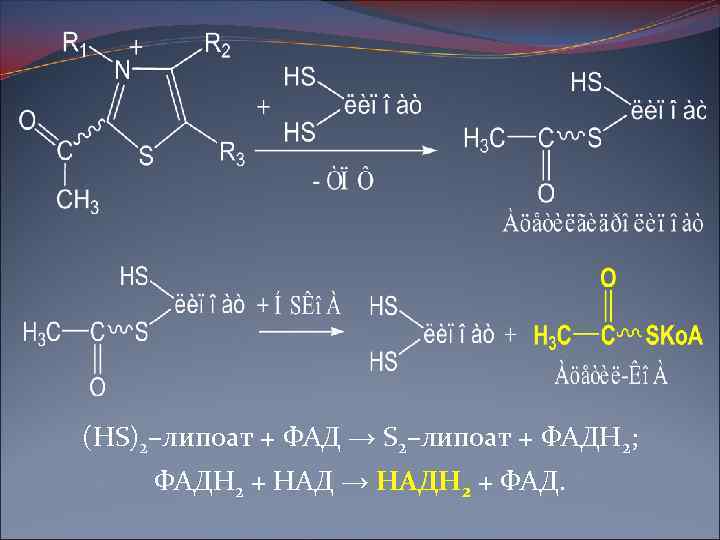
(HS)2–липоат + ФАД → S 2–липоат + ФАДН 2; ФАДН 2 + НАД → НАДН 2 + ФАД.
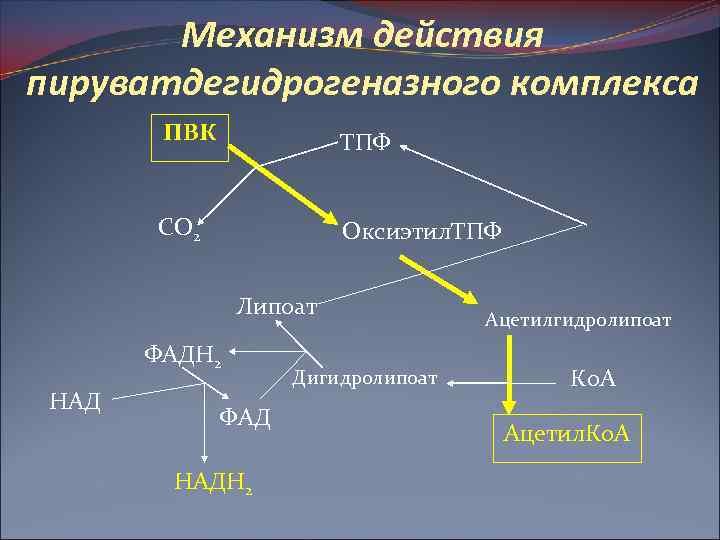
Механизм действия пируватдегидрогеназного комплекса ПВК ТПФ СО 2 Оксиэтил. ТПФ Липоат ФАДН 2 НАД ФАД НАДН 2 Дигидролипоат Ацетилгидролипоат Ко. А Ацетил. Ко. А


Цикл три- и дикарбоновых кислот впервые был открыт английским биохимиком Хансом Адольфом Кребсом в 1937 г. В 1953 г. он удостоился Нобелевской премии по физиологии и медицине. Х. А. Кребс впервые постулировал значение данного цикла для полного «сгорания» ПВК, главным источником которой является гликолитическое превращение углеводов. В дальнейшем было показано, что цикл Кребса является «фокусом» , в котором сходятся практически все метаболические пути. Цикл состоит из 8 -ми последовательных реакций. Ферменты цикла собраны в метаболон, локализованный в кристах митохондрий. Рядом с метаболоном цикла Кребса располагаются пируватдегидрогеназный комплекс и, вероятно, метаболон -окисления жирных кислот, поставляющие ему ацетил. Ко. А.
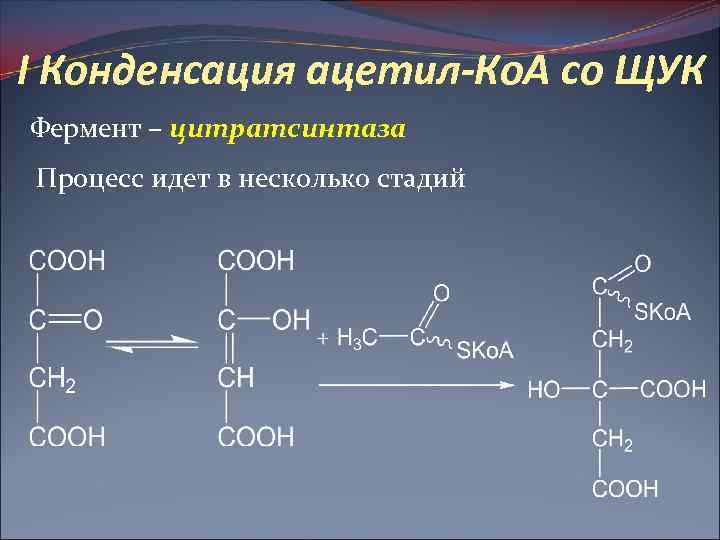
I Конденсация ацетил-Ко. А со ЩУК Фермент – цитратсинтаза Процесс идет в несколько стадий
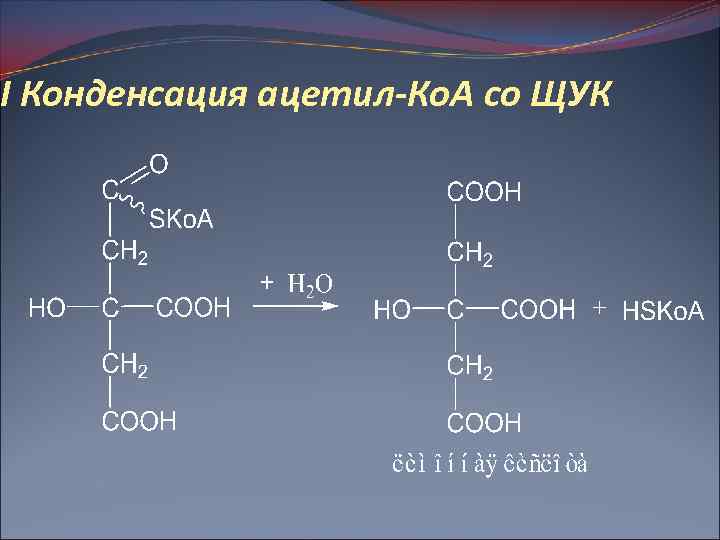
I Конденсация ацетил-Ко. А со ЩУК
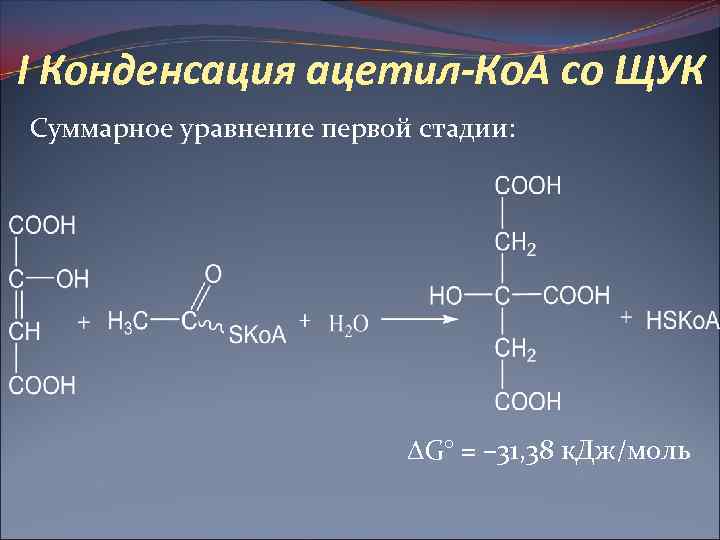
I Конденсация ацетил-Ко. А со ЩУК Суммарное уравнение первой стадии: G° = – 31, 38 к. Дж/моль

II Изомеризация лимонной кислоты в изолимонную Фермент – аконитатгидратаза Процесс идет в две стадии 2. 1. Дегидратация лимонной кислоты G° = 8, 37 к. Дж/моль
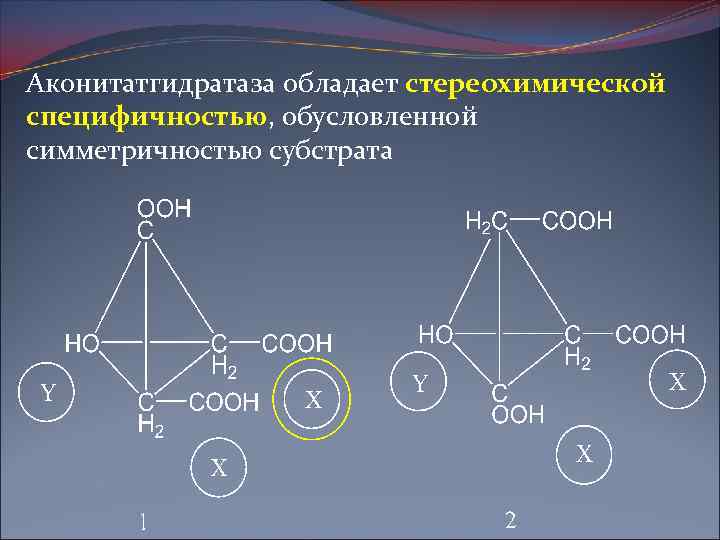
Аконитатгидратаза обладает стереохимической специфичностью, обусловленной симметричностью субстрата
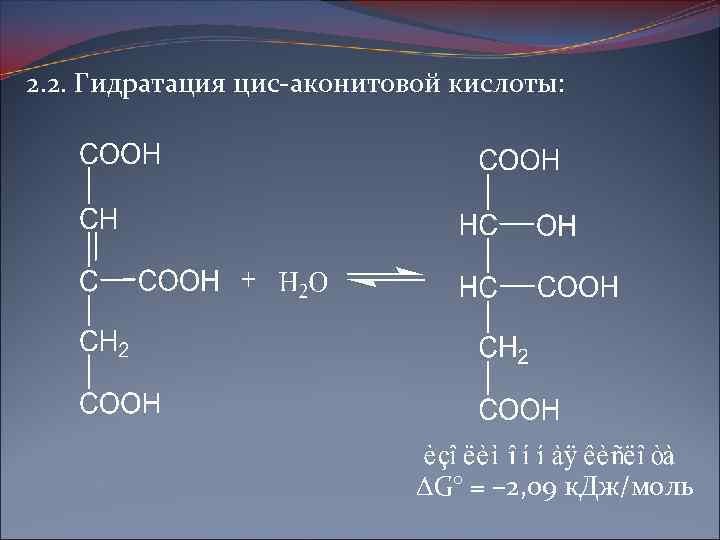
2. 2. Гидратация цис-аконитовой кислоты: G° = – 2, 09 к. Дж/моль
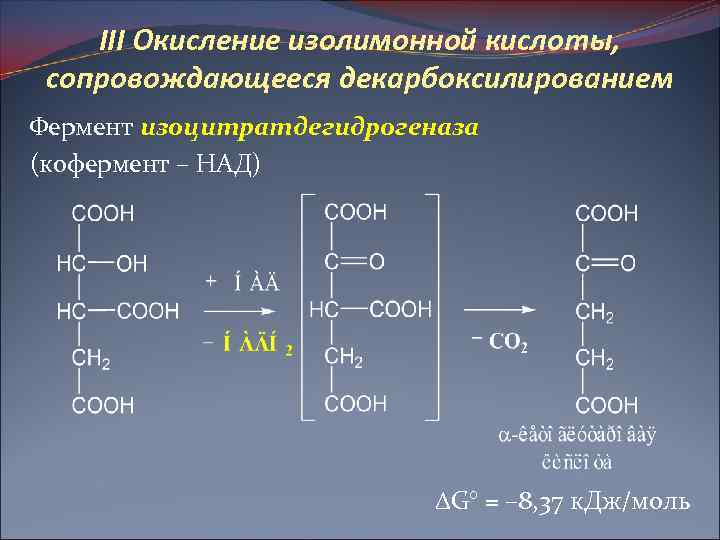
III Окисление изолимонной кислоты, сопровождающееся декарбоксилированием Фермент изоцитратдегидрогеназа (кофермент – НАД) G° = – 8, 37 к. Дж/моль
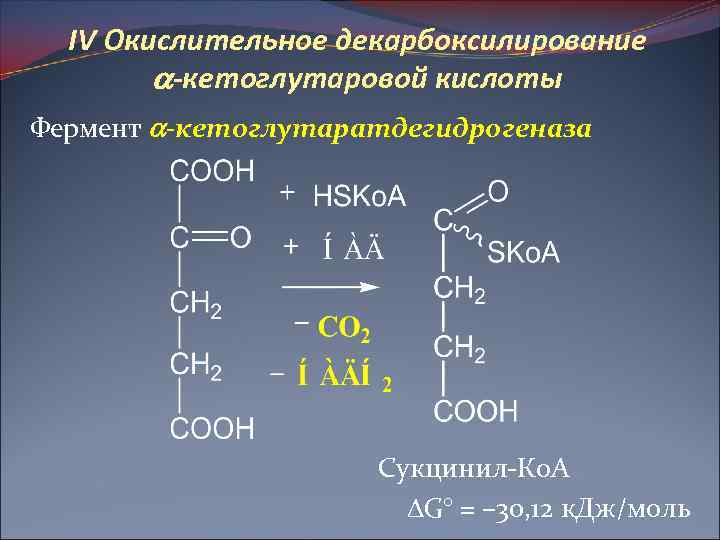
IV Окислительное декарбоксилирование -кетоглутаровой кислоты Фермент -кетоглутаратдегидрогеназа Сукцинил-Ко. А G° = – 30, 12 к. Дж/моль

V Субстратное фосфорилирование Фермент сукцинат: Ко. Алигаза G° = – 3, 35 к. Дж/моль ГТФ + АДФ ⇄ ГДФ + АТФ

VI Превращение янтарной кислоты в фумаровую (дегидрирование) Фермент сукцинатдегидрогеназа (кофермент – ФАД): G° = 0

VII Гидратация фумаровой кислоты с образованием яблочной кислоты Фермент фумаратгидратаза G° = – 3, 77 к. Дж/моль

VIII Окисление яблочной кислоты до кетоформы ЩУК Фермент малатдегирогеназа G° = 29, 71 к. Дж/моль

Суммарное уравнение цикла Кребса СН 3–СО SКо. А + 3 НАД + ФАД + АДФ + Н 3 РО 4 → → НSКо. А + 3 НАДН 2 + ФАДН 2 + АТФ + 2 СО 2.

За 1 оборот цикла Кребса происходит полное окисление 1 молекулы ацетил-Ко. А. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-Ко. А, а коферменты (НАД и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться в дыхательной цепи. Освобождающаяся в результате окисления ацетил-Ко. А энергия в значительной мере сосредоточивается в макроэргических связях АТФ. При окислении 1 молекулы ацетил-Ко. А в цикле Кребса образуется 12 молекул АТФ.

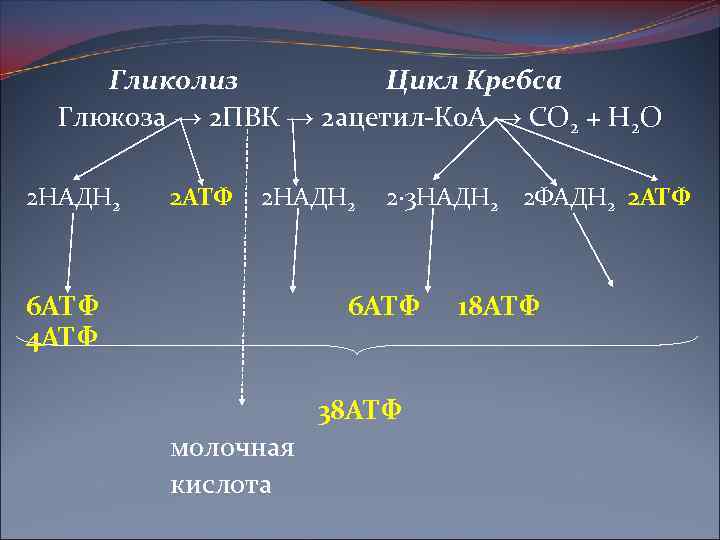
Гликолиз Цикл Кребса Глюкоза → 2 ПВК → 2 ацетил-Ко. А → СО 2 + Н 2 О 2 НАДН 2 2 АТФ 2 НАДН 2 6 АТФ 4 АТФ 2· 3 НАДН 2 2 ФАДН 2 2 АТФ 6 АТФ 38 АТФ молочная кислота 18 АТФ


Расхождение путей окисления углеводов – классического, при участии цикла Кребса, и пентозного – начинается со стадии образования гексозомонофосфата: если Г-6 -Ф превращается во Ф-1, 6 -д. Ф, то дальнейший распад углеводов идет по гликолитическому пути с образованием ПВК, которая, окисляясь до ацетил. Ко. А, затем «сгорает» в цикле Кребса. если же превращения Г-6 -Ф во Ф-1, 6 -д. Ф не происходит, то Г-6 -Ф может подвергаться прямому окислению до фосфопентоз В норме доля пентозного цикла в количественном превращении глюкозы обычно невелика и варьирует у разных организмов, зависит от типа ткани и ее функционального состояния

Значение пентозного пути в обмене веществ Пентозный цикл поставляет НАДФН 2, необходимый для биосинтеза жирных кислот, холестерина и т. д. За счет этого цикла потребность организма в НАДФН 2 покрывается практически на 50%. Пентозный цикл поставляет пентозофосфаты для синтеза нуклеиновых кислот (Р-5 -Ф) и многих коферментов. Роль пентозного цикла возрастает при ряде патологических состояний (так, НАДФН 2 используется для обезвреживания ядов в печени).

Реакции пентозофосфатного пути Пентозный цикл начинается с окислительного декарбоксилирования (от гексозофосфата отщепляется первый атом углерода). Это окислительная стадия цикла. Вторая стадия включает неокислительные превращения пентозофосфатов с образованием исходного глюкозо-6 -фосфата. Реакции пентозного цикла протекают в цитоплазме клеток.
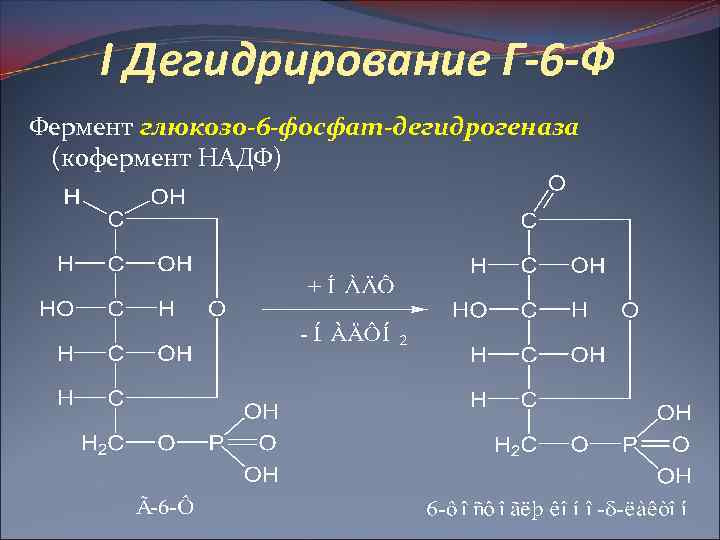
I Дегидрирование Г-6 -Ф Фермент глюкозо-6 -фосфат-дегидрогеназа (кофермент НАДФ)
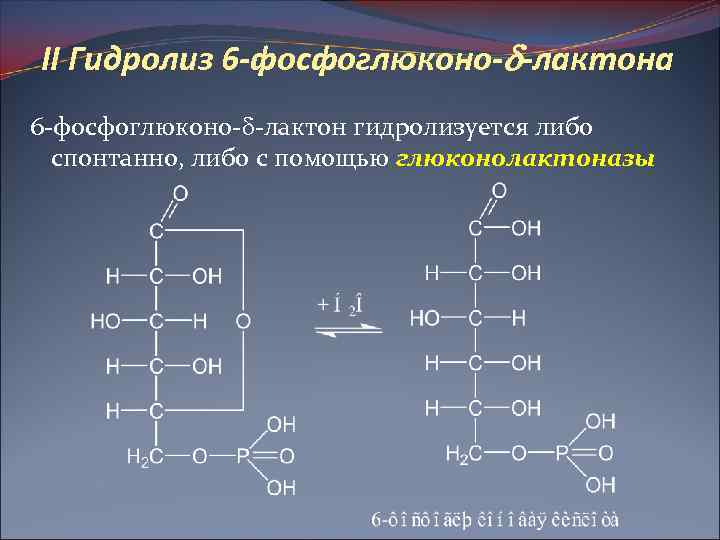
II Гидролиз 6 -фосфоглюконо- -лактона 6 -фосфоглюконо- -лактон гидролизуется либо спонтанно, либо с помощью глюконолактоназы
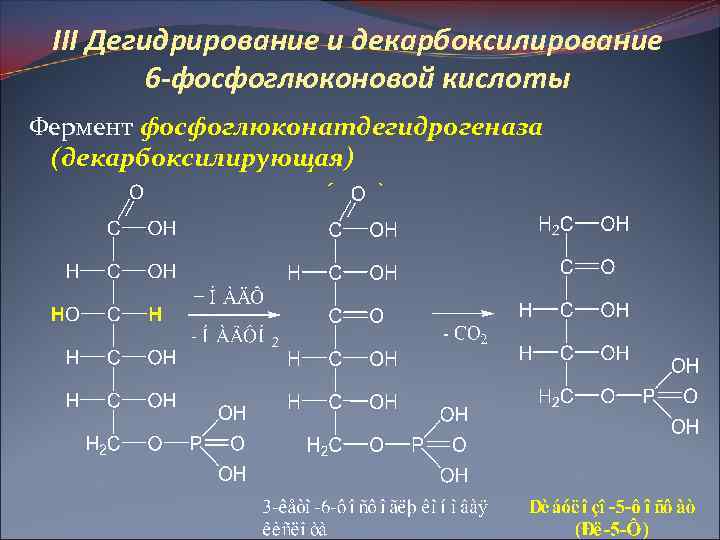
III Дегидрирование и декарбоксилирование 6 -фосфоглюконовой кислоты Фермент фосфоглюконатдегидрогеназа (декарбоксилирующая)
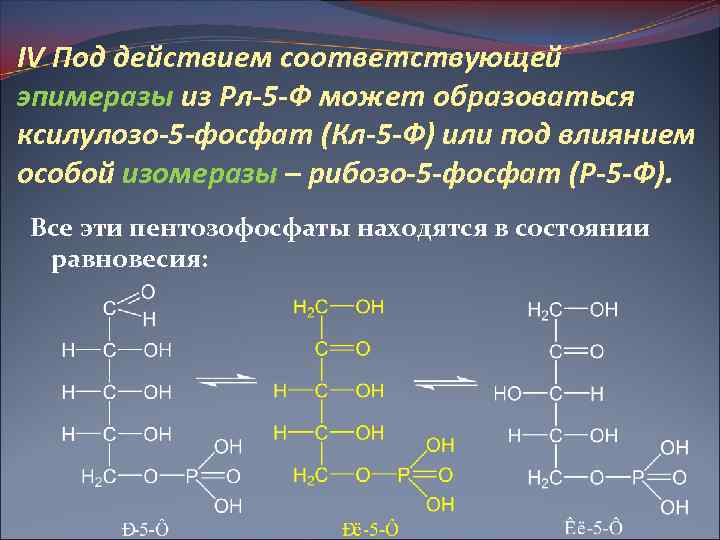
IV Под действием соответствующей эпимеразы из Рл-5 -Ф может образоваться ксилулозо-5 -фосфат (Кл-5 -Ф) или под влиянием особой изомеразы – рибозо-5 -фосфат (Р-5 -Ф). Все эти пентозофосфаты находятся в состоянии равновесия:

При определенных условиях пентозный путь на этом этапе может быть завершен. Однако может наступить и так называемый неокислительный этап пентозного цикла. Реакции этого этапа протекают в анаэробных условиях. При этом образуются как вещества, характерные для гликолиза (Ф-6 -Ф, Ф-1, 6 -д. Ф, фосфотриозы), так и специфические вещества – седогептулозо-7 фосфат (Сл-7 -Ф), пентозо-5 -фосфаты, эритрозо-4 фосфат (Э-4 -Ф). Основные реакции неокислительного этапа цикла – транскетолазные и трансальдолазные, заключаются в переносе трансальдолазные двухуглеродных фрагментов от одного фосфорного эфира к другому

Транскетолазные реакции Фермент транскетолаза Кофермент – тиаминпирофосфат, играющий роль промежуточного переносчика гликольальдегидной группы, которая затем присоединяется к Р-5 -Ф).
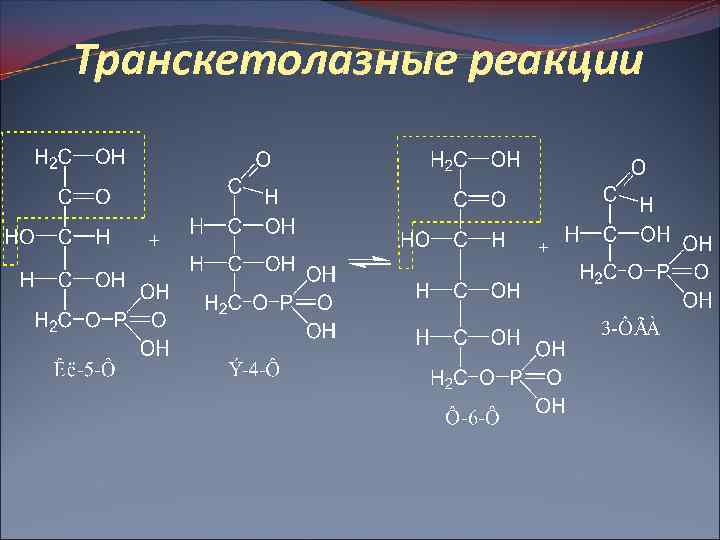
Транскетолазные реакции
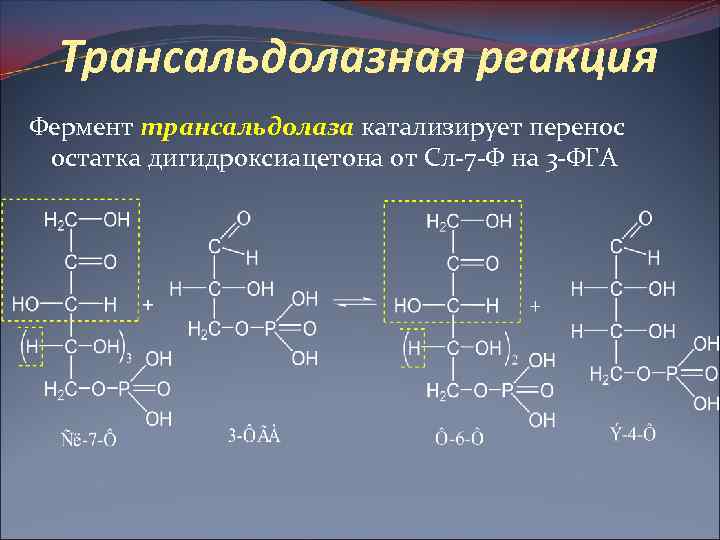
Трансальдолазная реакция Фермент трансальдолаза катализирует перенос остатка дигидроксиацетона от Сл-7 -Ф на 3 -ФГА

Таким образом 6 молекул Г-6 -Ф, вступая в пентозный цикл, дают 6 молекул Рл-5 -Ф и 6 молекул СО 2, после чего из 6 молекул Рл-5 -Ф снова регенерируют 5 молекул Г-6 -Ф. При этом молекула Г-6 -Ф, вступающая в цикл, полностью не окисляется. 6 молекул СО 2 образуются из С 1 -групп шести молекул Г-6 -Ф. Суммарное уравнение пентозофосфатного цикла 6 Г-6 -Ф + 7 Н 2 О + 12 НАДФ → 5 Г-6 -Ф + 6 СО 2 + 12 НАДФН 2 + Н 3 РО 4 или: Г-6 -Ф + 7 Н 2 О + 12 НАДФ → 6 СО 2 + 12 НАДФН 2 + Н 3 РО 4. Образовавшийся НАДФН 2 используется на восстановительные синтезы в цитоплазме и, как правило, не участвует в окислительном фосфорилировании в дыхательной цепи митохондрий, но если атомы водорода включаются в эту цепь, то синтезируется 12· 3 = 36 молекул АТФ на 1 молекулу глюкозы.

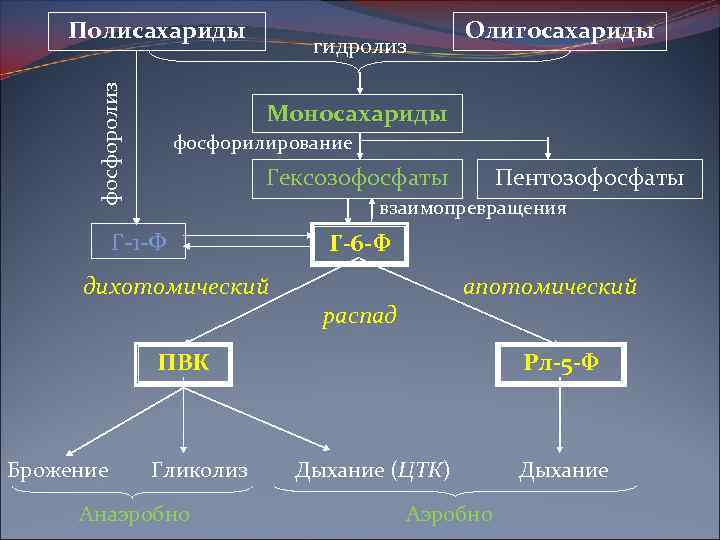
фосфоролиз Полисахариды гидролиз Олигосахариды Моносахариды фосфорилирование Гексозофосфаты Пентозофосфаты взаимопревращения Г-1 -Ф дихотомический Г-6 -Ф апотомический распад ПВК Брожение Гликолиз Анаэробно Рл-5 -Ф Дыхание (ЦТК) Аэробно Дыхание

Г-6 -Ф занимает центральное место в обмене углеводов, а из дальнейших продуктов узловые позиции принадлежат ПВК и Рл 5 -Ф Зависимости между различными путями распада углеводов сложны и определяются как видовыми особенностями, так и условиями жизнедеятельности организмов. Например, объем гликолиза в тканях находится в прямой зависимости от поступления кислорода: последний подавляет процесс образования молочной кислоты (эффект Пастера). Даже в различных тканях и органах одного и того же организма соотношения путей распада углеводов могут быть различными. Тем не менее можно установить некоторые общие закономерности: У подавляющего большинства организмов аэробный путь в общем преобладает над анаэробным, а дыхание подавляет гликолиз и брожение. Дихотомическому пути распада углеводов принадлежит в целом более видное место, чем апотомическому. В значительной степени эти соотношения путей распада



Простые углеводы возникают главным образом при первичном биосинтезе органического вещества на Земле. Этот процесс осуществляется автотрофными организмами – растениями, фотосинтезирующими и хемосинтезирующими бактериями. Первичный синтез органического вещества в природе идет путем восстановления СО 2 атмосферы с одновременным формированием органических молекул, новообразование которых сопровождается поглощением энергии.

Хемосинтезирующие бактерии Источником энергии служат реакции окисления неорганических соединений • нитрозобактерии: 2 NH 3 + 3 O 2 → 2 HNO 2 + 2 H 2 O • нитробактерии: 2 HNO 2 + O 2 → 2 HNO 3 • серобактерии: 2 S + 3 O 2 + 2 H 2 O → 2 H 2 SO 4 (избыток кислорода) 2 H 2 S + O 2 → 2 H 2 O + 2 S (недостаток кислорода)

Фотосинтезирующие бактерии и зеленые растения Используют для первичного синтеза органических веществ энергию световых лучей

Световая фаза фотосинтеза Высвобождение атомов водорода: НАДФ + Н 2 О → НАДФН 2 + ½О 2 (hν) Фосфорилирование АДФ (аналогично окислительному фосфорилированию): АДФ + Н 3 РО 4 → АТФ (hν)

Темновая фаза фотосинтеза Суммарное уравнение: 6 СО 2 + 12 НАДФН 2 → С 6 Н 12 О 6 + 12 НАДФ + 12 Н 2 О по стадиям: Рл-5 -Ф + АТФ → Рл-1, 5 -д. Ф + АДФ фосфорибулокиназа Рл-1, 5 -д. Ф + СО 2 → 2 3 -ФГК рибулозодифосфаткарбоксилаза 2 3 -ФГК + 2 НАДФН 2 → 2 3 -ФГА + 2 НАДФ + 2 Н 2 О 3 -ФГА ⇄ ДОАФ → Ф-1, 6 -д. Ф → Ф-6 -Ф → Г-6 -Ф (обращение дихотомического пути).

Исходными веществами для синтеза углеводов гетеротрофными организмами могут служить продукты распада липидов, белков и других органических соединений.


Глюконеогенез – синтез глюкозы из неуглеводных продуктов. Предшественниками глюкозы в нем могут быть ПВК или любое соединение, превращающееся в процессе катаболизма в нее или один из промежуточных продуктов ЦТК. У позвоночных наиболее интенсивно глюконеогенез протекает в печени и корковом веществе почек. Большинство стадий глюконеогенеза представляет собой обращение реакций гликолиза. Только три реакции гликолиза (гексокиназная, фосфофруктокиназная и пируваткиназная) необратимы, поэтому в процессе глюконеогенеза на трех этапах используются другие ферменты

I Образование ФЕП из ПВК Синтез ФЕП осуществляется в несколько этапов. 1. Карбоксилирование ПВК под влиянием пируваткарбоксилазы (кофермент – витамин Н (биотин))
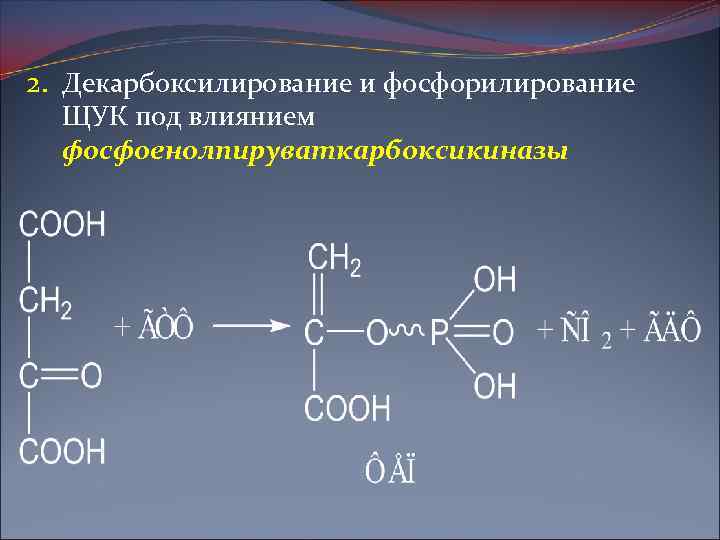
2. Декарбоксилирование и фосфорилирование ЩУК под влиянием фосфоенолпируваткарбоксикиназы

Первый этап локализуется в митохондриях. Мембрана митохондрий непроницаема для образовавшейся ЩУК. Последняя здесь же восстанавливается до яблочной кислоты при участии НАД-зависимой малатдегидрогеназы (митохондриальной) (в митохондриях отношение НАДН 2/НАД велико, а в цитоплазме – мало): Яблочная кислота легко проходит через мембрану митохондрий в цитоплазму, где вновь окисляется при участии НАД-зависимой малатдегидрогеназы (цитоплазматической). Дальнейший процесс происходит в цитоплазме.

II Превращение Ф-1, 6 -д. Ф во Ф-6 -Ф ФЕП в результате ряда обратимых реакций гликолиза превращается во Ф-1, 6 -д. Ф. Далее глюконеогенез идет в обход необратимой эндэргонической реакции превращения Ф-1, 6 -д. Ф во Ф-6 -Ф: Ф-1, 6 -д. Ф + Н 2 О → Ф-6 -Ф + Н 3 РО 4 Фермент фруктозодифосфатаза ингибируется АМФ и активируется АТФ Таким образом, когда концентрация АМФ мала, а концентрация АТФ велика, то стимулируется глюконеогенез. Напротив, когда величина отношения АТФ/АМФ низка, в клетке происходит расщепление глюкозы.

III Образование глюкозы из Г-6 -Ф В последующей обратимой стадии биосинтеза глюкозы Ф-6 -Ф превращается в Г-6 -Ф, который может дефосфорилироваться (в обход гексокиназной реакции) под влиянием глюкозо-6 -фосфатазы: Г-6 -Ф + Н 2 О → глюкоза + Н 3 РО 4

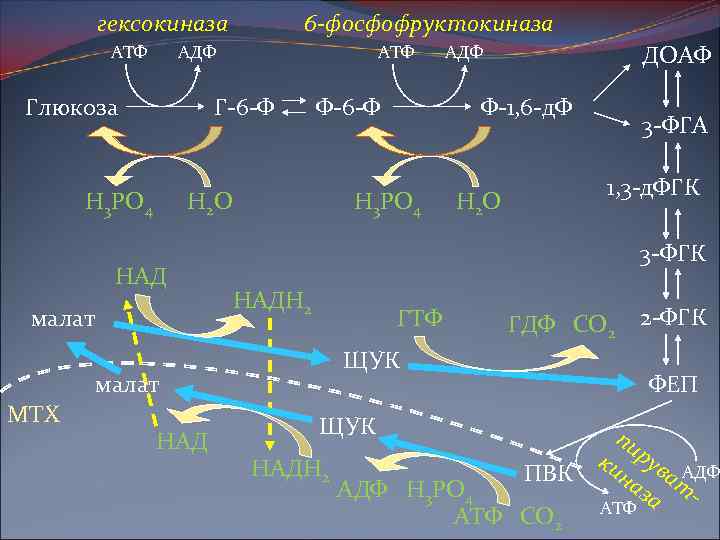
гексокиназа АТФ 6 -фосфофруктокиназа АДФ Глюкоза АТФ Г-6 -Ф Н 3 РО 4 Ф-6 -Ф НАД малат НАД 3 -ФГА 1, 3 -д. ФГК Н 2 О 3 -ФГК НАДН 2 ГТФ ГДФ СО 2 ЩУК малат МТХ ДОАФ Ф-1, 6 -д. Ф Н 3 РО 4 Н 2 О АДФ ФЕП ЩУК НАДН 2 2 -ФГК ПВК АДФ Н 3 РО 4 АТФ СО 2 пи ки рув АДФ на ат за АТФ

Между гликолизом, интенсивно протекающим в мышцах при их активной деятельности, и глюконеогенезом, особенно характерным для печени, существует тесная взаимосвязь При максимальной активности мышц в результате усиления гликолиза образуется избыток молочной кислоты, диффундирующей в кровь Значительная часть лактата в печени превращается в глюкозу (глюконеогенез) Образовавшаяся в печени глюкоза затем может быть использована как энергетический субстрат, необходимый для деятельности мышц.


У растений и микроорганизмов в процессе глюконеогенеза важную роль играет глиоксилатный цикл. Благодаря ему двухуглеродные метаболиты (и ацетил-Ко. А) способны превращаться в углеводы. Глиоксилатный цикл рассматривают как видоизмененный цикл Кребса, в котором изоцитратдегидрогеназа и кетоглутаратдегидрогеназа заменены на изоцитратлиазу и малатсинтазу

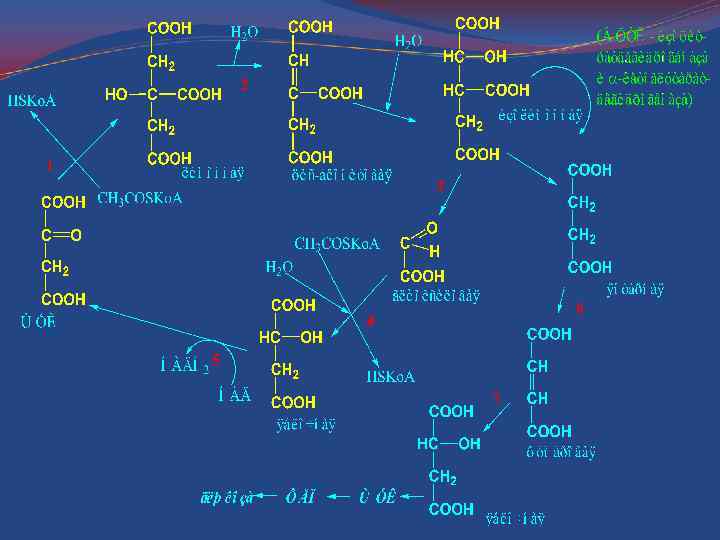

Ферменты глиоксилатного цикла 1 – цитратсинтаза 2 – аконитатгидратаза 3 – изоцитратлиаза 4 – малатсинтаза 5 – малатдегидрогеназа 6 – сукцинатдегидрогеназа 7 – фумаратдегидрогеназа


Биосинтез олигосахаридов осуществляется путем реакций трансгликозилирования Перенос гликозильного остатка на один моносахарид идет с фосфорного эфира другого моносахарида и ускоряется специфической гликозилтрансферазой Исходными соединениями, с которых в процессе синтеза олигосахаридов гликозильный остаток переносится на моносахарид, служат нуклеозиддифосфатсахара, при гидролизе которых изменение уровня свободной энергии значительно выше, чем при гидролизе других доноров, а нуклеотидная часть их молекул способна обеспечить избирательность гликозилтрансферазной реакции.

Синтез сахарозы Фермент сахарозосинтаза Только в растениях

Синтез сахарозы Фермент сахарозофосфатсинтаза: УДФ-глюкоза + Ф-6 -Ф → → УДФ + Сахарозо-6 -Ф Далее действует фермент фосфатаза: Сахарозо-6 -Ф + Н 2 О → → Сахароза + Н 3 РО 4

Синтез лактозы УДФ-глюкоза + глюкоза → лактоза + УДФ
Обмен углеводов.ppt