р-ры. теория ЭД. гидролиз.ppt
- Количество слайдов: 80

Общая характеристика растворов Кислоты, основания, соли в свете теории электролитической диссоциации. Гидролиз солей.

Раствор – однородная гомогенная система переменного состава, состоящая из двух компонентов и более Раствор растворитель (преобладает) + растворенное вещество

от размеров распределенных частиц: Øвзвеси (размер частиц – 10 -5 – 10 -7 м. ) Øистинные (менее 10 -9 м. ) -7 – 10 -9 м. ) Øколлоидные (10

качественная характеристика растворов: Øразбавленный (низкое содержание растворенного вещества) Øконцентрированный (высокое содержание)

количественный состав раствора молярная концентрация количество растворенного вещества, содержащееся в 1 литре раствора, мольл

количественный состав раствора моляльность - количество растворенного вещества, содержащееся в 1000 г. растворителя, мольг

количественный состав раствора массовая доля растворенного вещества (W) - отношение массы вещества к массе раствора, % W = m в-ва / m р-ра х 100%

РАСТВОРЕНИЕ – самопроизвольный физикохимический процесс, при котором происходит взаимодействие между частицами растворителя и растворенного вещества обратный ему процесс – выделение вещества из раствора (кристаллизация)
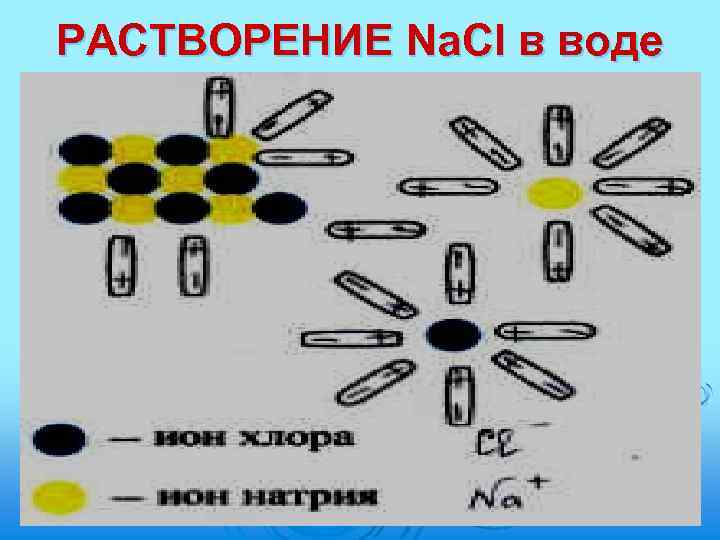
РАСТВОРЕНИЕ Na. Cl в воде
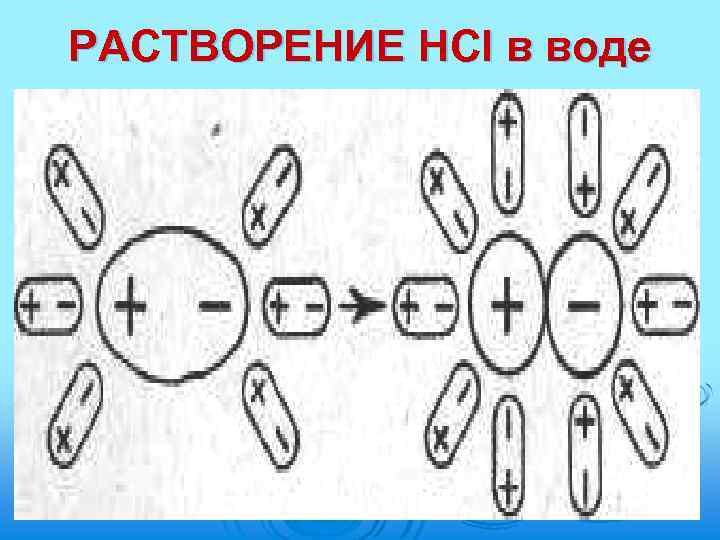
РАСТВОРЕНИЕ HCl в воде

РАСТВОРЕНИЕ HCl в воде ион гидроксония: Н Н. . + → [Н : О : Н]+ Н: О: +Н

Механизм диссоциации веществ с ионным типом связи 1. ориентация молекул – диполей воды около ионов кристалла

Механизм диссоциации веществ с ионным типом связи 2. гидратация (взаимодействие) молекул воды с противоположными ионами поверхностного слоя кристалла

Механизм диссоциации веществ с ионным типом связи 3. диссоциация (распад) кристалла электролита на гидратированные ионы.

Механизм диссоциации веществ с ковалентной полярной связью 1. ориентация молекул – диполей воды вокруг полюсов молекулы электролита

Механизм диссоциации веществ с ковалентной полярной связью 2. гидратация (взаимодействие) молекул воды с молекулами электролита

Механизм диссоциации веществ с ковалентной полярной связью 3. ионизация молекул электролита (превращение ковалентной полярной связи в ионную)

Механизм диссоциации веществ с ковалентной полярной связью 4. диссоциация (распад) кристалла электролита на гидратированные ионы.

Гидратная оболочка – окружение иона, состоящее из одного или нескольких слоев определенным образом ориентированных молекул воды. Гидратация – процесс образования гидратной оболочки.

теплота растворения - тепловая энергия, выделяемая или поглощаемая при растворении веществ

ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ Аррениус, 1877 г. ОСНОВНЫЕ ПОЛОЖЕНИЯ 1. При растворении в воде электролиты диссоциируют на «+» и «–» заряженные ионы

ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ ОСНОВНЫЕ ПОЛОЖЕНИЯ 2. Диссоциация – обратимый процесс. Кристаллизация.
ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ ОСНОВНЫЕ ПОЛОЖЕНИЯ 3. Под действием электр. тока ионы движутся: «+» к катоду (катионы) «-» к аноду (анионы)

Электролиты - вещества, водные растворы которых диссоциируют на ионы и проводят электрический ток (это соединения с ковалентной полярной или ионной связью)

электролитическая диссоциация - распад электролитов на ионы AB ↔ A+ + B-

ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ Д. Менделеев, И. Каблуков, Кистяковский В. В растворе находятся не свободные ионы, а гидратированные
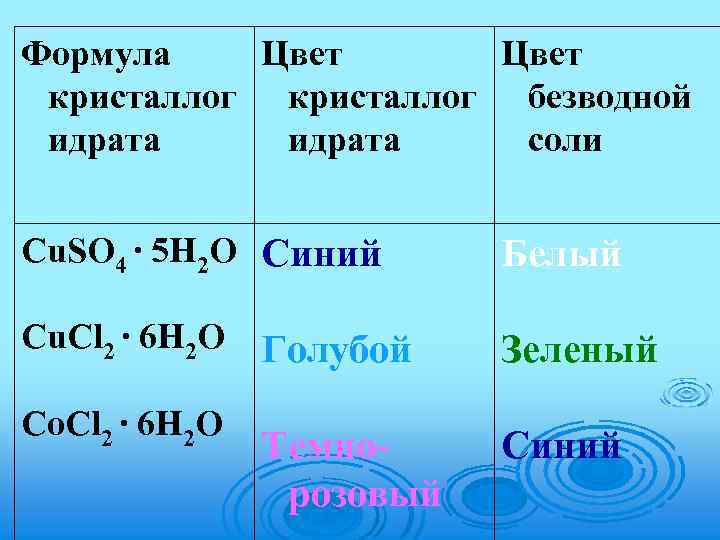
Формула Цвет кристаллог безводной идрата соли Cu. SO 4 ∙ 5 H 2 O Синий Белый Cu. Cl 2 ∙ 6 H 2 O Голубой Зеленый Темнорозовый Синий Cо. Cl 2 ∙ 6 H 2 O

Степень диссоциации ( - альфа) - отношение числа молекул, распавшихся на ионы, к исходному числу молекул растворенного вещества: = n/ N величина безразмерная (или %)

Степень диссоциации зависит от: Øприроды электролита, Øтемпературы, Øконцентрации раствора

В зависимости от : Øсильные электролиты ( 30%) HCl, Na. OH, почти все соли Øслабые ( 3%) H 2 S, Fe(OH)2, вода Øсредней силы (3% 30%) HF

Водородный показатель + Н р. Н – мера активности в растворе (1909 г. , Сёренсен – «сила водорода» )

Н 2 О ↔ + Н + ОН При 250 С И. П. = [Н+]. [ОН-] = 10 -14 моль2л 2 [Н+] = [ОН-] = 10 -7 мольл +] [H р. Н = - lg -] р. ОН = - lg [ОH р. Н + р. ОН = 14
![Водородный показатель «-» десятичный логарифм молярной концентрации ионов Н+ Ø Нейтральная среда – [H+] Водородный показатель «-» десятичный логарифм молярной концентрации ионов Н+ Ø Нейтральная среда – [H+]](https://present5.com/presentation/69237424_437194002/image-33.jpg)
Водородный показатель «-» десятичный логарифм молярной концентрации ионов Н+ Ø Нейтральная среда – [H+] = [ОH-], =7 Ø Кислотная среда – [H+] > [ОH-], р. Н < 7 Ø Щелочная среда – [H+] < [ОH-], >7 р. Н

Кислоты - электролиты, при диссоциации которых в качестве катионов образуются только ионы водорода HNO 3 H+ + NO 3 -

Многоосновные кислоты Ø H 3 PO 4 H+ + H 2 PO 4 - ( = 27%) Ø H 2 PO 4 - H+ + HPO 42 - ( = 0, 11%) Ø HPO 42 - H+ + PO 43 - ( = 0, 001%)

Основания - электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы KOH K+ + OH-

Многокислотные основания ØBa(OH)2 ØBa. OH+ + Ba. OH + OH Ba 2+ + OH-

Амфотерные соединения Øв кислой среде ведут себя как основания: Zn(OH)2 + 2 HCL Zn. CL 2 + 2 H 2 O

Амфотерные соединения Øв щелочной среде – как кислоты: Zn(OH)2 + 2 Na. OH Na 2 Zn. O 2 + 2 H 2 O

Амфотерные соединения Øв общем виде: 2 H+ + Zn. O 22 - H 2 Zn. O 2 Zn(OH)2 Zn 2+ + 2 OH-

Амфотерные соединения H+ + RO- ROH R+ + OHВ щелочной среде В кислой среде

Соли – электролиты, при диссоциации которых образуются катионы металлов и анионы кислотных остатков.

Средние соли Cu. SO 4 2+ Cu + 2 SO 4 Al 2(SO 4)3 2 Al 3+ + 3 SO 42 -

Кислые соли ØNa. HCO 3 ØHCO 3 - + Na + HCO 3 H+ + CO 32 -

Основные соли ØBa. OHCl Ba. OH+ + ØBa. OH 2+ Ba + + Cl- OH

Ионные реакции Ø KCl + Ag. NO 3 = KNO 3 + Ag. Cl↓ молекулярное уравнение Ø K+ + Cl- + Ag+ + NO 3 - = K+ + NO 3+Ag. Cl↓ полное ионное уравнение Ø Cl- + Ag+ = Ag. Cl↓ - сокращенное ионное уравнение

Ионные реакции Реакции обмена в р-рах электролитов происходят, если образуется: - малодиссоциирующее в-во, - осадок, - газ.

Задание 1. Напишите полные и сокращенные ионные уравнения реакций между растворами: Ø - гидроксида калия и нитрата меди, Ø - сульфата натрия и нитрата бария, Ø - сульфата алюминия и хлорида бария, Не забываем про коэффициенты в уравнениях реакций!!!

Задание 1. Напишите полные и сокращенные ионные уравнения реакций между растворами: Ø - гидроксида калия и серной кислоты, Ø - хлорида кальция и нитрата серебра, Не забываем про коэффициенты в уравнениях реакций!!!

Задание 1. Напишите полные и сокращенные ионные уравнения реакций между растворами: Ø - хлорида железа (III) и гидроксида натрия, Ø - фосфата натрия и нитрата алюминия (III), Не забываем про коэффициенты в уравнениях реакций!!!

Задание 1. Напишите полные и сокращенные ионные уравнения реакций между растворами: Ø - карбоната калия и хлорида кальция, Ø - нитрата цинка и карбоната натрия. Не забываем про коэффициенты в уравнениях реакций!!!

Гидролиз солей ØNa 2 Si. O 3 - щелочные свойства -ра ØAl 2(SO 4)3 – кислые ØNa. Cl - нейтральные Почему? р

Гидролиз Разложение воды ( «гидро» - вода, «лизис» – разложение) HOH H+ + OH-

Гидролиз – взаимодействие ионов соли с ионами воды, приводящее к образованию слабого электролита и к избыточному содержанию в растворе либо ионов H+ , либо ионов OH- (не всегда)

Гидролиз 1. 2. 3. 4. Соль образована сильным основанием и слабой кислотой Соль образована слабым основанием и сильной кислотой Соль образована слабым основанием и слабой кислотой Соль образована сильным основанием и сильной кислотой

Как определить слабое или сильное? В школьной таблице растворимости три сильных кислоты (H 2 SO 4, HCl, HNO 3), остальные – слабые.

Как определить слабое или сильное? Cлабые основания нерастворимы. Исключения: NН 4 ОН - растворимое, но слабое а Ca(OH)2 - малорастворимое, но сильное.

Как определить слабое или сильное? Вывод о силе кислородсодержащей кислоты можно сделать, если выразить ее состав общей формулой Нем(ОН)m. Оn Если n ≥ 2, то кислота – сильная, n = 1, кислота средней силы n = 0, кислота слабая.

ØХлорная: HCl. O 4 ØМышьяковая: H 3 As. O 4 ØОртоборная: H 3 BO 3 ØТелуровая: H 6 Te. O 6

ГИДРОЛИЗ 1. Соль образована сильным основанием и слабой кислотой Например, CH 3 COONa (образована СH 3 COOH – слабая кислота и Na. OH – сильное основание) Гидролиз по аниону А- + НОН HА + OH- , p. H>7
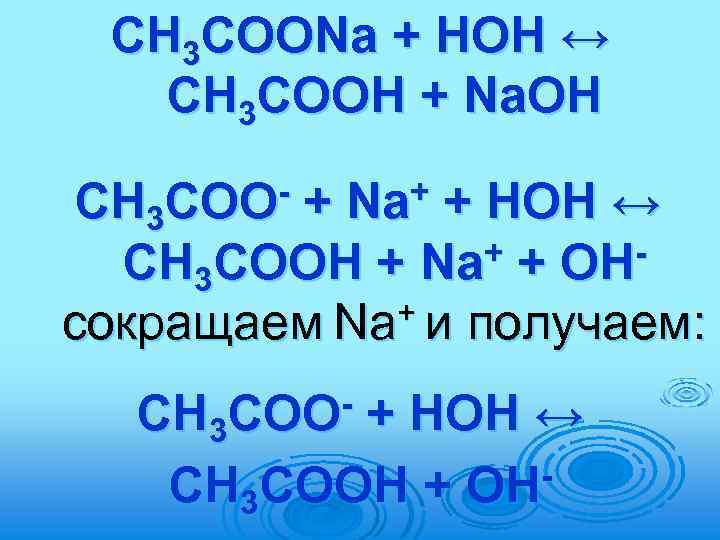
CH 3 COONa + HOH ↔ CH 3 COOH + Na. OH CH 3 COO + Na + + HOH ↔ + + OHCH 3 COOH + Na + и получаем: сокращаем Na CH 3 COO + HOH ↔ CH 3 COOH + OH

ГИДРОЛИЗ 2. Соль образована слабым основанием и сильной кислотой Например, NH 4 Cl (образована NH 4 OH – слабое основание и HCl – сильная кислота) Гидролиз по катиону М+ + НОН МОН + H+, p. H<7
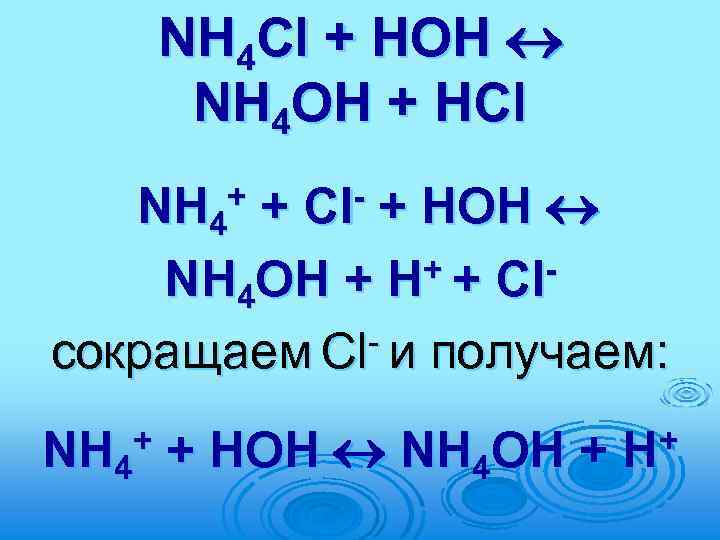
NH 4 Cl + НОН NH 4 ОН + HСl + + НОН NH 4 ОН + H+ + Clсокращаем Cl- и получаем: + NH 4 Cl + НОН NH 4 ОН + + H

ГИДРОЛИЗ 3. Соль образована слабым основанием и слабой кислотой Например, CH 3 COONH 4 (образована CH 3 COОН – слабая кислота и NH 4 ОН – слабое основание) Гидролиз и по катиону, и по аниону p. H зависит от относительной силы кислоты и основание М+ + А- + НОН МОН + HА, p. H≈7
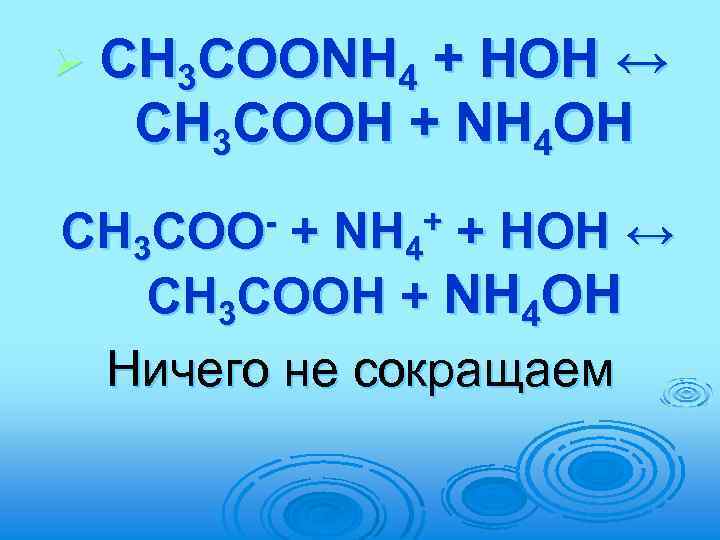
Ø CH 3 COONH 4 + HOH ↔ CH 3 COOH + NH 4 OH CH 3 COO- + NH 4+ + HOH ↔ CH 3 COOH + NH 4 OH Ничего не сокращаем

Константы диссоциации уксусной кислоты и гидроксида аммония близки между собой (1, 76 х 10 -5 и 1, 79 х 10 -5 соответственно). Среда нейтральная.

ГИДРОЛИЗ 4. Соль образована сильным основанием и сильной кислотой гидролизу не подвергается p. H = 7 Например, Na. Cl (образована Na. OH – сильное основание и HCl – сильная кислота)

Ступенчатый ГИДРОЛИЗ 1. Соль образована слабой многоосновной кислотой и сильным основанием На промежуточных стадиях образуются кислые соли

Например, Na 2 CO 3 (образована – H 2 CO 3 - слабая двухосновная кислота и Na. OH – сильное основание) На промежуточной стадии образуется кислая соль Na. HCO 3 Гидролиз по аниону p. H>7
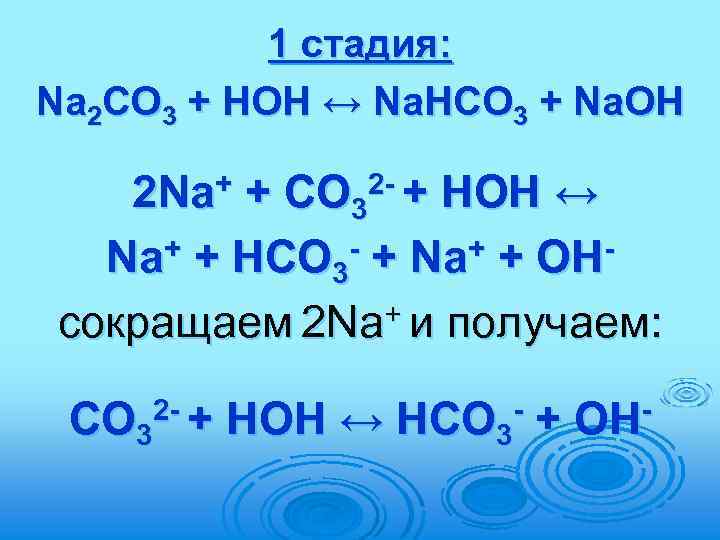
1 стадия: Na 2 СО 3 + HOH ↔ Na. НСО 3 + Na. OH 2 Na+ + СО 32 - + HOH ↔ + + НСО - + Na+ + OHNa 3 + и получаем: сокращаем 2 Na СО 32 - + HOH ↔ НСО 3 - + OH-
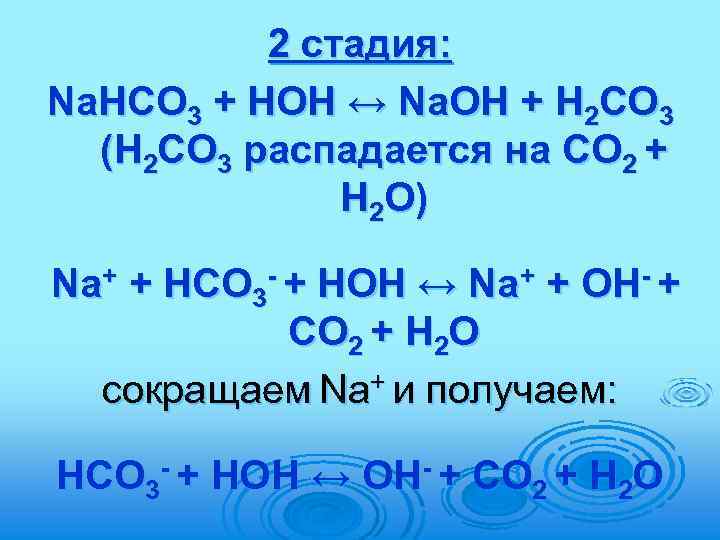
2 стадия: Na. НСО 3 + HOH ↔ Na. OH + Н 2 СО 3 (Н 2 СО 3 распадается на СО 2 + Н 2 О) Na+ + НСО 3 - + HOH ↔ Na+ + OH- + СО 2 + Н 2 О сокращаем Na+ и получаем: НСО 3 - + HOH ↔ OH- + СО 2 + Н 2 О

Ступенчатый ГИДРОЛИЗ 2. Соль образована слабым многокислотным основанием и сильной кислотой На промежуточных стадиях образуются основные соли

Например, Cu. Cl 2 (образована – Сu(OH)2 - слабое двухкислотное основание и HCl – сильная кислота) На промежуточной стадии образуется основная соль Сu. OHCl Гидролиз по аниону p. H<7
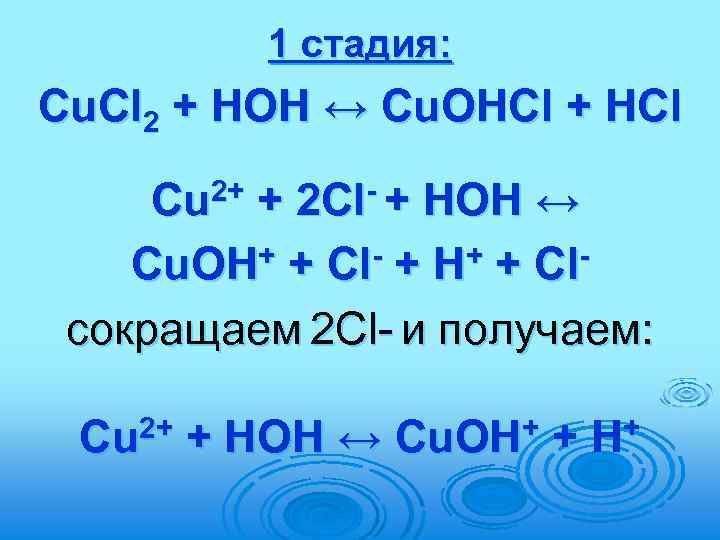
1 стадия: Cu. Cl 2 + HOH ↔ Cu. OHCl + HCl Cu 2+ + 2 Сl- + HOH ↔ Cu. OH+ + Cl- + H+ + Clсокращаем 2 Cl- и получаем: Cu 2+ + HOH ↔ Cu. OH+ + H+
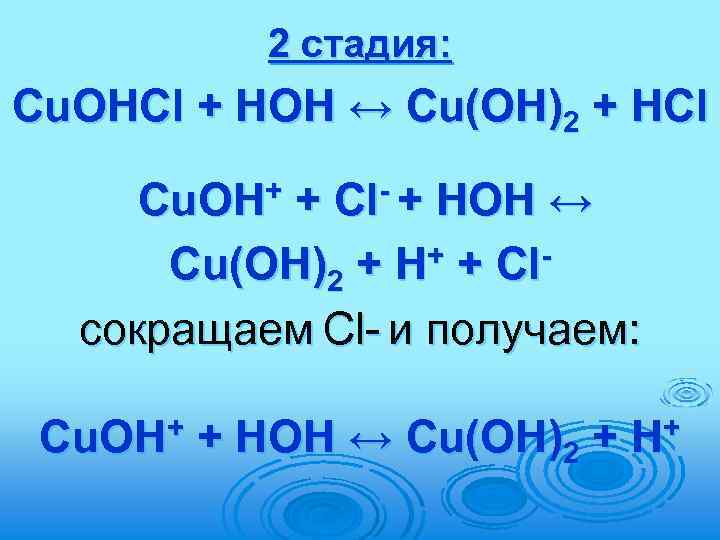
2 стадия: Cu. OHCl + HOH ↔ Cu(OH)2 + HCl Cu. OH+ + Сl- + HOH ↔ Cu(OH)2 + H+ + Clсокращаем Cl- и получаем: Cu. OH+ + HOH ↔ Cu(OH)2 + H+

ГИДРОЛИЗ Обратимый Усиливается при: • нагревании • разбавлении р-ра • удалении продуктов гидролиза

ГИДРОЛИЗ Необратимый (если продукты нерастворимы или летучи)

Задание 2. Составьте ионные уравнения, отвечающие гидролизу: Ø- цианида калия, Ø- нитрата калия, Ø- сульфида натрия, Какова реакция раствора в каждом случае?

Задание 2. Составьте ионные уравнения, отвечающие гидролизу: Ø- карбоната калия, Ø - хлорида железа (II), Ø - сульфата натрия. Какова реакция раствора в каждом случае?

Задание 2. Составьте ионные уравнения, отвечающие гидролизу: Ø - нитрата свинца, Ø - хлорида магния, Ø - сульфита натрия, Ø - силиката натрия Какова реакция раствора в каждом случае?
р-ры. теория ЭД. гидролиз.ppt