Обобщение по теме.ppt
- Количество слайдов: 9

Обобщение по теме: «Химические реакции» 11 класс

1. Укажите типы реакции, уравнение которой Mg(OH)2 Mg. O+ H 2 O
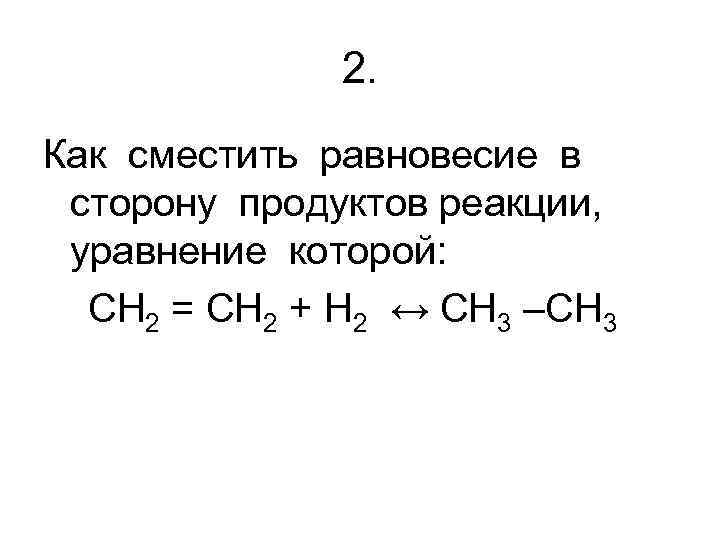
2. Как сместить равновесие в сторону продуктов реакции, уравнение которой: CH 2 = CH 2 + H 2 ↔ CH 3 –CH 3

3 Запишите уравнения возможных реакций в молекулярном, полном ионном и сокращённом ионном виде: А) карбонат калия + азотная кислота Б)нитрат натрия + сульфат калия В)серная кислота + гидроксид железа(III) Г) оксид меди + хлороводородная кислота
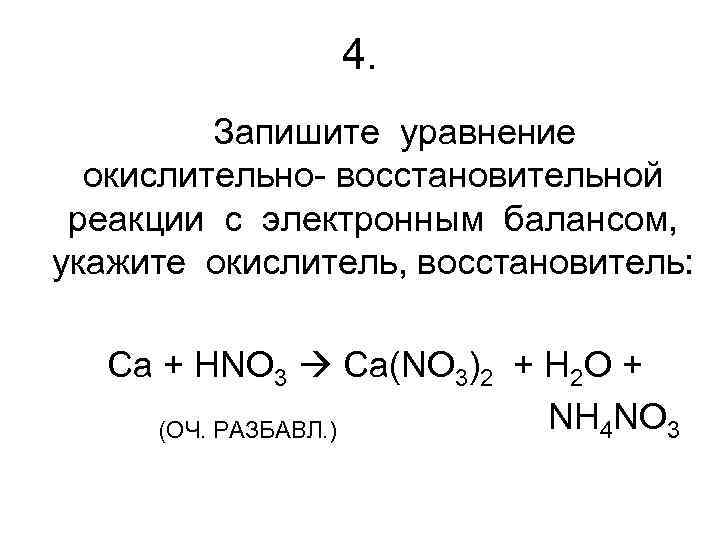
4. Запишите уравнение окислительно- восстановительной реакции с электронным балансом, укажите окислитель, восстановитель: Ca + HNO 3 Ca(NO 3)2 + H 2 O + NH 4 NO 3 (ОЧ. РАЗБАВЛ. )

5 Запишите уравнение окислительновосстановительной реакции с электронным балансом, укажите окислитель, восстановитель: Mg + H 2 SO 4 Mg. SO 4 + H 2 O + H 2 S

6. Определите какова среда раствора: А) хлорида кальция Б) нитрита натрия В) сульфата меди (II) Г) хлорида железа (III)

7. Задача Определите массу осадка, полученного при взаимодействии 200 г 15%ного раствора хлорида железа (lll) и 150 г 30%ного раствора гидроксида натрия.

8. Определите объём углекислого газа, полученного при взаимодействии 300 г мела, содержащего 10 % некарбонатных примесей и 150 г 20% азотной кислоты.
Обобщение по теме.ppt