Кислоты.ppt
- Количество слайдов: 6

Обобщение

Кислотыэлектролиты, при диссоциации которых образуются катионы водорода и анионы кислотных остатков HCL H 2 SO 4 H++CL 2 H++SO 42 -

Классификация кислот КИСЛОТЫ КИСЛОРОДНЫЕ БЕСКИСЛОРОДНЫЕ H 2 SO 4, HNO 3 HCL, HBr ОДНООСНОВНЫЕ HCL, HNO 3 ДВУХОСНОВНЫЕ H 2 SO 4, H 2 S ТРЕХОСНОВНЫЕ H 3 PO 4 СИЛЬНЫЕ H 2 SO 4, HCL СЛАБЫЕ H 2 SO 3, H 2 S РАСТВОРИМЫЕ НЕРАСТВОРИМЫЕ ЛЕТУЧИЕ НЕЛЕТУЧИЕ H 2 SO 4, HNO 3 H 2 Si. O 3 H 2 S, HCL H 2 SO 4, H 3 PO 4

Типичные реакции кислот • Кислота + основание = соль + вода H 2 SO 4 +2 Na. OH = Na 2 SO 4 + 2 H 2 O 2 H+ +2 OH- = 2 H 2 O • Кислота + оксид металла = соль + вода Cu. O + 2 HCL = Cu. CL 2 + H 2 O Cu. O + 2 H+ = H 2 O + Cu 2+ • Кислота + металл = водород + соль 2 HCL +Zn = Zn. CL 2 + H 2 2 H+ + Zn 0 =Zn 2+ +H 2 Условия: - в ряду напряжений металл должен стоять до водорода - в результате реакции должна получиться растворимая соль • Кислота + соль = новая кислота + новая соль Условия: - в результате реакции должны получиться газ, осадок или вода. Ba. CL 2 + H 2 SO 4 = Ba. SO 4 + 2 HCL Ba 2+ + SO 42 - = Ba. SO 4

ПРОВЕРЬ СЕБЯ 1. Формула кислоты это: а) Na. OH в) Cu. CL 2 б) HCL г) SO 3 2. Лакмус в растворе, полученном при взаимодействии оксида серы (IV) с водой: а) синий в) фиолетовый б) красный г) малиновый 3. С раствором серной кислоты взаимодействует: а) оксид магния в) оксид фосфора б) оксид углерода г) сера 4. Соляная кислота не взаимодействует с металлом: а) алюминием в) серебром б) железом г) цинком 5. Пара ионов, которая может одновременно находится в растворе: а) H+ и Si. O 3 в) Н+ и SO 42 б) Cu 2+ и ОНг) Ag+ и CL 6. Пара веществ взаимодействующих друг с другом: а) H 2 SO 4 u Si. O 2 в) Сu u H 3 PO б) Cu. O u Na 2 O г) НСL u Na. OH
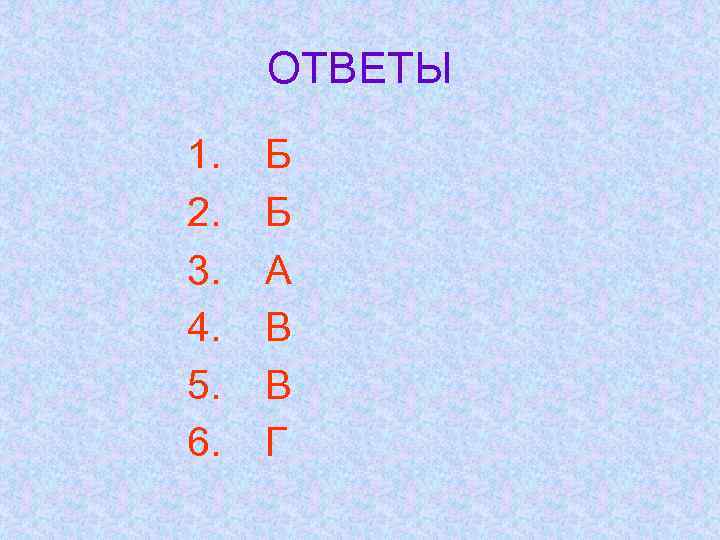
ОТВЕТЫ 1. 2. 3. 4. 5. 6. Б Б А В В Г
Кислоты.ppt