МФ Родионова Д..pptx
- Количество слайдов: 25

Обнаружение лекарственных средств в окрашенных волосах для целей химико-токсикологического анализа Родионова Д. Ю. (научный руководитель –Стрелова О. Ю. , к. х. н. , доцент) ФГБОУ ВО Санкт-Петербургская государственная химико-фармацевтическая академия, кафедра фармацевтической химии Химико-токсикологической лаборатория СПб ГБУЗ МНД-1 Центр экспериментальной фармакологии

Актуальность По данным Совета Безопасности РФ общее число наркозависимых граждан России составляет 640 тысяч человек. Но нелегальный оборот наркотических веществ является лишь частью проблемы. На сегодняшний день люди всё чаще умышленно употребляют лекарственные средства в немедицинских целях. Как пример – димедрол и производные барбитуровой кислоты. Согласно исследованиям, более 50% людей в возрасте от 20 лет изменяют цвет волос с помощью косметических средств, из них 17% женщин настолько долго окрашивают волосы, что даже не помнят их натуральный оттенок (Dailymail, 2013). Данные обстоятельства требуют разработки и внедрения в практику новых методов анализа биологических объектов. 2

Цели и задачи Целью работы является разработка методики обнаружения с помощью ферментативного гидролиза токсических веществ, на примере производных барбитуровой кислоты и димедрола, в окрашенных волосах как объекте химико-токсикологического исследования. Задачи: 1. Обзор литературных данных по вопросам накопления веществ искусственно окрашенных волосах, характеристики различных красителей для волос и этапов пробоподготовки волос. 2. Определение фонового уровня эндогенных веществ на хроматограммах после проведения кислотного, щелочного и ферментативного гидролиза окрашенных волос. 3. Создание модели длительного приема производного пиримидина (фенобарбитала), а также димедрола с участием экспериментальных животных (припродно окрашенные морские свинки). 4. Разработка методики ферментативного гидролиза окрашенной экспериментальных животных с целью выделения токсических веществ. 5. Статистическая обработка полученных данных и валидация методики. 3 в природно и искусственных шерсти
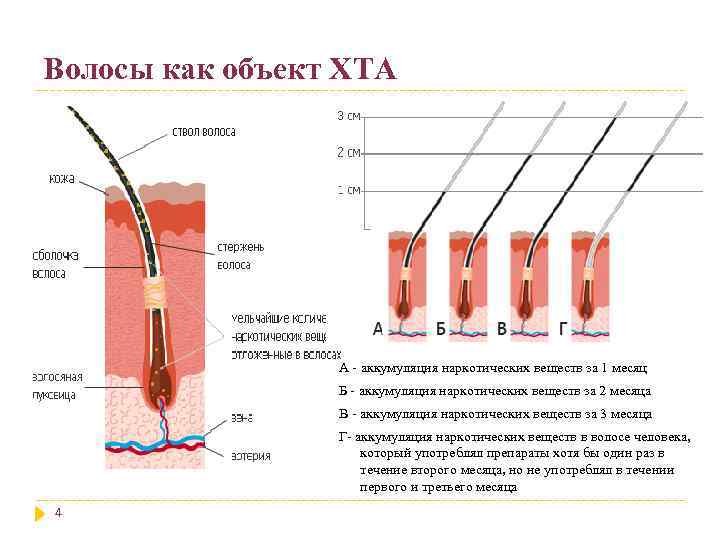
Волосы как объект ХТА А - аккумуляция наркотических веществ за 1 месяц Б - аккумуляция наркотических веществ за 2 месяца В - аккумуляция наркотических веществ за 3 месяца Г- аккумуляция наркотических веществ в волосе человека, который употреблял препараты хотя бы один раз в течение второго месяца, но не употреблял в течении первого и третьего месяца 4

Меланин и цвет волос Натуральный цвет волос обусловлен гранулами с пигментом меланином, который делят на два класса: эумеланин (выделяют подклассы – черный и коричневый) и феомеланин (от желтого до красного). Огромное разнообразие оттенков волосяного покрова головы людей и цвета шерсти/перьев животных определяется различным количественным соотношением эумеланина и феомеланина. 5

Меланин и ксенобиотики Исследования на животных, описанные в литературе, показали, что концентрация ксенобиотиков в волосах зависит от степени их пигментации. Наибольшее количество инкорпорированных веществ было отмечено в черных волосах, затем в каштановых и в наименьшей степени в светлых. Это можно объяснить наличием определенной аффиности токсикантов к меланину, а также фактом того, что меланин обусловливает кислый р. Н волос, стимулируя переход ксенобиотиков из плазмы крови в клетки фолликула. 6
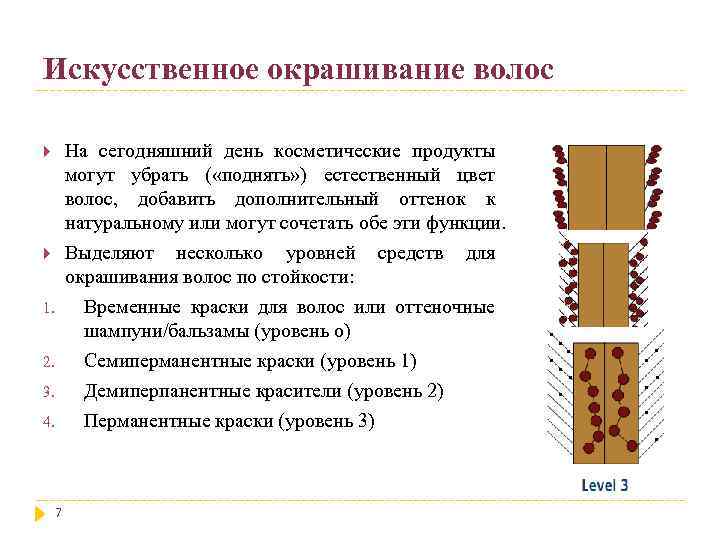
Искусственное окрашивание волос На сегодняшний день косметические продукты могут убрать ( «поднять» ) естественный цвет волос, добавить дополнительный оттенок к натуральному или могут сочетать обе эти функции. Выделяют несколько уровней средств для окрашивания волос по стойкости: Временные краски для волос или оттеночные шампуни/бальзамы (уровень о) Семиперманентные краски (уровень 1) Демиперпанентные красители (уровень 2) Перманентные краски (уровень 3) 1. 2. 3. 4. 7
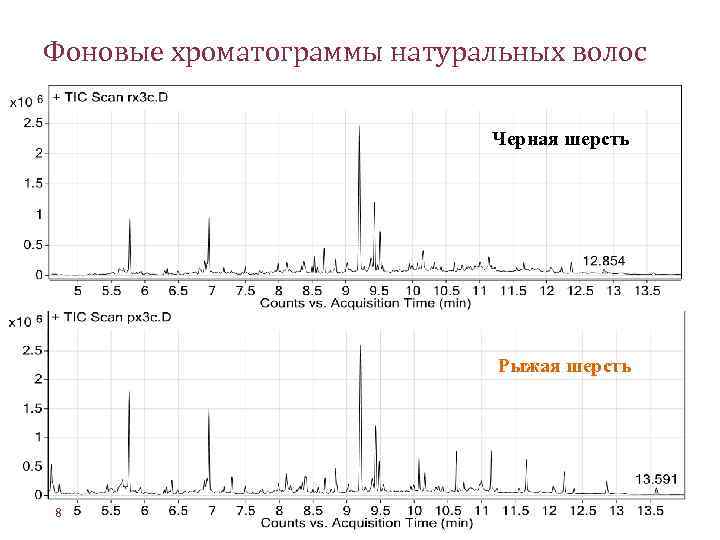
Фоновые хроматограммы натуральных волос Черная шерсть Рыжая шерсть 8
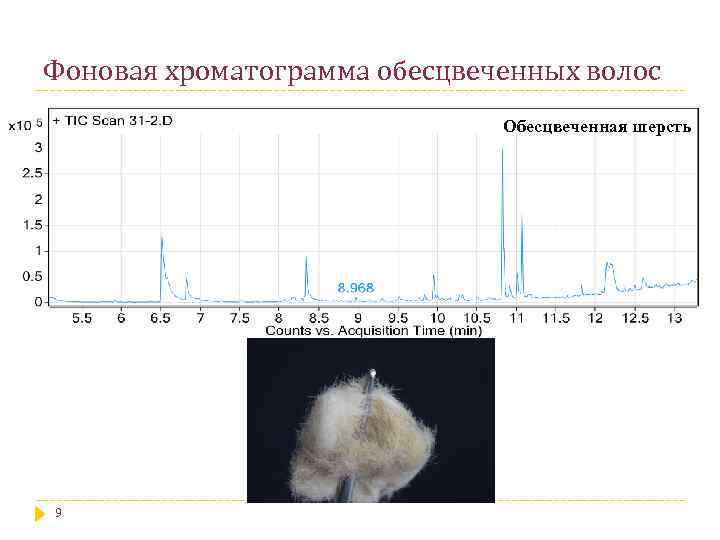
Фоновая хроматограмма обесцвеченных волос Обесцвеченная шерсть 9

Экспериментальная работа Ежесуточно животным в ротовую полость вводили заданный объем водного раствора фенобарбитала или димедрола. Отбор шерсти животных производили на каждый 28 -30 день после начала эксперимента. Полученные навески промывали от внешних загрязнений водой очищенной, затем метанолом. Высушенные при комнатной температуре навески измельчали ножницами, затем в шаровой мельнице до порошкообразной массы. Затем на аналитических весах отвешивали точные навески. 10
Исследуемые вещества Димедрол • Щелочной гидролиз • Ферментативны й гидролиз 11 Фенобарбита л • Кислотный гидролиз • Ферментативны й гидролиз

Методика щелочного гидролиза натуральных черных волос в целях изолирования димедрола К точной навеске образца шерсти в конической тубе с завинчивающейся крышкой объемом 15 мл добавляли 4 мл 2 М раствора калия гидроксида, плотно закрывали крышкой и выдерживали при 370 С в течение 12 ч в термостате. Гидролизат охлаждали, и проводили извлечение методом жидкость-жидкостной экстракцией 3 мл хлороформа 3 раза при р. Н 9 -10 среды. Полученные вытяжки объединяли и выпаривали досуха. Сухой остаток растворяли в 500 мкл комплексного растворителя (дихлорметан: дихлорэтан: гептан: изопропиловый спирт) и исследовали методом газовой хроматографии. 12

Методика кислотного гидролиза натуральных черных волос в целях изолирования фенобарбитала К навеске образца шерсти в пенициллиновом флаконе объемом 10 мл добавляли 5 мл 6 М раствора кислоты хлористоводородной, укупоривали и нагревали при 370 С в течение 12 -14 ч в термостате. Гидролизат охлаждали и извлечение проводили методом жидкость-жидкостной экстракцией при р. Н 2 среды. Экстрагировали 3 мл хлороформа 3 раза. Полученные вытяжки объединяли и выпаривали досуха. Сухой остаток растворяли в 500 мкл комплексного растворителя (состоит из дихлорэтана, дихлорметана, гептана и изопропилового спирта в соотношении 1: 1: 1: 0, 5) и исследовали методом газовой хроматографии с масс-селективным детектированием. 13

Методика ферментативного гидролиза с помощью химотрипсина Ферментативный гидролиз химотрипсином выполняли в следующих условиях: раствор фермента готовили в соотношение фермент : шерсть животного (субстрат) 1: 100. Навеску фермента растворяли в фосфатном буфере с р. Н 7, 4 среды, затем термостатировали при 37 о. С 3 ч. Полученные пробы центрифугировали при 4600 об/мин в течение 10 мин. Затем отбирали центрифугат. К осадку добавляли вторую порцию раствора фермента в равном объеме, перемешивали и термостатировали следующие 3 ч в аналогичных условиях. После чего данную операцию повторяли с третьей порцией фермента. Общее время гидролиза составило 9 ч. К центрифугату добавляли водный раствор аммиака до р. Н 9 -10 среды (димедрол) или 20% раствор серной кислоты до р. Н = 2 -3 среды (фенобарбитал) и проводили извлечение методом жидкость-жидкостной экстракцией 3 мл хлороформа 3 раза. Полученные вытяжки объединяли и выпаривали досуха. Сухой остаток растворяли в 500 мкл комплексного растворителя и исследовали методом газовой хроматографии с масс-селективным детектированием в условиях описанных ниже. 14

Проведение газовой хроматографии с массселективным детектором Условия анализа: газ-носитель гелий, скорость потока через колонку 0, 8 мл/мин, температура испарителя 2800 С, температура интерфейса МС детектора 2900 С, температура колонки программируемая: начальная - 800 С в течение 0, 4 мин, нагревание со скоростью 500 С/мин до 1000 С, далее 300 С/мин до 3000 С с выдержкой при конечной температуре 5 мин. Режим сканирования: по полному ионному току (SCAN) в диапазоне масс mz 40 -500 а. е. м. В газовый хроматограф автоматически с помощью автосамплера вводили 1 мкл исследуемого раствора. 15
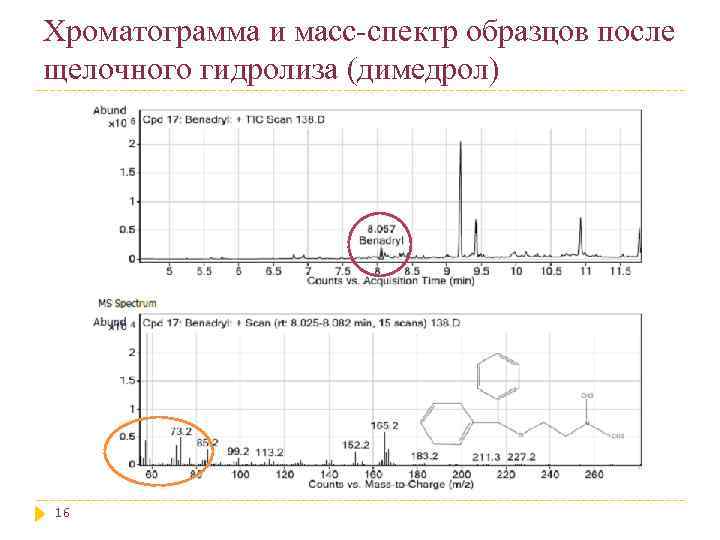
Хроматограмма и масс-спектр образцов после щелочного гидролиза (димедрол) 16
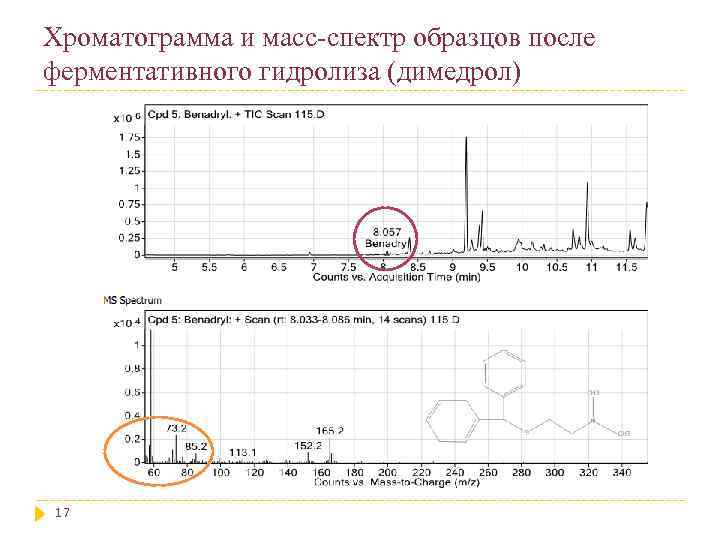
Хроматограмма и масс-спектр образцов после ферментативного гидролиза (димедрол) 17
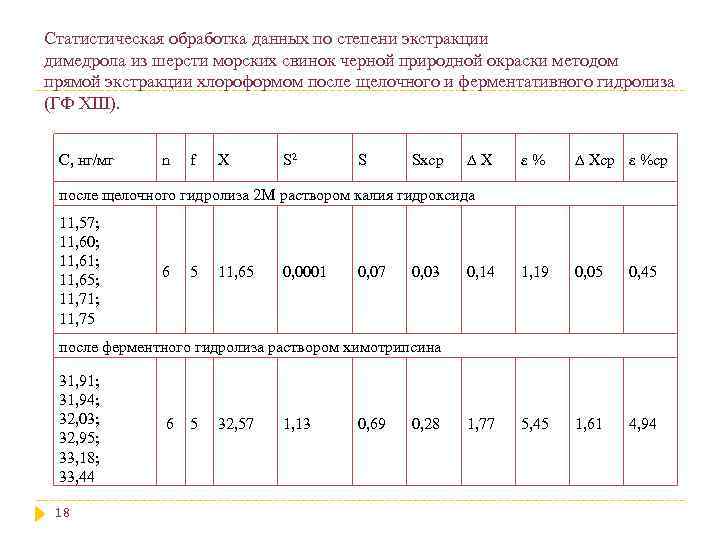
Статистическая обработка данных по степени экстракции димедрола из шерсти морских свинок черной природной окраски методом прямой экстракции хлороформом после щелочного и ферментативного гидролиза (ГФ XIII). С, нг/мг n f X S 2 S Sxср ∆Х ε% ∆ Хср ε %ср 0, 14 1, 19 0, 05 0, 45 1, 77 5, 45 1, 61 4, 94 после щелочного гидролиза 2 М раствором калия гидроксида 11, 57; 11, 60; 11, 61; 11, 65; 11, 71; 11, 75 6 5 11, 65 0, 0001 0, 07 0, 03 после ферментного гидролиза раствором химотрипсина 31, 91; 31, 94; 32, 03; 32, 95; 33, 18; 33, 44 18 6 5 32, 57 1, 13 0, 69 0, 28
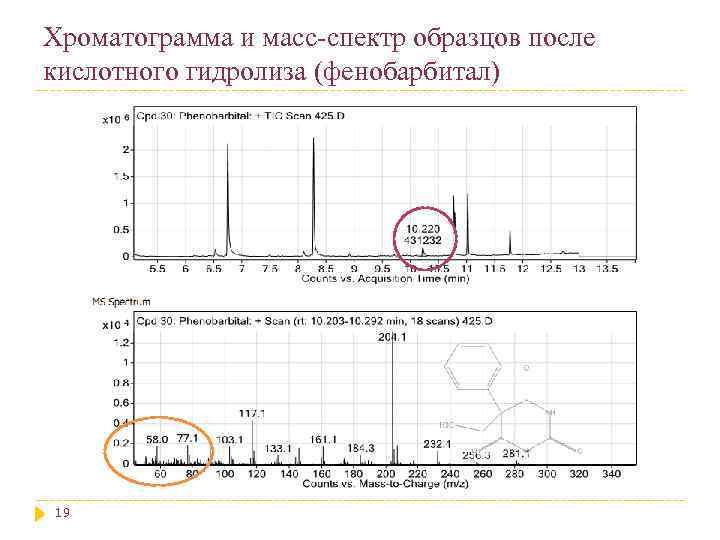
Хроматограмма и масс-спектр образцов после кислотного гидролиза (фенобарбитал) 19
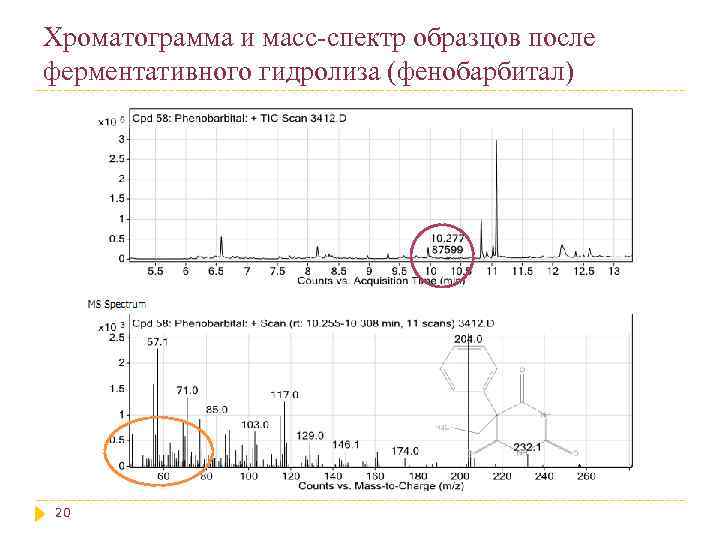
Хроматограмма и масс-спектр образцов после ферментативного гидролиза (фенобарбитал) 20
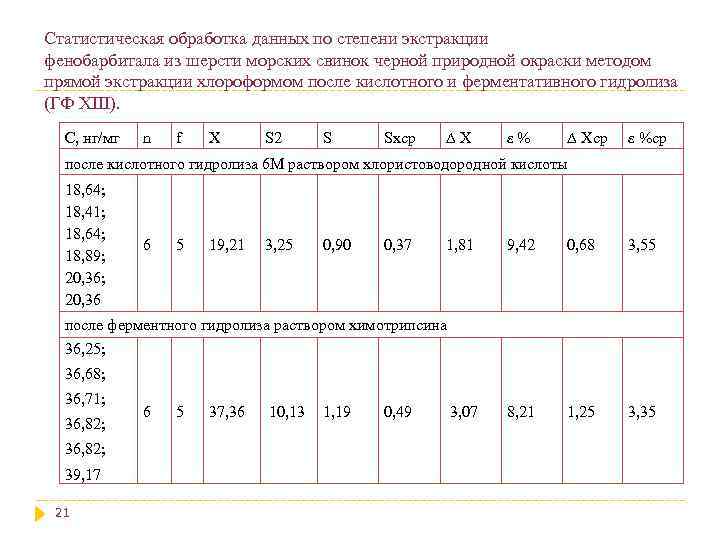
Статистическая обработка данных по степени экстракции фенобарбитала из шерсти морских свинок черной природной окраски методом прямой экстракции хлороформом после кислотного и ферментативного гидролиза (ГФ XIII). С, нг/мг n f X S 2 S Sxср ∆Х ε% ∆ Хср ε %ср после кислотного гидролиза 6 М раствором хлористоводородной кислоты 18, 64; 18, 41; 18, 64; 18, 89; 20, 36 6 5 19, 21 3, 25 0, 90 0, 37 1, 81 9, 42 0, 68 3, 55 8, 21 1, 25 3, 35 после ферментного гидролиза раствором химотрипсина 36, 25; 36, 68; 36, 71; 36, 82; 39, 17 21 6 5 37, 36 10, 13 1, 19 0, 49 3, 07
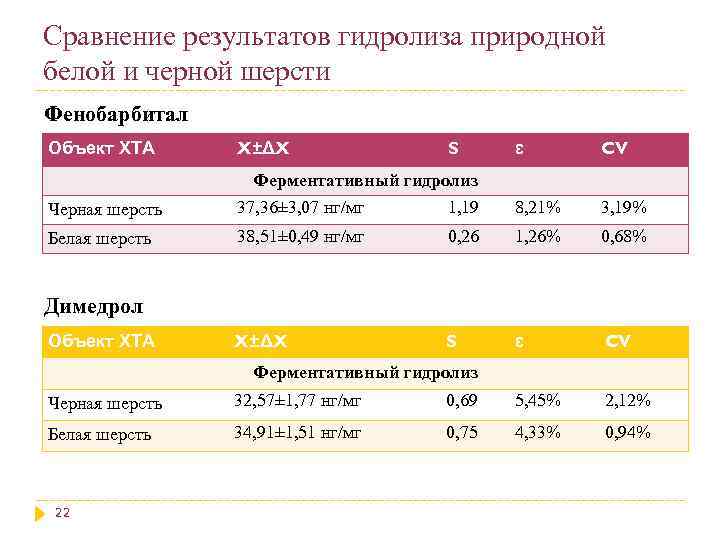
Сравнение результатов гидролиза природной белой и черной шерсти Фенобарбитал Объект ХТА X±ΔX S ɛ CV Черная шерсть Ферментативный гидролиз 37, 36± 3, 07 нг/мг 1, 19 8, 21% 3, 19% Белая шерсть 38, 51± 0, 49 нг/мг 0, 26 1, 26% 0, 68% X±ΔX S ɛ CV Димедрол Объект ХТА Ферментативный гидролиз Черная шерсть 32, 57± 1, 77 нг/мг 0, 69 5, 45% 2, 12% Белая шерсть 34, 91± 1, 51 нг/мг 0, 75 4, 33% 0, 94% 22

Валидация метода ферментативного гидролиза 23

Заключение 1. 2. 3. 4. 24 Показано, что фоновый уровень эндогенных веществ в природно окрашенных и неокрашенных волосах не влияет на интерпретацию результатов. Пробы искусственно осветленных волос после ферментативного гидролиза получаются чище. Работа по их анализу продолжается. Экспериментально проверено, что ферментативный гидролиз может быть использован на природно окрашенных в черный цвет волосах, полученные результаты сопоставимы с природно неокрашенными волосами. Разработана и валидирована методика ферментативного гидролиза для натуральных черных волос на примере фенобарбитала и димедрола.

Спасибо за внимание 25
МФ Родионова Д..pptx