Обменные реакции в растворах, гидролиз.ppt
- Количество слайдов: 12

Обменные реакции в растворах, гидролиз

Необходимым условием протекания обменных реакций в растворах электролитов является удаление из раствора тех или иных ионов вследствие образования малодиссоциирующих соединений (слабые электролиты и комплексные ионы) или малорастворимых веществ (осадки и газы ).

Образование малодиссоциирующих соединений: 1) HCI + Na. OH = Na. Cl + H 2 O Н++ОН- Н 2 О 2) СН 3 СОONа + HCI СН 3 СООН + Nа. СI СН 3 СОО- + Н+ СН 3 СООН Образование малорастворимых веществ: 1) Na. CI + Ag. NO 3 Ag. CI + Na. NO 3. Cl- + Ag+ Ag. CI

Образование газов 1) Na 2 S+2 HCI 2 Na. Cl + H 2 S S 2 - + 2 H+ H 2 S Реакции, в которых слабые электролиты или малорастворимые вещества входят в состав как продуктов, так и исходных веществ, протекают, как правило, не до конца. Равновесие обратимого процесса смещается в сторону образования наименее диссоциированных или наименее растворимых соединений.

Гидролиз солей Обменная реакция между водой и соединением называется его гидролизом. Гидролиз солей - реакция, обратная реакции нейтрализации слабых кислот (оснований) сильными основаниями (кислотами) или слабых кислот слабыми основаниями.

Типы гидролиза 1. Гидролиз по катиону Подвергаются соли, образованные катионом слабого основания и анионом сильной кислоты (NH 4 Br, Zn. Cl 2, Cu(NO 3)2 и др. ). Среда при гидролизе кислая (р. Н<7), процесс обратимый. Равновесие можно сместить по принципу Ле Шателье Молекулярное уравнение 1 ступени гидролиза Сu. Сl 2 + НОН Cu. OHCI + НСI. Гидролизом по 2 ступени при о. у. можно пренебречь.

2. Гидролиз по аниону. Подвергаются соли, образованные катионом сильного основания и анионом слабой кислоты (К 2 СО 3, Na 2 SO 3, К 3 РО 4 и др. ). При гидролизе создается щелочная среда (р. Н>7). СН 3 СОONa + HOH СН 3 СООН +Na. ОН CH 3 COO+ + НОН СН 3 СООН + OHПроцесс обратимый, равновесие гидролиза сильно смещено влево.

3. Гидролиз по катиону и аниону. По катиону и аниону гидролизуются соли, образованные катионом слабого основания и анионом слабой кислоты. Молекулярное уравнение: Cu. F 2 + НОН Cu. OHF + HF Cu 2+ + 2 F- +H 2 O Cu. OH+ + HF р. Н=7, процесс необратимый

Количественные характеристики Степенью h и константа гидролиза Кг : h = Сг/Сo, Сг - концентрация гидролизованной части соли, Сo- общая концентрация растворенной соли. Для гидролиза по аниону в общем виде А- + НОН = НА + ОНС(НА) С(ОН-) Кw С(Н 2 О)/С(А-)= Кг, используя соотношение С(ОН-)=Кw/С(H+), можно получить Кг= Кw/КНА или Кг= Кw/Кк

Гидролиз по катиону: К+ + НОН =КОН + Н+ аналогично: С(КОН) С(Н+) /С(К+)= Кг =Кw/Ко Гидролиз по катиону и по аниону : К+ +А- + НОН =КОН + НА С(КОН) С(НА) /С(К+) С(А-)= Кг =Кw/Ко Кк Связь Кг и h описывается выражением, подобным закону Оствальда: Кг=Сh 2 , h =(Кг/С)1/2
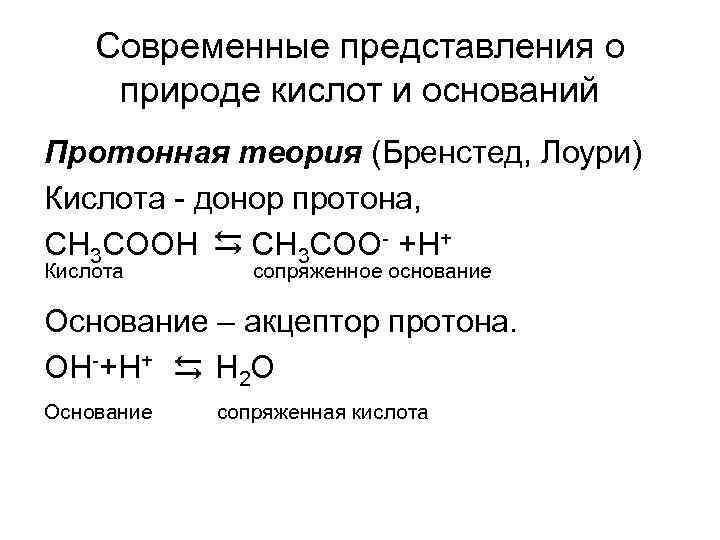
Современные представления о природе кислот и оснований Протонная теория (Бренстед, Лоури) Кислота - донор протона, СН 3 СООН СН 3 СОО- +Н+ Кислота сопряженное основание Основание – акцептор протона. ОН-+Н+ Н 2 О Основание сопряженная кислота

Электронная теория (Льюис) Кислота - акцептор электронных пар Основание – донор электронных пар HCl + NH 3 = NH 4 Cl кислота основание продукт Ag+ + 2 NH 3 = [Ag(NH 3)2]+
Обменные реакции в растворах, гидролиз.ppt