Обмен жирных кислот и кетоновых тел АТ.ppt
- Количество слайдов: 34

Обмен жирных кислот и кетоновых тел

План: • • • Обмен ЖК Основные условия и локализация процесса бета-окисления ЖК Активация ЖК – основное условие вовлечения ее в процессы метаболизма Роль карнитина в транспорте ЖК в митохондрии Последовательность реакций бета-окисления, энергетический выход Метаболическая судьба ацетил Ко. А: окисление в ЦТК Биосинтез и использование кетоновых тел в качестве источников энергии Биосинтез ЖК(условия, локализация процесса, роль малонил Ко. А) Характеристика синтетазной системы Последовательность реакций биосинтеза ЖК, пусковая реакция синтеза Элонгация углеводородной цепи ЖК, образование ненасыщенных ЖК

Жирные кислоты (ЖК) – структурные компоненты большинства липидов ЖК – это длинноцепочечные органические кислоты, содержащие от 4 до 24 атомов углерода, а также 1 карбоксильную группу (СООН) и длинный неполярный углеводородный «хвост» , из-за которого большинство липидов нерастворимы в воде и проявляют свойства масел или жиров. В клетках и тканях ЖК встречаются не в свободном состоянии, а в ковалентно связанной форме в составе липидов различных классов. В свободном виде ЖК можно получить только путем химического или ферментативного гидролиза.

Номенклатура ЖК Название ЖК происходит от названия исходного углеводорода путем присоединения окончания – овая. Например, насыщенная С 18 – ЖК называется октадекановой, потому что исходным углеводородом является октадекан. Насыщенной называется ЖК, содержащая только одинарные связи. Ненасыщенной называется ЖК, содержащая 1 или 2 двойные связи. В месте расположения двойной связи молекула ЖК делает изгиб цепи, что придает жесткость молекуле. С 18 -ЖК с одной двойной связью называется октадекеновой, с двумя двойными связями – октадекадиеновой, с тремя – октадекатриеновой. Символ 18 : 0 обозначает ЖК без двойных связей; символ 18 : 0 указывает на наличие двух двойных связей.

Ненасышенные ЖК при температуре тела находятся в жидком состоянии, а насыщенные – в воскоподобном. Нумерация углеродных атомов происходит с карбоксильного конца: 3 2 β 1 ά (ω) Н 3 С (СН 2)n С С СООН Положение двойной связи представлено знаком Δ с номером в верхнем индексе. Например, обозначение цисΔ 9 говорит о наличии цис-двойной связи между 9 -м и 10 -м углеродными атомами; транс-Δ 2 обозначает трансдвойную связь между 2 и 3 атомами углерода. Обычно 2 двойные связи не бывают сопряженными ( СН═СН а всегда между ними находиться ), метиленовая группа ( СН═СН 2 СН═СН Двойные СН ). связи практически во всех природных ЖК находятся в цисконформации, что приводит к изгибу алифатической цепи.

Свойства и особенности природных ЖК ЖК входят в состав различных классов липидов, образуя эфирные или амидные связи. • Монокарбоновые кислоты – содержат линейные углеводородные цепи (обычно С 12 – С 20); общая формула СН 3(СН 2)n. СООН. • ЖК обычно содержат четное число углеродных атомов (редко встречаются с нечетным числом) • ЖК делят на насыщенные и ненасыщенные (содержащие этиленовые связи). На долю ненасыщенных ЖК в природных липидах приходиться примерно ¾ всех ЖК • Как правило, природные ненасыщенные ЖК имеют цисконфигурацию, и крайне редко в полиеных кислотах встречается транс-конфигурация • ЖК являются гидрофобными соединениями. Большое число неполярных связей С и С в углеводородной цепи ЖК С Н придает неполярный характер молекуле липида в целом, хотя в ней имеется полярная (заряженная) группа – СОО.

Наряду с насышенными и ненасышенными ЖК в природе встречаются ЖК с разветвленной цепью, например, туберкулостеариновая кислота, выделенная из туберкулезной палочки (С 19): Н 3 С (СН 2)7 СН (СН 2)8 СООН │ СН 3 В некоторых бактериях и растениях найдены ЖК, содержащие циклопропановое кольцо, например, лактобациловая кислота (С 19): Н 3 С (СН 2)5 СН СН (СН 2)9 СООН СН 2
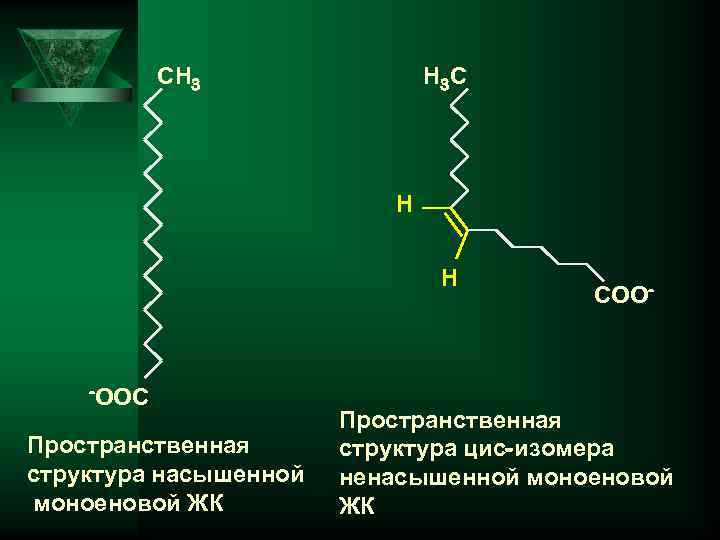
СН 3 Н 3 С Н Н -ООС Пространственная структура насышенной моноеновой ЖК СОО- Пространственная структура цис-изомера ненасышенной моноеновой ЖК

Большое число неполярных связей С и С в С Н углеводородной цепи ЖК придает неполярный характер молекуле липида в целом, хотя в ней имеется полярная, заряженная группа СОО- . Неполярность ВЖК является причиной нерастворимости липидов в воде. Помимо этого, фактор гидрофобности обусловливает также особую сборку липидов в биомембране. В водном растворе ЖК образуют мицеллы, конформация которых зависит от длины углеводородной цепи, числа двойных связей, соотношения полярной и неполярной частей молекулы. В обычных мицеллах гидрофильные полярные головки ( СОО- ЖК обращены в сторону водной фазы, тогда ) как неполярные углеводородные цепи образуют гидрофобное ядро, изолированное от водного окружения.

Мицелла – амфипатическое соединение; ионизированная карбоксильная группа образует полярную головку, а углеводородная цепь – неполярный хвост. Отрицательно заряженная карбоксильная группа Капля жира Гидрофобный хвост

Функции ЖК Ú Служат строительными фосфолипидов и гликолипидов; блоками Ú Важные компоненты биомембран; Ú Выполняют роль «топлива» , запасаются в виде ТАГ, не несущих заряда эфиров глицерола. Их называют также нейтральными жирами, или триацилглицеридами
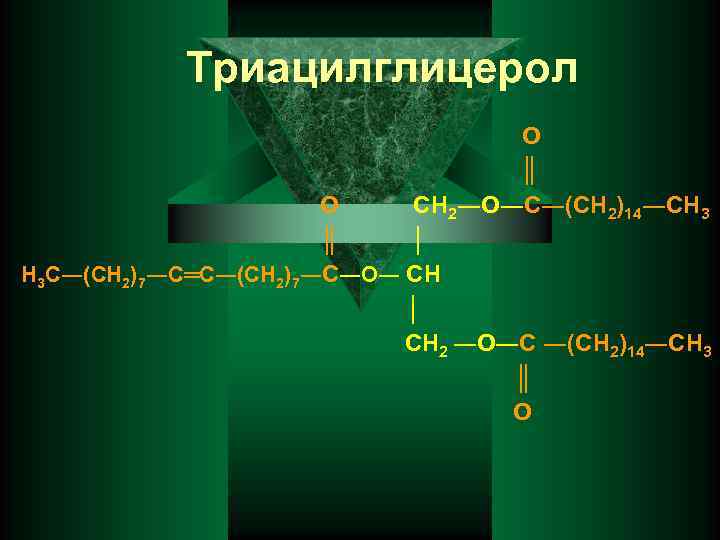
Триацилглицерол О ║ О СН 2―О―С―(СН 2)14―СН 3 ║ │ Н 3 С―(СН 2)7―С═С―(СН 2)7―С―О― СН │ СН 2 ―О―С ―(СН 2)14―СН 3 ║ О

Гидролиз ТАГ идет ступенчато под действием липазы: СН 2 ОН + С 15 Н 31 СООН пальмитиновая кислота ТАГ СНОН + С 17 Н 33 СООН олеиновая кислота СН 2 ОН + С 15 Н 35 СООН стеариновая кислота глицерин

ТАГ в силу своего восстановленного и обезвоженного состояния представляют собою высококонцентрированные резервы метаболической энергии, поскольку содержат большое количество С―Н связей. Выход энергии в результате полного окисления ЖК составляет около 9 ккал/г, а для углеводов и белков эта величина равна примерно 4 ккал/г. Следовательно, количество энергии, запасенной в одном грамме почти обезвоженного жира, более чем в 6 раз превышает количество энергии, запасенной в одном грамме гидратированного гликогена. Поэтому именно ТАГ, а не гликоген били отобраны в ходе эволюции в качестве основного источника энергии.

ЖК распадаются путем последовательного удаления двухуглеродных фрагментов. Окисление С―Н связей называется β-окислением, т. к. в основном окисляется β-углеродный атом. Открытие данного процесса принадлежит Franz Knoop (1904 г. ), который экспериментальным путем установил, что при скармливании собакам фенилбутирата (ЖК с четным числом атомов углерода) в моче обнаруживается производное фенилуксусной кислоты, а при скармливании фенилпропионата (ЖК с нечетным числом атомов углерода) – производное безойной кислоты. В 1949 г. Юджин Кеннеди и Альберт Ленинджер обнаружили, что окисление жирных кислот происходит в митохондриях.

β- окисление происходит в митохондриях печени, скелетной и сердечной мышц. Этапы: I этап: активация ЖК в цитозоле (1) и транспорт ацил-Ко. А в митохондрии (2); II этап: сам процесс β-окисления ацил-Ко. А путем отщепления двууглеродного фрагмента – ацетил. Ко. А; при этом образуются несколько молекул ацетил-Ко. А при участии кофермента А, и все последующие промежуточные продукты процесса окисления ЖК представляют собой тиоэфиры кофермента А. III этап: окисление образующегося ацетил-Ко. А в ЦТК

I этап. Образовавшиеся при гидролизе ТАГ под действием липаз свободные ЖК находятся в цитоплазме. Т. к. мембрана митохондрий непроницаема для ЖК, они попадают в матрикс митохондрий после активации в виде Со. А-эфиров в результате ряда ферментативных превращений под действием фермента карнитинацилтрансферазы (ацил-Ко. А синтетаза; 6 класс): R―СООН + НS Ко. А +АТФ R-CО-S-Ко. А + АМФ +Фн. Фн Кофермент карнитин обеспечивает транспорт кислот (ацильных остатков) через митохондриальную мембрану, непроникающих через нее в свободном виде. Во внешней мембране митохондрий имеется фермент карнитинацилтрансфераза I, который катализирует перенос ацил-Ко. А на молекулу карнитина.
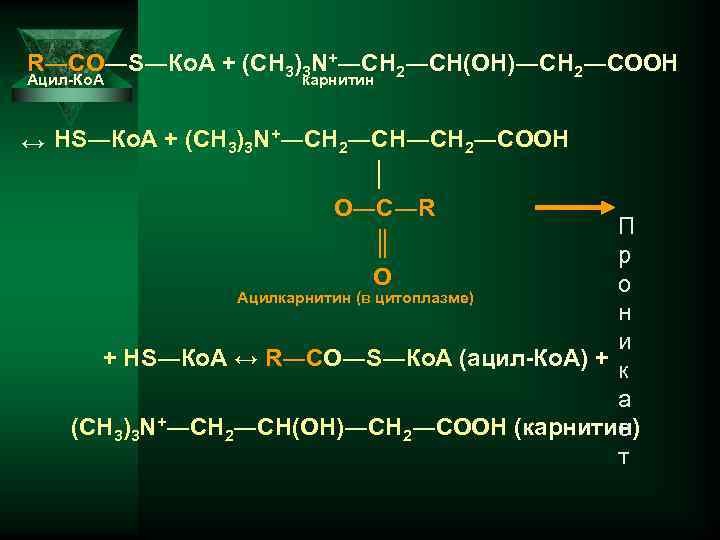
R―CО―S―Ко. А + (СН 3)3 N+―CН 2―СН(ОН)―СН 2―СООН Ацил-Ко. А карнитин ↔ НS―Ко. А + (СН 3)3 N+―CН 2―СН―СН 2―СООН │ О―С―R ║ О П р о Ацилкарнитин (в цитоплазме) н и + НS―Ко. А ↔ R―CО―S―Ко. А (ацил-Ко. А) + к а (СН 3)3 N+―CН 2―СН(ОН)―СН 2―СООН (карнитин) е т

Т. о. , ЖК первоначально активируются при участии АТФ и НS―Ко. А (коэнзима А). Переносчиком ацильныхгрупп из цитоплазмы в матрикс митохондрии служит карнитин. Ацил-Ко. А, соединяясь с карнитином, при участии специфического цитоплазматического фермента карнтин-ацетилтрансферазы образует ацилкарнитин (эфир карнитина и жирной кислоты), который обладает способностью проникать внутрь митохондрии. В митохондриях происходит обратная реакция – расщепление ацилкарнитина при участии НS―Ко. А и митохондриальной карнитинацилтрансферазы. При этом карнитин обратно возвращается в цитоплазму клетки, а ацетил-Ко. А подвергается в митохондриях окислению.

II этап. Ацил-Ко. А в митохондриях подвергается ферментативному дегидрированию (1 стадия дегидрировани). При этом ацил-Ко. А теряет два атома водорода а ά- и β положении, превращаясь в Ко. Аэфир ненасыщенной кислоты β ά R―СН 2―СН 2―СО―S―Ко. А + ФАД ↔ ацил-Ко. А-дегидрогеназа β ά R―СН 2―СН═СН―СО―S―Ко. А + ФАДН 2 Еноил-Ко. А
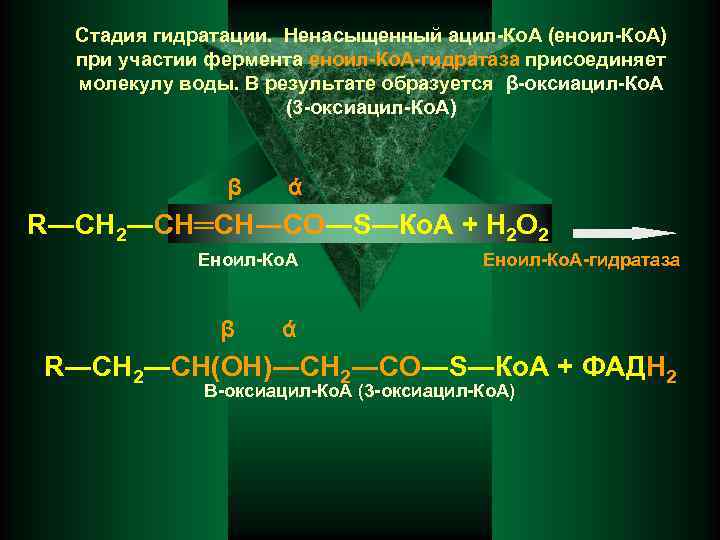
Стадия гидратации. Ненасыщенный ацил-Ко. А (еноил-Ко. А) при участии фермента еноил-Ко. А-гидратаза присоединяет молекулу воды. В результате образуется β-оксиацил-Ко. А (3 -оксиацил-Ко. А) β ά R―СН 2―СН═СН―СО―S―Ко. А + Н 2 О 2 Еноил-Ко. А β Еноил-Ко. А-гидратаза ά R―СН 2―СН(ОН)―СН 2―СО―S―Ко. А + ФАДН 2 Β-оксиацил-Ко. А (3 -оксиацил-Ко. А)
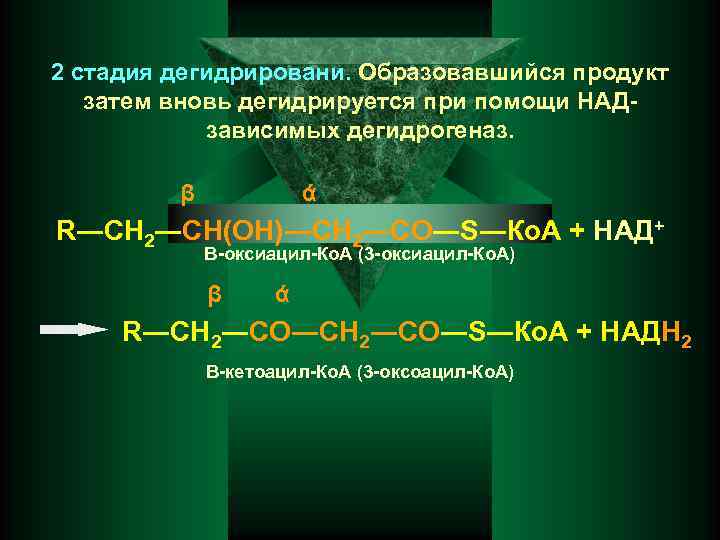
2 стадия дегидрировани. Образовавшийся продукт затем вновь дегидрируется при помощи НАДзависимых дегидрогеназ. β ά R―СН 2―СН(ОН)―СН 2―СО―S―Ко. А + НАД+ Β-оксиацил-Ко. А (3 -оксиацил-Ко. А) β ά R―СН 2―СО―S―Ко. А + НАДН 2 Β-кетоацил-Ко. А (3 -оксоацил-Ко. А)
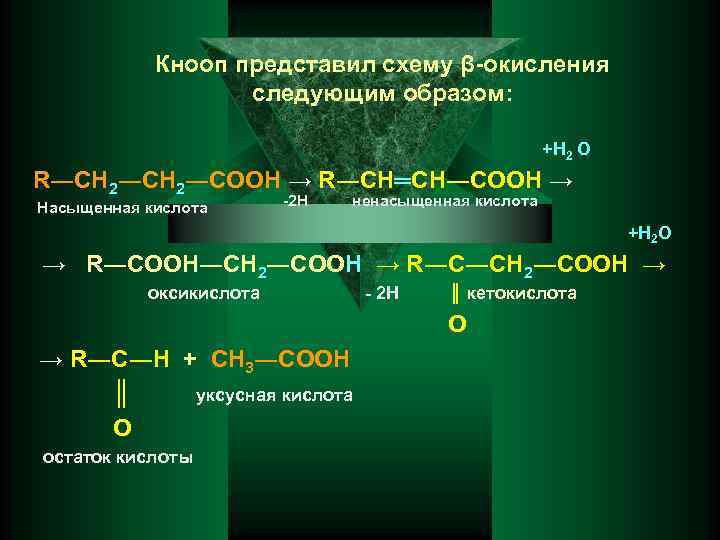
Кнооп представил схему β-окисления следующим образом: +Н 2 О R―CН 2―СООН → R―CН═СН―СООН → Насыщенная кислота -2 Н ненасыщенная кислота +Н 2 О → R―СООН―СН 2―СООН → R―С―СН 2―СООН → оксикислота - 2 Н ║ кетокислота О → R―С―Н + СН 3―СООН ║ уксусная кислота О остаток кислоты

Энергетический баланс При каждом цикле β-окисления образуется 1 молекула ФАД • Н 2 и 1 молекула НАД • Н 2. Всего за один цикл образуется 5 молекул АТФ (3 молекулы за счет НАД • Н 2 и 2 молекулы за счет ФАД • Н 2). При окислении пальмитиновой кислоты проходит 7 циклов β-окисления, что ведет к образованию 5 x 7=35 молекул АТФ. В процессе β-окисления пальмитиновой кислоты образуется 8 молекул ацетил-Ко. А. Каждая из которых, сгорая в ЦТК, дает 12 молекул АТФ. Т. о. , 8 молекул дадут 12 x 8=96 молекул АТФ. Следовательно, при окислении пальмитиновой кислоты образуется 35+96=131 молекул АТФ. однако

Продуктами окисления ЖК с четным числом углеродных атомов являются ацетил-Ко. А, ФАДН 2 и НАДН 2. Далее ацетил-Ко. А поступает в ЦТК, а ФАДН 2 и НАДН 2 – в дыхательную цепь. Особенности окисления ЖК с нечетным числом углеродных атомов состоят в том, что наряду с вышеперечисленными продуктами образуется одна молекула пропионил Ко. А (СН 3―СН 2―СО~SКо. А), которая затем превращается в метилмалонил-Ко. А, а затем в сукцинил-Ко. А (ферменты– пропионил-Ко. А-карбоксилаза, метилмалонил-Ко. А мутаза) АТФ АДФ СН 3―СН 2―СО~SКо. А СО 2 → НООС―СН 2―СО~SКо. А сукцинил-Ко. А СООН―СН 3―СН―СО~SКо. А

III этап. Тиолазная реакция. Происходит отщепление активированной уксусной кислоты (ацетил-Ко. А), которая затем окисляется в ЦТК, а ацил. Ко. А, укоротившийся на два углеродных атома, снова многократно проходит весь путь β-окисления до образования двух молекул ацетил-Ко. А β ά R―СН 2―СО―S―Ко. А + НS―Ко. А β-кетоацил-Ко. А (3 -оксоацил-Ко. А) R―CН 2―СО―S―Ко. А + СН 3―СО―S―Ко. А ацил-Ко. А ацетил-Ко. А

Особенности окисления ненасыщенных ЖК определяются положением и числом двойных связей в их молекулах. До места двойной связи ненасыщенные ЖК окисляются также, как насыщенные. Если двойная связь имеет ту же коньфигурацию (трансконфигурацию) и расположение Δ 2, 3, что и в еноил-Ко. А, образующемся при окислении насыщенных ЖК, то далее окисление идет обычным путем. В противном случае подключается дополнительный фермент – еноил-Ко. А-изомераза, который способствует перемещению двойной связи в нужное положение и изменяет ее конфигурацию из цис- в транс-. Скорость окисления ненасыщенных ЖК выше, чем насыщенных.

Регуляция β-окисления Ú Доступность ЖК Ú Скорость липолиза эндогенных липидов Ú Уровень запаса энергии в клетке: β- окисление активируется АДФ и ингибируется АТФ

Ацетил-Ко. А (СН 3―СО―S―Ко. А) служит субстратом для 3 -х важнейших метаболических путей: 1. окисление в ЦТК; 2. биосинтез ЖК; 3. образование мевалоновой кислоты и кетоновых тел Синтез кетоновых тел. Ацетил-Ко. А включается в ЦТК только при условии сбалансированного расщепления жиров и углеводов. В противном случае происходит накопление данного вещества и синтез кетоновых тел. К кетоновым телам относят ацетоуксусную кислоту (СН 3―СО―СН 2―СООН), β-гидроксимаслянную кислоту (СН 3―СНОН―СН 2―СООН) и ацетон (СН 3―СО―СН 3). Синтез кетоновых тел протекает в митохондриях, печени. Ацетоацетат образуется из ацетил-Ко. А в 3 стадии. Вначале 2 молекулы ацетил-Ко. А конденсируются с образованием ацетоацетил-Ко. А: 2 ацетил-Ко. А→ацетоацетил-Ко. А + ацетил Ко. А → β-гидрокси-βметилглутарил-Ко. А (ГМК-Ко. А) → ацетоацетат + ацетил-Ко. А.

Ацетоацетат спонтанно декарбоксилируется с образованием ацетона или гидрируется с помощью β -гидроксибутират-дегидрогеназы в βгидроксибутират. В процессе окисления всякой ЖК в качестве промежуточного продукта неизбежно образуется бутирил-Ко. А (СН 3 СН 2 2 СН СО~S Ко. А). Суммарная реакция этих процессов: 2 ацетил-Ко. А + Н 2 О → ацетоацетат + 2 Ко. А + Н+.

Метаболизм кетоновых тел СН 3 (СН 2)2 СО~ S Ко. А → СН 3 СН=СН СО~ S Ко. А → Бутирил-Ко. А - 2 Н+ кротонил-Ко. А +Н 2 О СН 3 СНОН СН 2 СО~ S Ко. А → СН 3 СО СН 2 СО~ S Ко. А Β-окибутирил-Ко. А + НS Ко. А - 2 Н+ ацетоацетил-Ко. А 2 СН 3 СО~S Ко. А ацетил-Ко. А Однако при некоторых заболеваниях и состояниях происходит гидролитическое расщепление β-оксибутирила-Ко. А и ацетоацетила. Ко. А с образованием свободных β-оксимасляной и ацетоуксусной кислот: СН 3 СНОН СН 2 СО~ S Ко. А → СН 3 СНОН СН 2 СО Β-окибутирил-Ко. А +Н 2 О β-оксимаслянная кислота + НS Ко. А → СН 3 СО СН 2 СО~ S Ко. А + Н 2 О → ацетоацетил-Ко. А → СН 3 2 СО СН СООН + НS Ко. А ацетоуксусная кислота

При нарушении нормального течения окислительных процессов ацетоуксусная кислота, вступая во взаимодействия с НАДН 2, может переходить в βоксимасляную кислоту СН 3 2 СО СН СООН + НАДН 2 ацетоуксусная кислота СН 3 СНОН СН 2 СО β-оксимасляная кислота + НАД Подвергаясь карбоксилированию, ацетоуксусная кислота служит источником образования ацетона. СН 3 │ СО │ СН 2 СООН │ С═О │ СН 3 ацетон + СО 2

Кетоновые тела – поставщики энергии для мыщц, мозга, почек и действуют, возможно как часть регуляторного механизма с обратной связью, предотвращая чрезвычайную мобилизацию жирных кислот из жировых депо. Исключением является печень, которая не использует кетоновые тела в качестве источника энергии. Существуют 2 ферментативных механизма активации ацетоуксусной кислоты 1 путь – использование АТФ и НS-Ко. А подобно активации ЖК (фермент – ацил-Ко. А-синтетаза): CН 3 -СО-СН 2 -СООН + АТФ + НS-Ко. А => СН 3 -СО-СН 2 -СО~S-Ко. А + АМФ + ФФн

2 путь – перенос Ко. А от сукцинил-Ко. А на ацетоуксусную кислоту (фермент – сукцинил. Ко. А-ацетоацетат-трансфераза): СООН-(СН 2)2 -СО~S-Ко. А ―> СН 3 -СО-СН 2 -СООН Сукцинил-Ко. А ацетоуксусная кислота <=> СН 3 -СО-СН 2 -СО~S-Ко. А + СООН-(СН 2)2 -СООН ацетоацетил-Ко. А янтарная кислота Образовавшийся ацетоацетил-Ко. Адалее подвергается тиолитическому расщеплению с образованием 2 молекул ацетил-Ко. А, которые поступают в ЦТК и распадаются там на СО 2 и Н 2 О. СН 3 -СО-СН 2 -СО~S-Ко. А + НS-Ко. А <=> 2 СН 3 -СО-S-Ко. А ацетоацетил-Ко. А
Обмен жирных кислот и кетоновых тел АТ.ppt