Обмен в-в (4 часа) для фарм заоч. (2).ppt
- Количество слайдов: 131

Обмен веществ

Углеводный обмен

Функции углеводов ü ü Обеспечивают около 57% суточного калоригенеза Являются составными частями более сложных соединений (НК, ГП, ГЛ и др. )

Функции углеводов l l l Служат предшественниками соединений других классов (липиды, заменимые аминокислоты) Выполняют структурообразовательную функцию Выполняют специфические функции
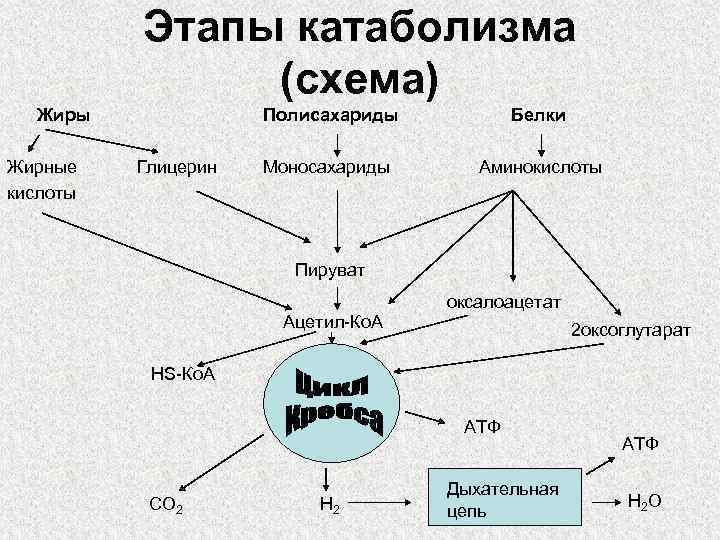
Этапы катаболизма (схема) Жиры Жирные кислоты Полисахариды Глицерин Белки Моносахариды Аминокислоты Пируват оксалоацетат Ацетил-Ко. А 2 оксоглутарат HS-Ко. А АТФ CO 2 H 2 Дыхательная цепь АТФ H 2 O
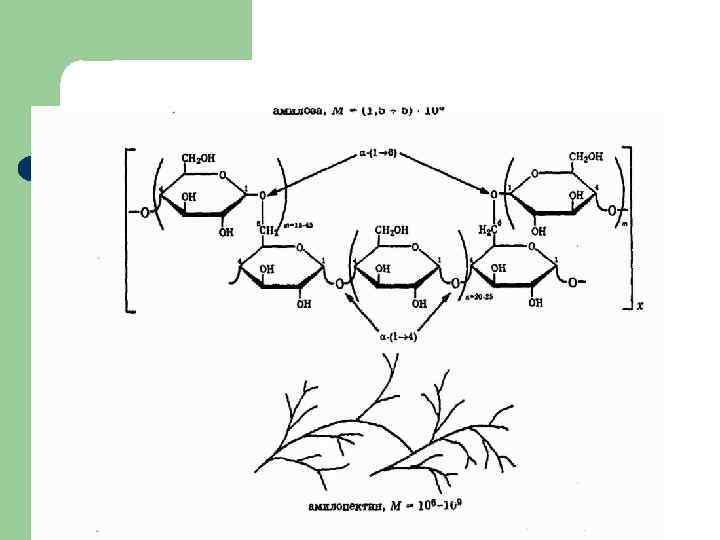
Строение крахмала

Строение гликогена
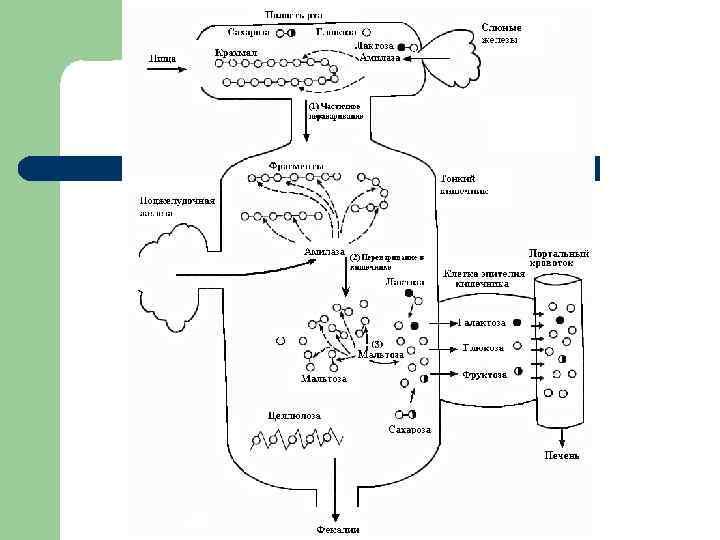

Роль печени в обмене углеводов Унификация моносахаридов 2. Гликогенная функция 3. Синтез углеводов из неуглеводных предшественников (глюконеогенез) 4. Синтез гликопротеинов крови 5. Образование глюкуроновой кислоты 1.
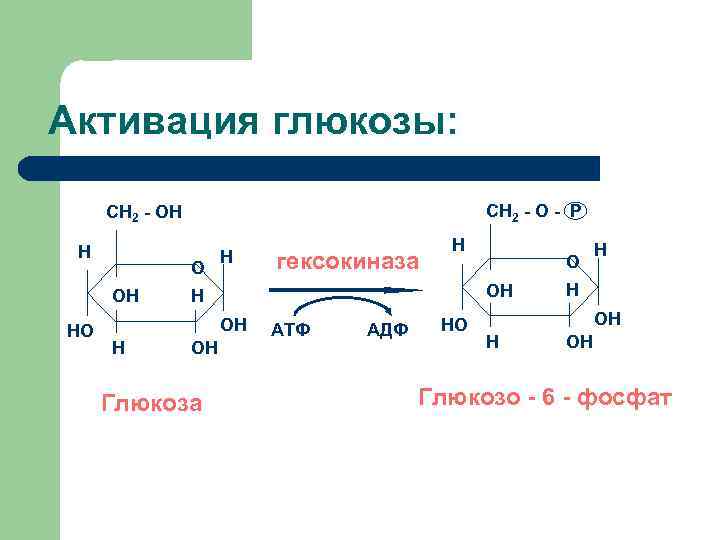
Активация глюкозы: CH 2 - O - P CH 2 - OH H O ОН HO H OH Глюкозa O ОH H OH H гексокиназа H АТФ АДФ HO H H OH Глюкозо - 6 - фосфат
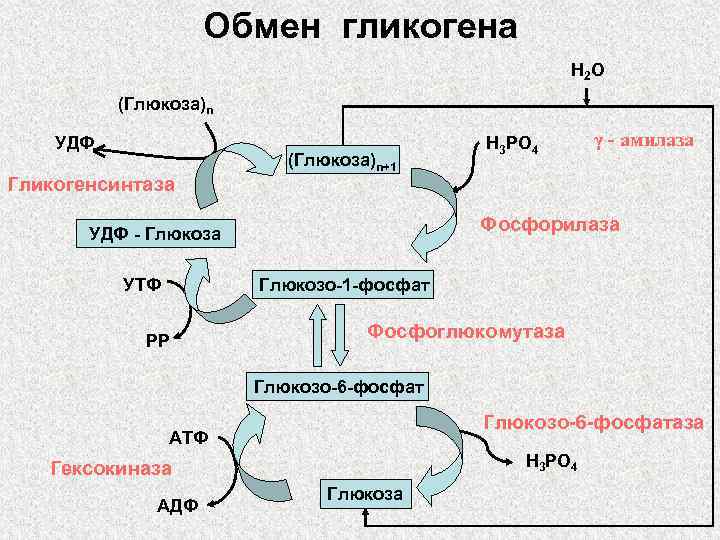
Обмен гликогена H 2 O (Глюкоза)n УДФ Гликогенсинтаза (Глюкоза)n+1 γ - амилаза Фосфорилаза УДФ - Глюкоза УТФ H 3 PO 4 Глюкозо-1 -фосфат РР Фосфоглюкомутаза Глюкозо-6 -фосфатаза АТФ H 3 PO 4 Гексокиназа АДФ Глюкоза

Значение гликолиза l l l Гликолиз имеет энергетическое значение Преимущества гликолиза: анаэробный процесс быстрый универсальный

Значение гликолиза l l Недостатки гликолиза: малоэффективный процесс продуктом гликолиза является лактат, накопление которого вызывает метаболиче-ский ацидоз.

Аэробное окисление глюкозы гликолиз ПДГ Глюкоза 2 пируват 2 НАД+ 2 НАДН+Н+ 2 АТФ (3 х2=6) 2 НАД+ 2 НАДН+Н + (3 х2=6) ЦТК + ДЦ 2 ацетил-Ко. А 12 х 2 = 24 АТФ СО 2 + Н 2 О

Значение ГНГ 1. 2. Является важным источником глюкозы в организме Удаляет большую часть лактата, что предохраняет клетки от метаболического ацидоза
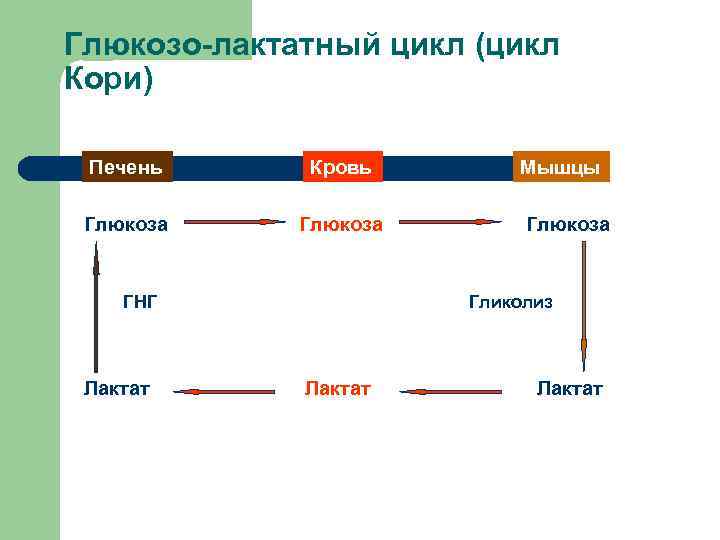
Глюкозо-лактатный цикл (цикл Кори) Печень Кровь Глюкоза ГНГ Лактат Мышцы Глюкоза Гликолиз Лактат
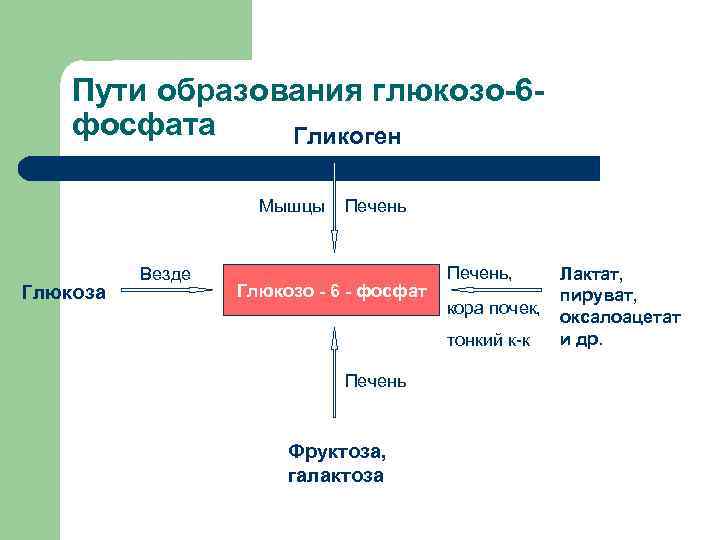
Пути образования глюкозо-6 фосфата Гликоген Мышцы Глюкоза Везде Печень Глюкозо - 6 - фосфат Печень, кора почек, тонкий к-к Печень Фруктоза, галактоза Лактат, пируват, оксалоацетат и др.
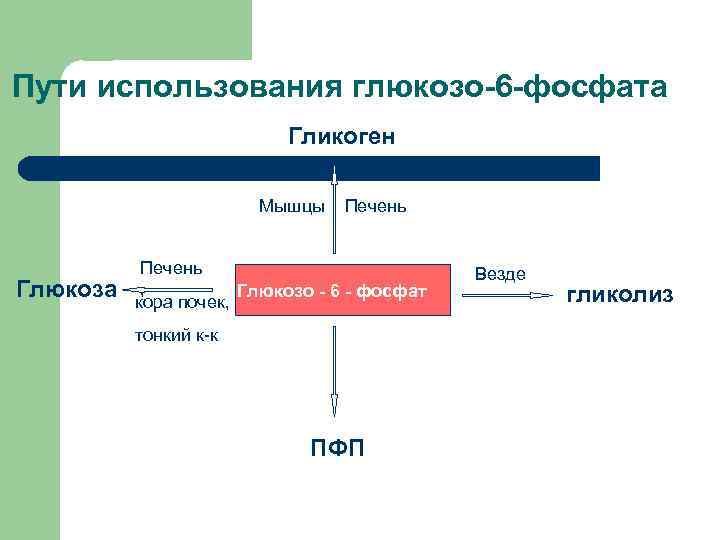
Пути использования глюкозо-6 -фосфата Гликоген Мышцы Глюкоза Печень , Глюкозо - 6 - фосфат кора почек, тонкий к-к ПФП Везде гликолиз

Значение пентозофосфатного пути 1) Амфиболическое –путь распада углеводов и одновременно - образования веществ, используемых в синтетических реакциях (НАДФН и рибозо-5 -фосфата)

Значение пентозофосфатного пути 2) Энергетическое - образующиеся метаболиты окислительной части могут использоваться в гликолизе 3) Синтетическое - связано с использованием рибозо-5 -фосфата и НАДФН

Глюкоза крови Нормальная концентрация глюкозы в крови составляет 3, 3 - 5, 5 ммоль/л Постоянство глюкозы обеспечивается двумя противоположно направленными процессами: - Поставляющими глюкозу в кровь - Использующими глюкозу Повышение концентрации глюкозы в крови (> 9 – 10 ммоль/л), сопровождается глюкозурией

Процессы, поставляющие глюкозу в кровь l Переваривание углеводов в ЖКТ l ГНГ l Распад гликогена печени

Процессы, использующие глюкозу в тканях l Гликолиз l Синтез гликогена l ПФП l Синтез жира

Регуляция глюкозы крови гормонами Гипогликемический гормон (инсулин) 1. 2. 3. Увеличение проницаемости клеточных мембран для глюкозы Ингибирование процессов, поставляющих глюкозу (ГНГ, распад гликогена печени) Активация процессов, использующих глюкозу (гликолиз, синтез гликогена, ПФП, синтез жира)

Регуляция глюкозы крови гормонами Гипергликемические гормоны (глюкагон, КА, ГКС и СТГ) 1. Активация распада гликогена в печени 2. Стимуляция ГНГ

Причины гипергликемии: 1) алиментарная (пищевая) 2) сахарный диабет 3) патология ЦНС (менингит, энцефалит) 4) стресс 5) избыток гипергликемических гормонов 6) повреждение островков поджелудочной железы (панкреатит, кровоизлияния) Невысокая и кратковременная гипергликемия не опасна.

Длительная гипергликемия приводит - К истощению запасов инсулина (что является одной из причин сахарного диабета) - К потере воды тканями, поступлению ее в кровь, увеличению кровяного давления, увеличению диуреза. Гипергликемия в 50 -60 ммоль/л может привести к гиперосмолярной коме.

Длительная гипергликемия Приводит к неферментативному гликозилированию белков - плазмы крови - эритроцитов - кровеносных сосудов - почечных канальцев - нейронов - хрусталика - коллагена

Длительная гипергликемия Гликозилирование изменяет свойства белков и является причиной тяжелых осложнений: тканевых гипоксий склерозирования сосудов катаракты почечной недостаточности нарушения нервной проводимости снижения срока жизни эритроцитов и т. д.

Причины гипогликемии: 1) алиментарная (пищевая) 2) усиленное использование глюкозы (при тяжелой мышечной работе) 3) патология ЖКТ (воспалительные процессы) 4) патология печени 5) патология ЦНС

Причины гипогликемии: 6) недостаток гипергликемических гормонов 7) избыток инсулина (опухоль поджелудочной железы, передозировка инсулина) Гипогликемия очень опасна, так как приводит к гипогликемической коме

Липидный обмен

Функции жиров 1. Энергетическая: при окислении 1 г жира выделяется около 9, 3 ккал энергии 2. Резерв эндогенной воды: при окислении 1 г жира образуется 1, 07 г воды 3. Источник жирорастворимых витаминов 4. Терморегуляторная 5. Защитная
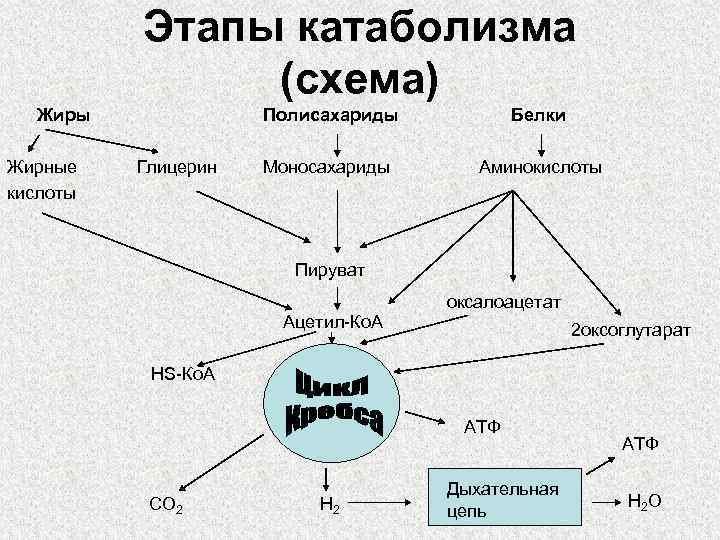
Этапы катаболизма (схема) Жиры Жирные кислоты Полисахариды Глицерин Белки Моносахариды Аминокислоты Пируват оксалоацетат Ацетил-Ко. А 2 оксоглутарат HS-Ко. А АТФ CO 2 H 2 Дыхательная цепь АТФ H 2 O

Роль желчных кислот в переваривании жира 1. Эмульгирование жира 2. Активация панкреатической липазы 3. Необходимы для всасывания продуктов переваривания жира, жирорастворимых витаминов
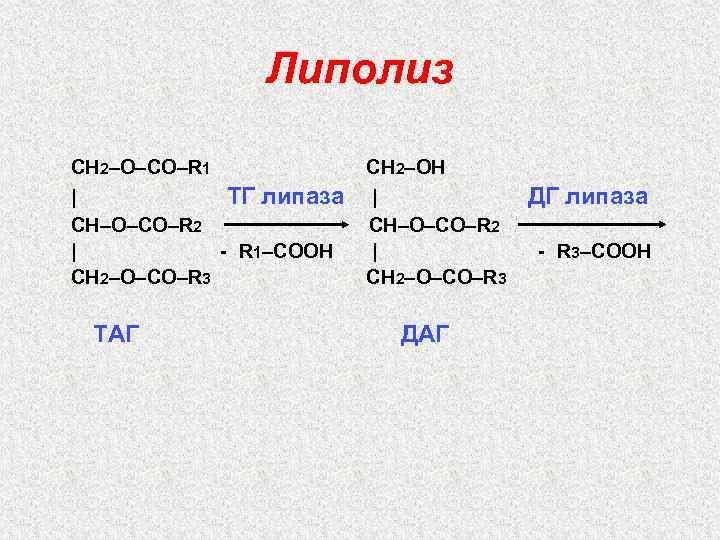
Липолиз СН 2–О–СО–R 1 СН 2–ОН | ТГ липаза CН–О–СО–R 2 | - R 1–CООН СН 2–О–СО–R 3 | CН–О–СО–R 2 | СН 2–О–СО–R 3 ТАГ ДГ липаза - R 3–CООН
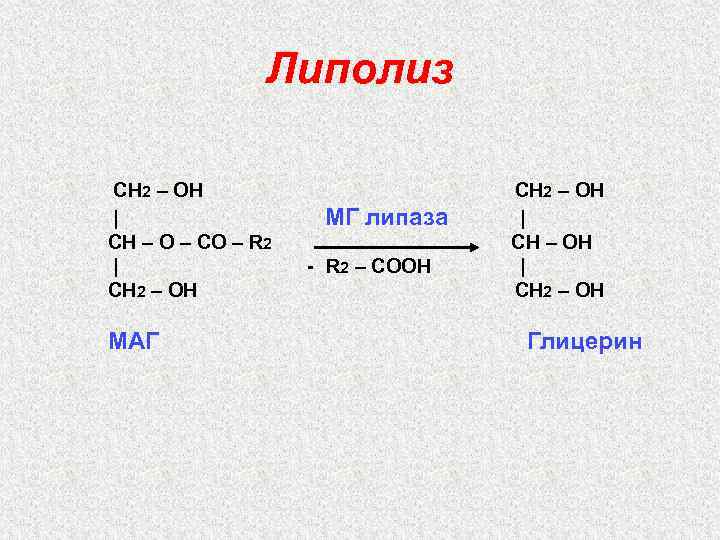
Липолиз CН 2 – ОН | CН – О – СО – R 2 | CН 2 – ОН МАГ МГ липаза - R 2 – CООН CН 2 – ОН | CН 2 – ОН Глицерин

Регуляция липолиза Активаторы: КА, глюкагон, СТГ, АКТГ, тироксин, липотропин гипофиза, ц. АМФ Ингибиторы: инсулин
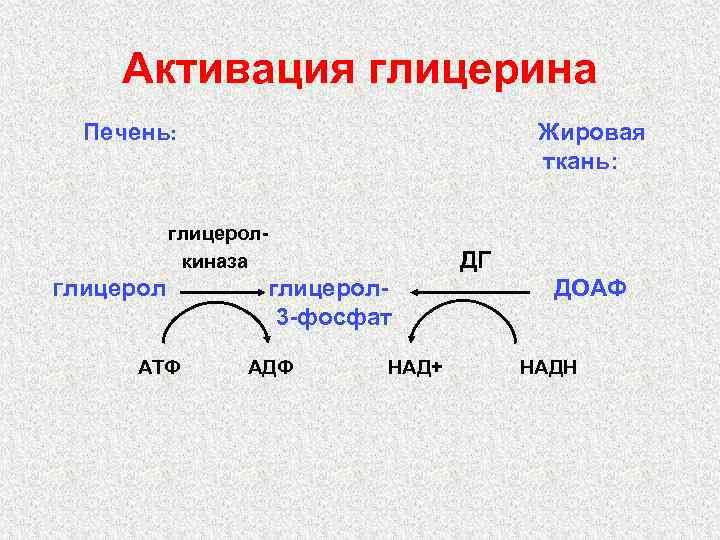
Активация глицерина Печень: Жировая ткань: глицеролкиназа Глицерол АТФ ДГ глицерол 3 -фосфат АДФ НАД+ ДОАФ НАДН
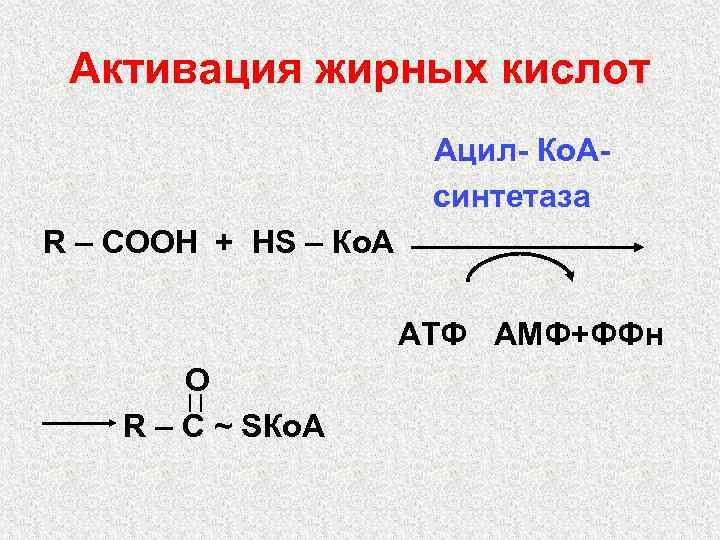
Активация жирных кислот Ацил- Ко. Асинтетаза R – СООН + НS – Ко. А АТФ АМФ+ФФн О R – С ~ SКо. А

Липогенез ацил-Ко. Атрансфераза Глицерол-3 фосфат + 2 ацил-Ко. А - 2 НS-Ко. А Фосфатидная кислота

Липогенез Ацил-Ко. Атрансфераза Фосфатаза + ацил-Ко. А ДАГ - Фн ТАГ - НS-Ко. А

Регуляция липогенеза Активаторы: инсулин, эстрогены и АТФ Ингибиторы : КА, СТГ, ЙТ, АКТГ, АДФ
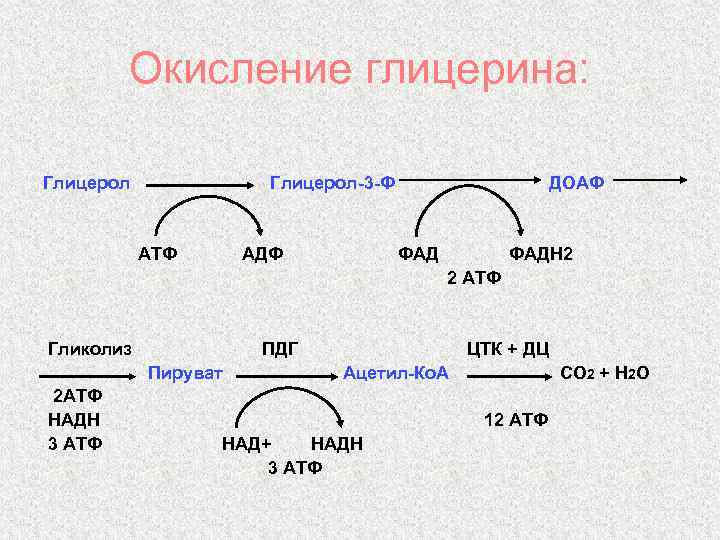
Окисление глицерина: Глицерол-3 -Ф АТФ АДФ ДОАФ ФАДН 2 2 АТФ Гликолиз ПДГ Пируват 2 АТФ НАДН 3 АТФ ЦТК + ДЦ Ацетил-Ко. А СО 2 + Н 2 О 12 АТФ НАД+ НАДН 3 АТФ

Окисление жирных кислот 1. Активация жирных кислот ацил-Ко. Асинтетаза Жирная + НS-Ко. А + АТФ кислота Ацил-Ко. А + АМФ + ФФн
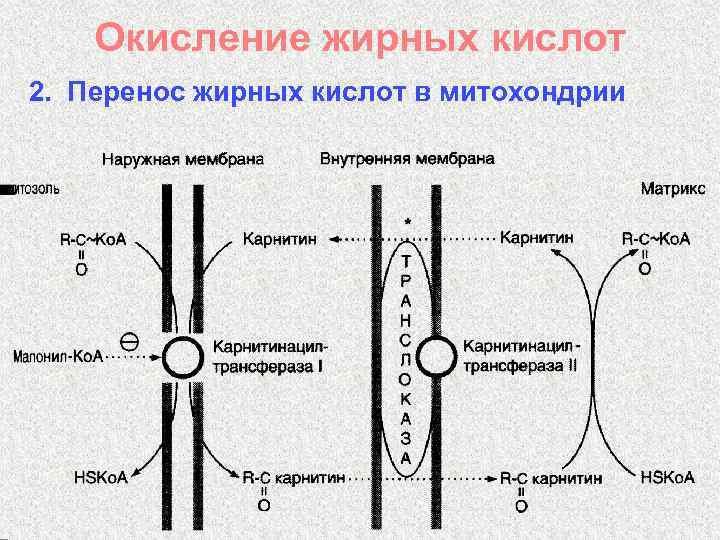
Окисление жирных кислот 2. Перенос жирных кислот в митохондрии
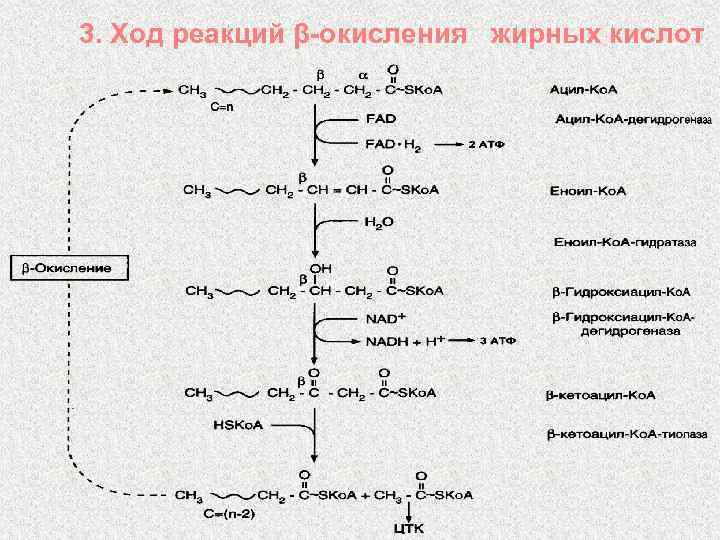
3. Ход реакций β-окисления жирных кислот

Общее уравнение β-окисления пальмитиновой кислоты С 15 Н 31 СО ~ SКо. А + 7 ФАД + 7 НАД+ + 7 НS – Ко. А 8 СН 3 – СО ~ SКо. А + + 7 ФАДН 2 + 7 (НАДН + Н+)

Регуляция β-окисления жирных кислот активаторы: КА, СТГ, глюкагон инргибиторы: инсулин

Пути образования ацетил-Ко. А 1. Из пирувата в ходе ПДГ- реакции 2. β-окисление жирных кислот.

Пути использования ацетил-Ко. А 1. Окисление в цикле Кребса 2. Синтез жирных кислот 3. Синтез холестерина и кетоновых тел

Кетоновые тела Ацетоацетат СН 3 С CH 2 СООН O β- гидроксибутират СН 3 СН OН Ацетон СН 3 С O CH 3 CH 2 СООН

Функции кетоновых тел 1. Энергетическая (скелетная и сердечная мышцы, головной мозг и другие внепеченочные ткани) 2. Кетоновые тела необходимы для образования миелиновых оболочек нервов и белого вещества головного мозга

Кетоз – это накопление кетоновых тел в организме. Сопровождается кетонемией и кетонурией Различают: 1. Физиологический кетоз (голодание, длительная мышечная работа, у новорожденных) 2. Патологический кетоз (сахарный диабет)
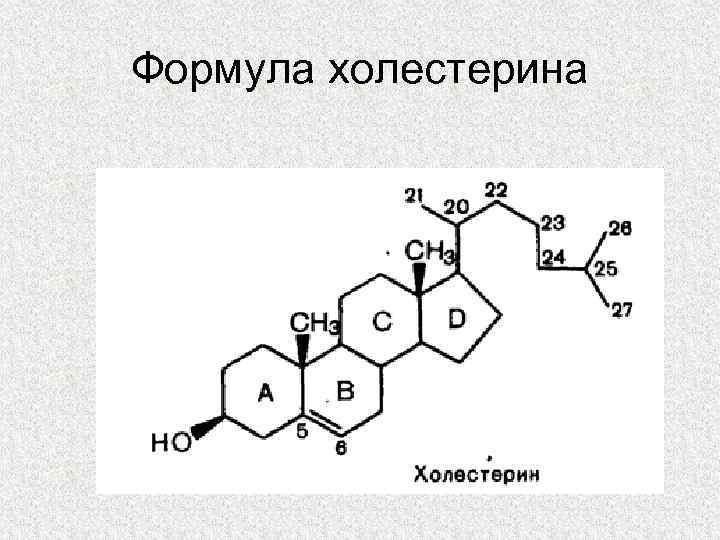
Формула холестерина

Роль холестерина в организме 1. Входит в состав клеточных мембран и обеспечивает их текучесть 2. Синтез желчных кислот в печени 3. Синтез витамина D в коже 4. Синтез стероидных гормонов (половые гормоны, минералокортикоиды, ГКС)

Источники холестерина 1. Пищевые продукты (желток куриного яйца, головной мозг, печень животных, сливочное масло и др. ) 2. Синтез из ацетил-Ко. А : - в печени (50%) - в слизистой тонкого кишечника (15 -20%) - в коже, коре надпочечников, половых железах (30 -35%)

Синтез холестерина • 1 -й этап: • 3 ацетил-Ко. А ГМГ-Ко. А мевалоновая кислота • 2 -й этап: • Мевалоновая кислота сквален • 3 -й этап: • Сквален ланостерин ХС

Регуляция синтеза ХС Активаторы: • КА, СТГ, ГКС, андрогены • насыщенные ЖК • пища, богатая углеводами • стресс • гиподинамия

Регуляция синтеза ХС Ингибиторы: • инсулин, эстрогены • ненасыщенные ЖК • ХС (по принципу отрицательной обратной связи) • желчные кислоты • физическая нагрузка
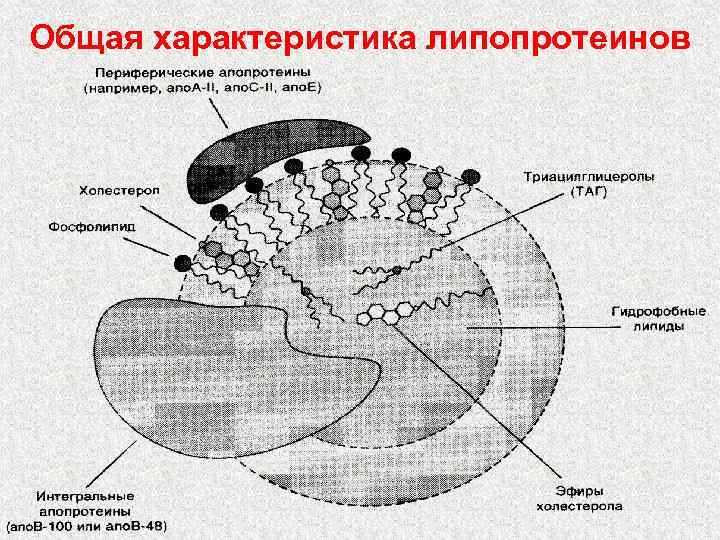
Общая характеристика липопротеинов

Липопротеины Ø хиломикроны (ХМ) Ø Содержат 1 -2% белка и 98 -99% липидов Ø имеют наименьшую плотность Ø Образуются в стенке кишечника Ø Транспортируют пищевые липиды Ø Метаболизируются липопротеинлипазой

Липопротеины пре β-липопротеины (или ЛПОНП) Ø Содержат 10% белка, 90% липидов Ø Образуются в печени и очень мало – в тощем кишечнике Ø Транспортируют эндогенные липиды (в основном жиры) в жировую ткань Ø Частично превращаются в кровяном русле в ЛПНП под действием липопротеинлипазы

Липопротеины β-липопротеины (ЛПНП) Содержат около 25% белка и 75% липидов ØГлавный поставщик ХС в ткани ØНа клеточных мембранах имеются рецепторы для ЛПНП
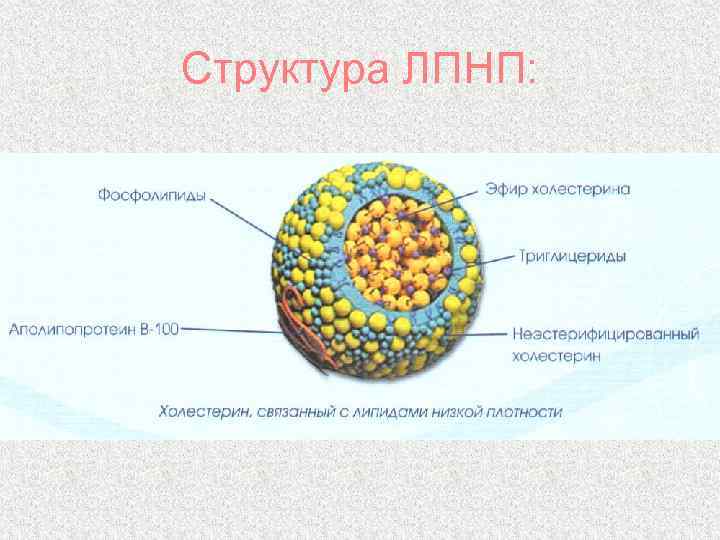
Структура ЛПНП:

Липопротеины α-липопротеины (ЛПВП) Содержат 50% белков, 25% фосфолипидов, 20% эфиров ХС и очень мало триацилглицеринов Ø Образуются главным образом в печени Ø Участвуют в переносе ХС из тканей в печень Ø Содержат лецитинхолестерол-ацилтрансферазу (ЛХАТ) ЛПОНП и ЛПНП считают атерогенными, то есть вызывающими атеросклероз ЛПВП - антитиатерогенными
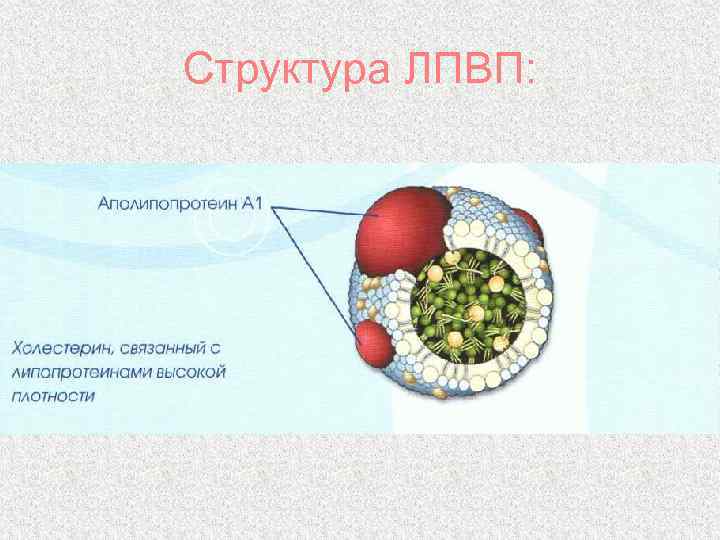
Структура ЛПВП:
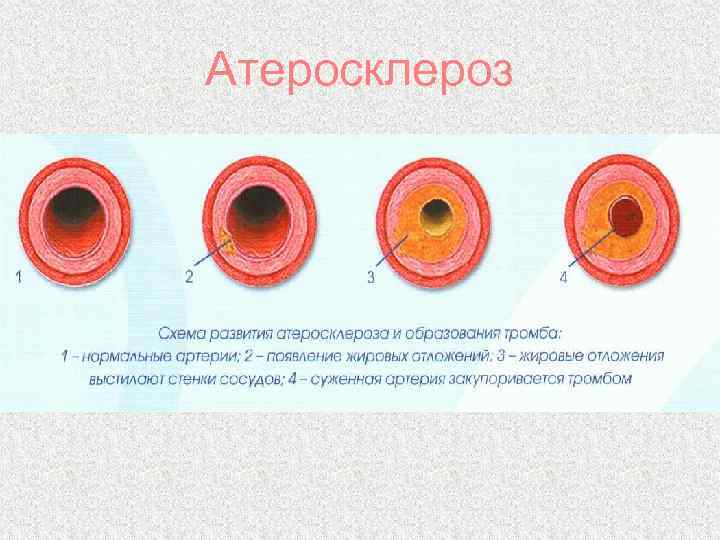
Атеросклероз

Атеросклероз

Механизмы защиты сосудов от атеросклероза 1. Действие липопротеинлипазы в стенке сосуда 2. Наличие ЛПВП в крови

Биохимические причины атеросклероза ü Увеличение атерогенных липопротеинов (ЛПОНП и ЛПНП) ü Снижение антиатерогенных ЛПВП ü Снижение активности липопротеинлипазы ü Снижение количества и/или чувствительности рецепторов к ЛПНП

Факторы риска развития атеросклероза ü Курение ü Стресс ü Переедание (пища, богатая насыщенными ЖК и углеводами)

Факторы риска развития атеросклероза ü Эндокринные факторы: - гипотиреоз - сахарный диабет - андрогены - климакс - гиперфункция гипофиза - гиперфункция надпочечников

Факторы риска развития атеросклероза ü Хронические гипоксии ü Гиподинамия ü Семейно-наследственные факторы

Коэффициент атерогенности Общий ХС – ХС ЛПВП У здоровых людей это соотношение не должно превышать 3 Если выше – имеется риск ИБС

Ожирение – это состояние, когда масса тела превышает 20% от «идеальной» для данного человека Причины первичного ожирения: • Генетические нарушения (до 80% случаев) • Состав и количество потребляемой пищи, метод питания в семье. Переедание • Низкий уровень физической активности • Психологические факторы

Липидозы Ø Болезнь Тея-Сакса (ганглиозидоз) Накопление ганглиозидов в клетках мозга, меньше в других тканях Ø Болезнь Гоше (цереброзидоз) Накопление глюкоцереброзидов в лизосомах печени, селезенки, костного мозга Ø Болезнь Нимана-Пика Накопление лецитинов и сфингомиелинов в лизосомах печени и селезенки

Белковый обмен
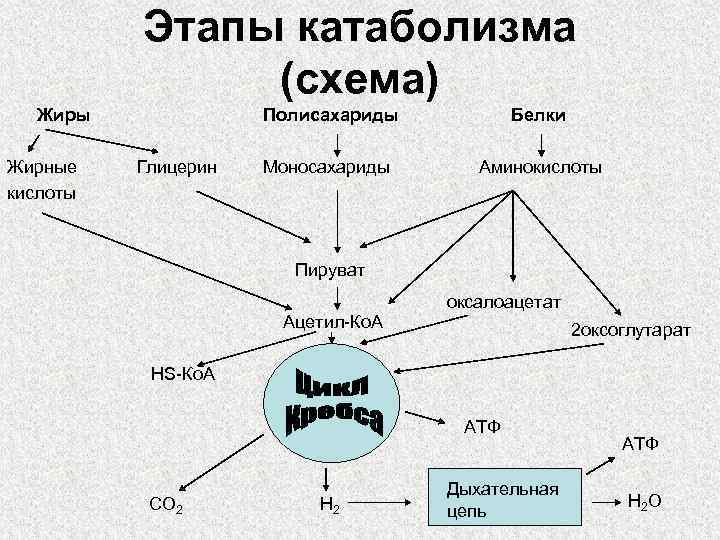
Этапы катаболизма (схема) Жиры Жирные кислоты Полисахариды Глицерин Белки Моносахариды Аминокислоты Пируват оксалоацетат Ацетил-Ко. А 2 оксоглутарат HS-Ко. А АТФ CO 2 H 2 Дыхательная цепь АТФ H 2 O
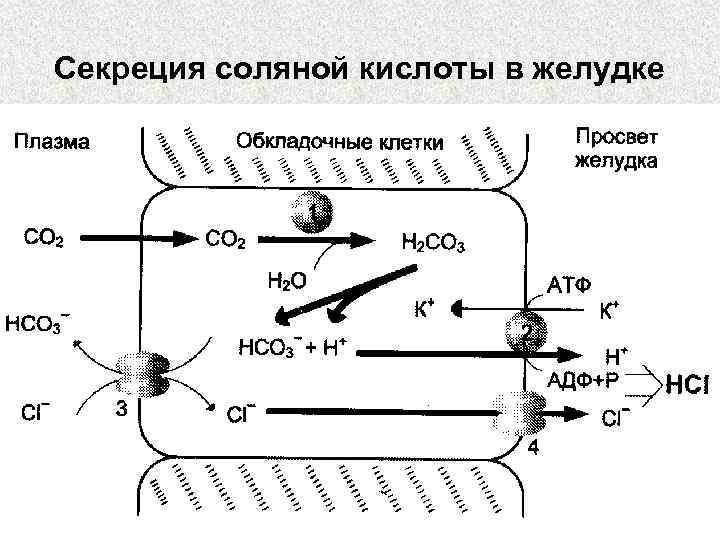
Секреция соляной кислоты в желудке

Роль НСl • • Превращение препепсина в пепсин Оптимум р. Н для работы пепсина Денатурация пищевых белков Бактерицидное действие

Источники аминокислот • • Переваривание пищевых белков в ЖКТ Расщепление клеточных белков лизосомальными пептидазами (катепсинами) Синтез из других аминокислот Образование из безазотистых соединений (кетокислот)

Пути использования аминокислот • Синтез белков • Синтез биологически важных соединений (пуринов, пиримидинов, гормонов, порфиринов и др. ) • Дезаминирование аминокислот с образованием кетокислот
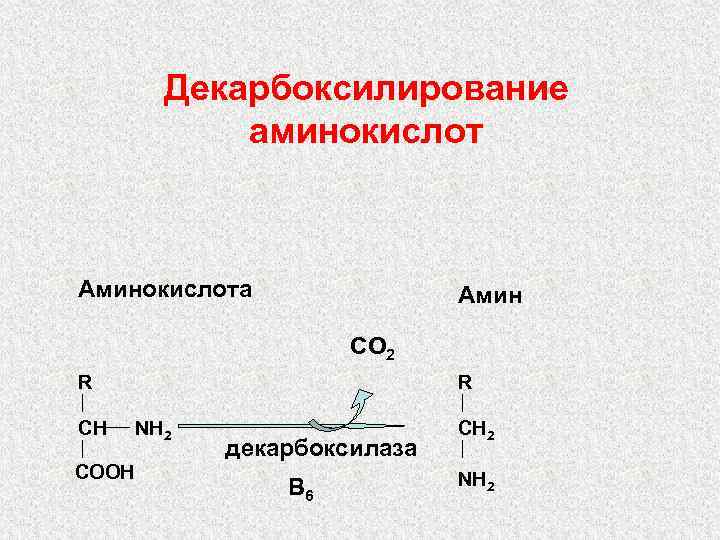
Декарбоксилирование аминокислот Аминокислота Амин CO 2 R CH COOH R NH 2 декарбоксилаза B 6 CH 2 NH 2
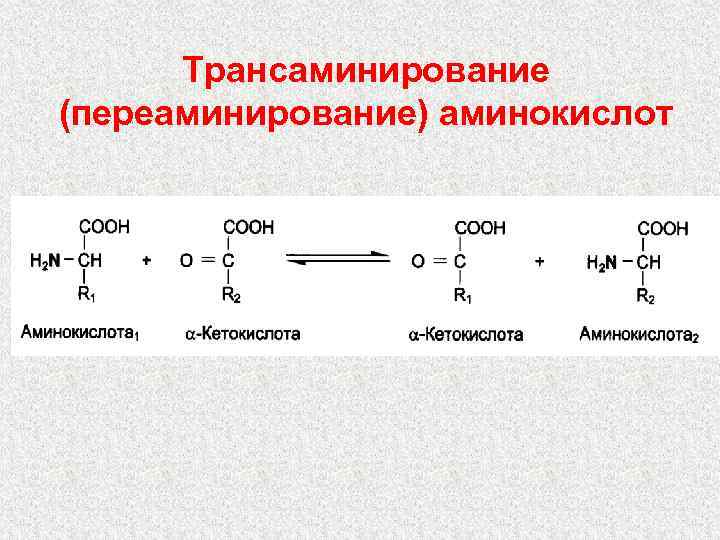
Трансаминирование (переаминирование) аминокислот
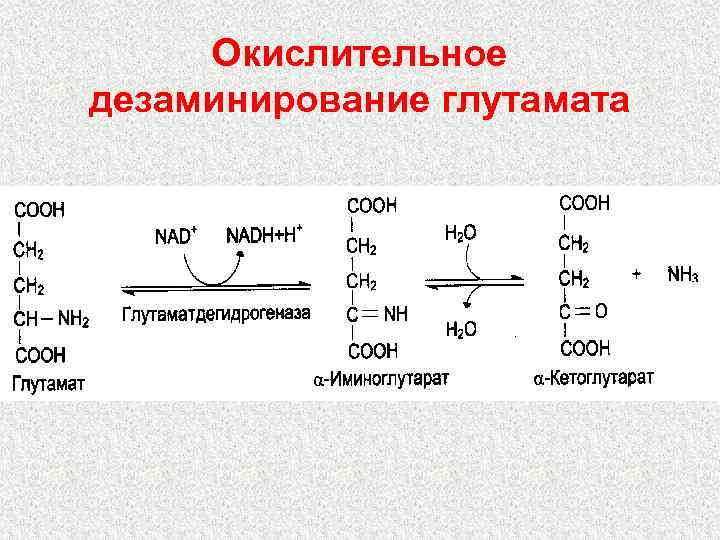
Окислительное дезаминирование глутамата .

Регуляция ГДГ Активаторы: АДФ Ингибиторы: АТФ, НАДН
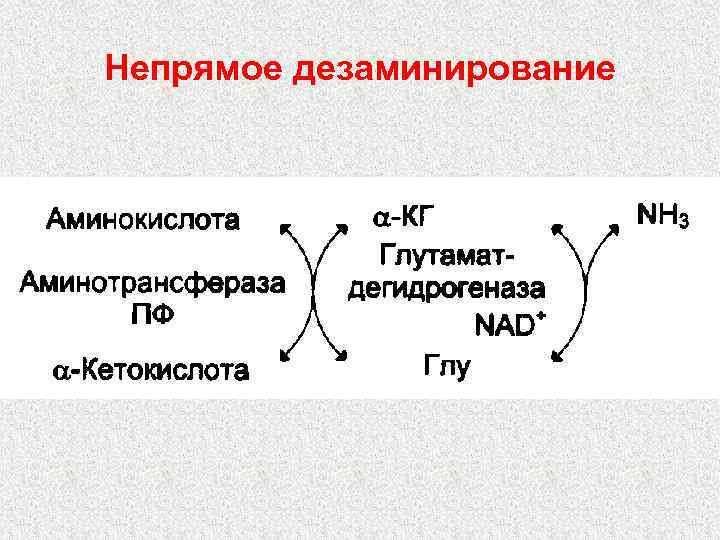
Непрямое дезаминирование

Продукты непрямого дезаминирования: • α-кетокислота, которая может 1) окисляться в цикле Кребса 2) использоваться в ГНГ на синтез глюкозы 3) превращаться в кетоновые тела • • НАДН NН 3
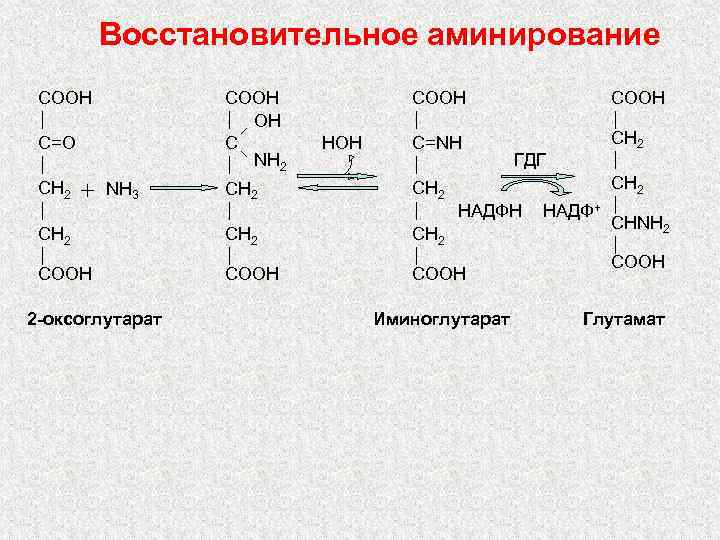
Восстановительное аминирование COOH OH C NH 2 C=O CH 2 COOH HOH COOH C=NH CH 2 CH 2 COOH NH 3 2 -оксоглутарат ГДГ НАДФH Иминоглутарат НАДФ+ CHNH 2 COOH Глутамат

Источники аммиака : 1) • • Реакции дезаминирования аминокислот биогенных аминов (ГА, СТ, КА и др. ) пуриновых и пиримидиновых азотистых оснований амидов (глутамина, аспарагина) 2) Образование в кишечнике в результате деятельности микрофлоры (гниение белков) всасывается в кровь воротной вены

Причины токсичности аммиака 1) Легко проникает через клеточные мембраны 2) Связывается с 2 -оксоглутаратом, угнетает обмен аминокислот (переаминирование) и цикл Кребса 3) Усиливает синтез глутамина из глутамата в нервной ткани. В результате снижается синтез ГАМК , что нарушает проведение нервного импульса и вызывает судороги

Причины токсичности аммиака 4) Накопление иона NH 4+ нарушает трансмембранный перенос ионов Na+ и К+, что влияет на проведение нервного импульса 5) Сдвиг р. Н в щелочную сторону метаболический алкалоз

Обезвреживание аммиака 1. Восстановительное аминирование 2. Образование амидов (глутамина и аспарагина) 3. Образование аланина в мышцах 4. Синтез мочевины в печени

Суммарное уравнение синтеза мочевины: CO 2 + NH 3 + Аспартат + 3 АТФ + 2 H 2 O = Мочевина + Фумарат + 2(АДФ + H 3 PO 4) + АМФ + H 4 P 2 O 7

Классификация аминокислот по судьбе безазотистого остатка
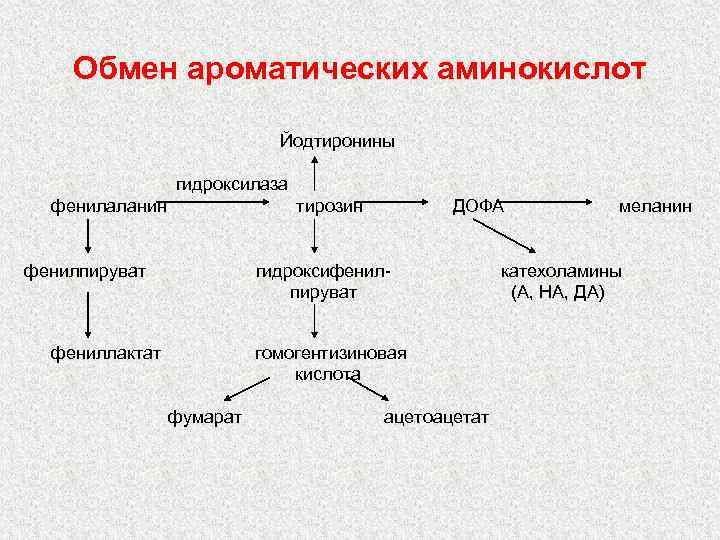
Обмен ароматических аминокислот Йодтиронины гидроксилаза фенилаланин тирозин фенилпируват ДОФА гидроксифенилпируват фениллактат гомогентизиновая кислота фумарат ацетоацетат меланин катехоламины (А, НА, ДА)

Биологическая роль креатина В мышцах: В покоящейся мышце Креатинкиназа Креатин + АТФ Креатинфосфат + АДФ В работающей мышце
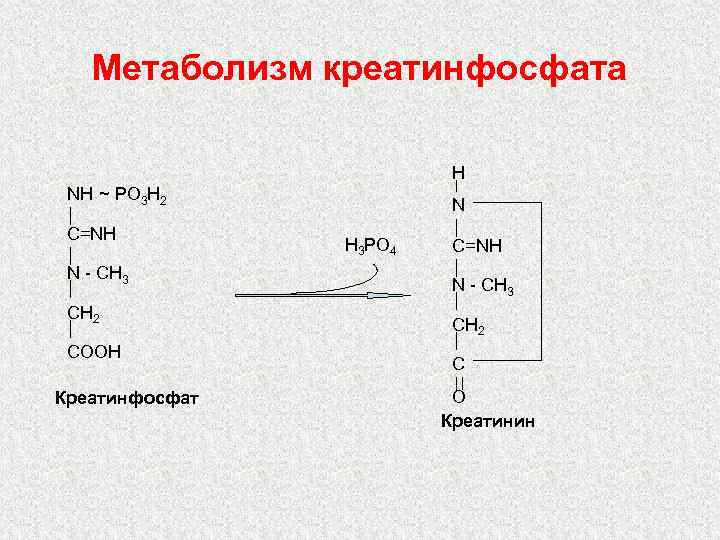
Метаболизм креатинфосфата H NH ~ PO 3 H 2 C=NH N - CH 3 CH 2 COOH Креатинфосфат N H 3 PO 4 C=NH N - CH 3 CH 2 C O Креатинин

Диагностическое значение: Креатинин мочи Клиренс = ------------- х диурез (мин) Креатинин крови

Диагностическое значение: Определение активности КК и ее изоферментов в крови используется для диагностики инфаркта миокарда, миопатий, мышечных дистрофий и др.

Азотистый обмен
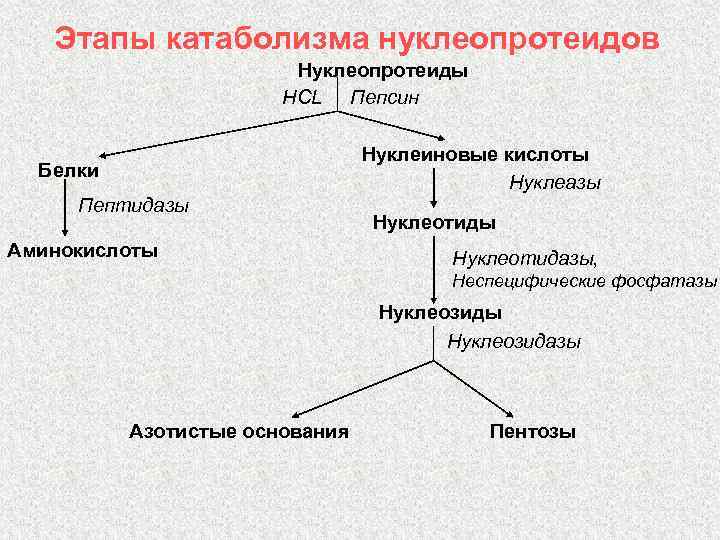
Этапы катаболизма нуклеопротеидов Нуклеопротеиды HCL Пепсин Нуклеиновые кислоты Нуклеазы Белки Пептидазы Аминокислоты Нуклеотидазы, Неспецифические фосфатазы Нуклеозидазы Азотистые основания Пентозы
Подагра
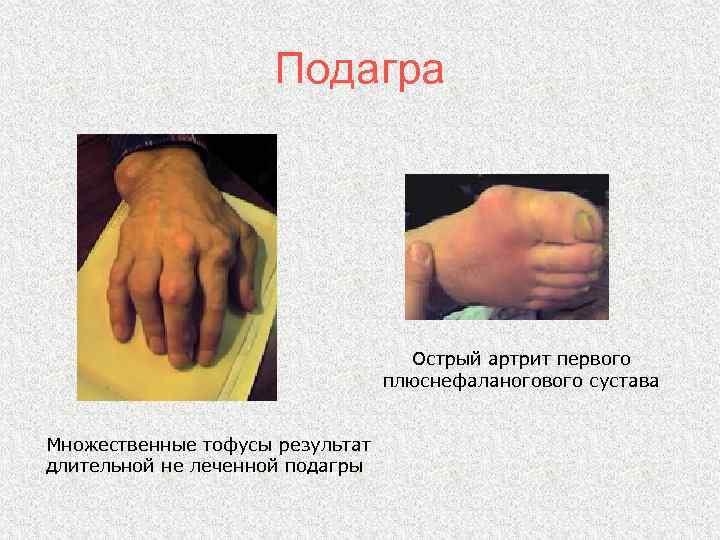
Подагра Острый артрит первого плюснефаланогового сустава Множественные тофусы результат длительной не леченной подагры
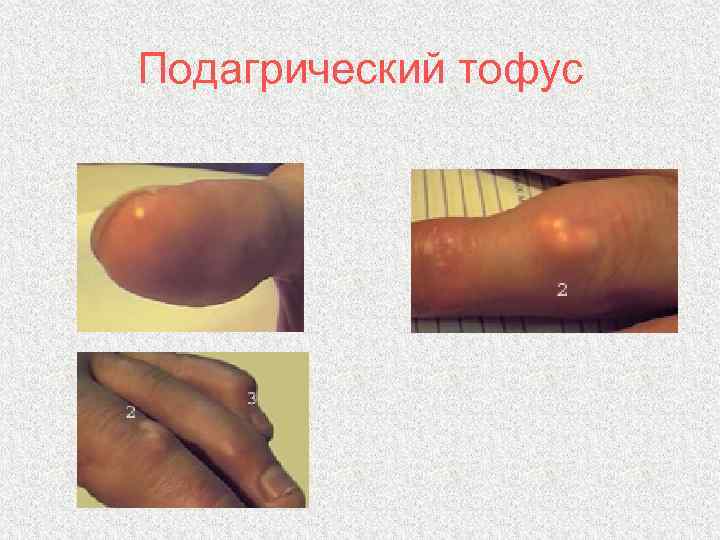
Подагрический тофус

ХРОМОПРОТЕИДЫ – сложные белки, небелковой частью которых являются окрашенные вещества • • • ФЛАВОПРОТЕИДЫ ГЕМПРОТЕИДЫ РОДОПСИН И ЙОДОПСИН ХЛОРОФИЛЛ КОБАМИДНЫЕ ФЕРМЕНТЫ
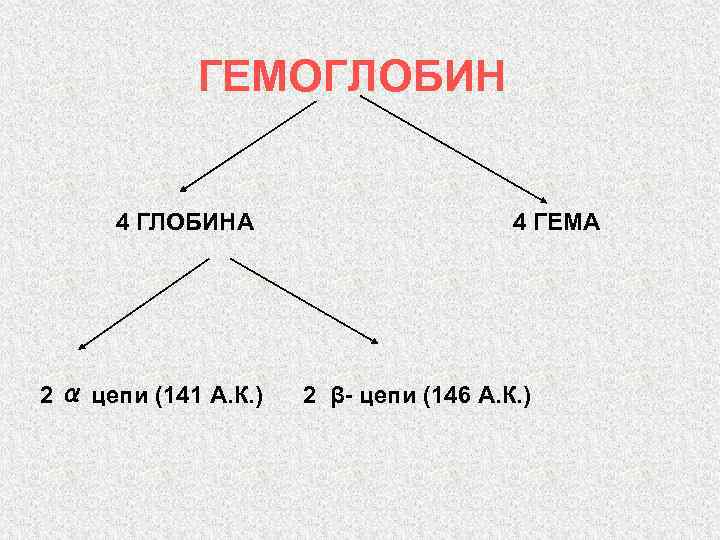
ГЕМОГЛОБИН 4 ГЛОБИНА 2 α цепи (141 А. К. ) 4 ГЕМА 2 β- цепи (146 А. К. )
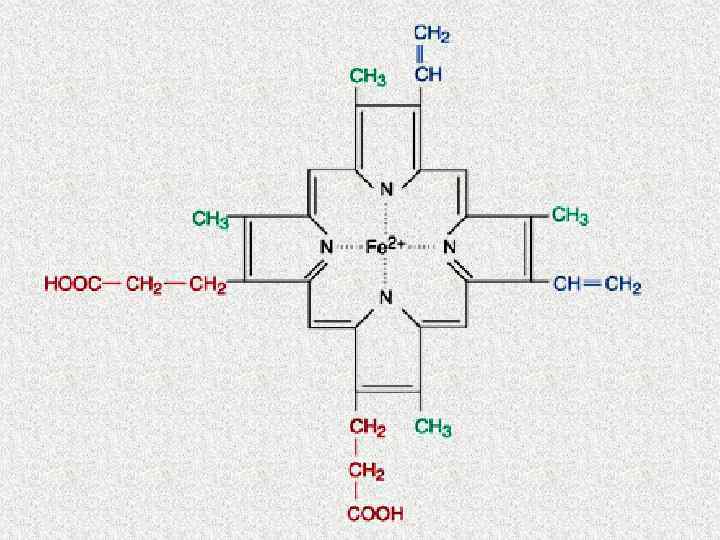
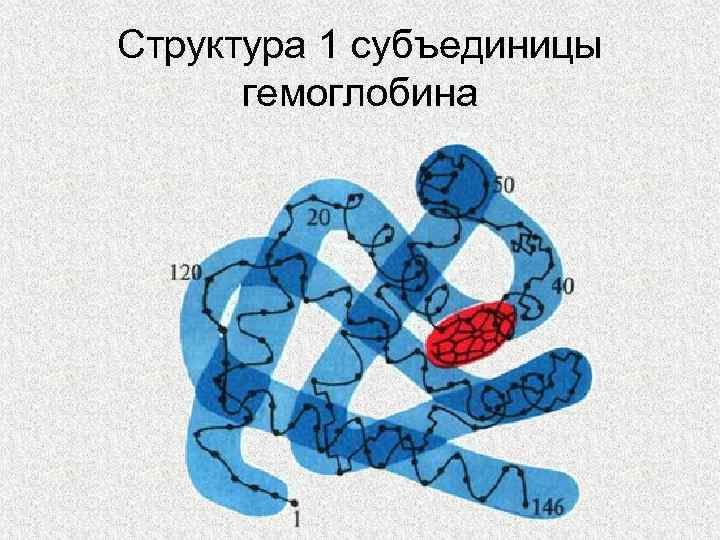
Структура 1 субъединицы гемоглобина

ДЛЯ СИНТЕЗА ГЕМА ТРЕБУЕТСЯ: Ø ГЛИЦИН Ø СУКЦИНИЛ-Ко. А Ø ВИТАМИНЫ В , В (ФОЛИЕВАЯ 6 Ø КИСЛОТА) Fe 2+ 12 9
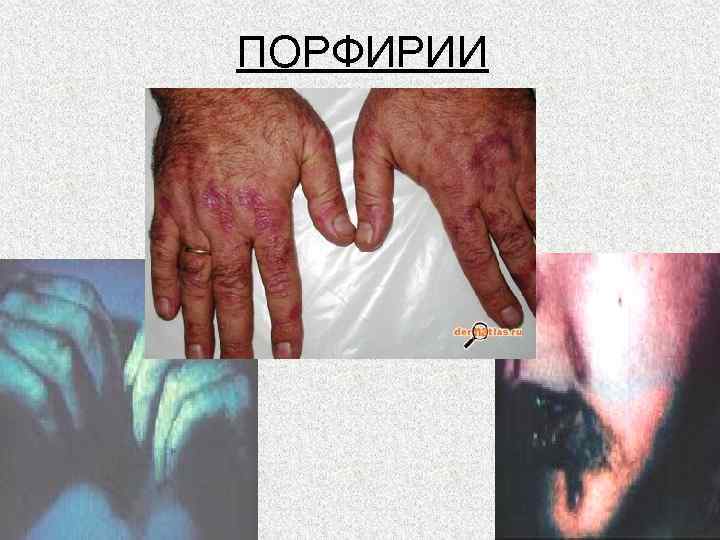
ПОРФИРИИ
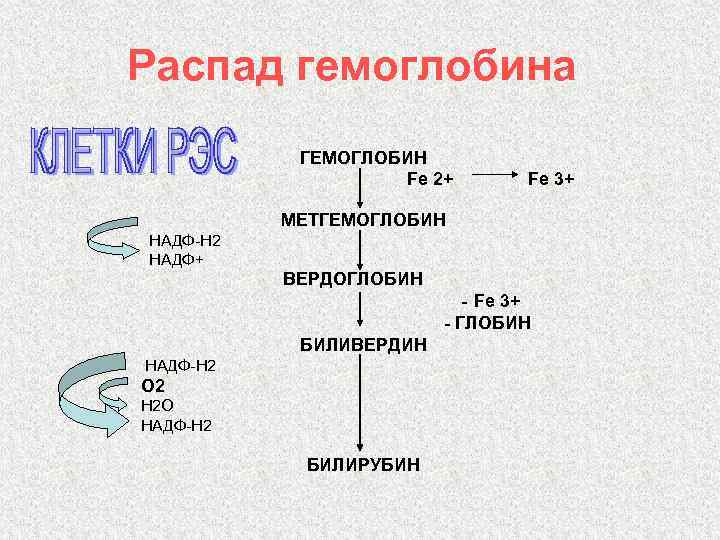
Распад гемоглобина ГЕМОГЛОБИН Fe 2+ Fe 3+ МЕТГЕМОГЛОБИН НАДФ-Н 2 НАДФ+ ВЕРДОГЛОБИН - Fe 3+ - ГЛОБИН БИЛИВЕРДИН НАДФ-Н 2 О 2 Н 2 О НАДФ-Н 2 БИЛИРУБИН

Распад гемоглобина БИЛИРУБИН УДФ-ГЛЮКУРОНИЛ ТРАНСФЕРАЗА БИЛИРУБИНГЛЮКУРОНИД - ГЛЮКУРОНОВАЯ КИСЛОТА БИЛИРУБИН

Распад гемоглобина БИЛИРУБИН МЕЗОБИЛИРУБИНОГЕН (УРОБИЛИНОГЕН) СТЕРКОБИЛИНОГЕН СТЕРКОБИЛИН (ФЕКАЛИИ)

ФОРМЫ БИЛИРУБИНА: СВОБОДНЫЙ БИЛИРУБИН (несвязанный, неконъюгированный, непрямой): — Не дает прямой реакции с реактивом Эрлиха — Не растворим в воде — Высоко токсичен — Не проходит через мембраны — В крови свободного билирубина – 75%

СВЯЗАННЫЙ БИЛИРУБИН (конъюгированный, прямой) — Дает прямую реакцию с реактивом Эрлиха — Мало токсичен — Растворим в воде — Легко проходит через мембраны — В крови связанного билирубина – 25%
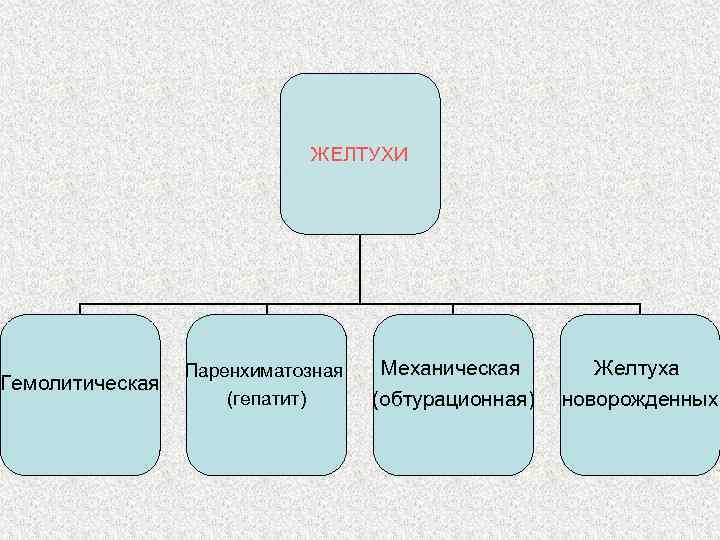
ЖЕЛТУХИ Гемолитическая Паренхиматозная (гепатит) Механическая (обтурационная) Желтуха новорожденных

БЕЛКИ ПЛАЗМЫ КРОВИ • альбумины 42 г/л - 57% • глобулины 31 г/л - 42% • фибриноген 3 г/л - 1%

Фракции глобулинов • α 1 -глобулины 3% 3 г/л • α 2 -глобулины 9% 6 г/л • β- глобулины 13% 9 г/л • γ -глобулины 16% 15 г/л

Функции альбуминов: • Поддержание онкотического давления • Транспорт НЭЖК, билирубина, холестерина, некоторых гормонов, лекарств • Резерв аминокислот

Нарушения белкового состава крови Гиперпротеинемия – увеличение концентрации белка в крови (почти всегда связана с гиперглобулинемией): • относительная (при дегидратации) • абсолютая (при активации иммунного ответа, миелопролиферативных заболеваниях)

Нарушения белкового состава крови Гипопротеинемия – понижение концентрации белка в крови (почти всегда связана с гипоальбуминемией) – возникает при нефротическом синдроме, печеночно-клеточной недостаточности, голодании, ожоговой болезни, патологии ЖКТ

Нарушения белкового состава крови Диспротеинемия – изменение соотношения различных фракций белков плазмы крови Парапротеинемия – появление аномальных форм белков, например, специфических белков при миеломной болезни, представляющих собой цепи иммуноглобулинов

Отдельные белки крови: • Белки-ферменты • Белки-переносчики • Белки-ингибиторы ферментов

Белки-переносчики 1) 2) 3) 4) 5) Церулоплазмин Трансферрин Гаптоглобин Преальбумин Специфический гликопротеид беременных

Белки –ингибиторы ферментов • α 1 - антитрипсин • α 2 - макроглобулин • Интер- α-трипсиновый ингибитор

Белки острой фазы 1. 2. 3. 4. 5. 6. Гаптоглобин Церулоплазмин Трансферрин С- реактивный белок Интерферон Фибриноген

Белки острой фазы • С- реактивный белок

Фракции остаточного азота Мочевина - 50% Аминокислоты - 25% Эрготионеин - 8% Мочевая кислота - 4% Креатин – 5% Креатинин - 2, 5% Аммиак – 0, 2% Индикан – 0, 3% Прочие – 5%
Гиперазотемиии ретенционная почечная продукционная внепочечная
Обмен в-в (4 часа) для фарм заоч. (2).ppt