Липиды(Г.Н.Рыжикова).ppt
- Количество слайдов: 33

Обмен липидов
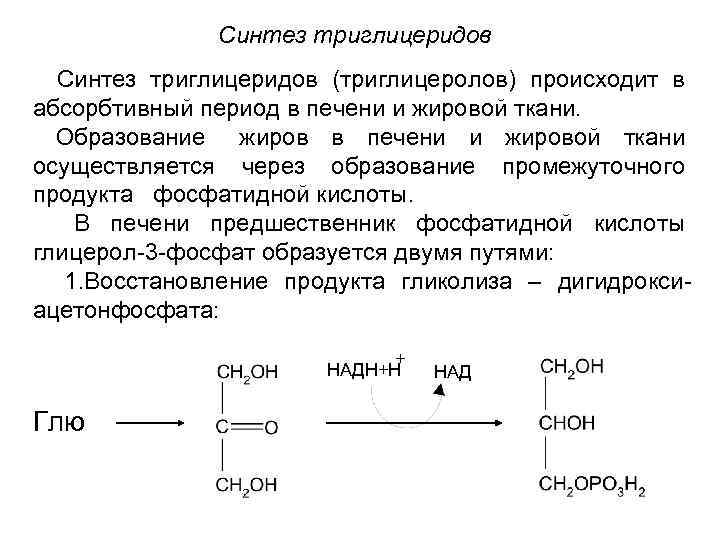
Синтез триглицеридов (триглицеролов) происходит в абсорбтивный период в печени и жировой ткани. Образование жиров в печени и жировой ткани осуществляется через образование промежуточного продукта фосфатидной кислоты. В печени предшественник фосфатидной кислоты глицерол-3 -фосфат образуется двумя путями: 1. Восстановление продукта гликолиза – дигидроксиацетонфосфата: + НАДН+Н Глю НАД
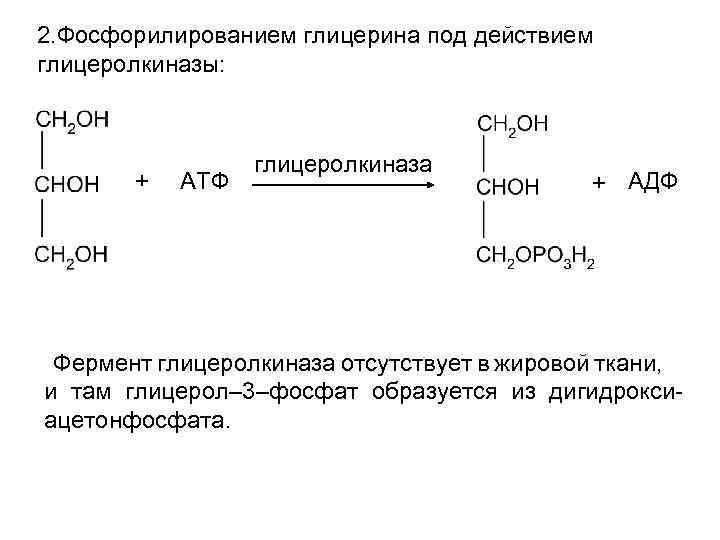
2. Фосфорилированием глицерина под действием глицеролкиназы: + АТФ глицеролкиназа + АДФ Фермент глицеролкиназа отсутствует в жировой ткани, и там глицерол– 3–фосфат образуется из дигидроксиацетонфосфата.

Синтез жиров в жировой ткани В жировой ткани для синтеза жиров используются в основном жирные кислоты, освободившиеся при гидролизе жиров хиломикроны и липопротеиды очень низкой плотности. Жирные кислоты поступают в адипоциты, превращаются в ацил-Ко. А и взаимодействуют с глицерол-3 -фосфатом, образуя лизофосфатидную кислоту, затем фосфатидную. Фосфатидная кислота после дефосфорилирования превращается в диацилглицерол, который ацилируется с образованием триацилглицерола. В жировой ткани синтез жирных кислот происходит из продуктов распада глюкозы. В адипоцитах распад глюкозы идет 2 путями: 1. Гликолиз, обеспечивающий образование глицерол-3 -ф; 2. Пентозофосфатный путь – поставляющий НАДФН, служащий донором водорода в синтезе жирных кислот.
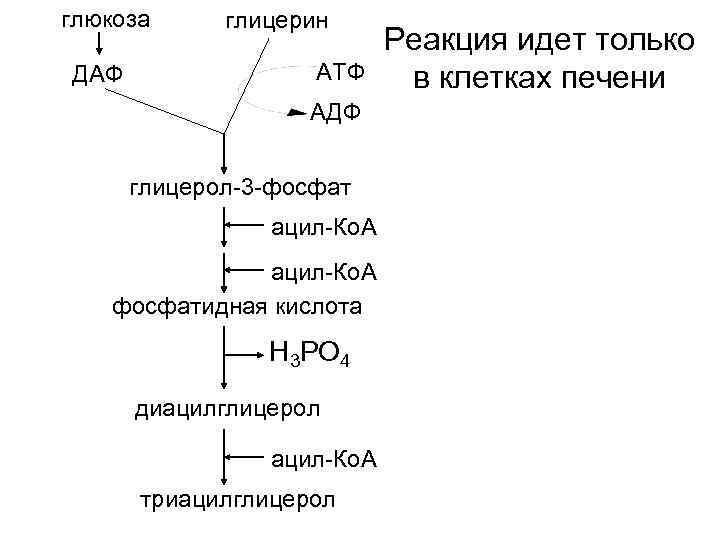
глюкоза ДАФ глицерин АТФ АДФ глицерол-3 -фосфат ацил-Ко. А фосфатидная кислота Н 3 РО 4 диацилглицерол ацил-Ко. А триацилглицерол Реакция идет только в клетках печени

Мобилизация жиров из жировой ткани Мобилизация жиров, т. е. гидролиз до глицерола и жирных кислот, происходит в постабсорбтивный период, при голодании и активной физической работе. Гидролиз внутриклеточного жира идет при участии фермента триацилглицероллипазы. Глицерин как водорастворимое вещество транспортируется кровью в свободном виде, а жирные кислоты (гидрофобные молекулы) в комплексе с белком плазмы – альбумином. Жирные кислоты как источник энергии окисляются в постабсорбтивный период, при голодании и физической работе. В их состояниях концентрация жирных кислот в крови увеличивается в результате их мобилизации из жировых депо, и они активно окисляются печенью, мышцами и др. тканями. При голодании часть жирных кислот в печени превращается в кетоновые тела, которые используются нервной тканью как источник энергии.

β - окисление β-окисление – специфический путь катаболизма жирных кислот, при котором от карбоксильного конца жирной кислоты последовательно определяется по 2 атома углерода в виде ацетил-Ко. А. β-окисление идет в митохондриях и происходит только в аэробных условиях. Активация жирных кислот RCOOH + HSKo. A + АТФ RCOSKo. A + АМФ + РР 1 Реакцию катализирует ацил-Ко. А-синтетаза. Активация жирных кислот (С 12 -С 20) происходит при участии ацил-Ко. Асинтетазы, которая расположена на внешней мембране митохондрий. Жирные кислоты переносятся через внутреннюю мембрану митохондрий с помощью карнитина. Затем комплекс ацил-Ко. А-карнитин распадается и свободный карнитин возвращается на цитозольную сторону внутренней мембраны митохондрий
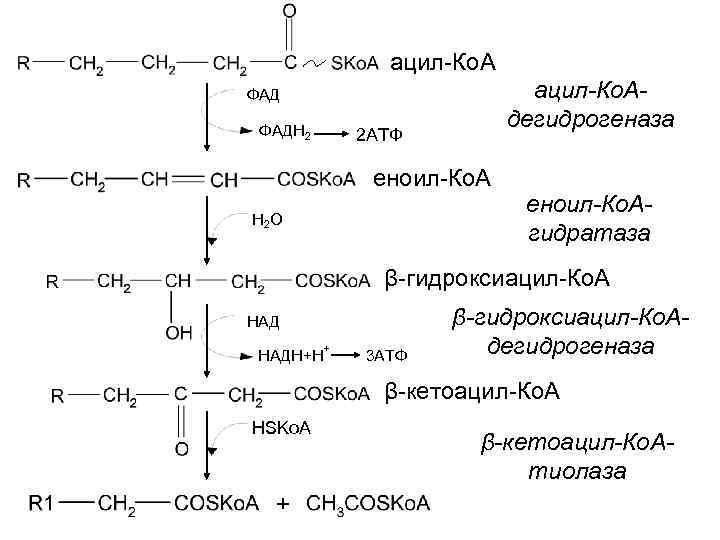
ацил-Ко. Адегидрогеназа ФАДН 2 2 АТФ еноил-Ко. А Н 2 О еноил-Ко. Агидратаза β-гидроксиацил-Ко. А НАДН+Н + 3 АТФ β-гидроксиацил-Ко. Адегидрогеназа β-кетоацил-Ко. А HSKo. A + β-кетоацил-Ко. Атиолаза

Биосинтез жирных кислот Значительная часть заменимых жирных кислот синтезируется в печени, в меньшей степени в жировой ткани и лактирующей молочной железе. Источником для синтеза жирных кислот служит ацетил. Ко. А, образующийся при распаде глюкозы. Таким образом, избыток углеводов, поступающих в организм, превращается в жирные кислоты, а затем в жиры. Синтез пальмитиновой кислоты Синтез жирных кислот происходит в цитоплазме. Ацетил -Ко. А взаимодействует с оксалоацетатом, и образовавшийся цитрат из митохондрий поступает в цитоплазму, где распадается под действием фермента цитратлиазы на ацетил-Ко. А и оксалоацетат.

Первая реакция синтеза жирных кислот – превращение ацетил-Ко. А в малонил-Ко. А. Реакцию катализирует биотинзависимый фермент ацетил-Ко. А-карбоксилаза: CH 3 COSKo. A + CO 2 + АТФ витамин Н HOOC CH 2 COSKo. A После образования малонил-Ко. А синтез жирных кислот идет на мультиферментном комплексе – синтазе жирных кислот (пальметоил-синтетазе). Этот фермент состоит из 2 протомеров и последовательно удлиняет радикал жирной кислоты на 2 углеродных атома, донором которых служит малонил-Ко. А.

1 -я реакция – перенос ацетил-Ко. А на ацилпереносящий белок. Затем на ацилпереносящий белок переносится малонил-Ко. А. Затем от малонил-Ко. А отделяется СО 2 и ацетильная группа конденсируется с остатком малонила по месту отделившейся СО 2. Образовавшийся радикал ацетоацетила последовательно восстанавливается кетоацилредуктазой, затем дегидратируется и опять восстанавливается еноил-редуктазой. В результате образуется радикал бутирила, связанный с субъединицей синтазы жирных кислот. Реакции цикла повторяются до тех пор, пока не образуется радикал пальмитиновой кислоты.
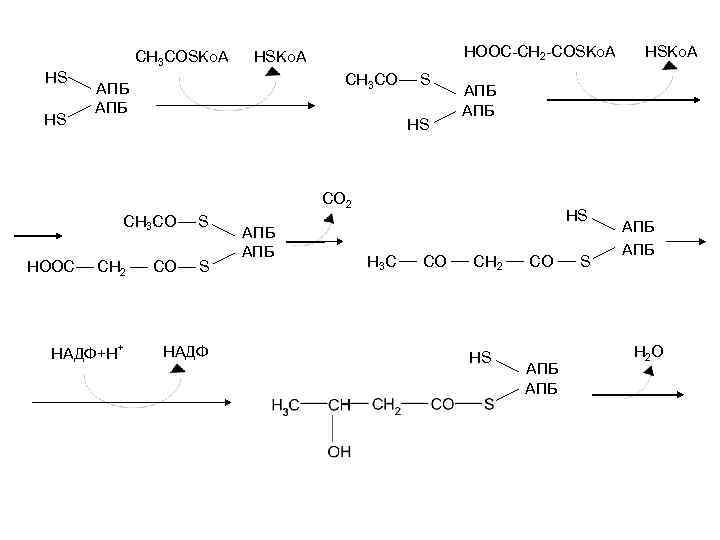
CH 3 COSKo. A HS HS HOOC-CH 2 -COSKo. A HSKo. A CH 3 CO АПБ S HS АПБ CO 2 CH 3 CO HOOC CH 2 НАДФ+Н + CO S S НАДФ АПБ HS H 3 C CО HSKo. A CH 2 HS CO АПБ S АПБ Н 2 О
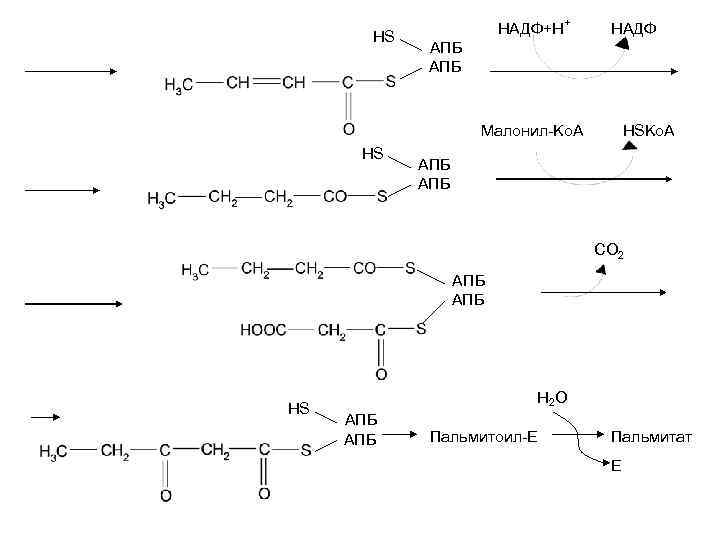
HS НАДФ+Н + НАДФ АПБ HSKo. A Малонил-Ko. А HS АПБ CO 2 АПБ HS Н 2 О АПБ Пальмитоил-Е Пальмитат Е

Окисление ненасыщенных жирных кислот Около половины жирных кислот в организме человека ненасыщенные. β-окисление этих кислот идет обычным путем до тех пор, пока двойная связь не окажется между третьим и четвертым атомами углерода. Затем фермент еноил-Ко. А-изомераза перемещает двойную связь из положения 3 -4 в положение 2 -3 и изменяет цисконформацию двойной связи в транс-, которая требуется для β-окисления. В этом цикле β-окисления первая реакция дегидрирования не происходит, т. к. двойная связь в радикале жирной кислоты уже имеется. Далее циклы β-окисления продолжаются, не отличаясь от обычного пути.
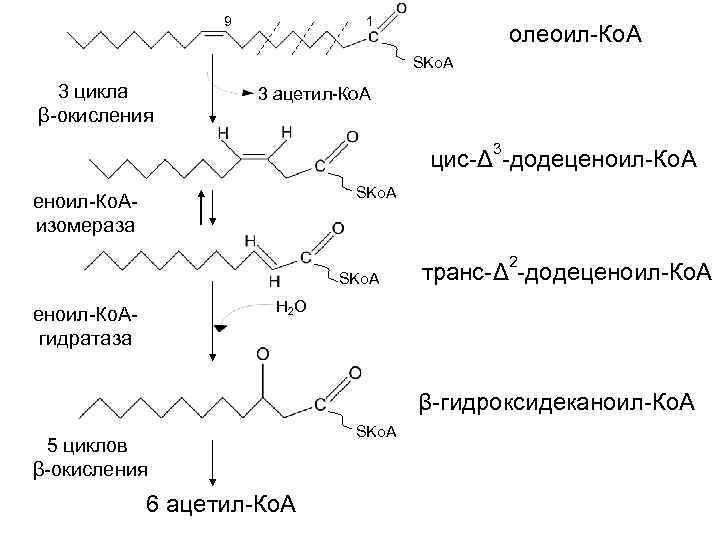
9 1 олеоил-Ко. А SKo. A 3 цикла β-окисления 3 ацетил-Ко. А 3 цис-Δ -додеценоил-Ко. А SKo. A еноил-Ко. Аизомераза SKo. A 2 транс-Δ -додеценоил-Ко. А Н 2 О еноил-Ко. Агидратаза β-гидроксидеканоил-Ко. А 5 циклов β-окисления 6 ацетил-Ко. А SKo. A

В жировой ткани обмен углеводов тесно связан с обменом жиров. В жировой ткани происходит гликолиз, который дает диоксиацетонфосфат. Диоксиацетонфосфат превращается в глицерол-3 -фосфат. Глицерол-3 -фосфат идет на синтез триглицеридов. В жировой ткани идет пентозофосфатный путь окисления глюкозы с образованием НАДФН 2, а также образуется ацетил-Ко. А в результате гликолиза, что обеспечивает синтез жирных кислот. В адипоцитах содержатся жирные кислоты, которые образовались в результате гидролиза триглицеридов ХМ и ЛПОНП, а также жирные кислоты, которые синтезированы в адипоцитах. Жирные кислоты в адипоцитах превращаются в ацил-Ко. А и взаимодействуют с глицерол-3 -фосфатом с образованием триглицеридов. Синтез жиров в адипоцитах идет только, когда глюкоза поступает в адипоциты.

Регуляция обмена липидов Уровень жирных кислот в крови колеблется в очень широких пределах и может повышаться на 400 -500%. Регуляция обмена липидов на уровне гепатоцита Процессы окисления и синтеза жирных кислот в клетке протекают в различных компартментах. Окисление жирных кислот протекает в митохондриях, а синтез жирных кислот идет в цитоплазме. Интенсивность синтеза и окисления жирных кислот зависит от концентрации глюкозы. При поступлении в организм большого количества глюкозы происходит образование пирувата, который превращается в ацетил-Ко. А. Ацетил-Ко. А взаимодействует со ЩУК с образованием цитрата. Цитрат активизирует ацетил-Ко. А-карбоксилазу, в результате ускоряется образование малонил-Ко. А и начинается синтез жирных кислот.

Накопление малонил-Ко. А ингибирует ацилкарнитинтрансферазу и прекращается поступление жирных кислот в митохондрии, т. е. тормозится окисление жирных кислот. Следовательно, если идет синтез жирных кислот, то процесс окисления жирных кислот тормозится и наоборот. При избытке глюкозы ускоряется пентозофосфатный путь окисления глюкозы, что приводит к окислению НАДФН 2 и, следовательно, ускоряется синтез жирных кислот. Все синтетические процессы требуют затраты АТФ. Следовательно, если в клетке много АТФ, то синтез жирных кислот ускоряется. Синтез жирных кислот активируют глюкоза, цитрат, АТФ, НАДФН 2. Окисление жирных кислот тормозят малонил-Ко. А, ацил. Ко. А, цитрат.

1. Цитрат ускоряет превращение ацетил-Ко. А в малонил-Ко. А 2. Малонил-Ко. А блокирует образование ацилкарнитина. карнитин Ацил-Ко. А - Ацилкарнитин малонил-Ко. А ацил-Ко. А цитрат При недостатке глюкозы прекращается: А) синтез жирных кислот; Б) использование глюкозы как источника энергии; При недостатке глюкозы ускоряется процесс окисления жирных кислот, и они используются как источник энергии.
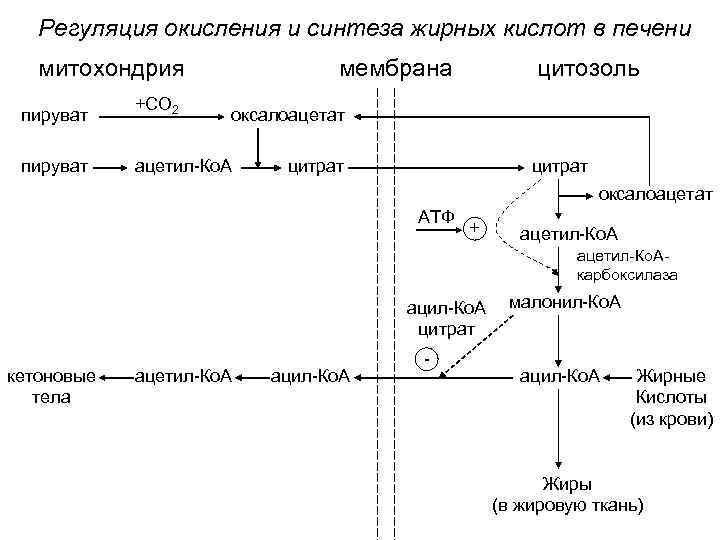
Регуляция окисления и синтеза жирных кислот в печени митохондрия мембрана пируват +СО 2 пируват ацетил-Ко. А цитозоль оксалоацетат цитрат оксалоацетат АТФ + ацетил-Ко. Акарбоксилаза ацил-Ко. А цитрат кетоновые тела ацетил-Ко. А ацил-Ко. А - малонил-Ко. А ацил-Ко. А Жирные Кислоты (из крови) Жиры (в жировую ткань)
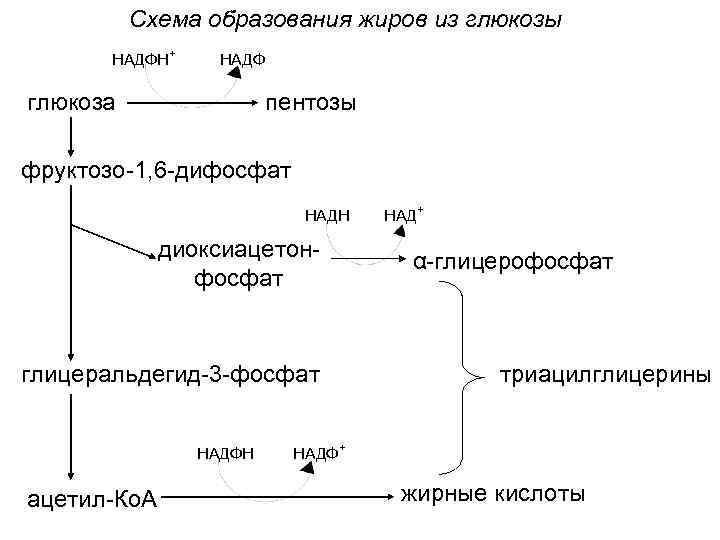
Схема образования жиров из глюкозы НАДФН + НАДФ глюкоза пентозы фруктозо-1, 6 -дифосфат НАДН диоксиацетонфосфат ацетил-Ко. А НАДФ + α-глицерофосфат глицеральдегид-3 -фосфат НАДФН НАД триацилглицерины + жирные кислоты

Гормональная регуляция обмена липидов Обмен липидов включает процесс синтеза липидов липогенез и процесс распада – липолиз. В регуляции обмена липидов участвуют инсулин, глюкагон, адреналин, СТГ. Инсулин стимулирует липогенез, т. е. синтез жирных кислот и триглицеридов. Механизм действия инсулина: 1. Инсулин способствует образованию глицеролфосфата в процессе гликолиза. 2. Инсулин ускоряет пентозофосфатный путь, который дает НАДФН 2, необходимый для синтеза жирных кислот. 3. Инсулин ускоряет биосинтез ферментов, участвующих в образовании триглицеридов. 4. В жировой ткани индуцирует синтез ЛП-липазы.

Результат действия инсулина на обмен углеводов и липидов – увеличение синтеза жиров и секреция их в кровь в составе ЛПОНП доставляют жиры в капилляры жировой ткани, где действие ЛП-липазы обеспечивает быстрое поступление жирных кислот в адипоциты, где они депонируются в составе триацилглицеридов. Мобилизация депонированных жиров стимулируется глюкагоном и адреналином и, в меньшей степени, соматотропным гормоном и кортизолом. Глюкагон, действуя на адипоциты через аденилатциклазную систему, активирует липазу, что стимулирует липолиз и выделение жирных кислот в кровь. При физической активности увеличивается секреция адреналина, что стимулирует липолиз. Для мышц, сердца, почек, печени при голодании и физической работе жирные кислоты становятся важным источником энергии. Печень перерабатывает часть жирных кислот в кетоновые тела, используемые мозгом, нервной тканью как источники энергии.

Патология липидного обмена Выделяют следующие виды нарушений липидного обмена: I. Нарушения переваривания и всасывания - наблюдается при заболеваниях поджелудочной железы, желчевыводящих путей, при гиповитаминозах A, D, E и К и при недостатке полиненасыщенных жирных кислот. II. Нарушения промежуточного обмена: 1. Ожирение; 2. Жировая инфильтрация печени; 3. Сахарный диабет; 4. Атеросклероз; 5. Гиперлипемии;

Ожирение Жировая ткань составляет 20 -25% от общей массы тела у женщин и 15 -20% у мужчин. Ожирением считают состояние, когда масса тела превышает 20% от «идеальной» . Первичное ожирение Развивается в результате алиментарного дисбаланса – избыточной калорийности питания по сравнению с расходами энергии. Причины первичного ожирения: -генетические нарушения; -состав и количество потребляемой пищи, метод питания в семье; -уровень физической нагрузки; -психологические факторы;

У человека и животных имеется «ген ожирения» . Продуктом экспрессии этого гена служит белок лептин. Лептин синтезируется и секретируется адипоцитами и взаимодействует с рецепторами гипоталамуса. В результате его действия снижается секреция нейропептида V, который стимулирует пищевое поведение. У 80% больных концентрация лептина в крови тучных людей больше в 4 раза, чем у людей с нормальной массой тела. В этих случаях имеется генетический дефект рецепторов лептина в гипоталамусе, поэтому, несмотря на секрецию лептина, центр голода в гипоталамусе продолжает секрецию нейропептида V. 20% больных имеют изменения в первичной структуре лептина. Патогенез ожирения при дефекте гена может быть следующим: низкий уровень лептина в крови служит сигналом недостаточного запаса жиров в организме; этот сигнал включает механизмы, приводящие к увеличению аппетита и в результате к увеличению массы тела.

Вторичное ожирение Ожирение, развивающееся в результате какого-либо основного заболевания, чаще всего эндокринного. Например, к развитию ожирения приводят гипотиреоз, синдром Иценко-Кушинга, гипогонадизм. Сахарный диабет При сахарном диабете наблюдается недостаток инсулина. Недостаток инсулина тормозит использование глюкозы как источника энергии. При недостатке инсулина тормозится гликолиз, ЦТК, пентозофосфатный путь, гликогенез (синтез гликогена). Это приводит к повышению концентрации глюкозы в крови и развивается гипергликемия. В качестве источника энергии используется жирные кислоты, которые подвергаются β-окислению с образованием ацетил-Ко. А. При недостатке инсулина тормозится ЦТК и ацетил-Ко. А не сгорает и идет на синтез кетоновых тел печени и в результате развивается кетонемия, кетоурия и кетоацидоз. Развитие кетоацидоза связано с тем, что 2 соединения, относятся к кислотам: β-гидроксибутират, ацетоацетат. Сахарный диабет часто осложняется атеросклерозом, т. к. избыток ацетил-Ко. А используется для синтеза холестерина.

Жировая инфильтрация печени В норме ТГ составляют 5% от массы печени, при патологии до 60%, что вызывает сдавление гепатоцитов, их гибель, нарушение функций печени. Причины: 1. Алиментарная (редко, мало белка, дисбаланс питания, много триглицеридов); 2. Вирусные агенты (в том числе алкоголь-1/3 всех случаев, химиканты с/х, промышленности, никотин, токсины); 3. Отсутствие липотропных веществ (холин, метионин, В 12, В 10, Ко. F); Во 2 и 3 случаях – патогенез развития одинаковой – нарушение печеночных ферментов, в первую очередь ферментов метилирования. В результате возникает следующая цепь нарушений:
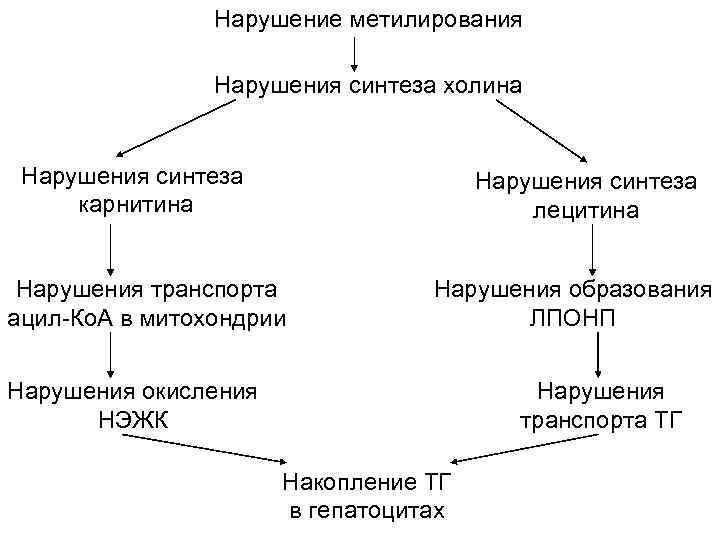
Нарушение метилирования Нарушения синтеза холина Нарушения синтеза карнитина Нарушения синтеза лецитина Нарушения транспорта ацил-Ко. А в митохондрии Нарушения образования ЛПОНП Нарушения окисления НЭЖК Нарушения транспорта ТГ Накопление ТГ в гепатоцитах
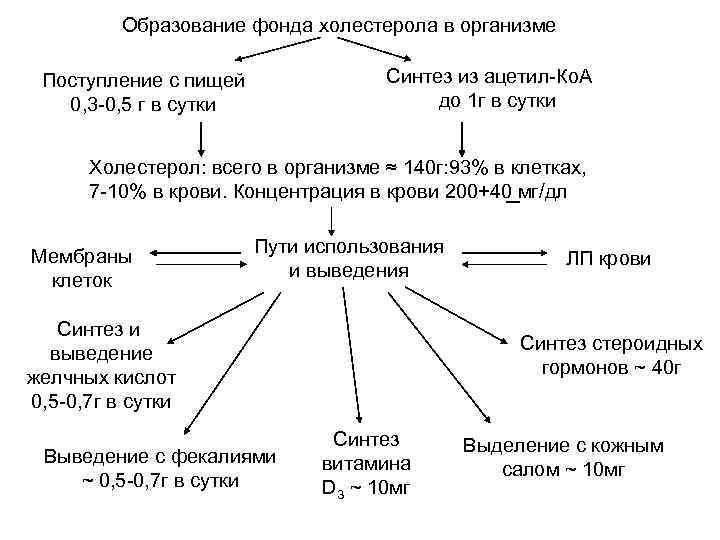
Образование фонда холестерола в организме Синтез из ацетил-Ко. А до 1 г в сутки Поступление с пищей 0, 3 -0, 5 г в сутки Холестерол: всего в организме ≈ 140 г: 93% в клетках, _ 7 -10% в крови. Концентрация в крови 200+40 мг/дл Мембраны клеток Пути использования и выведения Синтез и выведение желчных кислот 0, 5 -0, 7 г в сутки Выведение с фекалиями ~ 0, 5 -0, 7 г в сутки ЛП крови Синтез стероидных гормонов ~ 40 г Синтез витамина D 3 ~ 10 мг Выделение с кожным салом ~ 10 мг
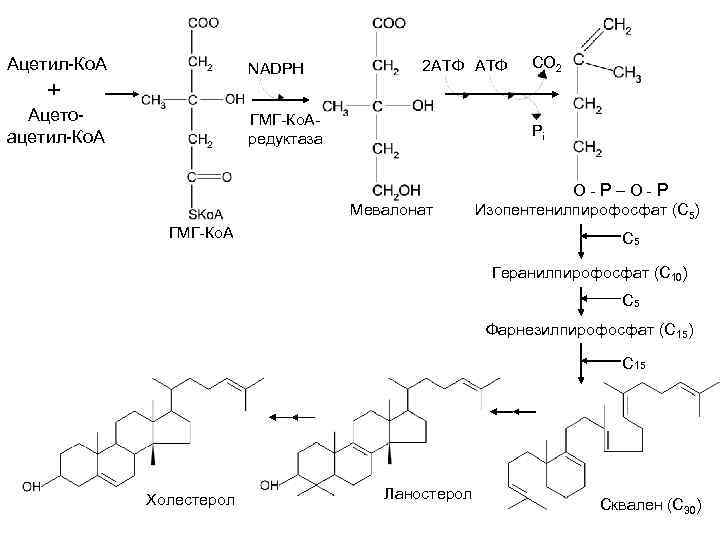
Ацетил-Ко. А NADPH + Ацетоацетил-Ко. А 2 АТФ ГМГ-Ко. Аредуктаза CO 2 Pi Мевалонат ГМГ-Ко. А O-P–O-P Изопентенилпирофосфат (С 5) С 5 Геранилпирофосфат (С 10) С 5 Фарнезилпирофосфат (С 15) С 15 Холестерол Ланостерол Сквален (С 30)
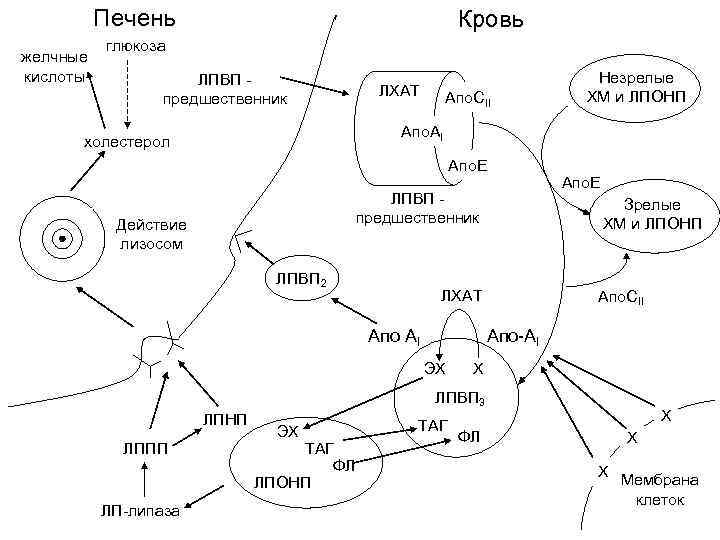
Печень желчные кислоты Кровь глюкоза ЛПВП предшественник ЛХАТ Апо. CII Незрелые ХМ и ЛПОНП Апо. АI холестерол Апо. E ЛПВП предшественник Действие лизосом ЛПВП 2 Зрелые ХМ и ЛПОНП ЛХАТ Апо АI Апо. E Апо. CII Апо-АI ЭХ Х ЛПВП 3 ЛПНП ЛППП ЛП-липаза ЭХ ТАГ ФЛ ЛПОНП ТАГ Х ФЛ Х Х Х Мембрана клеток
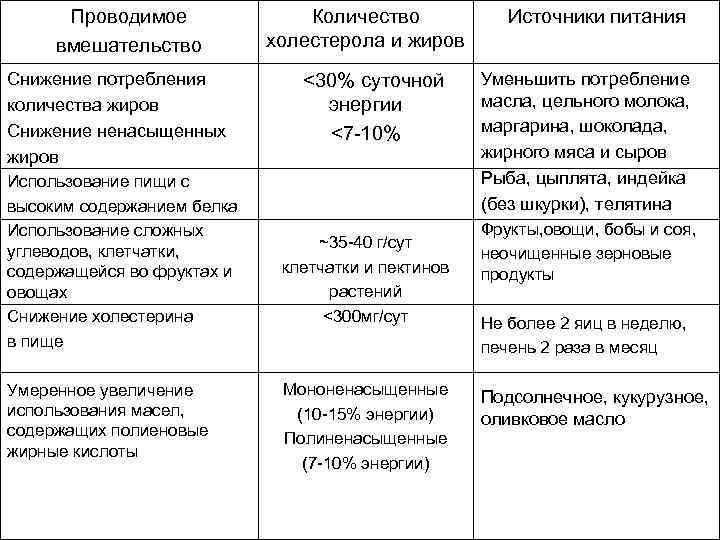
Проводимое вмешательство Снижение потребления количества жиров Снижение ненасыщенных жиров Использование пищи с высоким содержанием белка Использование сложных углеводов, клетчатки, содержащейся во фруктах и овощах Снижение холестерина в пище Умеренное увеличение использования масел, содержащих полиеновые жирные кислоты Количество холестерола и жиров <30% суточной энергии <7 -10% ~35 -40 г/сут клетчатки и пектинов растений <300 мг/сут Мононенасыщенные (10 -15% энергии) Полиненасыщенные (7 -10% энергии) Источники питания Уменьшить потребление масла, цельного молока, маргарина, шоколада, жирного мяса и сыров Рыба, цыплята, индейка (без шкурки), телятина Фрукты, овощи, бобы и соя, неочищенные зерновые продукты Не более 2 яиц в неделю, печень 2 раза в месяц Подсолнечное, кукурузное, оливковое масло
Липиды(Г.Н.Рыжикова).ppt